甲基紫动力学光度法测定双甘膦废水中微量甲醛
易灵红,韦后明,戴丽艳,施先义(广西现代职业技术学院资源工程系,广西 河池 547000)
实验室与分析
甲基紫动力学光度法测定双甘膦废水中微量甲醛
易灵红,韦后明,戴丽艳,施先义
(广西现代职业技术学院资源工程系,广西 河池 547000)
在硫酸介质中,甲醛能催化溴酸钾氧化甲基紫溶液褪色,褪色程度与甲醛含量成正比,由此建立了催化动力学光度法测定双甘膦废水中微量甲醛的方法。体系溶液在50℃水浴中反应10min后加入乙酸钠溶液以终止反应,于最大吸收波长585nm处测量吸光度。溶液中甲醛浓度在0.8~5.6μg·mL-1范围内呈良好的线性关系,表观摩尔吸光系数为2.5×104L··mol-1cm-1,相对标准偏差为1.78%(n=6),加标回收率在95.97%~102.62%之间。
催化光度法;甲基紫;甲醛;双甘膦
甲醛,化学式HCHO,已被世界卫生组织确定为致癌和致畸形物质,严重影响人类身体健康。双甘膦作为除草剂草甘膦的主要原料,其在制备过程中需采用甲醛作原料,从而导致排放的工业废水中含有甲醛。由于甲醛在水环境中极易与水缔和,因而容易造成水体污染。人类若长期饮用被甲醛污染的水体,将给身体健康带来严重危害。因此,对甲醛含量的测定研究,一方面对保障人体健康安全具有非常重要的现实意义,另一方面对企业树立绿色化学观、改进双甘膦生产工艺、减少废弃物排放等具有重要的研究价值。目前,催化动力学光度法测定微量甲醛得到了快速发展,主要有络黑T法[1]、溴酚蓝法[2]、次甲基蓝法[3]、甲基红法[4]、甲基橙法[5]以及甲基紫法[6]等。本文采用的甲基紫动力学光度法测定双甘膦废水中的微量甲醛,目前尚未见报道。方法用于测定双甘膦废水中的微量甲醛,结果满意。
1 实验部分
1.1 主要仪器与试剂
UV-1800PC型紫外可见分光光度计,HH-4数显恒温水浴锅。
0.2mol·L-1硫酸溶液,0.5g·L-1甲基紫溶液,0.1mol·L-1溴酸钾溶液,2.0mol·L-1乙酸钠溶液,1mg·mL-1甲醛标准贮备溶液,20μg·mL-1甲醛标准工作溶液。
实验所用试剂均为分析纯,实验用水均为去离子水。
1.2 实验方法
取2支25mL比色管,各依次准确加入0.2mol·L-1硫酸溶液2.0mL,0.5g·L-1甲基紫溶液1.0mL,0.1mol·L-1溴酸钾溶液4.0mL,其中一支比色管中加入一定量的甲醛标准工作溶液,另一支做试剂空白试验,用水定容至刻度,摇匀。在50℃水浴中加热10min,立即加入2.0mol·L-1乙酸钠溶液2.0mL,摇匀后放入冰水浴中冷却至室温,用1cm比色皿,以水作参比,在波长585nm处分别测出吸光度,其中含甲醛溶液吸光度为A,试剂空白试验吸光度为A0,计算ΔA=A0-A。
2 结果与讨论
2.1 吸收光谱
按1.2的实验方法在不同的波长下分别测定甲醛溶液及试剂空白溶液的吸光度,以波长λ为横坐标,吸光度A为纵坐标,绘制吸收光谱图,所得结果如图1所示。

图1 吸收光谱图
由图1可见,加入甲醛后,指示剂甲基紫的吸光度明显低于试剂空白,说明甲醛对溴酸钾氧化甲基紫溶液褪色反应有显著的催化作用。同时曲线1、2在波长为585nm处都有最大吸收峰。因此,本实验选择585nm作为测定波长。
2.2 酸度的影响
根据反应原理可知,反应必须在酸性条件下进行,溴酸钾氧化甲基紫溶液褪色是不可逆反应,且硫酸难以氧化甲基紫,因此,本实验选择在硫酸介质中进行。按照实验方法,改变加入硫酸的用量,测定各溶液的吸光度,探讨不同量硫酸溶液对褪色反应的影响。实验结果如图2所示。

图2 酸度的影响
由图2可知,随着硫酸用量的增加,溶液的吸光度先增加后减小。当硫酸用量为2.0mL时,ΔA值最大。小于2.0mL时,由于溶液酸度较低,催化反应速度较慢,褪色不明显。大于2.0mL时,由于空白反应速度加快,ΔA值迅速减小,因此,本实验选择硫酸用量为2.0mL。
2.3 甲基紫用量的影响
在反应体系中,甲基紫是吸光物质。甲基紫用量不同,溶液在585nm处吸光度ΔA值也不同。按照实验方法,探讨不同量甲基紫溶液对褪色程度的影响,以有较大的ΔA值为依据,实验结果如图3所示。

图3 甲基紫用量的影响
由图3可知,当甲基紫的用量为1.0mL时,ΔA值最大,用量少于1.0mL,A0值小,ΔA值也小;用量太大时,A0值太大,偏离朗伯-比尔定律,且ΔA值也小,因此,本实验选择甲基紫用量为1.0mL。
2.4 溴酸钾用量影响
从反应理论上可知,溴酸钾作为氧化剂,用量越多,反应速度越快,褪色程度越大,但用量太大时,终止反应不易控制,同时反应速率加快,反应时间太短,正常的操作时间误差也会使结果出现较大的误差。本实验溴酸钾用量以有较大的ΔA值且反应容易终止为依据,不同溴酸钾用量对褪色反应的影响如图4所示。

图4 溴酸钾用量的影响
由图4可知,随着溴酸钾溶液用量的增加,ΔA值先增大后减小,但反应速率逐渐加快。当溴酸钾用量为4.0mL时ΔA值最大,此时,加入乙酸钠溶液调节反应体系溶液pH值为碱性能够很好地终止反应。当用量大于4.0mL时,空白反应加快,ΔA值迅速变小。因此,本实验选择溴酸钾用量为4.0mL。
2.5 反应温度的影响
从反应理论得知,温度每升高10℃,反应速率增加2~4倍,对温度的考察主要是得到较大的ΔA值且稳定。实验结果表明,反应在常温下进行得较慢,温度增加,反应速度加快,当温度为50℃时,试样反应增大的速度明显大于空白反应,ΔA值最大,温度高于50℃时,空白及试样反应速度都太快,不易控制,同时ΔA值也趋于减小。因此,本实验选择反应温度为50℃。
2.6 反应时间的影响
从反应理论知道,反应时间越长,反应越彻底。考察加热时间的影响,主要是以得到较大ΔA值并符合测定要求为准,实验结果如图5所示。

图5 反应时间的影响
由图5可知,加热时间为10min时,ΔA值最大。加热时间太短,反应不完全,褪色不明显。加热时间太长,A0值小,ΔA值也小。因此,本实验选择水浴加热时间为10min。
2.7 反应的终止
反应体系在50℃水浴中反应10min,在冰水浴中冷却至室温后,通过测定溶液吸光度发现,甲基紫在585nm处的吸光度还在逐渐降低,说明体系冷却至室温后,反应并没有终止,褪色反应还在不断地进行着。由于反应需在酸性条件下进行,本实验采用加入乙酸钠溶液调节反应体系溶液pH值为碱性的方法以终止反应。体系终止反应后30min内吸光度基本稳定,表明乙酸钠溶液具有较好的终止反应的作用。
2.8 共存离子干扰实验
试验了部分常见离子对测定的影响。400μg·mL-1的 K+、Na+、Ca2+、Mg2+、Al3+、Zn2+、 NH4+、NO3-对测定没有干扰。
2.9 工作曲线
按照实验方法,移取一系列不同量的甲醛标准工作溶液绘制工作曲线。当测定溶液中甲醛的浓度在0.8~5.6μg·mL-1范围内时,ΔA值与浓度c呈良好的线性关系,其线性回归方程为:ΔA=0.0927c+0.0472,式中c为比色管中甲醛的浓度,单位为μg·mL-1,相关系数为0.997,摩尔吸光系数为2.5×104L·mol-1·cm-1。标准工作曲线如图6所示。
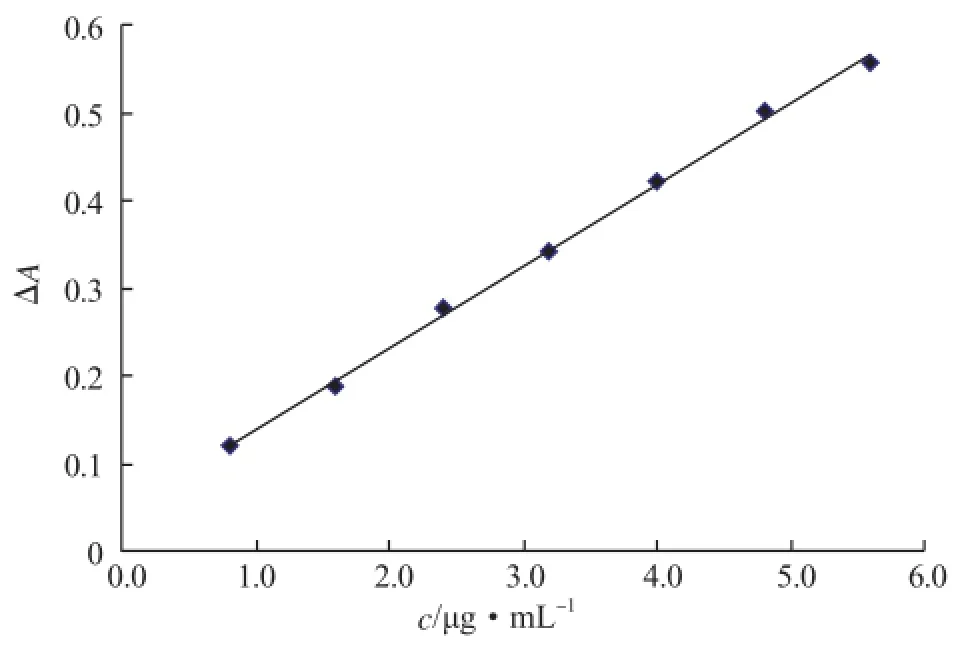
图6 标准工作曲线
3 样品测定
3.1 样品的处理
准确移取某化工厂双甘膦生产工段废水100mL,进行加热蒸馏,将蒸馏液收集于量杯中。当收集液大于80mL以上时,停止加热,用NaOH调节收集液pH值与甲醛标准溶液接近,再将收集液转移至100mL容量瓶中,用水稀释至刻度定容,摇匀,待用。
3.2 样品的测定
吸取一定体积经上述处理得到的试样溶液按实验方法进行预测定,最终确定合适的取样量,含量高的试样要进行适当的稀释。实验结果表明,废水经稀释5倍后,吸取1.0mL稀释液按1.2实验方法进行测定,甲醛含量较合适。样品测定结果见表1。
3.3 加标回收实验
按实验方法,其中一支比色管中加入一定量上述处理得到的试样稀释液和甲醛标准溶液使用液,另一支做试剂空白,进行加标回收实验,实验结果见表2。

表1 样品测定结果

表2 加标回收率实验结果
4 结论
采用催化动力学光度法测定双甘膦废水中的微量甲醛,采用加入乙酸钠溶液调节反应体系溶液pH值为碱性的方法以终止反应,通过单因素实验考察了酸度、甲基紫用量、溴酸钾用量、反应温度及时间对测定结果的影响。结果表明,当加入硫酸溶液2.0mL、甲基紫溶液1.0mL、溴酸钾溶液4.0mL、反应温度为50℃、加热时间为10min时,ΔA值最大。体系终止反应后30min内吸光度基本稳定。甲醛浓度在 0.8~5.6 μg·mL-1范围内呈线性关系,线性回归方程为:ΔA=0.0927c+0.0472,相关系数为0.997,样品废水中甲醛含量为0.634mg·mL-1,RSD为1.78%(n=6),加标回收率在95.97%~102.62%之间。
[1] 解凤霞,周蓓蓓,张逢星.络黑T褪色催化动力学光度法测定微量甲醛[J].理化检验-化学分册,2008,44(8):790-791.
[2] 解凤霞,赵春宝,陈立诚,等. KBrO3-溴酚蓝体系催化光度法测定微量甲醛[J].分析试验室,2007,26(8):91-93.
[3] 詹心琪,雷明杰.次甲基蓝-溴酸钾体系动力学光度法测定甲醛[J].理化检验-化学分册,2002,38(9):433-435.
[4] 严进.溴酸钾-甲基红体系测定水样中微量甲醛的研究[J].南通职业大学学报,2006,20(2):93-94.
[5] 王小波,李国强,孟建新.甲基橙-溴酸钾体系催化光度法测定微量甲醛[J].分析科学学报,2004,20(3):335-336.
[6] 王凯,韩志萍.甲基紫-溴酸钾褪色光度法测定微量甲醛[J].榆林学院学报,2005,15(5):12-14.
Determination of Trace Formaldehyde in Wastewater of PMIDA by Kinetic Spectrophotometry of Methyl Violet
YI Ling-hong, WEI Hou-ming, DAI Li-yan, SHI Xian-yi
(Department of Resources Engineering, Guangxi Modem Polytechnic College, Hechi 547000, China)
A catalytic kinetic spectrophotometric method was established for the determination of trace formaldehyde in wastewater of PMIDA. In sulfuric acid medium, potassium bromate could oxidize and decolorize the methyl violet under the catalysis of formaldehyde, the decolorization degree was proportional to the content of formaldehyde. At 50℃ water bath for reaction 10 min,sodium acetate solution was added into the system solution in order to stop the reaction. Absorbance was measured at the maximum absorption wavelength of 584nm. The formaldehyde had a good linear relation ship in the range of 0.8~5.6 µg/mL. The apparent molar absorptivity was 2.5×104L/mol/cm. The relative standard deviation was 1.78% (n=6). The adding standard recovery was between 95.97%~102.62%.
catalytic spectrophotometry; methyl violet; formaldehyde; PMIDA
O 657.3
A
1671-9905(2016)07-0052-04
2016年广西高校中青年教师基础能力提升项目(项目编号KY2016LX543)
易灵红(1983-),女, 湖南娄底人,硕士,讲师,主要从事化学教学及科研工作
2016-05-20

