正辛烷脱氢生成直链烯烃的热力学分析
于 宁, 王 铭, 秦 岭, 龙 军, 马爱增
(中国石化 石油化工科学研究院, 北京 100083)
正辛烷脱氢生成直链烯烃的热力学分析
于宁, 王铭, 秦岭, 龙军, 马爱增
(中国石化 石油化工科学研究院, 北京 100083)
摘要:计算了不同反应条件下正辛烷脱氢生成直链烯烃的主反应热力学平衡参数。计算结果显示,ΔH随温度上升变化不大,正辛烷脱氢反应的平衡常数较小。反应平衡时的产物中,1-辛烯含量最少,顺-4-辛烯次之;产品中绝大部分是双键位于第2到第4碳的烯烃,并且反式辛烯的物质的量大于相应的顺式。温度是一个很敏感的热力学参数,随着温度的升高,正辛烷的平衡转化率呈较大幅度的增加;增加体系压力和氢/烃摩尔比可以明显降低正辛烷的平衡转化率,同时这些参数处于较低值时的影响较大。
关键词:正辛烷; 烷烃脱氢; 热力学; 平衡组成
根据Mills等[1-2]提出的Pt/Al2O3-Cl双功能重整催化剂反应机理,重整反应过程中的链烷烃脱氢环化反应的步骤是烷烃首先在Pt金属表面脱除氢自由基生成烯烃,随后发生多步反应,在经历多种环烷烃结构后,最终生成芳烃。
目前,已有大量在催化重整反应动力学方面的研究[3]。但是,在集总动力学数学模型的构建中,均将烷烃脱氢环化过程简化为烷烃生成环烷烃和环烷烃生成芳烃两步。数学模型构建简单,未单独考虑烷烃脱氢生成烯烃等具体反应。在重整反应热力学方面,对于重整原料油中含量较多的C6~C9等短链烷烃脱氢反应鲜有报道,相类似的研究主要集中在用于生产化工用品的C9~C14等长链烷烃的脱氢反应[4-7]。
为了探索重整反应化学,加深对基元反应的认识,笔者[8-9]已从动力学角度研究了烷烃脱氢生成直链烯烃反应的基元反应路径及反应能垒。本研究中,笔者选取石脑油中单体烷烃含量较高的正辛烷作为模型化合物,对其脱氢生成直链烯烃的各主反应进行详细的热力学计算,并讨论了不同反应条件对产物平衡组成的影响,意在为重整反应化学的深入研究提供一些理论依据。
1 正辛烷脱氢生成直链烯烃的各主反应平衡常数的计算
采用Outokumpu公司HSC Chemistry 5.0软件进行热力学计算,各种物质的热力学数据由软件数据库导入。在低压时,体系各组分的逸度近似于它们的压力,可视为理想气体。不特别指明时,所有反应均以1 mol主反应物正辛烷为基准,反应热的单位为kJ/mol。假定所有反应体系均为封闭体系,不特别指明时,压力指绝对压力,计算所得的结果均为反应达到化学平衡时的组成,转化率为平衡转化率。
表1为不同温度下正辛烷脱氢生成直链烯烃各主反应的摩尔反应焓(ΔH)。从表1可以看出,单一反应均为吸热反应,同时ΔH随温度的增加变化不大;在相同温度下,对于并行的7个反应,生成1-辛烯较生成内位烯烃的ΔH高约10 kJ/mol。从能量角度而言,脱氢反应优先生成内位烯烃。
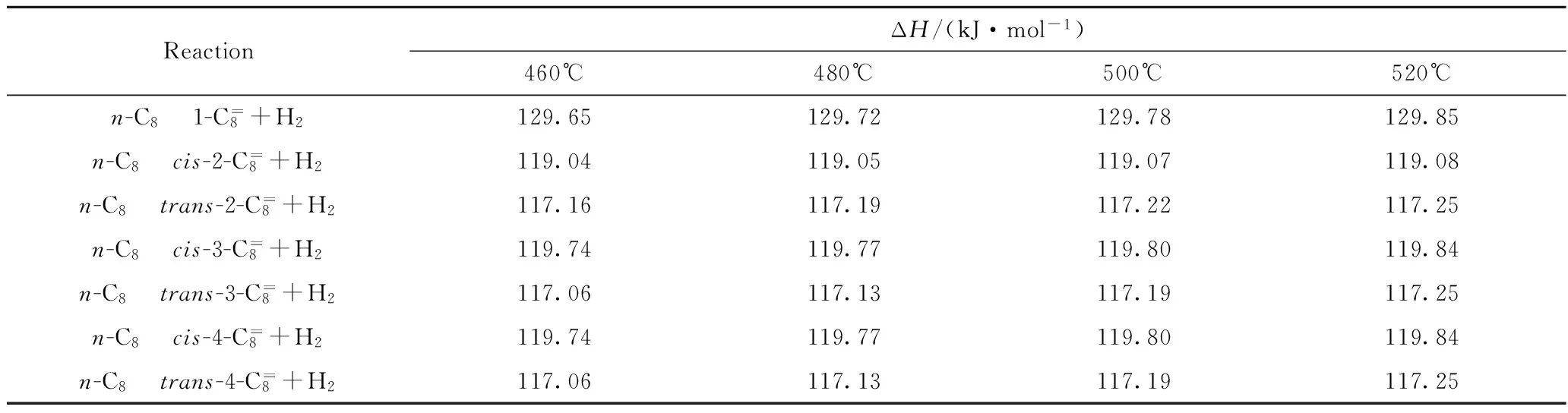
表1 不同温度下正辛烷脱氢生成各直链烯烃的ΔH
表2为不同温度下正辛烷脱氢生成直链烯烃各主反应的平衡常数(Kp)。可以看出,尽管随着温度的升高,Kp增加,但总的来看Kp值均较小;在相同温度下,对于并行的7个反应,Kp的大小顺序与其ΔH的大小顺序相同(见表1),反式烯烃相比顺式烯烃的平衡常数有明显增加。

表2 不同温度下正辛烷脱氢生成各直链烯烃的Kp
2 正辛烷脱氢生成直链烯烃组分平衡摩尔分数的计算
正辛烷脱氢生成的直链烯烃有7个异构体,因此有7个独立的反应平衡常数的计算式,如式(1)所示。
(1)
设定反应物中正辛烷(C8)含量为1 mol,反应达到平衡时共转化了xmol正辛烷,并生成了7种直链烯烃。式(1)中,i为 1,2,3……7;N为氢烃摩尔比(n(H2)/n(C8));p为反应压力;Ki表示正辛烷脱氢生成的第i种烯烃的反应平衡常数;xi表示第i种烯烃平衡时的摩尔分数。在计算时,N和p为已知的反应条件,同时,x和xi存在式(2)的关系。
x=x1+x2+x3+x4+x5+x6+x7
(2)
对正辛烷脱氢生成直链烯烃的反应,平衡时体系中共有8个未知数,包括正辛烷的总转化率x和7种直链烯烃的摩尔分数xi。平衡时共存在8个独立方程,方程数与未知数数目相等,故可采用牛顿迭代法求解。
在计算开始时,反应物中正辛烷的初始含量为1 mol。当反应结束后,产物中未反应的正辛烷和生成的各种直链烯烃的物质的量总和为1 mol。而产物中H2的物质的量为初始H2的物质的量加上生成的H2的物质的量。
3 计算结果与分析
表3为在常压、反应物中氢/烃摩尔比(N)为0的情况下,不同温度时产物中各直链烯烃的平衡摩尔分数xi及正辛烷的平衡转化率x。从表3可以看出,随着温度的升高,各直链烯烃的平衡摩尔分数增加,正辛烷的平衡转化率增加。从产物分布看,1-辛烯最少(这是因为伯碳原子上的C—H键的解离能大于仲碳原子上的C—H键的解离能[8]),顺-4-辛烯次之。产物中绝大多数烃类是双键位于第2到第4碳的烯烃,并且,由于几何结构稳定,反式辛烯的物质的量大于相应的顺式辛烯的物质的量。
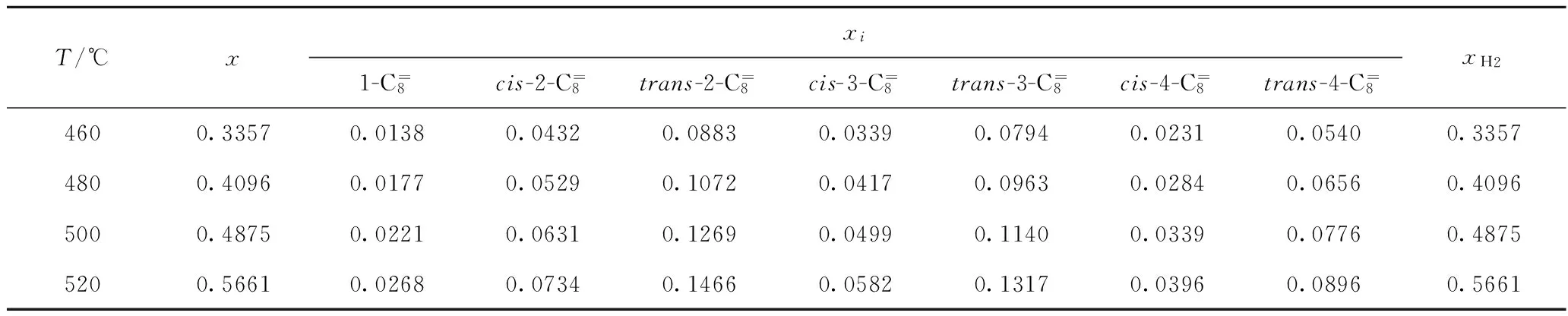
表3 不同温度下正辛烷脱氢生成直链烯烃的平衡摩尔分数(xi)和平衡转化率(x)
p=0.1 MPa;N=0
选用重整工艺中常用的反应温度500℃,计算了常压下不同氢/烃摩尔比时正辛烷脱氢生成直链烯烃的平衡摩尔分数xi和平衡转化率x,结果列于表4。由表4可以看出,随着氢/烃摩尔比的增加,反应平衡向左移动,各直链烯烃的平衡摩尔分数逐步降低;正辛烷平衡转化率的降低极为明显,并且低氢/烃摩尔比时降低的幅度要比在高氢/烃摩尔比时大得多。
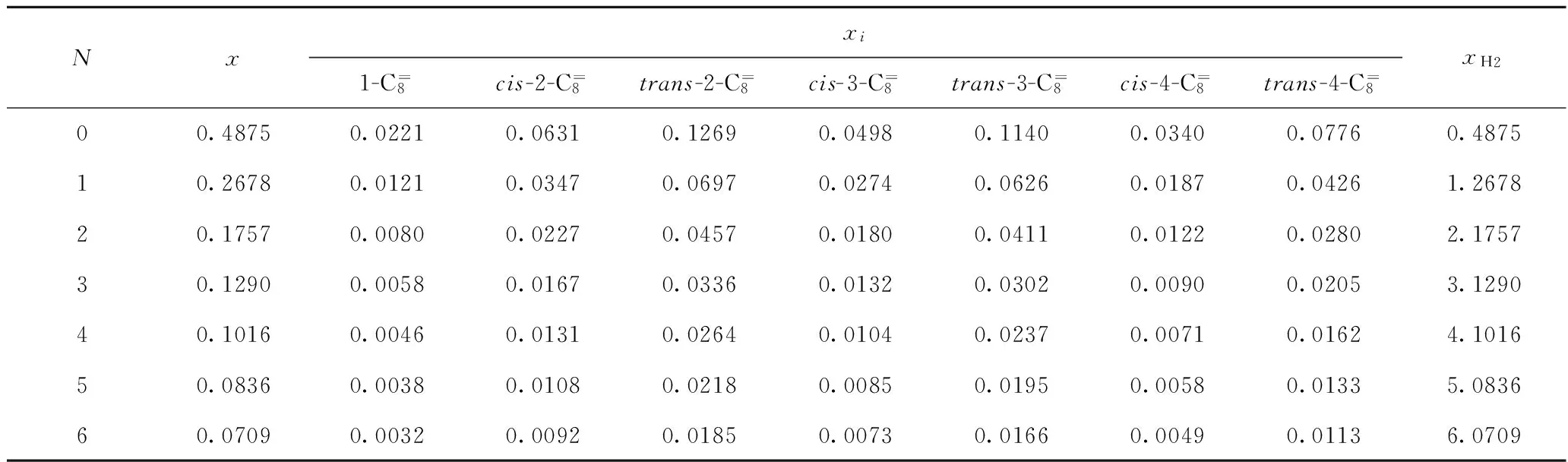
表4 不同氢/烃摩尔比(N)下正辛烷脱氢生成直链烯烃的平衡摩尔分数(xi)和平衡转化率(x)
T=500℃;p=0.1 MPa
以反应温度500℃、氢/烃摩尔比为5作为计算条件,计算了不同绝对压力下正辛烷脱氢生成直链烯烃的平衡摩尔分数xi和平衡转化率x,结果列于表5。如表5所示,当温度和氢/烃摩尔比不变时,随着反应压力增加,各直链烯烃的平衡摩尔分数和正辛烷的平衡转化率明显降低,并且低压时降幅比高压时大。从表5还可以看出,如在负压(绝对压力0.05 MPa、0.08 MPa)下操作,即使在较高氢/烃比下,正辛烷平衡转化率仍比较高。
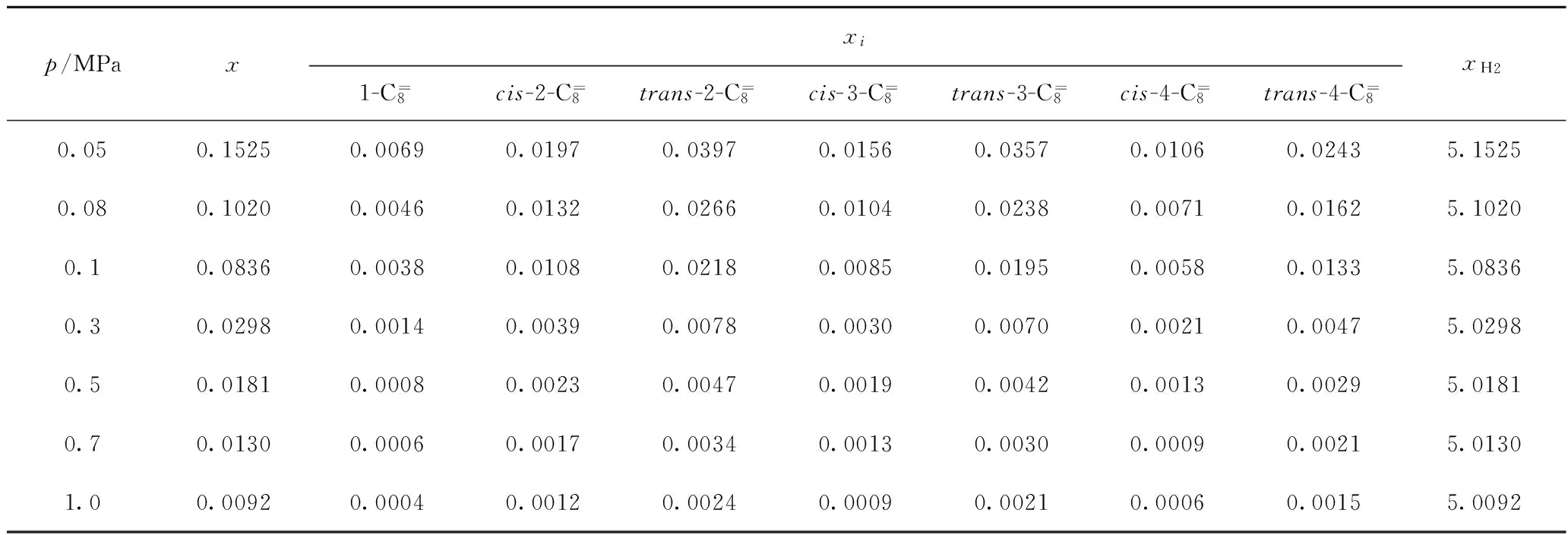
表5 不同绝对压力下正辛烷脱氢生成直链烯烃的平衡摩尔分数(xi)和平衡转化率(x)
T=500℃;N=5
结合重整工艺生产条件,综合对比表3、表4、表5数据。当p=0.1 MPa、N=0、T=500℃时,正辛烷的平衡转化率为48.75%;当p=0.1 MPa、N=5、T=500℃时,正辛烷的平衡转化率为8.36%;当p=0.3 MPa、N=5、T=500℃时,正辛烷的平衡转化率为2.98%。可以看出,增加反应压力和氢/烃摩尔比均可大幅度的降低脱氢反应的平衡转化率。
对于重整反应过程中的链烷烃脱氢环化反应,烷烃通过脱氢反应生成烯烃后,烯烃随后发生环化等反应最终生成芳烃。为了便于说明,现将脱氢环化反应简单划分为烷烃脱氢反应和烯烃环化反应两部分。对于单独的烷烃脱氢反应,从热力学平衡数据得出,反应存在热力学平衡限制,在与真实重整工艺条件相对应的p=0.3 MPa、N=5、T=500℃时,正辛烷的平衡转化率为2.98%。而在该条件下的实验中,当烷烃脱氢反应和后续的环化反应同时进行时,正辛烷的转化率可达到98%,可完全摆脱热力学平衡的限制。在真实的重整反应过程中,由于烷烃脱氢反应生成的烯烃作为后续环化反应的反应物在不断的被转化掉,可有效的降低脱氢反应中烯烃产物的含量,因此可以有效的促进脱氢反应向右侧进行。
4 结 论
(1)对于烷烃脱氢生成烯烃的吸热反应,ΔH随温度的增加变化不大。正辛烷脱氢生成各直链烯烃反应的平衡常数均较小。
(2)烷烃脱氢反应平衡时的产物中,1-辛烯含量最少,顺-4-辛烯次之;产品中绝大部分是双键位于第2到第4碳的烯烃,并且反式辛烯的物质的量大于相应的顺式。
(3)温度是一个很敏感的热力学参数,随着温度的升高,正辛烷的平衡转化率呈较大幅度的增加。
(4)增加体系压力、氢/烃摩尔比可以明显降低正辛烷的平衡转化率,同时这些参数处于较低值时的影响较大。
参考文献
[1] MILLS G A, HEINEMANN H, MILLIKEN T H, et al. Catalytic mechanism[J].I E C, 1953, 45(1): 134-224.
[2] KEULEMANS A I M, VOGE H. Reactivities of naphthenes over a platinum reforming catalyst by a gas chromatographic technique[J].Journal of Physical Chemistry, 1959, 63(4): 476-480.
[3] 徐承恩. 催化重整工艺与工程[M].北京:中国石化出版社, 2006, 192-281.
[4] 刘伟成, 田志坚, 徐竹生. 正癸烷脱氢生成直链单烯烃的热力学分析[J].石油学报(石油加工), 2001, 17(4): 39-43.(LIU Weicheng, TIAN Zhijian, XU Zhusheng. A thermodynamic analysis on dehydrogenation ofn-decane to decene[J].Acta Petrolei Sinica (Petroleum Processing Section), 2001, 17(4): 39-43.)
[5] 张高勇, 刘骥, 唐鸿鑫. 长链烷烃脱氢主反应及其失活过程表观动力学研究[J].燃料化学学报, 1983, 11(2): 48-59.(ZHANG Gaoyong, LIU Ji, TANG Hongxin. Kinetics of catalytic dehydrogenation of long chain paraffins and its deactivation[J].Journal of Fuel Chemistry and Technology, 1983, 11(2): 48-59.)
[6] 康保安, 唐鸿鑫, 张高勇, 等. 长链烷烃脱氢动力学的研究[J].日用化学工业, 1986, (3): 1-6.(KANG Baoan, TANG Hongxin, ZHANG Gaoyong, et al. Research into the dynamics of long-chain alkenes dehydrogenation[J].Daily Chemical Industry, 1986, (3): 1-6.)
[7] 张高勇, 刘骥. C9~C14烷烃脱氢主反应热力学计算——长链正构烷烃脱氢热力学分析Ⅰ[J].日用化学工业, 1983, (3): 7-13.(ZHANG Gaoyong, LIU Ji. Thermodynamic calculation of dehydrogenation reaction of C9~C14paraffin——Thermodynamic analysis of dehydro-genation reaction of long-chainparaffins Ⅰ[J].Daily Chemical Industry, 1983, (3): 7-13.)
[8] 于宁, 龙军, 周涵, 等. 正庚烷脱氢生成烯烃反应的分子模拟[J].石油学报(石油加工). 2013, 29(2):181-185.(YU Ning, LONG Jun, ZHOU Han, et al. Study on molecule simulation of dehydrogenation ofn-heptane to produce olefins[J].Acta Petrolei Sinica (Petroleum Processing Section), 2013, 29(2): 181-185.)
[9] 于宁.正庚烷脱氢环化生成甲苯反应化学的研究[D].北京:石油化工科学研究院,2013.
收稿日期:2015-03-26
基金项目:中国石油化工股份有限公司项目(R14056)资助
文章编号:1001-8719(2016)04-0762-05
中图分类号:TE624
文献标识码:A
doi:10.3969/j.issn.1001-8719.2016.04.015
A Thermodynamic Analysis on Dehydrogenation of n-Octane to Octenes
YU Ning, WANG Ming, QIN Ling, LONG Jun, MA Aizeng
(ResearchInstituteofPetroleumProcessing,SINOPEC,Beijing100083,China)
Abstract:Thermodynamic equilibrium parameters of n-octane dehydrogenation to octenes were calculated in detail. The calculated results showed that ΔH of n-octane dehydrogenation changed little with the increase of temperature and the equilibrium constants were small. In the equilibrium products the amount of 1-octene was the least, the amounts of 2- to 4-octenes were the most, and the mole number of trans-octene was more than that of the corresponding cis-octene. Reactant temperature was a very sensitive thermodynamic parameter. As temperature increased, the equilibrium conversion of n-octane relatively substantially increased. The equilibrium conversion was significantly reduced with the increases of the pressure and the molar ratio of H2 to n-octane, at lower values of which the equilibrium conversion was more sensitive.
Key words:n-octane; dehydrogenation of alkanes; thermodynamics; equilibrium composition
通讯联系人: 于宁,男,高级工程师,博士,从事催化重整反应机理的研究;Tel:010-82368768;E-mail:yuning.ripp@sinopec.com

