不同终点pH值溶液制备的Fe/ATP吸附剂的脱硫性能
魏 燕, 张智宏, 李 敏, 杜晓刚
(常州大学 石油化工学院, 江苏 常州 213164)
不同终点pH值溶液制备的Fe/ATP吸附剂的脱硫性能
魏燕, 张智宏, 李敏, 杜晓刚
(常州大学 石油化工学院, 江苏 常州 213164)
摘要:以凹凸棒石(ATP)为载体,采用直接沉淀法制备了不同反应终点溶液pH值的Fe/ATP吸附剂。采用XRD、H2-TPR、UV-vis和CO2-TPD表征了所制备的吸附剂,并在室温下固定床反应器中考察了其脱硫性能。结果表明,ATP负载铁氧化物可以有效提高吸附剂的脱硫性能。增加反应终点溶液pH值,可以使所制备的Fe/ATP吸附剂的堆密度减小,孔体积以及孔隙率增大,分散性和表面碱性增强,从而提高了吸附剂的脱硫活性,穿透硫容可达到20.50%。添加载体以及提高反应终点溶液pH值可以显著改善吸附剂的脱硫性能。
关键词:Fe/ATP;吸附剂; 分散性; 表面性质
H2S是一种高刺激性剧毒气体,凡含硫的化合物通过各类反应都有生成H2S的可能性。工业废气中的H2S主要源于炼油厂、天然气净化厂、煤气净化厂、冶炼厂、制革厂、氮肥厂、农药厂等,其污染环境、腐蚀设备,造成催化剂中毒。氧化铁吸附剂因其工艺简单、硫容高、价廉易得,被广泛应用于气体中H2S的脱除[1]。通常所说的氧化铁是铁的各种氧化物的统称,其种类繁多,活性各异。但现在工业应用中的氧化铁吸附剂,操作空速不高(100~3000 h-1),活性组分各不相同,脱硫性能差别较大,使用场合存在局限性。对于很多无水含硫气体的脱除,吸附剂的脱硫性能不佳,人为在气体中补充水分,则会影响整个工艺过程。
凹凸棒石(ATP)是一种层链状的含水富铝镁硅酸盐矿物,其结构中含有的水分可以提供脱除H2S所需的解离环境;同时ATP也是一种很好的黏结剂,有利于吸附剂的成型。相比于活性炭、半焦这些常用的吸附剂载体,还具有价格低廉、预处理简单等优点,将是未来负载型吸附剂载体的新选择。
制备条件会影响吸附剂的孔结构、活性铁含量和表面性质,进而影响脱硫活性。Fan等[2]通过添加黏土载体,吸附剂机械强度和活性组分分散性明显增强,提高了脱硫活性。Liu等[3]认为,吸附剂表面性质和孔结构是影响硫容的关键因素,吸附剂表面的酸碱性对铁氧化物脱硫性能的影响也显示出复杂性。通过酸碱浸渍和添加碱性助剂都能提高铁氧化物的脱硫性能[4],但酸碱浸渍会出现浸渍不均匀,过多的碱性助剂会堵塞孔道,脱硫活性反而下降。溶液终点pH值是沉淀法制备吸附剂时影响脱硫性能的重要因素,目前,溶液终点pH值对所制备的负载型吸附剂的影响鲜有报道。因此,将铁氧化物与ATP结合,制备Fe/ATP吸附剂,研究其对H2S的吸附规律,探讨制备时溶液终点pH值对所制备的吸附剂表面性质的影响具有现实意义。
笔者以ATP为载体,采用直接沉淀法,通过控制反应终点时溶液的pH值(以下简称终点pH值),制备了Fe/ATP吸附剂。在流速60 mL/min(空速为14550 h-1)下,将其用于常温低浓度H2S的脱除,并采用XRD、UV-vis、TPR、TPD表征手段比较了在不同终点pH值制备的Fe/ATP吸附剂的H2S穿透曲线及硫容,说明了终点pH值与Fe/ATP吸附剂的表面酸碱性、分散状态以及吸附剂脱硫性能之间的关系,为提高吸附剂脱硫性能提供一种简单可行的方案。
1 实验部分
1.1吸附剂的制备
1.1.1Fe吸附剂的制备
将一定浓度的Fe(NO)3·9H2O和Na2CO3溶液缓慢并流加入烧杯中,搅拌并控制终点pH值为8,搅拌老化30 min,抽滤,用去离子水洗涤至中性,100℃烘干,得到Fe吸附剂,记为Fe。
1.1.2Fe/ATP吸附剂的制备
将一定质量的ATP制成浆液,其余步骤同Fe吸附剂的制备。控制终点pH值分别为4、6、8、10,搅拌老化30 min,抽滤,100℃烘干,得到产物Fe/ATP。采用碘量法[5]测定反应前后溶液中残留的Fe3+的含量,计算得到该吸附剂的Fe负载量为45.86%。
1.2吸附剂的表征
采用日本理学D/ma×2500 PC型X射线仪测定样品的XRD谱。铜靶,功率40 kV×100 mA=4 kW,步进0.02°。
采用美国康塔仪器公司ASIQ-MP-C化学吸附仪进行H2-TPR分析。TCD检测器;载气为N2,流量28.5 mL/min;还原气为H2,流量1.5 mL/min。
采用美国康塔仪器公司ASIQ-MP-C化学吸附仪进行CO2-TPD分析。称取0.1 g试样装入石英反应管中,先用He吹扫1 h,切换CO2吸附饱和,再用He吹扫,待基线稳定后,以10℃/min升温至800℃。
采用日本岛津UV3600型紫外光谱仪测定样品的UV-vis谱。以BaSO4为参比压片,波长范围240~800 nm。
1.3吸附剂的脱硫性能评价
将0.2 g粒度为150~180 μm的吸附剂装入φ4.5 mm×1.5 mm的U型管中,装填高度35 mm。25℃下,以N2和H2S的模拟混合气体为吸附气体样品,在气体流量60 mL/min、空速14550 h-1、进口气体质量浓度为600 μg/L的条件下进行吸附实验。采用上海天美科学仪器有限公司GC7890FP型气相色谱仪,每20 min检测出口H2S气体浓度。色谱仪配有火焰光度检测器(FPD),气化温度323 K,色谱柱温度323 K,检测器温度393 K,检测精度可达到4×10-10。按式(1)计算吸附剂穿透硫容。
(1)
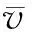
2 结果与讨论
2.1Fe/ATP吸附剂的物理结构
金属氧化物脱除H2S属于气-固反应,反应过程要受到内扩散和外扩散两方面的阻力,而吸附剂的孔隙结构对脱硫性能有着重要的影响,通过测定吸附剂的密度、孔隙率、孔体积,考察制备条件对Fe/ATP吸附剂结构的影响,结果列于表1。

表1 不同终点pH值制备的Fe/ATP吸附剂的性能参数及硫容
由表1可以看出,随着终点pH值的增大,所制备的Fe/ATP吸附剂的密度、颗粒密度均逐渐变小,孔隙率和孔体积均逐渐变大;硫容也逐渐增加,并且,终点pH值从4增大到8,硫容增加幅度逐渐变大,pH值由8增大到10,硫容增加幅度降低。
终点pH值为10时,Fe/ATP的孔隙率和孔体积增加幅度有所下降。较大的孔隙率和孔体积有利于H2S气体在孔道中的扩散,并且提供可供反应的空间,增加H2S气体活性组分接触的机会,提高脱硫速率与利用率。因此,增大终点pH值有利于提高Fe/ATP吸附剂的脱硫性能。
2.2Fe/ATP吸附剂的脱硫性能
图1是在25℃下测得的ATP和Fe吸附剂以及不同终点pH值制备的Fe/ATP吸附剂的H2S穿透曲线。可以看出,ATP吸附剂初始出口H2S质量浓度均超过了320 μg/L,脱硫效率很低,说明ATP虽然具有较大的比表面积,但在高空速下,脱除低浓度H2S不可行,而Fe吸附剂的硫容只有0.64%,也不利于硫的脱除。ATP负载Fe氧化物后,H2S脱除效率有了显著提高,且制备时终点pH值大的Fe/ATP对H2S的脱除效率越高,表明添加载体以及增加终点pH值可以有效提高Fe/ATP吸附剂的脱硫性能。

图1 ATP、Fe吸附剂和不同终点pH值制备的Fe/ATP吸附剂的H2S穿透曲线Fig.1 Breakthrough curves for ATP, Fe and Fe/ATP adsorbents prepared at differen terminal pH values (a)ATP and Fe adsorbents; (b)Fe/ATP adsorbents
2.3Fe/ATP吸附剂的物相
图2为ATP及不同终点pH值制备的Fe/ATP吸附剂的XRD谱。由图2可知,ATP在2θ为8.4°、19.8°、34.8°有明显的特征衍射峰,负载活性组分后,ATP的这些特征衍射峰变弱,而且随着终点pH值的增加,Fe/ATP吸附剂没有出现明显的Fe氧化合物晶相的特征衍射峰。这是因为,一方面带负电的ATP抑制了Fe氧化合物的结晶[6],并没有完成由无定型向晶体的转变;另一方面,Fe氧化合物高度分散在ATP表面,XRD中未能检测到相应的衍射峰[7]。从脱硫性能也可以看出,Fe/ATP吸附剂形成的高度分散的无定型Fe氧化物的脱硫性能优于无载体Fe吸附剂的脱硫性能。

图2 ATP和不同终点pH值制备的Fe/ATP 吸附剂的XRD谱Fig.2 XRD patterns of ATP and Fe/ATP adsorbents prepared at different terminal pH values
2.4终点pH值对Fe/ATP吸附剂性质的影响
2.4.1对Fe/ATP表面酸碱性的影响
采用CO2-TPD方法考察了不同终点pH值所制备的Fe/ATP吸附剂的表面碱性,表征结果示于图3。
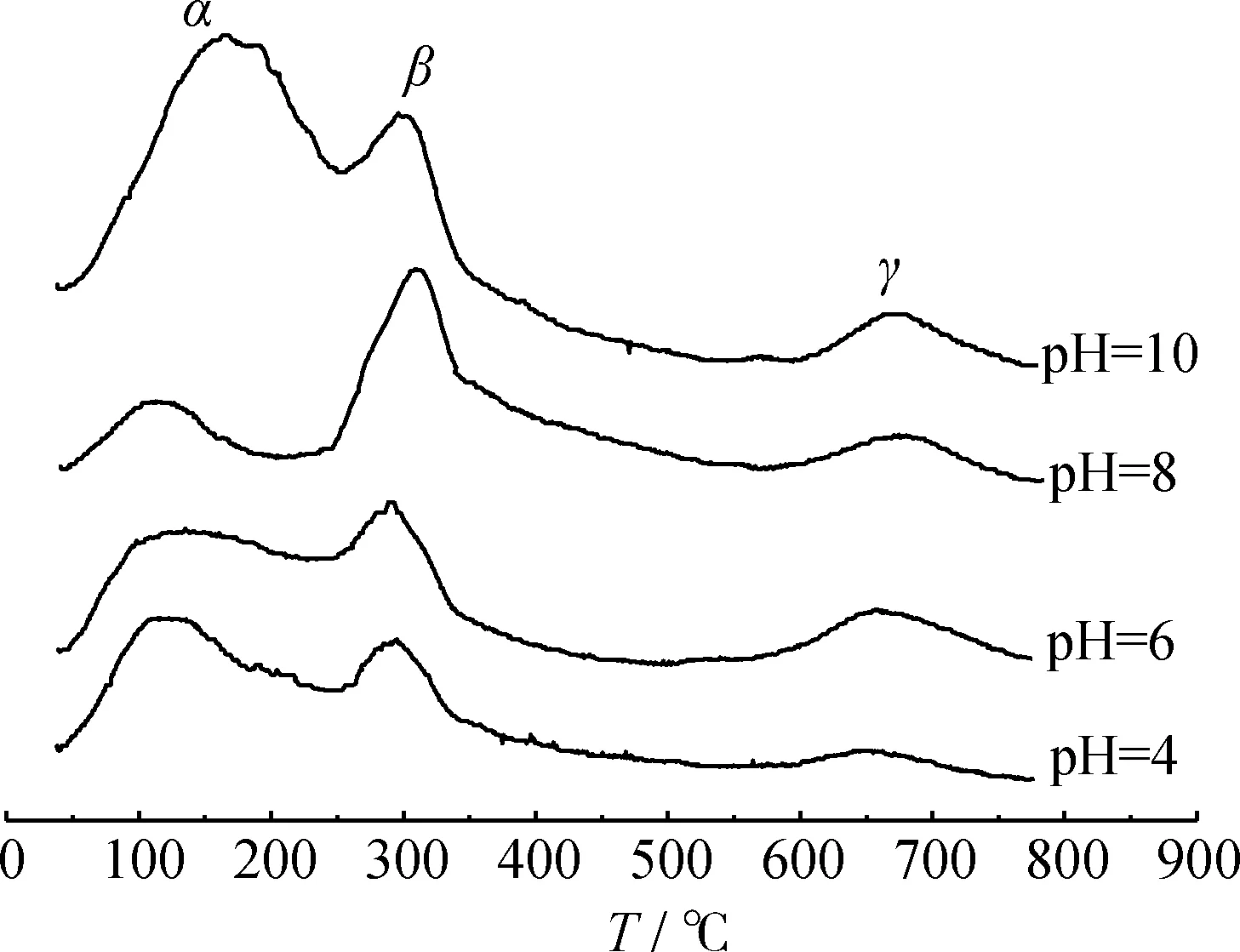
图3 不同终点pH值制备的Fe/ATP 吸附剂的CO2-TPD曲线Fig.3 CO2-TPD profiles of Fe/ATP adsorbents prepared at different terminal pH values
图3显示,不同终点pH值制备的Fe/ATP吸附剂的CO2-TPD曲线均存在3个CO2的脱附峰,表明它们表面存在强、中、弱3个碱性中心[8],而且随着终点pH值的升高,制备所得Fe/ATP的脱附温度向高温方向移动,表明吸附剂碱性增强[9]。随着终点pH值的增大,3个峰的面积和逐渐增大,表明吸附剂总碱量增加。终点pH值为4、6和8所制备的Fe/ATP的β脱附峰变化明显,峰面积越来越大;终点pH值为10的Fe/ATP的α脱附峰明显向高温方向移动,且峰面积变大,并与β脱附峰有重叠,表明吸附剂表面碱性对CO2吸附中心的数量及吸附强度有调变作用。碱性增强使脱附中心向高温方向移动,即在某种程度上增强了对CO2的吸附能力[10-11]。随着终点pH值的升高,吸附剂表面形成的水膜碱性增加,而H2S属于酸性气体,随着碱性的增强,其解离能力增强,这将提高吸附剂表面HS-的浓度,有利于脱硫反应的进行。
2.4.2对Fe在ATP表面分散性的影响
(1)UV-vis分析
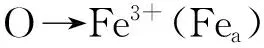
图4 不同终点pH值制备的Fe/ATP吸附剂的UV-vis谱Fig.4 UV-vis spectra of Fe/ATP adsorbent prepared at different terminal pH values

图5 终点 pH值为8制备的Fe/ATP吸附剂UV-vis分峰图Fig.5 UV-vis peak figure points of Fe/ATP adsorbent prepared at pH=8

表2 不同终点pH值制备的Fe/ATP吸附剂的UV-vis谱量化结果
(2)H2-TPR分析

图6 不同终点pH值制备的Fe/ATP吸附剂H2-TPR曲线Fig.6 H2-TPR profiles of Fe/ATP adsorbents prepared at different terminal pH values表3 不同终点pH制备的Fe/ATP吸附剂的H2-TPR分析结果Table 3 H2-TPR analysis results of Fe/ATP adsorbents prepared at different terminal pH values
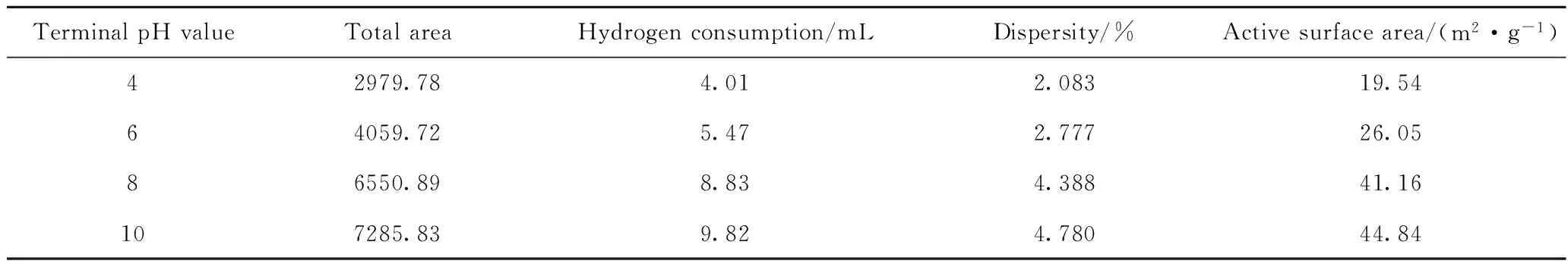
TerminalpHvalueTotalareaHydrogenconsumption/mLDispersity/%Activesurfacearea/(m2·g-1)42979.784.012.08319.5464059.725.472.77726.0586550.898.834.38841.16107285.839.824.78044.84
2.5Fe/ATP吸附剂脱硫机理分析
ATP以及Fe吸附剂的脱硫活性很低,但Fe负载在ATP表面制备的Fe/ATP吸附剂的硫容大幅度提高,穿透硫容可以达到20.50%。Bandosz[16]和Haimour等[17]认为,氧化铁脱除H2S的过程分阶段进行,①H2S先吸附在吸附剂表面;②在吸附剂表面形成的水膜中溶解,并解离为HS-;③与吸附剂中的活性组分中的氧结合最终进行硫化反应。反应过程如式(2)~式(5)所示,或者如式(6)、式(7)所示。
(2)
(3)
(4)
(5)
(6)
lg(Ka)+pH+lg(H2Sgas)
(7)
式(7)中,KS,KH,Ka分别为3.1,330,6.3×10-8,于是得到式(8)。
(8)
ATP作为载体,其结构中的沸石水、结晶水以及结构水[18]提供了H2S解离为HS-和S2-离子的条件,而pH值是影响吸附剂表面HS-浓度的关键因素。随着终点pH值的增大,所得Fe/ATP吸附剂的孔隙率和孔体积增大,同时表面碱性增强。表面碱性增强,有利于H2S的吸收和解离,对脱硫反应速率有促进作用;孔隙率和孔体积增大,增加H2S气体活性组分接触的机会,提高吸附剂的利用率。由UV-vis和XRD分析可知,Fe氧化合物在ATP载体表面高度分散,并没有形成晶相Fe氧化合物,实验证明这种负载型吸附剂具有较高的硫容;随着终点pH值的增加,吸附剂中低聚态的Fe含量增多,分散性增强,减小了载体表面Fe物种层的厚度,使HS-,S2-更容易扩散进入氧化物晶格中进行反应,提高了吸附剂脱硫活性。
3 结 论
(1)ATP作为载体,其结构中的水分为H2S提供了解离环境,在碱性条件下可以提高HS-和S2-的浓度,有利于加快脱硫反应速率,负载Fe氧化物后制备的Fe/ATP吸附剂的穿透硫容显著提高。
(2)控制制备溶液的终点pH值,是一种有效改善所制备吸附剂脱硫性能的方法。制备的Fe/ATP吸附剂的活性组分为高度分散的Fe氧化合物,在高空速下脱除低浓度H2S,硫容为20.50%。
(3)制备溶液的终点pH值对所制备Fe/ATP吸附剂的结构性能、表面酸碱性、活性组分分散性有很大的影响。随着终点pH值的增加,所制备Fe/ATP吸附剂的孔隙率和孔体积增大,表面碱性增强,可以提高吸附剂表面HS-的浓度,有利于硫化反应的进行;Fe/ATP吸附剂中低聚态Fe含量增高,分散性增强,吸附剂脱硫活性提高。
参考文献
[1] WANG J, ZHANG Y P, HAN L, et al. Simultaneous removal of hydrogen sulfide and mercury from simulated syngas by iron-based sorbents[J].Fuel, 2013, 103: 73-79.
[2] FAN H L, JU S G, LI T L, et al. A comparative study of the effect of clay binders on iron oxide sorbent in the high-temperature removal of hydrogen sulfide[J].Process Safety and Environmental Protection, 2013, 91(3): 235-243.
[3] LIU X M, MENG X, ZHAO J T. Synthesis of nanocrystalline iron oxides with mesostructure as desulfurizer[J].Materials Letters, 2013, 92(1): 255-2582.
[4] 贺恩云,樊惠玲,王小玲,等.氧化铁常温脱硫研究综述[J].天然气化工(C1 化学与化工),2014,39(5):70-74.(HE Enyun, FAN Huiling, WANG Xiaoling, et al. A review on studies of ambient temperature ferric oxide desulfurizers[J].Natural Gas Chemical Industry, 2014, 39(5): 70-74. )
[5] 郑大中,魏书云.矿石中铁的快速测定——强酸度、小体积碘量法[J].化学世界,1980,(7):207-209. (ZHENG Dazhong, WEI Shuyun. Rapid determination of iron in ores——Strong acidity small volume iodometry[J].Chemical World, 1980, (7): 207-209.)
[6] BHATTCHARYYA K G, GUPT S S. Kaolinite and montmorillonite as adsorbents for Fe(Ⅲ), Co(Ⅱ) and Ni(Ⅱ) in aqueous medium[J].Applied Clay Science, 2008, 41: 1-9.
[7] GONGSHIN Q, RALPH T Y. Ultra-active Fe/ZSM-5 catalyst for selective catalytic reduction of nitric oxide with ammonia[J].Applied Catalysis B: Environmental, 2005, 60: 13-22.
[8] WU G D, WANG X L, WEI W, et al. Fluorine modified Mg-Al mixed oxides: A solid base with variable basic sites and tunable basicity[J].Applied Catalysis A, 2010, 377(1): 107-113.
[9] 曲佳伟,王敏炜,王仁浪,等.固体碱KF/γ-Al2O3催化合成聚甘油[J].精细化工,2013,30(7):757-760.(QU Jiawei, WANG Minwei, WANG Renlang, et al. Synthesis of polyglycerol catalyzed by KF/γ-Al2O3solid base[J].Fine Chemicals, 2013, 30(7): 757-760.
[10] 王继元,曾崇余,林陵.助剂对Cu-ZnO-Al2O3-SiO2催化剂性质和催化性能的影响[J].石油化工高等学校学报,2005,18(3):9-14.(WANG Jiyuan, ZENG Chongyu, LIN Ling. Effect of promoters on the catalytic performance and properties of Cu-ZnO-Al2O3-SiO2catalysts[J].Journal of Petrochemical Universities, 2005, 18(3): 9-14.)
[11] 王自庆,林建新,王榕,等.改性ZrO2负载钌氨合成催化剂的制备及其构效关系研究[J].燃料化学学报,2012,40(12):1472-1479.(WANG Ziqing, LIN Jianxin, WANG Rong, et al. Ammonia synthesis over ruthenium supported on modified zirconia: Relationships between the catalyst structure and activity[J].Journal of Fuel Chemistry and Technology, 2012, 40(12): 1472-1479.
[12] GERVASINI A, MESSI C, CARNITI P, et al. Insight into the properties of Fe oxide present in high concentrations on mesoporous silica[J].Journal of Catalysis, 2009, 262(2): 224-234.
[13] SCHWIDDER M, KUMAR M S, KLEMENTIEVA K, et al. Selective reduction of NO with Fe-ZSM-5 catalysts of low Fe content: I. Relations between active site structure and catalytic performance[J].Journal of Catalysis, 2005, 231(2): 314-330.
[14] LIANG M S, KANGW K, XIE K C. Comparison of reduction behavior of Fe2O3, ZnO and ZnFe2O4by TPR technique [J].Journal of Natural Gas Chemistry, 2009, 18(1): 110-113.
[15] JOZWIAK W K, KACZMAREK E, MANIECKI T P, et al. Reduction behavior of iron oxides in hydrogen and carbon monoxide atmospheres[J].Applied Catalysis A, 2007, 326(1): 17-27.
[16] BANDOSZ T J. On the adsorption/oxidation of hydrogen sulfide on activated carbons at ambient temperatures[J].Journal of Colloid and Interface Science, 2002, 246(1): 1-20.
[17] HAIMOUR N, EL-BISHTAWI R, AIL-WAHBI A. Equilibrium adsorption of hydrogen sulfide onto CuO and ZnO[J].Desalination, 2005, 181(1-3): 145-152.
[18] NEAMAN A, SINGER A. The effects of palygorskite on chemical and physico-chemical properties of soils: A review[J].Geoderma, 2004, 123(3-4): 297-303.
收稿日期:2015-05-13
基金项目:江苏省产学研前瞻项目(BY2014037-10)资助
文章编号:1001-8719(2016)04-0688-07
中图分类号:X701.3
文献标识码:A
doi:10.3969/j.issn.1001-8719.2016.04.005
Desulfurization Performance of Fe/ATP Adsorbent Prepared in the Solution of Different Terminal pH Values
WEI Yan,ZHANG Zhihong,LI Min,DU Xiaogang
(SchoolofPetrochemicalEngineering,ChangzhouUniversity,Changzhou213164,China)
Abstract:The Fe/attaulgite (Fe/ATP) adsorbents were prepared in the solution of different pH values by using a direct precipitation, and characterized by using XRD, H2-TPR, UV-vis and CO2-TPD. The desulfurization performance of Fe/ATP was investigated in a fixed-bed at room temperature. The results showed that the desulfurization of Fe adsorbent was improved significantly by using ATP as the support. With the increase of the terminal pH value of solution, the pore volume, porosities, and dispersibility of the prepared Fe/ATP adsorbents were increased in contrast to the reduction of bulk density. Furthermore, the surface alkaline strength of adsorbent was effectively improved, which was beneficial to the performance improvement of the adsorbent effectively. The sulfur capacity of Fe/ATP adsorbent could reach 20.50%. The performance of the adsorbent could be achieved by adding the carrier and raising the terminal pH value of the solution.
Key words:Fe/ATP;adsorbent;dispersion;surface properties
第一作者: 魏燕,女,硕士研究生,从事含硫气体脱除方面的研究;E-mail:weiyan131027@163.com
通讯联系人: 张智宏,女,教授,从事环境中污染物的检测和净化研究;E-mail:zzhfine@163.com

