羧基对羟基酸脱铬性能的影响
杨春江,田荟琳,付丽红(齐鲁工业大学皮革化学与工程学院,山东济南250353)
羧基对羟基酸脱铬性能的影响
杨春江,田荟琳,付丽红*
(齐鲁工业大学皮革化学与工程学院,山东济南250353)
摘要:根据乳酸、苹果酸及柠檬酸脱铬过程中脱铬液pH值、铬含量和胶原水解量的变化,研究了羧基对羟基酸脱铬性能的影响。结果表明:羧基数多,脱铬量小,胶原水解轻,脱铬液平衡pH低;升高温度可减少位阻对脱铬的影响,高温短时有利于低元羧酸脱铬,高温长时有利多元羧酸脱铬;苹果酸和乳酸脱铬前期以H+为主,柠檬酸脱铬与温度有关,低温以H+为主,高温以酸根为主;胶原水解物对脱铬体系的pH值有缓冲作用,量越多,缓冲作用越大。
关键词:乳酸;苹果酸;柠檬酸;脱铬性能;羟羧酸
从纤维状胶原的利用角度考虑,有机酸脱铬效果好,脱铬率高、胶原纤维水解轻、性能好,可充分发挥胶原纤维的结构优势[1]。有机酸中草酸与三价铬离子的络合能力最强,酒石酸根能与金属离子形成非常稳定的螯合型配位化合物[2],因而草酸、酒石酸及其盐被广泛用于蓝湿皮的漂洗和脱铬中[3-4]。但乳酸和柠檬酸提取的纤维状胶原具有强度高、热性能好的特点[5-7]。从分子结构看,草酸为二元酸酸,乳酸、柠檬酸均为羟基酸,我们对系列有机酸的脱铬性能的研究中发现羟基对脱铬效果影响大,羟基数增加,二元羧酸脱铬效果增强[8]。然而,羧基数增多对羟基酸的脱铬性能有何影响,未见报道。为此,本文将在前期工作的基础上,以均含一个羟基的乳酸、苹果酸及柠檬酸为研究对象,探讨羟基酸分子中羧基数量对脱铬性能的影响,为优化脱铬条件提供理论依据。
1 试验部分
1.1试验试剂和仪器
黄牛沙发蓝湿革,济南鲁日钧达皮革有限公司;乳酸、苹果酸、柠檬酸,分析纯,天津市科密欧化学试剂有限公司;明胶(批号:F20030131),分析纯,中国医药(集团)上海化学试剂公司。
UV-2550紫外分光光度计,SHIMADZU;PHS-3C精密 pH计,上海雷磁仪器厂。
1.2试验方案
1.2.1溶液配制1.2.1.1 0.1 mol/L铬液(以Cr2O3含量计,B=20%)
精称0.8560 g葡萄糖,少量蒸馏水溶解。精称重铬酸钾2.9420 g,少量蒸馏水溶解,搅拌下先缓慢加入2 mL浓硫酸,再将葡萄糖溶液慢慢加入。微沸状态反应5 min,冷却至室温,蒸馏水定容至100 mL。
1.2.1.25 g/L明胶溶液的配制
精称5.0018 g明胶,室温溶胀4 h,转移至50℃水浴溶解,定容至1 000 mL。
1.2.1.3乳酸溶液的配制
(1)0.5 mol/L乳酸溶液
移取乳酸12.50 mL,蒸馏水定容至250 mL,测得溶液的pH 为1.91。
(2)0.1 mol/L乳酸溶液
移取 0.5 mol/L乳酸溶液10.00 mL于50 mL容量瓶中,定容。
1.2.1.4苹果酸溶液的配制
(1)0.5 mol/L苹果酸溶液
精称苹果酸16.7649 g,蒸馏水溶解后定容至250 mL,测得溶液的pH为1.58。
(2)0.1 mol/L苹果酸溶液
移取0.5 mol/L苹果酸溶液10.00 mL于50 mL容量瓶中,定容。
1.2.1.5柠檬酸溶液的配制
(1)0.5 mol/L柠檬酸溶液
精称柠檬酸26.2677 g,蒸馏水溶解后定容至250 mL,测得溶液的pH为1.57。
(2)0.1 mol/L柠檬酸溶液
移取0.5 mol/L柠檬酸溶液10.00 mL于50 mL容量瓶中,定容。
1.2.2蓝湿皮脱铬工艺(1)称量:皮1.00g(干皮)(2)预处理
(3)有机酸脱铬
①有机酸种类:乳酸、苹果酸、柠檬酸
②有机酸用量:0.5 mol/L有机酸溶液20 mL
③温度:25℃、35℃、45℃④时间:24 h
1.2.3脱铬液的分析
1.2.3.1脱铬液pH值的测定
用酸度计测定脱铬液pH值的变化。
1.2.3.2脱铬液中胶原水解量的测定
脱铬液中胶原水解物酪氨酸和苯丙氨酸的芳香基团吸收使其在280 nm处有最大吸收峰,故利用紫外分光光度计在280 nm处测定的脱铬液吸光度变化表征胶原水解量的变化。
1.2.3.3脱铬过程中铬含量的测定方法
(1)脱铬液铬含量测定波长的确定
吸取5 g/L明胶溶液36 mL 与0.1 mol/L的铬液4.00 mL混合均匀,后加入10%NaHCO3溶液1.00 mL,置于35℃水浴中反应30 min,加入0.1 mol/L的有机酸溶液6.00 mL,转移至60℃水浴中,反应24 h,反应过程中用紫外可见分光光度计对不同反应时间的溶液进行全波长扫描,以确定不同反应液的最大吸收波长。

图1 乳酸、苹果酸及柠檬酸脱铬过程中溶液pH的变化
(2)脱铬液中铬含量的测定
用有机酸、明胶和铬液混合液中铬络合物的最大吸收波长处吸光度的值,表征脱铬液中铬含量的变化。
1.2.3.4相对脱铬量的计算
相对脱铬量(%)=[(A2-A1)/A1]×100,相对胶原水解量(%)=[(B2-B1)/B1]×100
其中:A1、B1为25℃时脱铬液中的相对铬含量和胶原水解量;A2、B2为45℃时脱铬液中的相对铬含量和胶原水解量
2 结果与讨论
2.1脱铬过程中pH的变化
pH值的大小反映溶液中H+浓度的高低,脱铬液pH值的变化是H+、有机酸根脱铬及皮胶原水解共同作用的结果。不同结构的有机酸,不仅起始pH值不同,且有机酸根与Cr(Ⅲ)的配位能力不同,相同时间内消耗的有机酸根量以及脱铬消耗的H+也不同,故脱铬液中游离的H+量不同;另外,由于胶原水解物可以结合脱铬液中的H+,且不同脱铬液中的胶原水解物的量不同,故胶原水解物结合的H+量亦不同。因此,脱铬液pH值的变化反映了整个脱铬体系的物理化学变化。乳酸、苹果酸及柠檬酸脱过程中溶液pH值的变化见图1。
由图1可知,不同温度、相同时间内,乳酸脱铬液的pH值最高,其次是苹果酸,柠檬酸最低;不同温度下,乳酸脱铬液pH值于3h达到最大值之后基本保持稳定;25℃下,苹果酸脱铬液pH值的变化趋势与乳酸相似;但35℃、45℃时,苹果酸脱铬液pH值于3 h升至最大值后略有下降,7 h后基本不变;25℃下,柠檬酸脱铬液pH值于5 h升至最大值后开始下降,于9 h后基本保持稳定;35℃、45℃下,柠檬酸脱铬液pH值先降后升,3 h后基本保持不变;乳酸、苹果酸脱铬液平衡pH值均高于起始pH值,且乳酸pH值增加的幅度远大于苹果酸;随着反应温度的升高,乳酸脱铬液的平衡pH值略有升高,而苹果酸脱铬液平衡pH值降低;温度越高,柠檬酸脱铬液平衡pH值越低。
其原因一是三种酸的起始pH值不同(乳酸pH1.91、苹果酸pH1.58、柠檬酸pH1.57),因起始pH值越低,溶液中H+浓度越大,对平衡pH值的影响越大;另外,三种有机酸分子中羧基数不同,即与三价铬配位的原子数不同,因而形成的螯合物稳定性不同,所以溶液中剩余的H+量不同,故三种酸脱铬过程的平衡pH值不同,其由高到低的顺序为:乳酸>苹果酸>柠檬酸。
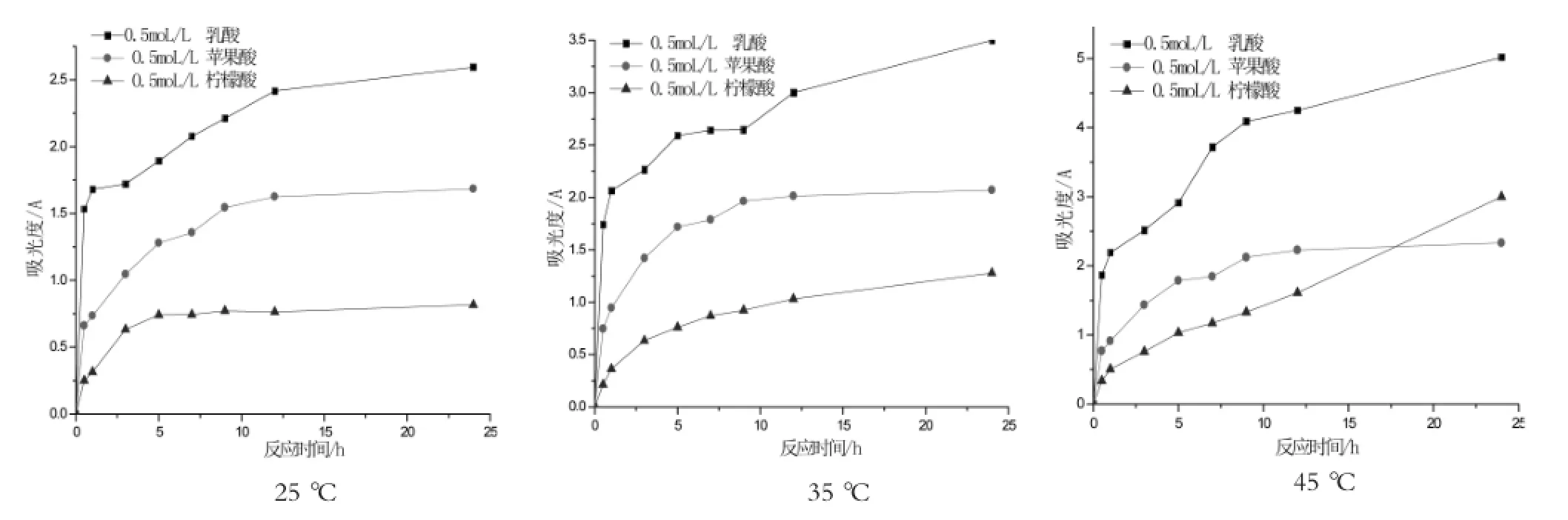
图2 乳酸、苹果酸及柠檬酸脱铬过程中胶原水解量的变化(280 nm)
二是有机酸脱铬是H+和有机酸根共同作用的结果,如果前者为主,则溶液pH值升高;反之,溶液pH值下降[1]。由此可见,不同反应温度下,乳酸、苹果酸3 h内均以H+脱铬为主;柠檬酸在25℃下、3 h内以H+脱铬为主,温度升高则以柠檬酸根脱铬为主。这是因为柠檬酸分子大,移动阻力大,温度升高可减少空间位阻的影响,表明温度升高可大大增加柠檬酸根的脱铬能力。温度升高,乳酸平衡pH值变化不大、苹果酸平衡pH值则降低,表明温度对乳酸根脱铬影响不大,但对苹果酸根脱铬影响大。这是因为温度升高,皮板的间隙增大,减少了空间位阻对酸根向皮内的渗透阻力,同时酸根的能量增加,移动速度加快,因而有利于酸根向皮内渗透。综上所述,温度升高,有利于提高有机酸根的脱铬能力,三种酸根脱铬大小顺序为柠檬酸根>苹果酸根>乳酸根,即羧基数越多,分子体积越大,其移动、皮内渗透、以及与铬结合的阻力越大,但升高温度可以减少位阻对有机酸脱铬的影响。
三是胶原水解物的影响。反应一定时间后,三种酸脱铬液pH值均能基本保持稳定,这可能是因为胶原水解物都是两性聚电解质,对脱铬液的pH值具有一定的缓冲作用。乳酸脱铬液pH值平衡最快、最稳定,应该与乳酸相同时间内的胶原水解量有关,这可从脱铬过程中胶原水解物的量变化加以验证。
2.2三种酸脱铬对胶原的影响
随着皮内铬的脱除,皮胶原的结构稳定性减弱,有机酸加剧胶原肽键的水解作用,故有机酸脱铬过程中必然引起皮胶原的破坏,通过测定脱铬液中胶原的水解量,可以了解有机酸脱铬对皮胶原水解的影响。
从三种酸脱铬液胶原水解量的变化可以看出(见图2),不同温度下,乳酸的胶原水解量远远大于苹果酸及柠檬酸,这与前面的推测结果相同;且随着温度的升高,三种酸胶原水解量均增加,尤其是柠檬酸。这表明柠檬酸脱铬时,温度对其胶原水解影响很大,因为柠檬酸分子体积较大、位阻大,低温下与皮纤维间的铬结合困难,而温度升高可以减少空间位阻对柠檬酸脱铬的影响,酸根与铬的配位能力增强,有利于脱铬,而脱铬必然会引起对胶原的破坏,所以柠檬酸的胶原水解量随着温度的升高而急剧增加。因三种有机酸pH均小于2,H+对皮胶原的水解作用很强,所以三种酸的胶原水解量均很大。从前面的分析可知,乳酸脱铬以H+为主,且乳酸分子较小,易于渗透到皮中,在破坏铬与皮胶原的交联键的同时,也作用于皮胶原间的各种化学交联,因而加剧了皮胶原的水解,故乳酸的胶原水解量远远大于苹果酸及柠檬酸。随着温度的升高,皮胶原纤维间距增大,且分子能量增加,均有利于酸根渗透于皮中并破坏各种化学键,故三种酸胶原水解量均随温度升高而增加,但苹果酸水解胶原的增加幅度不大。
2.3三种酸脱铬液中铬含量的变化
2.3.1脱铬液铬含量测定波长的确定
因不同有机酸的脱铬液中主要含有未反应的有机酸、有机酸与脱下的铬以及胶原水解物生成的新铬络合物、胶原水解物,故可用有机酸、明胶和铬液混合液中铬络合物的最大吸收波长处的吸光度来表征脱铬液中铬含量的相对变化。乳酸、苹果酸、柠檬酸与明胶和铬液混合液长波特征吸收峰位的变化见表1。
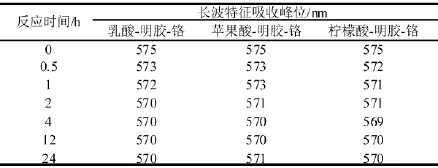
表1 有机酸与明胶和铬液混合液长波特征吸收峰位的变化
由表1可知,乳酸、苹果酸、柠檬酸与明胶-铬液反应过程中,溶液的长波特征吸收峰位均在570~573 nm之间变化,为便于与起始溶液的比较,三种有机酸脱铬过程中选用570 nm作为溶液中铬含量的测定波长。
2.3.2脱铬过程中铬含量的变化
乳酸、苹果酸、柠檬酸脱铬过程中溶液中铬含量的变化见图3。
由图3可知,不同温度下,苹果酸和乳酸两者的脱铬量随时间的变化趋势相似(苹果酸在45℃,10 h除外),脱铬量相近,但除25℃(小于7 h),柠檬酸的脱铬量均小于另外两种酸。这是因为在25℃下,三种酸脱铬前期均以H+为主,故相同反应时间的脱铬量与脱铬液pH值有关。三种酸脱铬液的pH值乳酸>苹果酸>柠檬酸,故5 h之前,相同反应时间内,三种酸的脱铬量柠檬酸>苹果酸>乳酸。但随着反应的进行,H+浓度降低,酸根与铬的络合配位便成为提高脱铬量的关键,因柠檬酸分子大,低温下分子能量较低,向皮内渗透与铬结合位阻较大,而且低温下胶原纤维间隙小,所以柠檬酸的脱铬速率首先开始降低;苹果酸次之;而乳酸因分子相对较小,由于其位阻小,低温下便可渗透到皮内进攻铬和胶原的交联,所以温度升高对乳酸脱铬影响不大,但对苹果酸、柠檬酸影响较大,尤其是柠檬酸。可见羧基数增多,分子变大,向皮内渗透和与铬结合的阻力也相应增大,故必须通过适当的提高温度以减少位阻对脱铬性能的影响。
综上所述,乳酸脱铬量最高,胶原水解重,脱铬液平衡pH最高;柠檬酸脱铬量最低,胶原水解最轻,脱铬液平衡pH最低;苹果酸脱铬量与乳酸相当,但胶原水解量及脱铬液平衡pH介于两者之间。即脱铬量和胶原水解量由大到小顺序均为:一元羧酸>二元羧酸>三元羧酸。
2.4温度对有机酸脱铬性能的影响
温度变化将影响化学反应的进行,当脱铬温度由25℃升至45℃时,三种酸的脱铬量及胶原水解量的变化见表2。
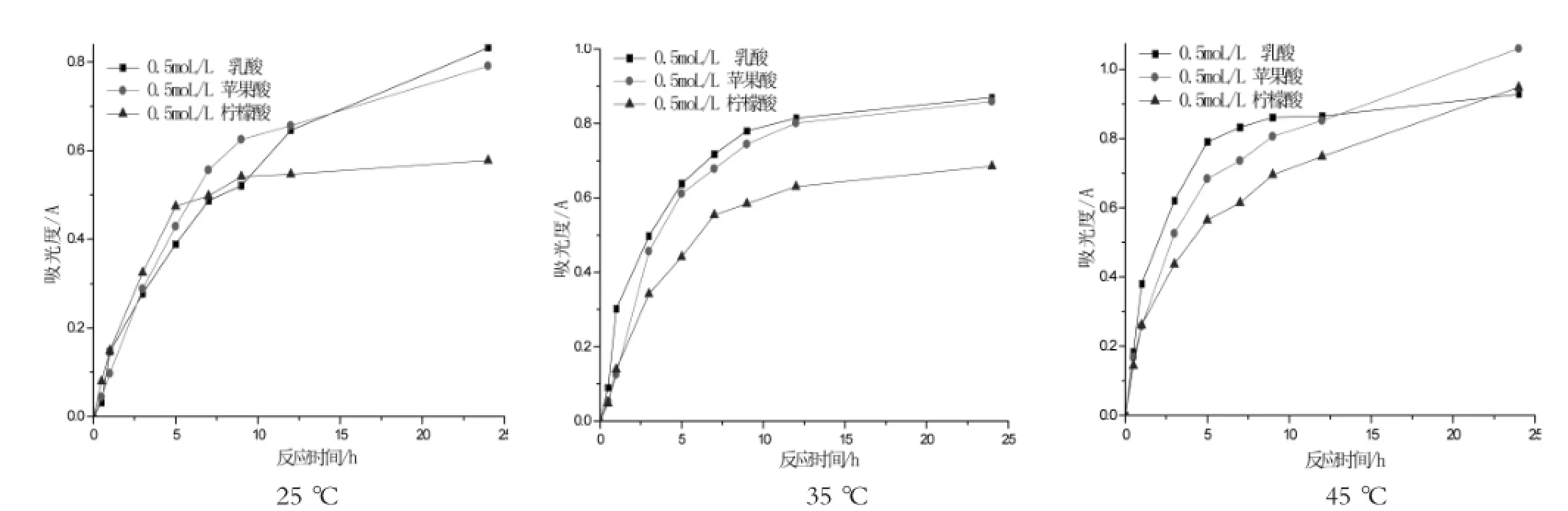
图3 乳酸、苹果酸及柠檬酸的脱铬量与脱铬时间的关系(570 nm)

表2 温度对有机酸脱铬及胶原水解的影响
由表2可知,温度升高,三种酸脱铬量和胶原水解量随着反应时间的增加,而且出现不同的变化规律,即乳酸的脱铬量急剧下降,但胶原水解量却显著增加;苹果酸的脱铬量逐渐降低,但胶原水解量几乎不变;柠檬酸的脱铬量逐渐增大、胶原水解量急剧升高。表明脱铬温度和时间对乳酸、柠檬酸脱铬的影响很大,但对苹果酸脱铬的影响相对较小。
因随着温度的升高,柠檬酸脱铬从以H+为主转变为以柠檬酸根为主,而柠檬酸分子体积大,即使具备了一定的能量,向皮内渗透及与铬结合的阻力也较大,故需要较长的反应时间其脱铬量才有较大的提高,因此温度对提高柠檬酸脱铬量的影响程度大;但同时温度提高,胶原水解的程度急剧增大,因此,柠檬酸脱铬需要综合考虑温度及反应时间对脱铬效果的影响,长时适当温度(35℃)下脱铬量多,胶原水解轻。乳酸脱铬前期以H+为主,随着温度的升高,H+活性增大,短时间内脱铬量显著增加,但随着反应的进行,溶液中H+减少,且由于乳酸分子较小,升高温度对促进乳酸根脱铬影响不大,故反应一段时间后即使升温,其相对脱铬量也大大减小,但胶原的水解量却急剧增加,因此,乳酸脱铬低温长时有利,脱铬量大,胶原水解轻;苹果酸脱铬前期也是以H+为主,故温度对其脱铬前期影响较大,而后期影响不大。其原因是因为随着温度的升高,苹果酸分子能量增加,苹果酸根对脱铬量的贡献增大,增加反应时间有利于增进苹果酸根与铬配位,但对提高苹果酸脱铬量的影响并不大。另外,因苹果酸根的螯合作用低于柠檬酸高于乳酸,所以后期其相对脱铬量高于乳酸而低于柠檬酸,可见,苹果酸脱铬适当提高温度、延长反应时间,可以增加脱铬量,而且对胶原水解影响不大。
综上所述,短时间内(<5 h),温度升高对三种酸的脱铬量的影响由大到小顺序为:乳酸>苹果酸>柠檬酸,长时间内(<24 h)的影响由大到小顺序为:柠檬酸>苹果酸>乳酸;而短时间内对胶原水解量的影响,由大到小顺序为:乳酸>苹果酸和柠檬酸,长时间内是柠檬酸>乳酸>苹果酸。即高温短时有利于低元羧酸脱铬,高温长时有利多元羧酸脱铬。
3 结论
(1)羧基数多,脱铬量少,胶原水解轻,脱铬液平衡pH低;脱铬量和胶原水解量由大到小顺序均为:一元羧酸>二元羧酸>三元羧酸。
(2)温度对三种酸的脱铬和胶原水解均有影响,对苹果酸脱铬的胶原水解影响较少,但对柠檬酸的脱铬和胶原水解影响较大;高温短时有利于低元羧酸脱铬,高温长时有利多元羧酸脱铬。
(3)胶原水解物对脱铬体系的pH值有缓冲作用,胶原水解物量越多,缓冲作用越强。
(4)苹果酸和乳酸反应前期以H+脱铬为主,柠檬酸脱铬与温度有关,低温脱铬以H+为主(25℃);高温以酸根为主(35~45℃)。
参考文献:
[1]马金辉,付丽红.有机酸脱铬机理的探讨[J].中国皮革,2007,36(17):23-28.
[2]Ammar Maleka,Messaoud Hachemi,Villemin Didier.New approach of depollution of solid chromium leather waste by the use of organic chelates[J]. Journal of Hazardous Materials,2009,(170):156-162.
[3]单志华.制革化学与工艺学(下册)[M].北京:科学出版社,2005:10-17.
[4]廖隆理.制革化学与工艺学(上册)[M].北京:科学出版社,2005:320.
[5]张业聪,付丽红.蓝湿革脱铬过程中纤维干热性能的研究 [J].中国皮革,2009,38(9):12-15.
[6]张业聪,付丽红.蓝湿皮脱铬过程中皮块湿热性能的变化 [J].中国皮革,2008,37(19):14-17.
[7]王希安,付丽红.蓝湿皮乳酸脱铬的研究[J].中国皮革,2009,38(1):14-17.
[8]田荟琳,付丽红.羟基对二元羧酸脱铬性能的影响 [J].中国皮革,2014,43 (5):19-24.
中图分类号:TS 513
文献标识码:A
文章编号:1671-1602(2016)07-0036-06
基金项目:国家级大学生创新创业训练计划(201510431025)
第一作者简介:杨春江(1993-),男,本科生。研究方向:胶原蛋白的改性与应用。
Study on the Influnence of Carboxyl Group on the Dechroming Performance of Hydroxy Acids
YANG Chun-jiang,TIAN Hui-lin,FU Li-hong*
(School of Leather Chemistry and Engineering,Qilu University of Technology,Jinan 250353,China)
Abstract:The effects of carboxyl group on the dechroming performance were studied according to the changes of pH values and the amounts of chrome complexes and hydrolyzed collagen proteins in the dechroming solutions while using lactic acid,malic acid and citric acid.The results showed that with the increase of carboxyl groups,both the amounts of dechroming and hydrolyzed collagen proteins decreased and the final equilibrium pH values reduced.The effect of steric hindrance decreased with the increase of temperature.At high temperature,the short-time processing benefited the dechroming performance of monocarboxylic acid and the long-term treatment facilitated the dechroming of polycarboxylic acid.While dechroming,H+has higher priority than lactic acid groups and malic acid groups at early stage of dechroming.As to citric acid,the reaction temperature had bigger positive impact on the dechroming and H+gave way to citric acid groups with the increase of temperature.The hydrolyzed collagen of dechroming solutions could constitute buffer system and the buffering effect was enhanced with the increase of amount of the hydrolyzed collagen.
Key words:lactic acid;malic acid;citric acid;dechroming performance;hydroxyl acid
*通信联系人:付丽红,E-mail:flh891006@163..com。

