膜化学强化反冲洗中副产物的生成及变化规律分析
张新波,李红霞,贾辉,温海涛,3(.天津城建大学 环境与市政工程学院,天津 300384;.天津凯英科技发展有限公司,天津 30007;3.天津工业大学 环境与化学工程学院,天津 300387;4.天津工业大学 省部共建分离膜与膜过程国家重点实验室,天津 300387)
膜化学强化反冲洗中副产物的生成及变化规律分析
张新波1,李红霞2,贾辉3,4,温海涛1,3
(1.天津城建大学 环境与市政工程学院,天津 300384;2.天津凯英科技发展有限公司,天津 300072;3.天津工业大学 环境与化学工程学院,天津 300387;4.天津工业大学 省部共建分离膜与膜过程国家重点实验室,天津 300387)
对混凝-超滤工艺在线化学强化反冲洗(chemically enhanced blackwash,CEB)过程中产生的副产物进行了分析,建立和优化了高效液相色谱质谱法(HPLC-MS/MS)测定反冲洗副产物中卤乙酸的分析方法.方法采用Zobax Plus Eclipse C8色谱柱,流速0.3 mL/min,进样量10 μL,R2均在99.9%以上,最小检出限为0.08 μg/L.在此基础上监测了CEB后24 h卤乙酸浓度的变化规律.结果表明:CEB过程中有清洗副产物卤乙酸的生成,且随着膜过滤出水时间的延长,大部分卤乙酸浓度逐渐降低.其中三氯乙酸生成量最高;其次为三溴乙酸.另外二溴乙酸浓度随时间无明显变化;二氯乙酸、三溴乙酸、一氯一溴乙酸和一氯二溴乙酸分别会在16、17、18、19 h达到浓度动态平衡.
超滤;化学强化反冲洗;副产物;卤乙酸;高效液相色谱质谱
由于环境污染的加剧以及居民日益增长的环境需求,膜处理技术快速发展,超滤膜在饮用水处理中应用日益增多[1-2].但是超滤膜经过较长时间的运行,膜表面和膜孔内就会积聚一定量的污染物质,这不仅导致膜运行效率的降低,同时也会缩短膜寿命,增加运行成本,所以就需要对膜组件进行清洗[3-4].化学强化反冲洗(chemically enhanced blackwash,CEB)是减缓膜污染的有效手段[5-6],但在CEB过程中,化学清洗药剂会与膜表面的污染物发生反应,生成化学强化反冲洗副产物(chemically enhanced blackwash by pro-ducts,CEBBPs),从而带来潜在的水质二次污染问题.化学清洗药剂常选用NaClO溶液[7-8],NaClO会与膜表面污染物产生具有三致作用的化学副产物,其中副产物种类较多的为挥发性卤代烃以及卤乙酸类有机化合物.挥发性卤代烃中三卤甲烷以及卤乙酸可对人体健康造成潜在危害.
张晓健等[9]通过实验研究发现,卤乙酸HAAs的致癌风险是三卤甲烷的11倍,总致癌风险的首要指标参数是卤乙酸.HAAs由于沸点高、不可吹脱、单位致癌风险远远高于THMs,引起美国EPA高度重视.目前美国EPA对以下5种进行了限定(HAA5):一氯乙酸、二氯乙酸、三氯乙酸、一溴乙酸和二溴乙酸,2000年后,饮用水中HAA5总量不得超过30 μg/L[10].我国最新颁布的《生活饮用水卫生标准》也规定了二氯乙酸和三氯乙酸的最高限量分别为50、100 μg/L[11].目前我国对其他HAAs类消毒副产物总量暂无限定标准.国外已发布的有关饮用水中HAAs的标准分析方法主要有美国环保局(EPA)和国际标准化组织的标准. EPA方法均采用气相色谱/电子捕获检测器测定,主要的差别是萃取的方法和衍生的条件不同.国际标准化组织(ISO)颁布的卤乙酸类化合物的测定方法为EN ISO23631-2006[12],GC-ECD或GC-MS检测.国内在2006年发布了饮用水中卤乙酸类化合物的测定标准,即GB/T5750.10-2006《生活饮用水标准检验方法消毒副产物指标》,该方法采用MTBE萃取、酸化甲醇衍生、GC-ECD测定,具有灵敏度高、准确性好等特点,但对一氯乙酸的灵敏度低.归结起来,饮用水中卤乙酸的分析方法主要有3类,分别是直接测定-离子色谱法(ion chromatogram,IC)、衍生化-气相色谱法(gas chromatogram electronic capture detector,GC-ECD),和衍生化-气相色谱/质谱法(gaschromato-grammass,GCMS).其中:离子色谱法测定时易受其他离子干扰,检测灵敏度低;衍生化-气相色谱法是最早使用检测饮用水中卤乙酸的方法,其前处理操作复杂;衍生化-气相色谱/质谱法的前处理及衍生步骤与衍生化-气相色谱法相同,与之相比具有干扰少、定性更准确的特点,但仪器设备昂贵、灵敏度较差.
与众多膜污染研究相比,对CEB过程的研究较少,CEB的调控以及潜在的二次污染和给饮用水处理带来的水质安全尚未引起关注,研究CEB过程有助于补充膜污染处理的理论内容,提高膜法饮用水水质安全保障,并对水厂的实际生产运行起到指导作用.因此本文用超高效液相色谱-质谱联用仪建立了CEBBPs中卤乙酸的检测方法,对CEB过程中产生的卤乙酸进行测定,并分析卤乙酸在CEB后膜出水中的变化规律.
1 实验部分
1.1实验材料与仪器
材料:本实验采用的超滤膜为中空纤维膜,天津膜天膜科技有限公司研制,膜材质为聚偏氟乙烯(PVDF),压力类型为外压式,膜通量为10~70 L/(m2· h),公称孔径为0.02 μm,膜丝内径为0.65 mm,膜丝外径为1.20 mm.
仪器:TURBO550便携式浊度计,德国WTW公司产品;TOC-Vcph总有机碳分析仪,日本岛津公司产品;TU-1810紫外可见分光光度计,北京谱元仪器有限公司产品;HQ40d pH计,美国HACH公司产品;Agilent 1200/6410高效液相色谱-质谱联用仪,美国安捷伦公司产品.
联用仪包括:Agilent MassHunter质谱数据软件系统、Agilent 1200高效液相色谱系统,带有自动进样器、二元泵系统以及柱温箱等;Agilent 6410B三重串联四极杆质谱系统;液相色谱柱采用Zorbax Eclipse Plus(3.5 μm,2.1 mm×100 mm)的C8分析柱.
1.2实验试剂
混凝剂硫酸铝Al2(SO4)3·18H2O,天津市北海科贸发展有限公司产品;化学清洗药剂次氯酸钠NaClO,天津市北海科贸发展有限公司产品;甲醇与乙腈,色谱纯,美国Fisher公司产品;CNW甲酸,上海安谱科学仪器有限公司产品;9种卤乙酸混合标准溶液分别是二溴乙酸质量浓度为20 mg/L,一溴乙酸、一氯一溴乙酸、一溴二氯乙酸质量浓度为40 mg/L,一氯乙酸、二氯乙酸、三氯乙酸质量浓度为60 mg/L,一氯二溴乙酸质量浓度为100 mg/L,三溴乙酸质量浓度为2 000 mg/ L,内标为2,2-二氯丙酸,质量浓度为60 mg/L,替代物为2,3-二溴丙酸,质量浓度为60 mg/L;卤乙酸标准品,百灵威科技公司产品.9种卤乙酸的化合物性质如表1所示.
1.3实验装置
图1所示为混凝-超滤系统实验装置示意图.图1中,进水箱中原水以及加药箱中混凝剂药液通过原水泵的抽吸作用进入混凝水箱,并通过调节2个水箱前管道上的流量计控制进入混凝水箱中的原水流量以及混凝剂药液流量.混凝水箱内设置搅拌器对混合液进行搅拌,经过絮凝后的原水直接进入超滤膜(UF)反应器.UF组件对反应器中原水进行膜过滤,在抽吸泵的作用下,过滤出水进入出水箱,流量计控制膜出水流量.清洗药剂箱中的反洗药剂与出水箱的出水在反洗泵的作用下进入UF膜组件,反洗曝气泵同时对膜进行曝气,实现膜在线化学强化反洗.系统通过压力传感器、液位计实现自控.可编程逻辑控制器可对阀门a、阀门b、阀门c、阀门d、原水泵、抽吸泵、反洗曝气泵和液位计进行控制,并且对压力传感器输出的信号进行记录.当压力传感器监测到UF膜组件运行时跨膜压差大于30 kPa时,装置将停止运行,对UF进行一次离线反洗,同时对UF反应器进行彻底清洗,废水和底泥通过阀门e排入回流调节池中.
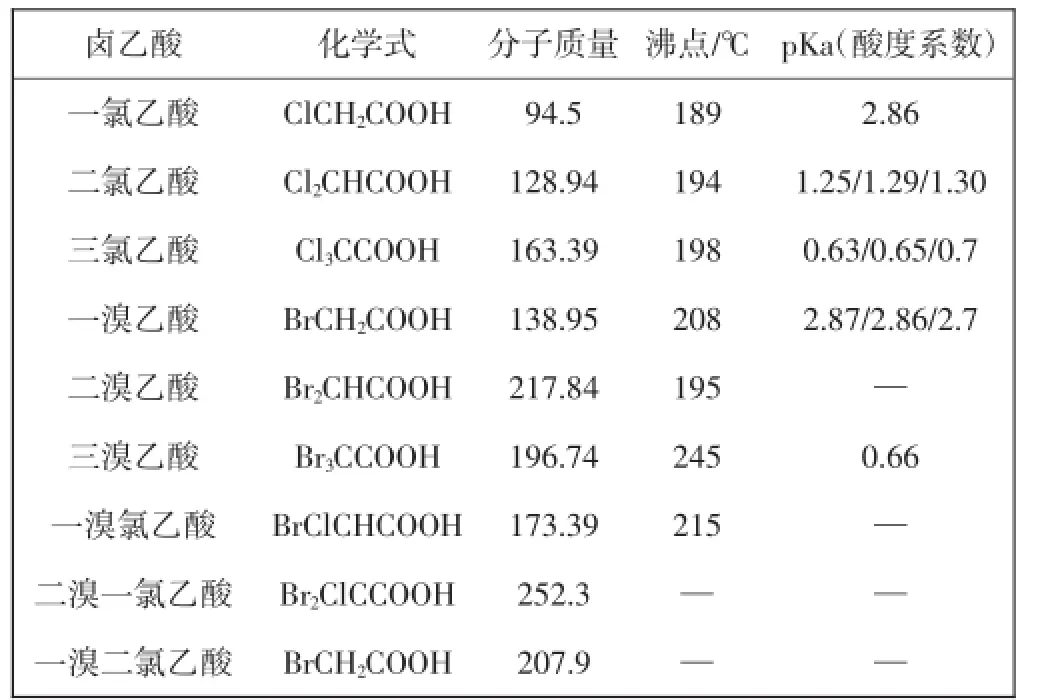
表1 卤乙酸类化合物的性质Tab.1 Characters of HAA9
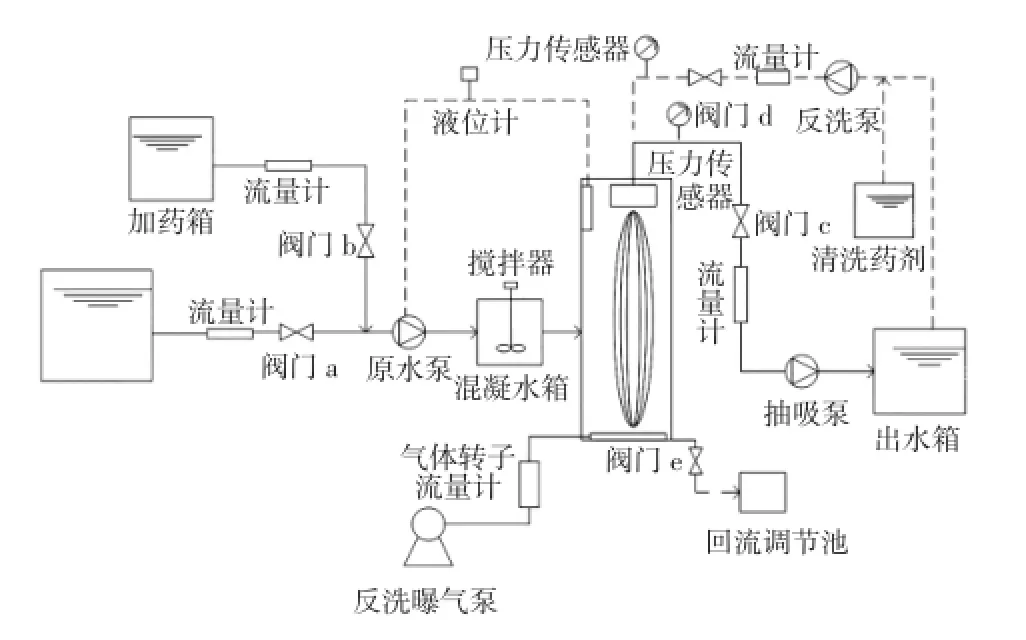
图1 中试混凝-超滤处理工艺实验装置示意图Fig.1 Diagram of coagulation-ultrafiltration process
1.4实验方法
实验用水取自天津市芥园水厂原水,其浊度为(2.52±0.92)NTU,DOC为(3.52±1.51)mg/L,UV254为(0.187±0.009)cm-1,pH为7.1~7.3.本实验中投加的混凝剂浓度为0.06 mmol/L;次氯酸钠投加浓度为25 mg/L;反洗时间为10 min;反洗周期为30 min;反洗流量为40 L/(m2·h).
采用高效液相色谱-质谱联用仪测定水样中9种卤乙酸含量,其中质谱条件与参数为:干燥气温度300℃,干燥气流量6 L/min,雾化器压力40 psi,鞘流气温度350℃,鞘流气气流量11 L/min,离子源温度为100℃,去溶剂气温度为350℃,实验中使用的氮气均为高纯氮气,流速为9.0 L/min,毛细管电压为-1 500 V.液相色谱条件为甲醇和乙腈混合液作为流动相的有机相,二者比例为1∶1;实验中采用甲酸溶液作为无机相,甲酸质量分数为1%.
实验针对液相色谱-质谱联用中的毛细管电压、碎裂电压、碰撞能、进样量、流速、梯度洗脱等条件进行了优化.实验时每批样品至少做一个实验空白,至少做10%的平行样品以保证质量.根据建立和优化后的卤乙酸检测方法,对CEB过程中产生的卤乙酸进行测定,并分析其在膜出水中的变化.
2 结果与讨论
2.1卤乙酸检测的液相色谱-质谱参数优化
卤乙酸极性较强且容易脱氢,故采用负离子喷雾模式.此条件下对混标溶液进行了全扫,其中二氯乙酸、一溴二氯乙酸等物质出峰效果较好,优化过程以二氯乙酸为指示物质.接下来,在SIM扫描条件下对碎裂电压进行了优化.
在子离子扫描模式下寻找各物质子离子并对碰撞能进行优化,最终优化结果如表2所示.
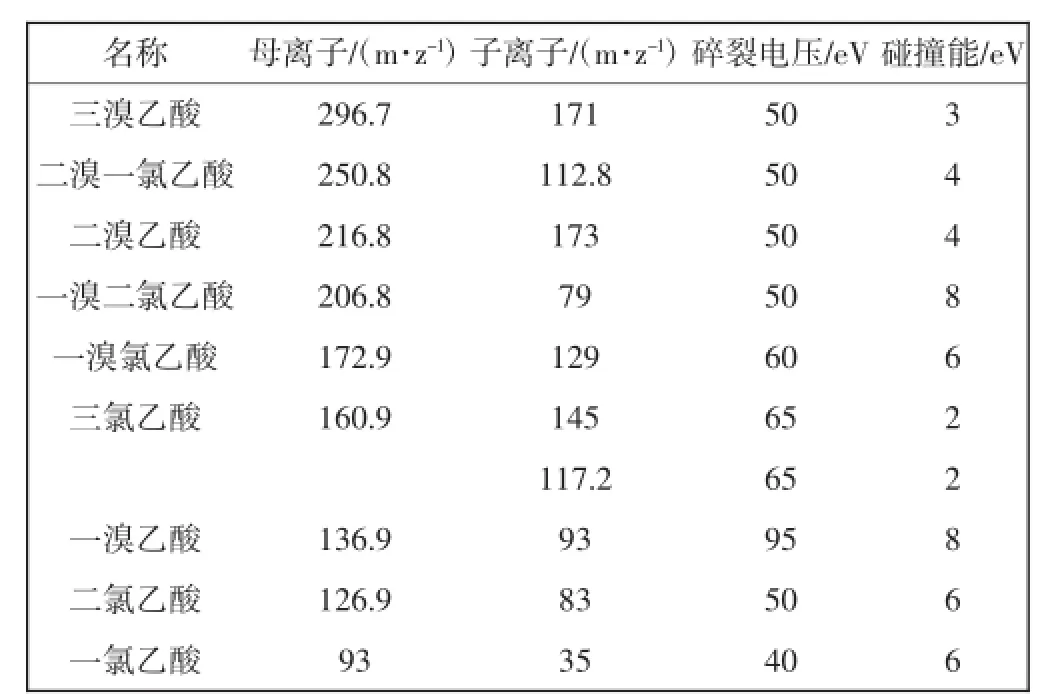
表2 各物质液相色谱参数优化结果Tab.2 Liquid chromatographic parameters of HAA9
实验对10 μL、15 μL、20 μL 3种不同的进样量进行了优化,理论上进样量越大,出峰效果越好,但是随着进样量增大,清洗难度也增大.最后在保证出峰效果的前提下选择进样量为10 μL.流速方面,主要选择了0.2 mL/min、0.3 mL/min 2种条件进行了出峰效果的对比,最终选择0.3 mL/min作为最终流速.由于各物质均在5 min内出峰完毕,故梯度洗脱程序主要在0~6 min进行了优化,有机相比例在5%~100%范围,对比了十几种方案的洗脱结果,最终选择的梯度洗脱方案为:0~1 min,5%;1~3 min,5%~30%;3~4.5 min,30%~100%,4.5~5.5 min,100%;5.5~6.5 min,100%~5%.
2.2方法评价
9种卤乙酸的标准曲线方程、R2、检出限、相对标准偏差等数值如表3所示.
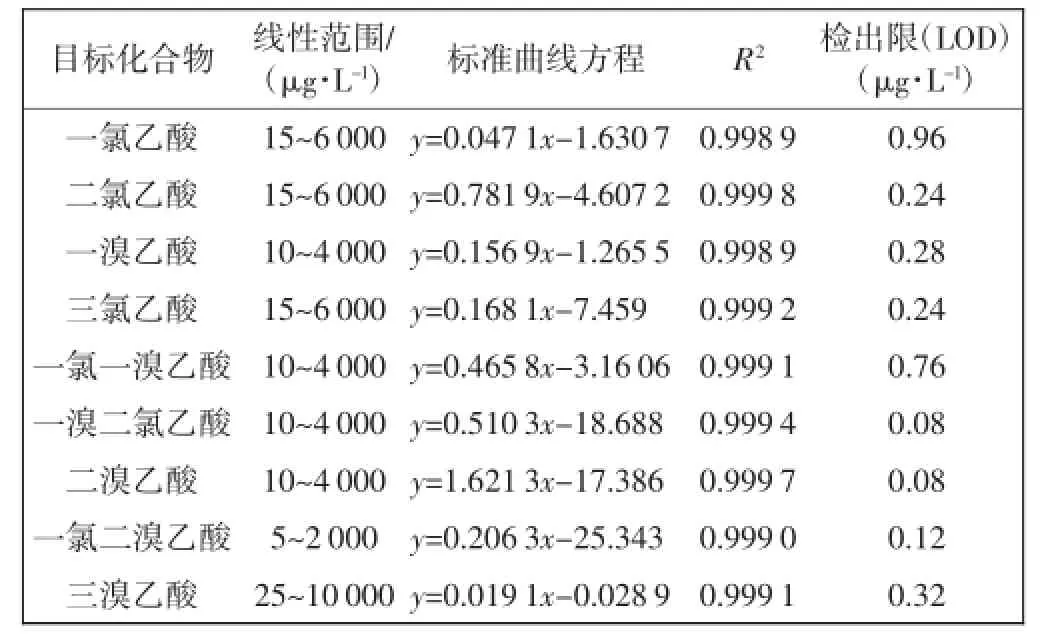
表3 各物质标准曲线及检出限Tab.3 Standard curve and detection limit of HAA9
由表3可以看出,9种卤乙酸的标准曲线方程相关系数均大于0.99,线性相关性好,满足要求.本方法对单个样品的分子时间仅为6 min,较之其他方法明显提高了分析速度和工作效率[13-14];与EPA推荐的方法[15-16]相比,本方法无需衍生化,节省了实验试剂用量;与液相色谱相比,减少了流动相损耗.由于本方法建立在安捷伦6 400基础上,检测限达到了0.08~0.96 μg/L,实现了低浓度快速准确定量检测.
2.3CEB后膜出水中卤乙酸的变化规律
化学清洗前膜出水和清洗后膜过滤0~24 h出水所有卤乙酸含量的变化情况如表4所示.
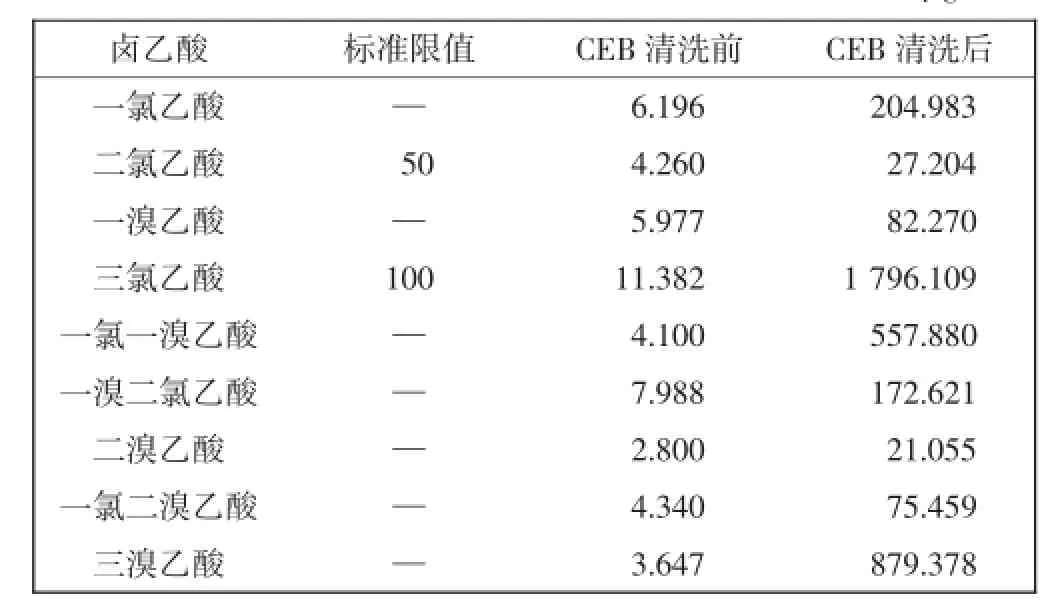
表49 种卤乙酸的出水质量浓度Tab.4 Concentration of HAA9in water after ultrafiltrationμg/L
由表4可见,虽然清洗前原水中含有一定浓度的卤乙酸,但其浓度水平较低,在2.8~11.382 μg/L之间,远低于《生活饮用水卫生标准》(GB5749-2006)规定的标准限值.经膜化学强化反冲洗后9种卤乙酸浓度都有明显变化,二氯乙酸倍数为6.38倍,变化最小;变化最大的是三氯乙酸,由此前的11.382 μg/L上升至1 796.109 μg/L,增长了157倍之多,远高于标准限值.
9种卤乙酸24 h膜出水中的浓度变化情况如图2所示,取样间隔为1 h.
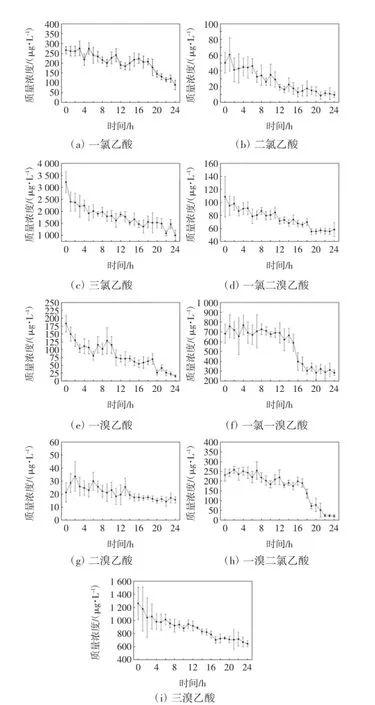
图29 种卤乙酸24 h浓度变化情况Fig.2 Concentration variety of HAA9in water after ultrafiltration during 24 h
由图2可见,一氯乙酸出水0 h质量浓度为240 μg/L,在0~17 h期间浓度下降速率较低,且有反弹现象出现.以17 h为转折点,在之后7 h内,浓度下降明显,从208 μg/L下降至80 μg/L,取样结束时并未达到平衡状态,推测在之后的时间里浓度会持续降低.二氯乙酸出水起始质量浓度较低为51 μg/L,至16 h达到浓度动态平衡,质量浓度在12 μg/L左右,因此对于二氯乙酸来讲最佳取水时间为出水16 h后.三氯乙酸起始浓度较二氯乙酸高出2个数量级,24 h内浓度降低明显,降幅达到69%.但其质量浓度仍保持在1 000 μg/L以上.同时三氯乙酸属致癌率较高的物质,大浓度的残留无疑增加了致癌风险.一溴乙酸的起始浓度与一氯乙酸相近,但其降幅却高于一氯乙酸,24 h后质量浓度变为12 μg/L,93%以上的一溴乙酸被去除.二溴乙酸浓度随时间无明显变化,在前12 h略有波动,之后稳定在18 μg/L.三溴乙酸虽不及三氯乙酸的浓度大,但也维持在3个数量级,整体下降趋势明显,17 h之后达到动态平衡,质量浓度保持在700 μg/L上下.一氯二溴乙酸、一氯一溴乙酸、一溴二氯乙酸在9种卤乙酸中致癌风险不及其他几种.一氯二溴乙酸虽降幅不明显,但均维持在较低浓度水平.一氯一溴乙酸虽起始浓度较高,但变化明显,18 h后达到平衡,平衡时质量浓度为250 μg/L.一氯二溴乙酸的变化明显分为2个阶段,19 h后达到动态平衡,质量浓度为20 μg/L.
9种卤乙酸24 h总浓度变化情况如图3表示.
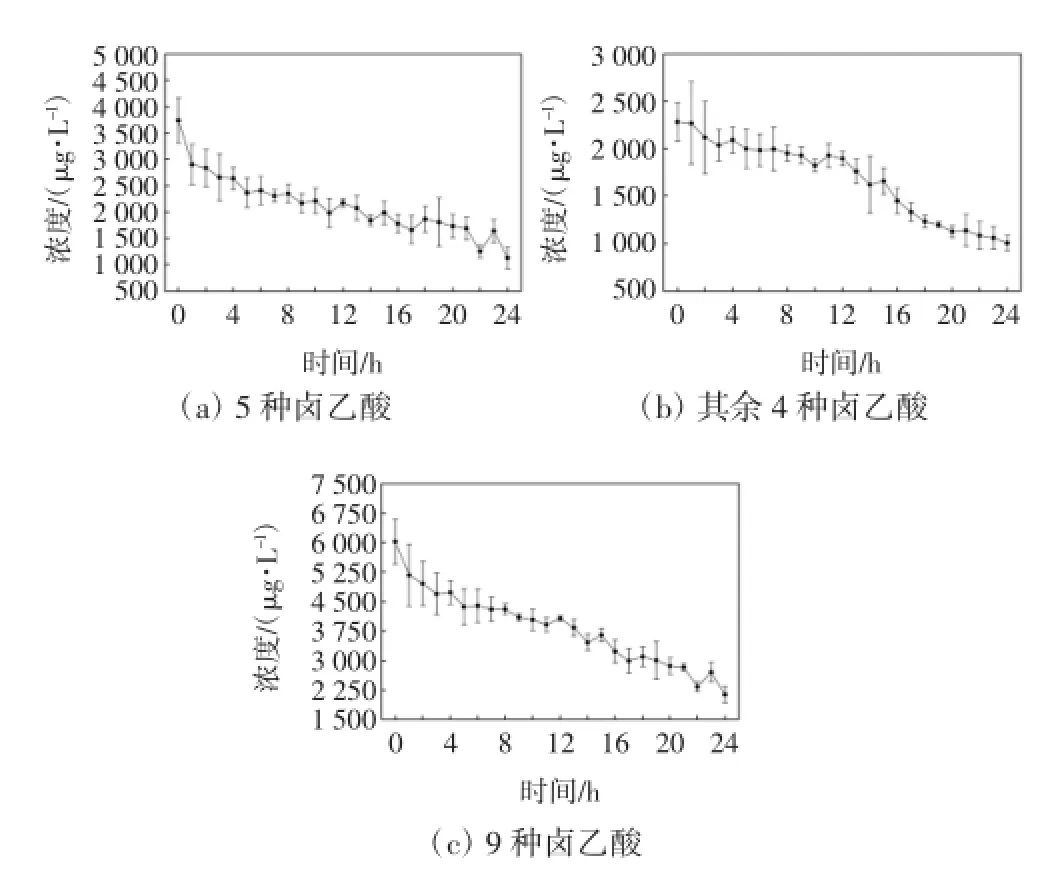
图39 种卤乙酸24 h总浓度变化情况Fig.3 Concentration variety of HAA9in water after ultrafiltration during 24 h
由图3可以看出,在膜过滤0 h出水卤乙酸的总质量浓度达到了约6 000 μg/L,随着出水时间的延长,总浓度基本呈线性降低,最终达到2 000 μg/L.HAA5是卤乙酸类化学物中最受关注的5种物质,也同时被认为是致癌风险最大的5种.从图3可以看出,HAA5占卤乙酸总量50%~60%左右,而其他4种物质占总量的40%~50%.
3 结论
(1)建立和优化了HPLC-MS/MS分析检测膜化学强化反冲洗副产物中卤乙酸的方法,实现了9种卤乙酸完全分离.标准曲线方程相关系数均大于0.99,线性相关性好;检出限和相对标准偏差均较低,准确度高、稳定性好;所有物质的加标回收率在80%~120%之间,满足实验的要求.本方法对单个样品的分子时间仅为6 min,可以大大提高分析速度和工作效率.
(2)CEB后24 h卤乙酸浓度变化规律表明:随着膜过滤出水时间的延长,其浓度逐渐降低.其中HAA5占卤乙酸总量50%~60%左右,而其他4种物质占总量的40%~50%.根据CEB后卤乙酸24 h浓度变化规律,可以对CEB过程中的反洗参数进行调控,既达到膜通量恢复的效果,又减少副产物生成,保证膜出水水质.
[1]刘利,方佩晖.超滤技术用于饮用水处理领域案例分析[J].中国给水排水,2009,25(24):72-75.
LIU L,FANG P H.Case analysis on application of ultrafiltration technology to drinking water treatment[J].China Water and Wastewater,2009,25(24):72-75(in Chinese).
[2]田宝义.超滤膜处理滦河水工艺研究[D].西安:西安建筑科技大学,2010.
TIAN B Y.Study on ultrafiltration process for luan river water treatment[D].Xi′an:Xi′an University of Architecture and Technology,2010(in Chinese).
[3]刘婷.三种预处理技术对超滤膜污染的影响及其机理研究[D].哈尔滨:哈尔滨工业大学,2011.
LIU T.Effect of three pretreatment methods on fouling of ultrafiltration membrane and involved mechanisms[D].Harbin:Harbin Institute of Technology,2011(in Chinese).
[4]JANG N Y,WATANABE Y,MINEGISHI S.Performance of ultrafiltration membrane process combined with coagulation and sedimentation[J].Water Science and Technology,2005,51(6/7):209-219.
[5]朱建文,顾渊,代荣.饮用水深度处理中膜清洗方式的研究[J].中国给水排水,2009,25(23):41-44.
ZHU J W,GU Y,DAI R.Research on cleaning of membraneusedin advanced water treatment[J].China Water and Wastewater,2009,25(23):41-44(in Chinese).
[6] PORCELLI N,JUDD S.Chemical cleaning of potable water membranes:A review[J].Separation and Purification Technology,2010,71(2):137-143.
[7]ZONDERVAN E,ROFFEL B.Evaluation of different cleaning agents used for cleaning ultra filtration membranes fouled by surface water[J].J Membrane Science,2007,304(1/2):40-49.
[8] KIMURA K,HANE Y,WATANABE Y,et al.Irreversible membrane fouling during ultrafiltration of surface water[J].Water Research,2004,38:3431-3441.
[9]张晓健,李爽.消毒副产物总致癌风险的首要指标参数-卤乙酸[J].给水排水,2000,26(8):1-6.
ZHANG X J,LI S.Halo-acetic acids as an indicator of the total carcinogentic risk of disinfection by-products[J].Water and Wastewater Engineering,2000,26(8):1-6(in Chinese).
[10]赵玉丽,李杏放.饮用水消毒副产物:化学特征与毒性[J].环境化学,2011,30(1):20-33.
ZHAO Y L,LI X F.Drinking water disinfection bypro-ducts chemical characterization and toxicity[J].Environment Chemistry,2011,30(1):20-33(in Chinese).
[11]中华人民共和国卫生部,国家标准化管理委员会.GB5749-2006生活饮用水卫生标准[S].北京:中国标准出版社,2006.
Ministry of Health,P.R.China and Standardization Administration of China.GB5749-2006 Standards for Drinking Water Quality[S].Beijing:Standards Press of China,2006(in Chinese).
[12]DIN-adopted European-adopted ISO Standard.Water quality-Determination of dalapon,trichloroacetic acid and selected haloacetic acids-Method using gas chromatography(GC-ECD and/or GC-MS detection)after liquid-liquid ex-traction and derivatization(EN ISO23631:2006)[S].Germany:Beuth Verlag,2006.
[13]刘艳,饶竹,路国慧,等.饮用水中9种卤乙酸的超高效液相色谱法测定[J].分析测试学报,2011,30(3):248-253.
LIU Y,RAO Z,LU G H,et al.Determination of ha-loacetic acids in drinking water using ultra performance liquid chromatography coupled with solid-phase extraction[J].Journal of Instrumental Analysis,2011,30(3):248-253(in Chinese).
[14]李建中,陈伟,薄涛,等.生活饮用水中消毒副产物卤乙酸的UHPLC-MS/MMS分析[J].环境化学,2012,31(5):757-759.
LI J Z,CHEN W,BO T,et al.Analysis of halo-acetic acids in drinking water using UHPLC-MS/MS[J].Environment Chemistry,2012,31(5):757-759(in Chinese).
[15]HODGESON J W,BECKER D.Method 552.1,Determination of haloacctic acid and dalapon in drinking water by ion-exchange liquid-solid extraction and gas chromatography with an electron capture detector[S].New York:Environmental Protection Agency,1992.
[16]MUNCH D J,MUNCH J W,PAWLECKI A M,et a1.Method 552.2,Determination of halo acetic acid and dalapon in drinking water by liquid-liquid extraction,derivitization and gas chromatography with electron capture detection[S].New York:Environmental Protection Agency,1995.
Determination and variety of by products during chemically enhanced blackwash
ZHANG Xin-bo1,LI Hong-xia2,JIA Hui3,4,WEN Hai-tao1,3
(1.School of Environmental and Municipal Engineering,Tianjin Chengjian University,Tianjin 300384,China;2.Tianjin Caring Technology Development Co Ltd,Tianjin 300072,China;3.School of Environmental and Chemical Engineering,Tianjin Polytechnic University,Tianjin 300387,China;4.State Key Laboratory of Seperation Membranes and Membrane Processes,Tianjin Polytechnic University,Tianjin 300387,China)
The by products during chemically enhanced blackwash(CEB)in coagulation ultrafiltration process was analyzed.The method for the determination of haloacetic acids(HAAs)was developed with high-performance and ultra-performance liquid chromatography tandem mass spectrometry.HAAs were separated on an Zobax Plus Eclipse C8 chromatography,column with the injection volume of 10 μL and flow rate of 0.3 mL/min.The correlation coefficients of the calibration curves were greater than 99.9%,and the minimum limits of detections were 0.08 μg/L.The variety of by products(HAAs)during 24 h after CEB showed that HAAs were produced during CEB and the concentration of most HAAs decreased gradually.Among them,trichloroacetic acid was the highest followed by tribromoacetic acid.In addition,dibromoacetic acid did not change obviously,and dichloroacetic acid,tribromoacetic acid,bromodichloroacetic acid and dibromochloroacetic acid reached steady at 16,17,18 and 19 h respectively.
ultrafiltration process;chemically enhanced blackwash;by product;HAAs;HPLC-MS/MS
TS102.54
A
1671-024X(2016)03-0060-06
10.3969/j.issn.1671-024x.2016.03.012
2015-12-21
国家自然科学基金资助项目(51308373);天津市优秀青年教师资助计划(03010601).
张新波(1978—),女,环境工程博士,副教授,主要研究方向为水污染控制技术.E-mail:zxbcj2006@126.com

