基于手性金纳米粒子圆二色光谱法识别与检测银离子
韦克毅,王 猛,杜 宇,蔡 波,江云宝
(1.云南中烟工业有限责任公司技术中心,云南昆明650231;2.厦门大学化学化工学院,福建厦门361005)
·研究简报·
基于手性金纳米粒子圆二色光谱法识别与检测银离子
韦克毅1,2,王猛1,杜宇1,蔡波1,江云宝2*
(1.云南中烟工业有限责任公司技术中心,云南昆明650231;2.厦门大学化学化工学院,福建厦门361005)
摘要:采用液相制备方法获得具有光学活性的手性金纳米粒子,通过吸收光谱和圆二色光谱及高分辨透射电镜对手性金纳米粒子进行表征.利用圆二色光谱法建立手性金纳米粒子对Ag+选择性识别方法,结果表明手性金纳米粒子对Ag+响应时间仅需12 min,手性金纳米粒子能够从13种常见金属离子中选择性识别Ag+,并对多种常见金属离子具有较好的抗干扰能力,检测灵敏度高并且具有良好的重现性.所建立标准曲线线性范围为0.2~30 μmol/L,线性相关系数R2=0.995(n=15),Ag+的检测限为0.2 μmol/L;为环境水样中Ag+的识别和检测提供了一种简单、精确、快速、环境友好的新方法.
关键词:手性金纳米粒子;圆二色光谱;识别;检测;Ag+
Ag+对细菌、病毒、水藻和真菌等有较强的毒性,被用于医疗器材和消毒剂等领域.每年平均有约2 500 t的银随工业废弃物排放进入环境中,其中约150 t进入了土壤,对植物产生严重的危害,而约80 t进入地表水体中[1-2].Ag+与Cr3+、Cd2+、Cu2+和Hg2+一起被认为是毒性最强的一类物质,其毒性仅次于Hg2+.研究表明Ag+是对水生物毒性最强的离子之一,例如:对广泛研究的淡水鱼——彩虹鳟鱼,Ag+通过抑制鱼鳃上皮细胞中Na+和K+-ATP酶对Na+和Cl-的摄入,引起离子传输的紊乱,造成心血管崩溃,最终导致鱼类的死亡[1,3-5].因此,建立高选择性、高灵敏度的Ag+识别和检测方法对环境监测具有重要意义.
圆二色光谱(circular dichroism spectrum,CD光谱)是用于推断手性分子或粒子的构型和构象的一种旋光光谱,具有快速、简单和准确的特点,常用于研究手性金纳米粒子的微观结构和手性来源[6-8].在实际应用中,主要是利用手性金纳米粒子吸收光谱[3]和荧光光谱[5]的性质,对手性金纳米粒子CD光谱性质的实际应用鲜有报道.本研究将手性金纳米粒子的CD光谱信号的变化与Ag+的浓度相关联,既拓展了金纳米粒子的应用范围[9-10],又对Ag+的识别与检测提供了新的方法.
1实验部分
1.1仪器与试剂
紫外-可见吸收光谱在Thermo Evolution 分光光度计上测试.CD光谱在JASCO J-810旋光光谱仪上测试,扫描速率为500 nm/min,光栅狭缝为2 nm.光谱测绘采用1 cm石英液池.高分辨透射电镜(TEM)加速电压为300 kV.
三水合氯金酸、羧甲基纤维素钠、巯基乙胺盐酸盐购自阿拉丁试剂公司,氯化汞、硝酸银、氯化钠、氯化钾、氯化锌、氯化钙、氯化镉、硝酸铅、氯化镍、氯化钡、氯化铁、七水合硫酸亚铁、氯化铜、硫酸锰、硝酸钴、氯化镁和氯化铬购自上海化学试剂公司,实验中涉及的其他化学药品及试剂购自上海国药试剂公司,以上试剂均为分析纯.实验用水为超纯水.
1.2手性金纳米粒子的制备
取1.00 g羧甲基纤维素钠溶解于400 mL水中,搅拌6 h,静置待用.取1.36 g巯基乙胺盐酸盐溶解于400 mL水中,用1 mol/L NaOH溶液调节pH值至近中性,待用.将上述羧甲基纤维素钠和巯基乙胺溶液分别用六次甲基四胺盐酸缓冲液(5 mmol/L,pH 4.0)稀释10倍后等体积混合,搅拌10 min后加入等体积0.5 mmol/L氯金酸溶液继续搅拌30 min,静置陈化2 h即得手性金纳米粒子储备液,待用.
1.3实验方法

图1 手性金纳米粒子的吸收光谱和CD光谱(a)、TEM图(b)及粒径分布图(c)Fig.1Absorption spectra and CD spectra(a),TEM images(b) and size distributions(c) of chiral gold nanoparticles
手性金纳米粒子对Ag+的选择性实验:分别取1 mL手性金纳米粒子储备液,分别加入1 mL一定浓度的金属离子,用六次甲基四胺盐酸缓冲液分别定容至10 mL,摇匀稳定后测定其CD光谱.
共存离子干扰实验:取1 mL手性金纳米粒子储备液,加入1 mL 10 mmol/L的乙二胺四乙酸(EDTA)溶液和1 mL 100 μmol/L Ag+,分别加入1 mL一定浓度的金属离子,用六次甲基四胺盐酸缓冲液分别定容至10 mL,摇匀稳定后测定其CD光谱.
标准曲线实验:分别取1 mL手性金钠米粒子储备液,各加入1 mL 10 mmol/L的EDTA溶液和1 mL一定浓度的Ag+,用六次甲基四胺盐酸缓冲液分别定容至10 mL,摇匀稳定后测定其CD光谱.
2结果与讨论
2.1手性金纳米粒子的吸收光谱、CD光谱及TEM表征
图1为所合成的手性金纳米粒子的吸收光谱、CD光谱、TEM图和粒径分布图.吸收光谱和CD光谱(图1(a))在230 nm附近有最大吸收峰,说明所合成的金纳米粒子粒径小于常规合成方法[11-12],手性光学活性很强达到0.24°.从TEM图像中可以看出大部分金纳米粒子大小均一,单分散性较好(图1(b)).随机选取100个金纳米粒子进行粒径统计分析,获得金纳米粒子的粒径为(3.6±0.5) nm,其粒径分布如图1(c)所示.
2.2手性金纳米粒子对Ag+的响应时间
图2为手性金纳米粒子溶液中加入10 μmol/L Ag+后,在0,0.5,1.0,3.0,4.0,6.0,7.5,10,11,14,15,20,25 min时的CD光谱和在230 nm处CD光谱强度的猝灭图.从图中可以看出,手性金纳米粒子的CD光谱强度随着Ag+的加入迅速下降最终趋于稳定,稳定时间为12 min.从响应时间的角度考虑,该方法可以应用于Ag+的快速识别与检测.
2.3手性金纳米粒子对Ag+识别的选择性
为了考察手性金纳米粒子对Ag+的选择性,还分别测定了12种其他常见金属离子(Ca2+、Mg2+、 Co2+、Cd2+、Hg2+、Zn2+、K+、Na+、Ba2+、Cu2+、Fe3+、Pb2+)存在下手性金纳米粒子CD光谱强度的变化情况.如图3所示:仅10 μmol/L Ag+能引起(ICD0-ICD)/ICD0的显著增大;其他离子,包括200 μmol/L Fe3+、Pb2+、Cu2+、Co2+、Hg2+和1 mmol/L Ca2+、Mg2+、Cd2+、Zn2+、K+、Na+、Ba2+,均未使(ICD0-ICD)/ICD0发生显著增大.实验结果表明,本方法对水溶液中的Ag+识别具有较好的选择性.
2.4共存离子干扰
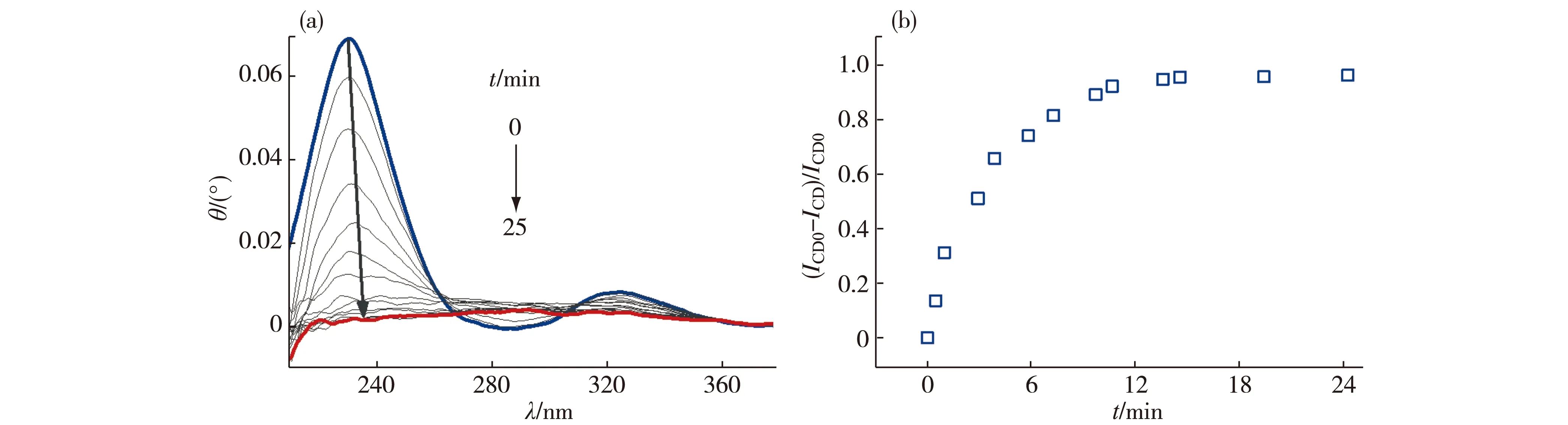
(ICD0-ICD)/ICD0 表示Ag+对手性金纳米粒子的CD光谱强度猝灭,其中ICD0 表示未加Ag+时的 CD光谱强度,ICD表示加入Ag+后的CD光谱强度,下同.图2 手性金纳米粒子溶液加入Ag+后CD光谱图(a)和CD光谱强度猝灭图(b)Fig.2The response of CD spectra(a) and CD spectral intensity quenching diagram(b) for chiral gold nanoparticles to Ag+

Fe3+、Pb2+、Cu2+、Co2+、Hg2+的浓度均为200 μmol/L; Ca2+、Mg2+、Cd2+、Zn2+、K+、Na+、Ba2+的浓度均为 1 mmol/L;Ag+浓度为10 μmol/L;CK为空白对照.图3 手性金纳米粒子的离子识别选择性Fig.3Selectivity on the ion recognition of chiral gold nanoparticles
离子识别与检测的抗干扰性,体现在当环境样品中有其他离子与目标离子共存时,目标离子的识别与检测不受其他离子干扰.如图4所示,本研究考察了常见金属离子和Ag+共存时,手性金纳米粒子的CD光谱强度猝灭响应的竞争实验.其中Ag+浓度为10 μmol/L,Fe3+、Pb2+、Hg2+和Cr3+的浓度是Ag+的4倍;Cd2+、Cu2+、Co2+、Fe2+和Ni2+浓度是Ag+的10倍;Ba2+、Ca2+、Mg2+、Mn2+和Zn2+浓度是Ag+的20倍.结果表明,上述离子与Ag+共存时对Ag+的识别与检测没有明显干扰,手性金纳米粒子CD光谱法应用于Ag+的识别与检测具有良好的抗干扰性.

Ag+浓度为10 μmol/L;Fe3+、Pb2+、Cr3+、Hg2+的浓度均为 40 μmol/L;Cd2+、Cu2+、Fe2+、Co2+、Ni2+浓度均为100 μmol/L; Zn2+、Ba2+、Ca2+、Mg2+、Mn2+浓度均为200 μmol/L.图4 Ag+识别与检测的抗干扰性Fig.4Anti-interference study of Ag+identification and detection
手性金纳米粒子的手性来源于配体的协同作用和Au…Au亲金属相互作用引起的金纳米粒子螺旋排布.手性金纳米粒子能够选择性识别众多金属离子中的Ag+,其中有3个原因:1) Ag+和硫醇(HSR)的稳定常数远高于除Hg2+外的绝大部分金属离子,2) Ag+和EDTA的稳定常数远小于绝大部分的金属离子(表1),3) Ag+和Au可以形成亲金属相互作用.因此,Ag+的识别机理如图5所示:当加入Ag+时EDTA几乎不起作用,Ag+和Au竞争与HSR相互作用并和Au形成亲金属相互作用破坏原来金纳米粒子的螺旋排布导致CD光谱强度下降;而加入其他金属离子时,Pb2+、Cu2+、Fe3+和Cd2+和EDTA发生螯合反应而减小干扰,其他金属离子则不会影响手性金纳米粒子的螺旋排布,CD光谱强度没有明显的变化.
2.5Ag+的定量检测
利用手性金纳米粒子在230 nm处的CD光谱强度猝灭值((ICD0-ICD)/ICD0)对Ag+浓度作图,通过线性拟合得到标准曲线(图6),线性范围为0.2~30 μmol/L,线性相关系数R2=0.995(n=15).方法检测限
表1 金属离子在pH 4.0时和HSR及EDTA的稳定常数
Tab.1 Stability constants(pKsp) of metal ions with HSR or EDTA in solution of pH 4.0

配体金属离子与配体稳定常数pKspAg+Fe3+Pb2+Cu2+Co2+Hg2+Ba2+Ca2+Cd2+Mg2+Mn2+Ni2+Zn2+HSR48.727.935.224.752.426.112.725.721.7EDTA0.714.79.410.27.811.3<1.3<2.26.0<2.15.510.17.9
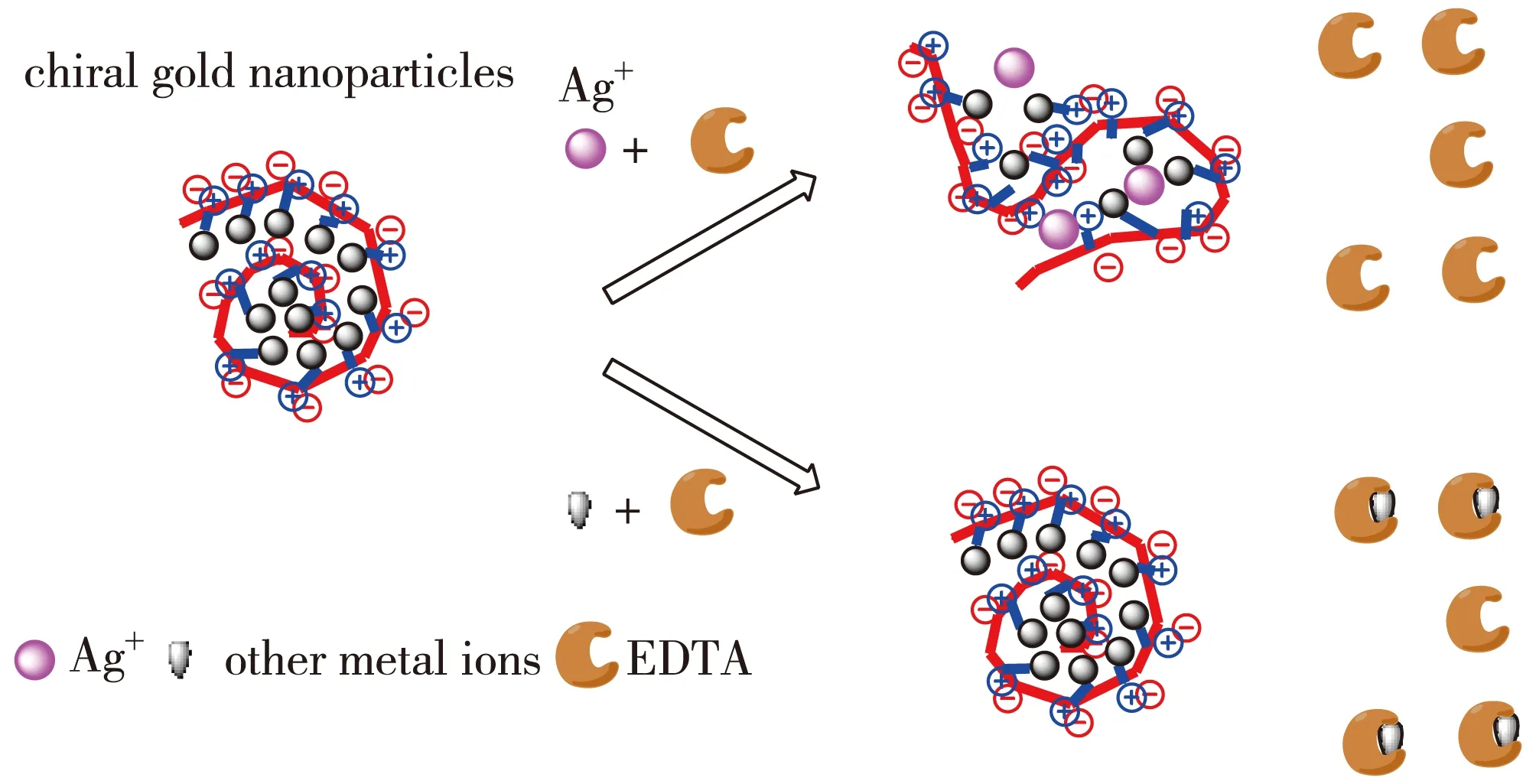
图5 手性金纳米粒子识别Ag+示意图Fig.5Schematic illustration of the chiral sensor for Ag+ based on chiral gold nanoparticles
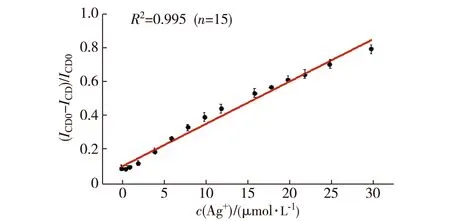
图6 Ag+检测的标准曲线Fig.6Standard curve for Ag+ detection
(3σ/K)[7]为0.2 μmol/L.本方法与文献[13]报道的荧光猝灭法相比,Ag+的检测线性范围更宽,检测限更低;与文献[14]报道的离子选择性电极法相比,Ag+的检测线性范围相近,检测限更低.
2.6实际样品的检测
采集了昆明市附近两处湖水和当地自来水样品,对3种实际环境水样中的Ag+进行了检测,均未检出Ag+.对实际水样进行了Ag+的加标回收实验,结果如表2所示,当加入的Ag+在4~15 μmol/L时,Ag+平均回收率在92%~104%之间,相对标准偏差(RSD)均不高于3.6%(n=3).根据《生活饮用水卫生标准》[15]规定,饮用水中Ag+的限量为0.05 mg/L(0.463 μmol/L),因此本研究所提出的检测方法满足国家限量标准的要求,可用于实际水样中Ag+的检测.

表2 实际水样中的加标回收实验结果Tab.2 Recovery of spiked Ag+ in natural water samples
3结论
本研究利用手性金纳米粒子的CD光谱对Ag+进行选择性识别和检测.实验结果表明手性金纳米粒子探针对Ag+响应时间短,具有很好的选择性和抗干扰能力,检测灵敏度高并且具有良好的重现性.在本实验条件下建立的Ag+检测标准曲线,线性范围为0.2~30 μmol/L,线性相关系数R2=0.995(n=15),检测限为0.2 μmol/L.本研究为环境水样中Ag+的识别和检测提供了一种简单、精确、快速、环境友好的新方法.
参考文献:
[1]ARNAL H C,BANU A,BARBOIU M,et al.Amplification and transcription of the dynamic supramolecular chirality of the guanine quadruplex[J].Angew Chem Int Ed,2007,46(23):4268-4272.
[2]SIMONYI M,BIKADI Z,ZSILA F,et al.Supramolecular exciton chirality of carotenoid aggregates[J].Chirality,2003,15(8):680-698.
[3]BOROVKOV V V,HEMBURY G A,YAMAMOTO N,et al.Supramolecular chirogenesis in zinc porphyrins:investigation of zinc-freebase bis-porphyrin,new mechanistic insights,extension of sensing abilities,and solvent effect[J].J Phys Chem A,2003,107(41):8677-8686.
[4]ISHII Y,ONDA Y,KUBO Y.2,2′-Biphenyldiol-bridged bis(free base porphyrin):synthesis and chiroptical probing of asymmetric amino alcohols[J].Tetrahedron Lett,2006,47(47):8221-8225.
[5]AIMI J,OYA K,TSUDA A,AIDA T.Chiroptical sensing of asymmetric hydrocarbons using a homochiral supramolecular box from a bismetalloporphyrin rotamer[J].Angew Chem Int Ed,2007,46(12):2031-2035.
[6]HEMBURY G A,BOROVKOV V V,INOUE Y.Chirality-sensing supramolecular systems[J].Chem Rev,2008,108(1):1-73.
[7]YAO Z Y,LI C,SHI G Q.Optically active supramolecular complexes of water-soluble achiral polythiophenes and folic acid:spectroscopic studies and sensing applications[J].Langmuir,2008,24(22):12829-12835.
[8]KATOONO R,KAWAI H,FUJIWARA K,et al.Dynamic molecular propeller:supramolecular chirality sensing by enhanced chiroptical response through the transmission of point chirality to mobile helicity[J].J Am Chem Soc,2009,131(46):16896-16904.
[9]马立娜,刘殿骏,王振新.基于金纳米粒子的动态光散射法检测溶液中的汞离子[J].分析化学,2014,42(3):332-336.
[10]柯庆青,裴继影,杨帆,等.谷胱甘肽修饰的金纳米粒子探针比色法检测神经元素3[J].分析化学,2014,42(7):955-961.
[11]JIANG Z L,FAN Y Y,CHEN M L,et al.Resonance scattering spectral detection of trace Hg2+using aptamer-modified nanogold as probe and nanocatalyst[J].Anal Chem,2009,81(13):5439-5445.
[12]TURKEVICH J,STEVENSON P C,HILLIER J.A study of the nucleation and growth processes in the synthesis of colloidal gold[J].Discuss Faraday Soc,1951,11:55-75.
[13]欧阳振中,白珊,潘玉兰,等.对氨基苯磺酸存在下银纳米粒子的生成及银离子检测[J].湖南科技大学学报(自然科学版),2015,30(3):106-109.
[14]赖奕坚,王菲,赵斌元.离子选择性电极对痕迹量银离子的检测[J].实验室研究与探索,2009,28(10):38-39,44.
[15]中国疾病预防控制中心环境与健康相关产品安全所.生活饮用水卫生标准:GB 5749—2006[S].北京:中国标准出版社,2006.
doi:10.6043/j.issn.0438-0479.201512004
收稿日期:2015-12-03录用日期:2016-02-22
基金项目:云南中烟工业有限责任公司技术中心科技项目(HYHH2013CL02)
*通信作者:ybjiang@xmu.edu.cn
中图分类号:O 651
文献标志码:A
文章编号:0438-0479(2016)04-0601-05
Recognition and Detection of Silver Ion by Circular DichroismSpectrum Based on Chiral Gold Nanoparticles
WEI Keyi1,2,WANG Meng1,DU Yu1,CAI Bo1,JIANG Yunbao2*
(1.Research & Development Center,China Tobacco Yunnan Industrial Co.,Ltd.,Kunming 650231,China;2.College of Chemistry and Chemical Engineering,Xiamen University,Xiamen 361005,China)
Abstract:In this work,chiral gold particles with optical activity can be obtained by a facile liquid phase method.The textural properties of the as-prepared samples were characterized by high resolution transmission electron microscopy, circular dichroism spectrum and absorption spectrum.The results show that the average particle size for the production is 3.6 nm and silver ion can be selectively recognized from 13 kinds of metal ions in 12 min with universal recurrence.We also established the standard curve for detecting silver ion. This study demonstrates that the linear range for this curve is 0.2-30 μmol/L,the linearly dependent coefficient is 0.995(n=15),which supplies a simple new environmentally friendly method for quickly detecting and recognizing silver ion in environmental water samples with high precision.
Key words:chiral gold nanoparticles;circular dichroism spectrum;recognition;detection;silver ion
引文格式:韦克毅,王猛,杜宇,等.基于手性金纳米粒子圆二色光谱法识别与检测银离子[J].厦门大学学报(自然科学版),2016,55(4):601-605.
Citation:WEI K Y, WANG M,DU Y,et al.Recognition and detection of silver ion by circular dichroism spectrum based on chiral gold nanoparticles[J].Journal of Xiamen University(Natural Science),2016,55(4):601-605.(in Chinese)

