HPLC-ELSD法测定胆南星中胆酸类成分的含量
蔡宇忆,叶永浩,杨丽莹,黄玉梅,吴志坚,马永德,李书渊
HPLC-ELSD法测定胆南星中胆酸类成分的含量
蔡宇忆1,叶永浩1,杨丽莹1,黄玉梅2,吴志坚2,马永德2,李书渊1
(1.广东药科大学 中药学院,广东 广州 510006;2.广州市药材公司中药饮片厂,广东 广州510360)
摘要:目的 建立HPLC-ELSD法测定胆南星中4种胆酸类成分质量分数的方法。方法 色谱柱为WELCH AQ-C18柱(4.6 mm×250 mm,5 μm),流动相为乙腈-0.2%(体积分数)冰醋酸(体积比60∶40),柱温为30℃,流速为1.0 mL/min,检测器为ELSD,载气流速为2.2 mL/min,漂移管温度为90℃。结果胆酸、猪去氧胆酸、鹅去氧胆酸、去氧胆酸均在定量范围内呈良好的线性关系,平均回收率分别为97.62%、98.38%、97.32%、97.86%。结论本方法操作简单,测定结果准确,可用于胆南星中胆酸类成分的质量分数测定及质量控制。
关键词:胆南星;HPLC-ELSD法;胆酸;猪去氧胆酸;鹅去氧胆酸;去氧胆酸
2015年版《中国药典》所记载的“胆南星”为制天南星的细粉与牛、羊或猪胆汁经加工而成,或为生天南星细粉与牛、羊或猪胆汁经发酵加工而成[1]。目前,胆南星疗效成分不完全清楚,胆汁为胆南星主要加工辅料,据现代实验药理学研究报道胆汁具有一定镇静、安神、调节心血管系统作用[2-3],因此测定胆汁酸质量分数可以部分反映胆南星药用质量。古代胆南星炮制一般用牛胆汁,现在逐步发展成用牛胆汁、猪胆汁、羊胆汁,甚至可以采用混合胆汁。2015年版《中国药典》“胆南星”项下尚无检查项和含量测定项,其质量评价标准还未完善。由于有关原药材天南星的毒性物质基础研究比较少,与传统
网络出版时间:2016-05-24 15:34 网络出版地址:http://www.cnki.net/kcms/detail/44.1413.R.20160524.1534.003.html药效相对应的活性成分还不清楚,不容易从中选择质量控制的指标成分,所以本研究参照文献[4-5],选用胆酸、猪去氧胆酸、鹅去氧胆酸、去氧胆酸作为对照品,首次建立HPLC-ELSD法同时测定胆南星中4种胆酸类成分的质量分数测定方法。
1 仪器与试药
高效液相色谱仪(日本岛津公司),WELCH AQC18色谱柱,Dikma EasyGuard保护柱;3300 ELSD蒸发光散射检测器(美国奥泰公司);XWK-Ⅲ无油空气泵(天津市津分分析仪器制造有限公司);BP211D十万分之一电子天平(德国赛多利斯集团);AY120万分之一电子天平(日本岛津公司);SK250HP科导超声仪(上海科导超声仪器有限公司);ANKE TGL-16G-A恒温高速离心机(上海安亭科学仪器厂)。
胆酸对照品(中国食品药品检定研究院,批号:10078-0013),猪去氧胆酸对照品(成都曼思特生物科技有限公司,批号:MUST-14060906),鹅去氧胆酸对照品(中国食品药品检定研究院,批号:110806-200303),去氧胆酸对照品(中国食品药品检定研究院,批号:724-8601);甲醇(分析纯);乙腈(色谱纯);蒸馏水。
10批胆南星样品均产自四川,经广东药科大学中药学院李书渊教授鉴定符合《中国药典》标准,其来源详见表1。
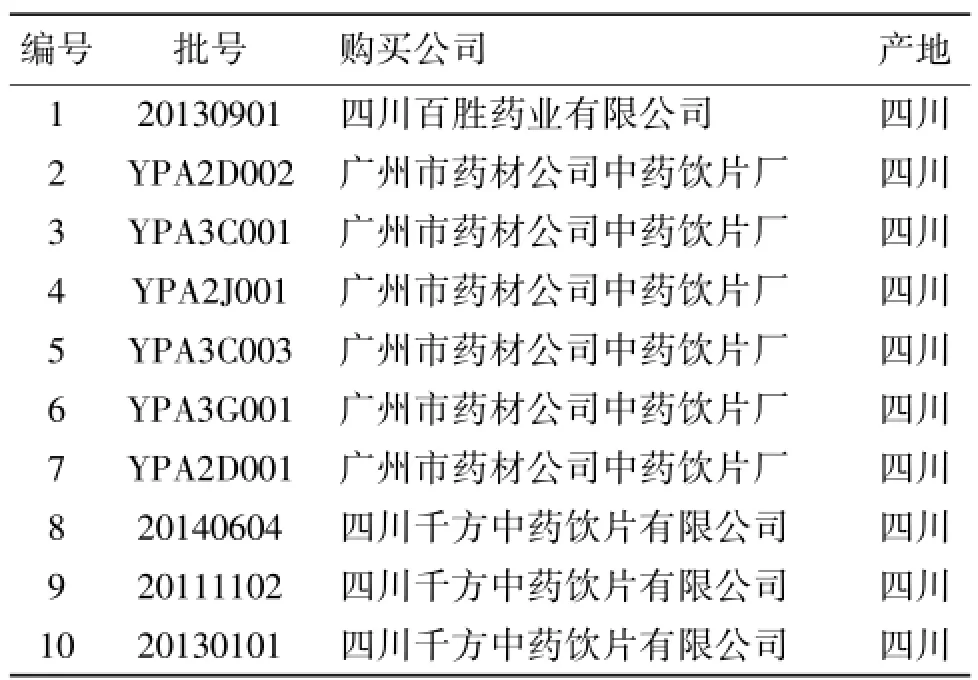
表1 10批胆南星样品来源信息表Table 1 The information of 10 batches of Arisaema cum Bile
2 方法与结果
2.1 混合对照品溶液的制备
分别取胆酸、猪去氧胆酸、鹅去氧胆酸、去氧胆酸对照品适量,精密称定,置于50 mL容量瓶中,加甲醇制成每1 mL含胆酸、猪去氧胆酸、鹅去氧胆酸、去氧胆酸分别为0.205、1.024、0.952、0.398 mg的混合对照品溶液。
2.2 供试品溶液的制备
取胆南星(过4号筛)0.5 g,精密称定,置50 mL锥形瓶中,加甲醇10 mL,称定质量,超声处理(功率250 W,频率40 kHz)30 min,冷却,称定质量,加甲醇补足减失质量,置离心管中离心(12 000 r/min)10 min,取上清液,用0.45 μm微孔滤膜滤过,即得。
2.3 色谱条件及适应性试验
色谱柱:WELCH AQ-C18色谱柱(4.6 mm×250 mm,5 μm),Dikma EasyGuard保护柱;流动相:乙腈-0.2%(体积分数,下同)冰醋酸(体积比60∶40),流速:1.0 mL/min;柱温:30℃;蒸发光检测器载气流速:2.2 mL/min,漂移管温度:90℃。精密吸取混合对照品、供试品溶液各20 μL,按上述条件进行测定。色谱图见图1。
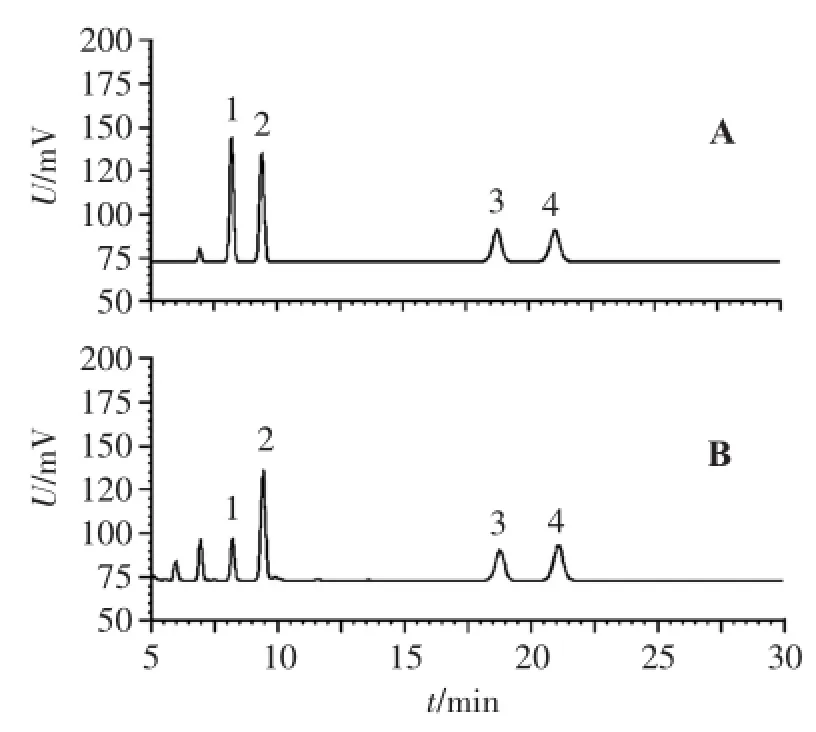
1.胆酸;2.猪去氧胆酸;3.鹅去氧胆酸;4.去氧胆酸。图1 混合对照品(A)、胆南星供试品(B)溶液的HPLCELSD色谱图Figure 1 The HPLC-ELSD chromatogram of mixed references (A)and Arisaema cum Bile(B)
2.4 线性关系的考察
分别取胆酸、猪去氧胆酸、鹅去氧胆酸、去氧胆酸混合对照品溶液0.1、1、2.5、5、10 mL置于10 mL容量瓶中,用甲醇定容至刻度,摇匀,得系列混合对照品溶液。分别精密吸取各混合对照品溶液20 μL,按照“2.3”项下条件进行测定。以对照品进样量对数为横坐标(X),峰面积的对数为纵坐标(Y)绘制标准曲线,结果见表2。由表2可知,4种胆酸成分均在测定范围内呈良好的线性关系。
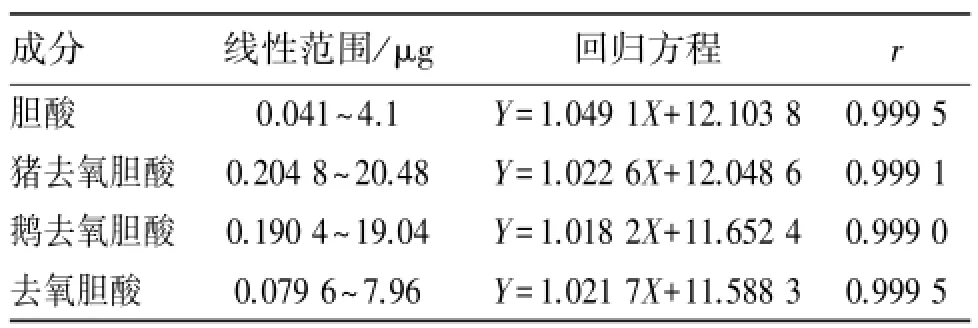
表2 胆南星中4种胆酸类成分的线性范围、回归方程及r值Table 2 The linear relationship,regression equations and rvalues of four cholic acids in Arisaema cum Bile
2.5 精密度试验
精密吸取混合对照品溶液20 μL,按“2.3”项下条件进行测定,重复6次,记录胆酸、猪去氧胆酸、鹅去氧胆酸和去氧胆酸的峰面积,计算其RSD值分别为0.38%、0.86%、0.84%、1.33%,表明仪器精密度良好。
2.6 稳定性试验
取同一批胆南星粉末(批号:20130901)约0.5 g,精密称定,按“2.2”项下制备供试品溶液,于室温下放置0、2、4、8、12、24 h后分别进样,按“2.3”项下色谱条件测定,记录胆酸、猪去氧胆酸、鹅去氧胆酸和去氧胆酸的峰面积,计算其RSD值分别为1.81%、1.48%、 1.72%、1.43%,表明供试品溶液在24 h内稳定。
2.7 重复性试验
取同一批胆南星粉末(批号:20130901)约0.5 g,精密称定,按“2.2”项下方法制备供试品溶液,重复操作6份。分别按“2.3”项下色谱条件测定并记录胆酸、猪去氧胆酸、鹅去氧胆酸和去氧胆酸的峰面积。计算得胆酸、猪去氧胆酸、鹅去氧胆酸和去氧胆酸质量分数的RSD值分别为2.86%、1.98%、2.21%、2.50%,表明方法重复性好。
2.8 加样回收率试验
取已知胆酸成分总质量分数的同一批胆南星粉末(批号:20130901)约0.25 g,共6份,精密称定,分别加入适量胆酸、猪去氧胆酸、鹅去氧胆酸和去氧胆酸对照品溶液,分别按照“2.2”项下方法制备供试品溶液,按“2.3”项下色谱条件测定,记录胆酸、猪去氧胆酸、鹅去氧胆酸和去氧胆酸的峰面积,计算其平均回收率分别为97.62%、98.38%、97.32%、97.86%,RSD值分别为2.11%、1.96%、1.86%、2.48%。结果见表3。
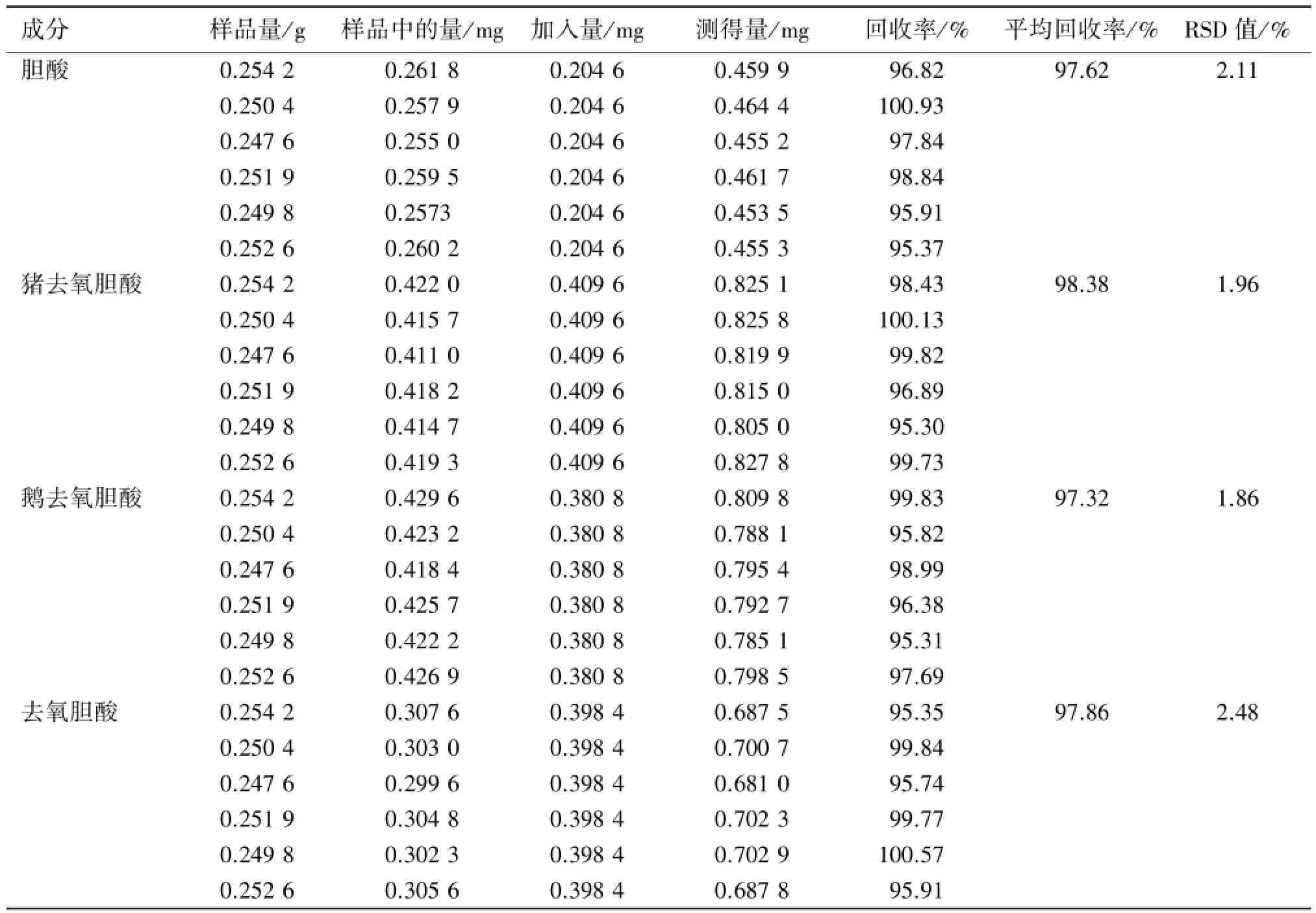
表3 胆南星中4种胆酸类成分的加样回收率试验结果Table 3 The recovery results of four cholic acids in Arisaema cum Bile(n=6)
2.9 样品测定
分别取10批胆南星样品粉末,各0.5 g,精密称定,每批重复操作2份,分别按“2.2”项下方法制备供试品溶液,按“2.3”项下条件测定并记录胆酸、猪去氧胆酸、鹅去氧胆酸、去氧胆酸的峰面积,分别计算4种胆酸类成分的质量分数及其总质量分数。结果见表4。
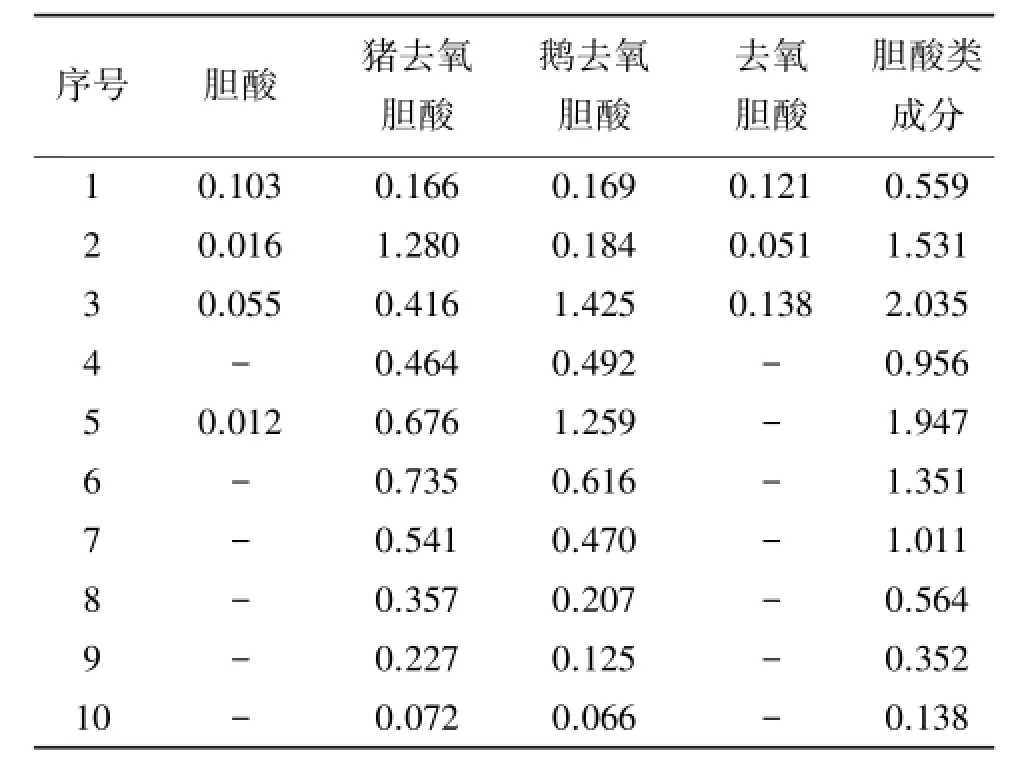
表4 胆南星中4种胆酸成分及总质量分数的测定结果Table 4 The determination results of four cholic acids in Arisaema cum Bile(n=2) w/%
3 讨论
本实验旨在研究建立同时测定胆南星中4种胆酸类成分的方法,从而为制定胆南星的质量标准提供依据。由张能荣[6]对牛、羊、猪胆汁中15种成分的研究结果可知:牛、羊胆汁中无猪去氧胆酸,猪胆汁中不含胆酸与去氧胆酸,而鹅去氧胆酸为3种胆汁共有的成分,据此可以判断市售的胆南星药材在炮制过程中加入了何种胆汁。从本试验结果可以看出,所检测10个批次的胆南星中采用的胆汁辅料大多是猪胆汁,部分批次采用的是混合胆汁;各样品胆酸类成分的质量分数差异较大,可能是由于加工过程中加入胆汁类型和加入胆汁量不同导致的——因此把胆酸类成分作为胆南星的质量控制指标是必不可少的。方法学考察结果表明,本法操作简单,测定结果准确、重复性好,可用于胆南星胆酸类成分的质量分数测定和质量控制。
参考文献:
[1]国家药典委员会.中华人民共和国药典:2015年版一部[M].北京:中国医药科技出版社,2015:245.
[2]王凯平,石朝周.动物胆汁药用研究的概况与展望[J].中国中医药科技,2000,7(5):350-352.
[3]白万富,鞠爱华,杨乾.牛胆汁的化学成分及临床应用的研究进展[J].中华中医药杂志,2008,23(2):149-151.
[4]赫炎,张永欣,赵惠东,等.HPLC测定胆南星中猪去氧胆酸的含量[J].中国中药杂志,2007,32(16):1634-1636.
[5]王光函,姜鸿,邹桂欣,等.HPLC-ELSD法测定胆南星中胆酸含量[J].亚太传统医药,2014,10(22):8-9.
[6]张能荣.牛羊胆汁质量的研究[J].中草药,1983,14(7):15.
(责任编辑:刘晓涵)
中图分类号:R284.1
文献标志码:A
文章编号:1006-8783(2016)03-0311-04
DOI:10.16809/j.cnki.1006-8783.2016032301
收稿日期:2016-03-23
基金项目:广州市荔湾区科技计划(20133115008)
作者简介:蔡宇忆(1991—),女,2013级硕士研究生,Email:406371983@qq.com;通信作者:李书渊(1963—),女,教授,从事中药物质基础和质量标准研究,Email:1018720684@qq.com。
Determination of cholic acid constituents from Arisaema cum Bile by HPLC-ELSD
CAI Yuyi1,YE Yonghao1,YANG Liying1,HUANG Yumei2,WU Zhijian2,MA Yongde2,LI Shuyuan1
(1.School of Traditional Chinese Medicine,Guangdong Pharmaceutical University,Guangzhou 510006,China;2.Guangzhou Materia Company,Guangzhou 510360,China)
AbstractObjective To develop a HPLC-ELSD method for the determination of cholic acids from Arisaema cum Bile.Methods WELCH AQ-C18column 4.6 mm×250 mm 5 μm was employed and eluted at 30℃with a mobile phase consisting of acetonitrile-0.2%glacial acetic acid 60∶40 and the flow rate was 1.0 mL/min.The drift-tube temperature of ELSD was 90℃ and the flow rate of air was 2.2 mL/min. Results Cholic acid hyodeoxycholic acid chenodeoxycholic acid and deoxidation cholic acid had good linearity within the quantitative range and their mean recovery ratios were 97.62% 98.38% 97.32%and 97.86% respectively.Conclusion The method was simple and accurate which could be used for the determination and quality control of cholic acid constituents from Arisaema cum Bile.
Key wordsArisaema cum Bile HPLC-ELSD cholic acid hyodeoxycholic acid chenodeoxycholic acid deoxidation cholic acid

