RP-HPLC法同时测定天黄颗粒中阿魏酸和姜黄素的含量
谭敏秀,何锦钧,关杏英,周 清,任燕芬
(1.佛山市中医院,佛山 528000;2.广东药学院,广州 510006)
RP-HPLC法同时测定天黄颗粒中阿魏酸和姜黄素的含量
谭敏秀1,何锦钧1,关杏英1,周清2*,任燕芬1
(1.佛山市中医院,佛山528000;2.广东药学院,广州510006)
摘要:目的建立同时测定天黄颗粒中阿魏酸和姜黄素含量的方法。方法采用反相高效液相色谱法。色谱柱为Diamond-C18柱(250 mm×4.6 mm,5 μm);流动相为乙腈-1 mL·L-1磷酸水溶液(二元梯度洗脱);流速为0.8 mL·min-1;检测波长为354 nm;柱温约为20 ℃。结果阿魏酸和姜黄素质量浓度分别在7~148和20~200 μg·mL-1范围内与各自峰面积线性关系良好,平均回收率分别为108.4%和103.7%,RSD值分别为1.9%和1.2%。样品中阿魏酸和姜黄素平均含量分别为0.4和1.27 mg·g-1。结论该方法精密度好,结果准确,可用于天黄颗粒中阿魏酸和姜黄素的含量测定。
关键词:天黄颗粒;阿魏酸;姜黄素;反相高效液相色谱法;含量测定
天黄颗粒是医院在制剂天柏金黄散基础上开发的颗粒剂型外用药,由黄柏、姜黄、当归和大黄等多味药材制成,具有凉血、活血、化瘀、止痛的功效。在处方中,当归味辛,有活血化瘀、去肿止痛的作用;姜黄味辛,泄苦通温,为血中气药,古今医家视之为风湿肩臂疼痛的要药。为了更好地控制制剂的质量,本实验以该方中主要有效成分阿魏酸和姜黄素为指标,拟建立1种简便可靠的含量测定方法。经查阅,同时对天黄颗粒中阿魏酸[1-6]和姜黄素[7-11]进行含量测定未见文献报道,本方法分离效果好,定量准确,专属性较强。
1仪器与试药
1.1仪器高效液相色谱仪(LC-10ATvp plus,UV检测器,日本岛津公司);LC Solution色谱工作站。
1.2试药对照品:阿魏酸(批号0773-9910)、姜黄素(批号110823-200603),购自中国药品生物制品检定研究院;天黄颗粒(批号141101-141103),由佛山市中医院提供。甲醇、乙腈均为色谱纯;其他试剂均为分析纯;实验用水为屈臣氏蒸馏水。
2方法与结果
2.1样品液制备
2.1.1对照品溶液的制备准确称取阿魏酸对照品14.8 mg、姜黄素对照品20.0 mg,分别置于100 mL量瓶中,加700 mL· L-1甲醇溶解并稀释至刻度,摇匀,得到质量浓度分别为148和200 μg·mL1的阿魏酸和姜黄素对照品储备液。
2.1.2供试品溶液的制备称取2 g天黄颗粒,加入700 mL· L-1的甲醇30 mL,加热回流处理30 min,滤过,收集滤液,再用0.45 μm的滤膜过滤,得供试品溶液。
2.1.3阴性对照溶液的制备按照处方组成,取除当归、姜黄外的其余药味,按照工艺要求制成不含当归和姜黄的天黄颗粒;按照2.1.2项下操作方法制成阴性对照溶液。
2.2色谱条件与系统适用性实验Diamond-C18柱(250 mm×4.6 mm,5 μm,迪马公司)为色谱柱;乙腈-1 mL·L-1磷酸水溶液(二元梯度洗脱,洗脱程序见表1)为流动相;流速为0.8 mL·min1;检测波长为354 nm;柱温为室温(约20 ℃)。分别取对照品、供试品、阴性对照溶液20 μL注入液相色谱仪,依法测定;以阿魏酸或姜黄素计算理论板数均不低于5 000;阿魏酸和姜黄素峰的拖尾因子分别为0.91和0.97;保留时间分别约为15.7和31.1 min;与相邻未知峰的分离度均大于1.5;阴性对照无干扰,见图1。
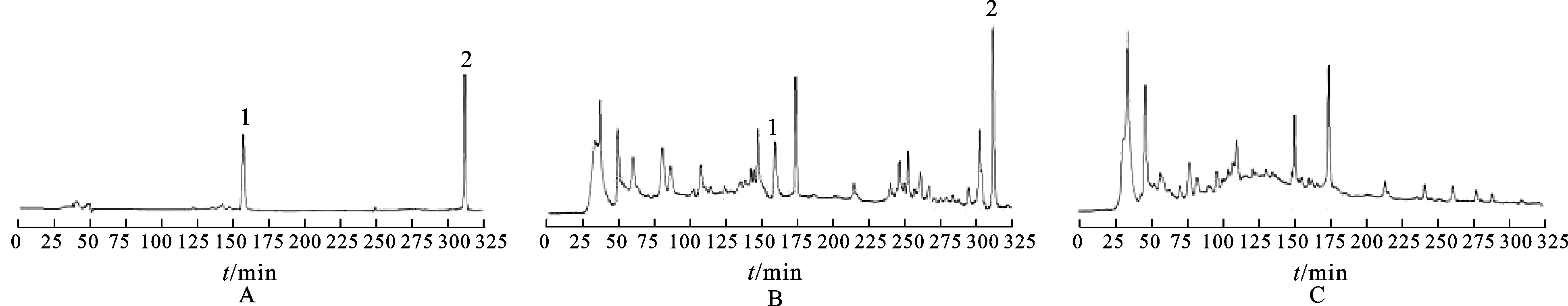
图1HPLC图
A.对照品; B.样品;C.阴性;1.阿魏酸;2.姜黄素
Fig.1 HPLC chromatograms
A.reference substance;B.sample;C.negative;1.ferulic acid;2.curcumin
表1流动相梯度洗脱程序
Tab.1 The gradient elution programs of mobile phase

时间/min乙腈/%1mL·L-1磷酸/%0~15 20→50 80→5015~30 50→100 50→0>301000
2.3方法学考察
2.3.1标准曲线与线性范围分别精密吸取2.1.1项下的阿魏酸和姜黄素储备液,加700 mL·L-1的甲醇稀释成不同质量浓度的阿魏酸(质量浓度分别为7,14,21,28,35,70和148 μg·mL1)、姜黄素(质量浓度分别为20,40,60,80,120,160和200 μg·mL1)溶液,依次进样(进样量20 μL)。以溶液质量浓度为横坐标,峰面积均值为纵坐标,绘制阿魏酸和姜黄素标准曲线。得阿魏酸的回归方程Y=43 181X+20 201(r=0.999 4),姜黄素的回归方程Y=35 416X-161 847(r=0.999 3)。表明阿魏酸质量浓度在7~148μg·mL1之间、姜黄素质量浓度在20~200 μg·mL1之间与峰面积呈良好线性关系。
2.3.2精密度实验取质量浓度为21 μg·mL1的阿魏酸和80 μg·mL1的姜黄素对照品混合溶液连续测定6次,记录峰面积。阿魏酸和姜黄素峰面积的RSD值分别为0.41%和0.33%,表明仪器的精密度良好。2.3.3稳定性实验取供试品溶液(批号141101),分别在0,2,4,6,8和12 h进样,记录峰面积,阿魏酸和姜黄素峰面积的RSD值分别为0.71%和0.41%,表明供试品溶液在12 h内稳定。
2.3.4重复性实验取供试品溶液(批号141101)6份,按照2.1和2.2项下所述方法处理、测定,结果阿魏酸平均质量浓度为27.32 mg·mL1、姜黄素平均质量浓度为84.71 mg·mL1,RSD值分别为0.98%和0.41%,表明分析方法的重复性良好。
2.3.5加样回收实验称取同一批号样品(批号141101)9份,每份2 g,按照2.1项下所述方法处理,取适量已知含量的供试品,每3份中分别加入约80%,100%和120%的阿魏酸和姜黄素混合对照品溶液,按照2.2项下所述方法进行测定,计算回收率,见表2,阿魏酸的平均回收率为108.4%,RSD值为1.9%;姜黄素的平均回收率为103.7%,RSD值为1.2%。结果表明,本方法准确可靠。
表2回收率实验结果
Tab.2 Results of the recovery test
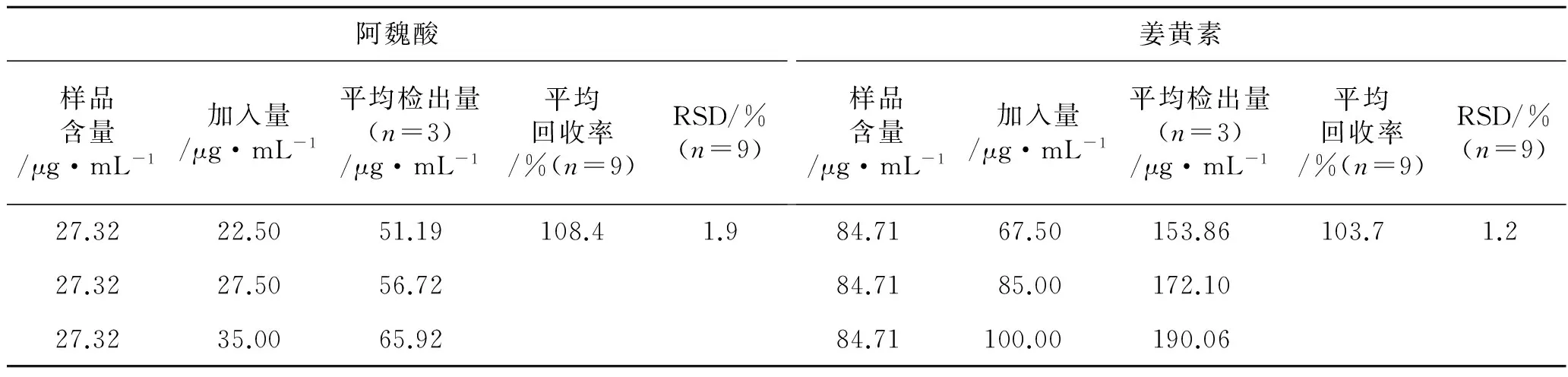
阿魏酸样品含量/μg·mL-1加入量/μg·mL-1平均检出量(n=3)/μg·mL-1平均回收率/%(n=9)RSD/%(n=9)姜黄素样品含量/μg·mL-1加入量/μg·mL-1平均检出量(n=3)/μg·mL-1平均回收率/%(n=9)RSD/%(n=9)27.3222.5051.19108.41.984.7167.50153.86103.71.227.3227.5056.7284.7185.00172.1027.3235.0065.9284.71100.00190.06
2.4样品测定取天黄颗粒样品3批,按照2.1项下方法制备样品溶液,按照2.2项下所述方法进行测定,计算得出样品中阿魏酸和姜黄素的平均含量分别为0.40和1.27 mg·g-1。
3讨论
阿魏酸易溶于热水、乙醇和乙酸乙酯,稍溶于乙醚,难溶于苯和石油醚;因此常采用醇-水混合溶剂提取,提取方式常采用回流、超声等;姜黄素不溶于水,溶于醇类溶剂。因此在提取分离条件的摸索过程中,采用醇-水混合溶剂提取,比较了超声和回流2种不同的提取方式,并比较了提取时间、溶剂量和溶剂比率对提取率的影响。结果表明,15倍(质量比)的混合溶剂(体积分数70%甲醇-水)回流提取30 min,离心,过滤后制得的样品溶液,阿魏酸和姜黄素的提取率均较高。
阿魏酸具有一定的弱酸性,且出峰时间较短,存在峰形拖尾的现象,因此在流动相中加酸后色谱峰峰形明显改善,分离度也大大提高。文献报道[2-6],阿魏酸含量测定流动相体系较多,如乙腈-磷酸水、甲醇-醋酸水、乙腈-水、甲醇-水、乙腈-甲醇等,本文也选用了这几种流动相分别进行考察,发现选用乙腈-1mL·L-1磷酸水溶液(梯度洗脱)为流动相效果最好,故采用了表1的流动相体系及梯度变换方式。
参考文献:
[1]国家药典委员会.中国药典2010年版 [S].一部.北京:中国医药科技出版社,2010:124-125.
[2]黄罗生,郭健新,刘咏梅,等.HPLC测定阿魏酸含量的探讨[J].中成药,2004,26(2):134-136.
[3]张继东.HPLC法测定当归片中阿魏酸的含量[J].药物分析杂志,2011,31(10):1979-1981.
[4]赵辉,武晓红,蒲晓辉.HPLC法同时测定天舒胶囊中阿魏酸和天麻素[J].中成药,2014,36(1):111-114.
[5]张霞,王荣,侯延辉,等.HPLC法同时测定复方芸归颗粒中松果菊苷、阿魏酸和柚皮苷含量[J].西北药学杂志,2010,25(6):403-405.
[6]许江,张庆,俞小陶.HPLC法测定活血止痛胶囊中阿魏酸的含量[J].广东药学院学报,2000,16(4):309-310.[7]国家药典委员会.中国药典2010年版 [S].一部.北京:中国医药科技出版社,2010:879-880.
[8]李明,周欣,赵超,等.HPLC同时测定姜黄中3种姜黄素的含量[J].药物分析杂志,2008,28(11):1810-1814.
[9]金岩,赵铁,姜清华,等. HPLC法测定消瘤丸中姜黄素的含量[J].中国药师,2012,15(7):980-981.
[10]毕晓黎,孙冬梅,罗文汇,等.HPLC法同时测定复方姜黄微囊中姜黄素和胡椒碱的含量[J].中国实验方剂学杂志,2010,16(2):20-22.
[11]郑少华,李欣,周莉,等.姜黄素缓释片的制备及释放度研究[J].西北药学杂志,2015,30(1):65-67.
基金项目:广东省医学科研基金项目(编号:B2014212);2014年佛山市医学类科技攻关项目(编号:2014AB00341)
作者简介:谭敏秀,女,副主任药师
*通信作者:周清,男,讲师
doi:10.3969/j.issn.1004-2407.2016.04.014
中图分类号:R927.2
文献标志码:A
文章编号:1004-2407(2016)04-0374-03
(收稿日期:2015-09-15)
Simultaneous determination of ferulic acid and curcumin in Tianhuang Granules by RP-HPLC
TAN Minxiu1,HE Jinjun1,GUAN Xingying1,ZHOU Qing2*,REN Yanfen1
(1.Foshan Hospital of Traditional Chinese Medicine,Foshan 528000,China;2.Guangdong Pharmaceutical University,Guangzhou 510006,China)
Abstract:Objective To establish a determination method for ferulic acid and curcumin in Tianhuang Granules.Methods An RP-HPLC method was established.The chromatographic column was Diamond-C18(250 mm×4.6 mm,5 μm).The mobile phase was a mixture of acetonitrile-1 mL·L-1phosphoric acid (gradient elution).The flow rate was 0.8 mL·min-1,the UV detection wavelength was 354 nm,and the column temperature was 20 ℃.Results The linear range of ferulic acid was between 7-148 μg·mL-1with a good linear relationship and the average recovery was 108.4%,RSD was 1.9%.The linear range of curcumin was between 20-200 μg·mL-1with a good linear relationship and the average recovery was 103.7%,RSD was 1.2%. The average contents of ferulic acid and curcumin were 0.4 and 1.27 mg·g-1,respectively.Conclusion The method is accurate with high precision, and can be used for the quantitative determination of Tianhuang Granules.
Key words:Tianhuang Ganules;ferulic acid;curcumin;RP-HPLC;assay

