两种镍基口腔修复合金在漱口水中镍离子析出的比较
田陶然 张扬根 黄鑫琪 李龙飚 张心曦 朱卓立口腔疾病研究国家重点实验室 华西口腔医院(四川大学) 成都 610041
两种镍基口腔修复合金在漱口水中镍离子析出的比较
田陶然 张扬根 黄鑫琪 李龙飚 张心曦 朱卓立
口腔疾病研究国家重点实验室 华西口腔医院(四川大学) 成都 610041
[摘要]目的通过连续浸泡实验探究两种镍基口腔修复常用合金在漱口水中的镍离子析出情况。方法将镍基铸造合金和镍铬烤瓷合金的标准试件逐级打磨后,放在分别由漱口水、蒸馏水和人工唾液配制的实验组和对照组溶液中,连续恒温(37±1)℃浸泡96 h后,使用电感耦合等离子体发射光谱仪(ICP-OES)测定溶液中析出的镍离子的量。结果在没有金属浸泡的空白对照的实验组和对照组溶液中镍离子含量低于ICP-OES的检出限。在对照组溶液及实验组溶液中浸泡后镍基铸造合金组测得的镍离子析出均大于镍铬烤瓷合金组。两种金属试件在实验组溶液中的析出均大于在对照组溶液中的析出,差异明显。结论漱口水对两种镍基合金中镍离子的析出均有促进作用,其中又以镍基铸造合金为甚。
[关键词]漱口水;牙科合金;浸渍;镍
镍基合金由于良好的物理性能以及较低的价格,在口腔修复中的使用较为广泛。但是镍基合金在口腔环境中易于发生腐蚀,使得这种合金的使用饱受争议[1-2]。腐蚀过程中产生的镍离子与组织细胞直接接触,其产生的生物学效应在体内、体外实验中均可被发现,在口腔中主要表现为炎症及过敏,其中过敏在女性患者中发生率可达10%~20%[3]。此外,在对镍过敏患者的修复治疗中如使用含镍合金则会影响其牙周健康[4]。
研究[5-6]显示,含氟以及低pH的液体环境会加速口内修复体合金的腐蚀,金属离子的析出为其主要表现之一。商品漱口水作为维持口腔卫生的一种方式,被广泛使用[7]。李施德林齿龈防护漱口水是商品漱口水中推广较好的一个品种,适用人群广泛,但其含氟及低pH的特性,可能对于镍基合金产生不利的影响。但使用此种漱口水对于镍基合金可产生多大影响,目前未见文献报道。
现有对修复体合金口内腐蚀研究所使用的溶液多为将标准人工唾液配制成不同氟浓度或pH的实验溶液[5]。但在配制的过程中,由于液体的添加,人工唾液中各成分的浓度已发生变化,直接导致了控制变量的改变,存在实验结果的偏倚。本实验所选用的李施德林漱口水呈酸性,在鼓漱的过程中会刺激唾液分泌,故本研究使用等量蒸馏水和商品漱口水为变量,分别加入等量人工唾液配制为对照组、实验组溶液,避免了其余控制变量的变化。实验方法上选择镍基铸造合金、镍铬烤瓷合金制备的试件进行定时浸泡,使用检出限较高的电感耦合等离子体发射光谱仪(inductively coupled plasma optical emission spectrometer,ICP-OES)测定镍离子的析出量,用以精确比较两种镍合金在特定液体环境中镍离子的析出情况。
1 材料和方法
1.1材料
镍基铸造合金、镍铬烤瓷合金(上海医疗器械股份有限公司齿科材料厂);牙科磷酸盐铸造包埋材料(洛阳北苑特种烤瓷有限公司);Bellavest SH烤瓷包埋料(BEGO公司,德国);李施德林齿龈防护漱口水(强生公司,美国);镍基铸造合金以镍、铬为主体材料,Pb≤0.02%,As≤0.01%,Be≤0.02%,Cd≤0.02%;镍铬烤瓷合金主要成分为:Ni 63.6%,Cr 22.9%,Mo 11.3%。
1.2方法
1.2.1溶液的制备人工唾液参考ISO/TR10271标准,其成分具体为:NaCl 0.4 g、KCl 0.4 g、CaCl2·2H2O 0.795 g、NaH2-PO4·2H2O 0.78 g、Na2S·2H2O 0.005 g、尿素1 g、蒸馏水1 000 mL,将配置成功后的人工唾液pH值调至6.80。由于漱口水呈酸性,以酸刺激状态下动态唾液总流率2.64 g·min-1为参考值,依据消费者每次使用漱口水的时间和量,在每100 mL漱口水中添加6.60 g人工唾液制成实验组溶液,在每100 mL蒸馏水中添加6.60 g人工唾液制成对照组溶液。常温下多次测量实验组溶液pH值后求得平均值为4.23。两组溶液均高温高压灭菌后保存。
1.2.2试件的制备用铸造蜡制备规格为10 mm× 10 mm×1 mm方蜡模20个,镍基铸造合金、镍铬烤瓷合金常规包埋铸造,形成合金试件共20件,每种金属10件。按口腔金属义齿加工工艺喷砂处理去除试件表面包埋料,将试件两面依次经300、400、600、800、1 000目金相砂纸及绒轮打磨抛光。所有试件置于去离子水中超声清洗5 min,然后在无水乙醇中浸泡5 min,干燥备用,以上程序由同一人完成。
1.2.3商品漱口水浸泡将20个5 mL EP管高温高压灭菌后按每组10个分为实验、对照两组。实验组EP管内加入3 mL实验组溶液,对照组EP管内加入3 mL对照组溶液。将每种金属试件按每组5件随机分成两组,分别称为实验组、对照组。然后将干燥备用的金属试件放置在相应实验组、对照组EP管内,每个EP管内放置1种金属共1个试件。所有金属试件的表面均充分暴露于液体环境中。用胶带将EP管口密封。另设两组每组5个高温高压灭菌后的5 mL EP管分别注入3 mL实验组、对照组溶液作为空白对照。将所有EP管放置于温度为(37± 1)℃的恒温水槽内,浸泡96 h。
1.2.4离子析出的测定浸泡完毕后用塑料镊子取出试件,封存溶液。用无水乙醇冲洗试件,干燥保存。将EP管内的实验组、对照组溶液样本送四川大学分析测试中心,使用ICP-OES(德国斯派克分析仪器公司,德国)定量测其溶液里的镍离子浓度。
1.2.5扫描电子显微镜观察所有金属试件编号,在浸泡前后均使用扫描电子显微镜(FEI公司,荷兰)放大2 000、10 000倍观察表面形貌,加速电压20 kV。
1.3统计学处理
采用SPSS 19.0统计分析软件对浸泡前后溶液里相关金属离子浓度的变化进行统计学处理,计量资料以均数±标准差表示。对于实验组、对照组与空白对照组的对比以及对于实验组与对照组的对比均采用t检验进行分析,检验水准P<0.05。
2 结果
96 h的恒温浸泡之后,在所有10个未加入金属试件的实验组、对照组空白对照溶液中析出的镍离子均低于ICP-OES检出限。在对照组溶液浸泡后镍基铸造合金组测得的镍离子析出大于镍铬烤瓷合金组(P<0.05)。在加入了漱口水的实验组溶液中镍基铸造合金测得的镍离子析出大于镍铬烤瓷合金(P<0.01)。两种金属试件在实验组溶液中的析出均大于在对照组溶液中的析出,差异均具有统计学意义(P<0.01)。
扫描电子显微镜观察参见图1、2。

图1 浸泡实验前后镍铬烤瓷合金扫描电子显微镜图片Fig1 The scanning results of Ni-Cr porcelain fused to metal as-received and after the immersion test
镍铬烤瓷合金浸泡前,金属表面打磨痕迹连续,见一些小圆孔可能为铸造缺陷。对照组溶液浸泡后镍铬烤瓷合金表面无明确腐蚀表现。实验组溶液浸泡后,2 000倍下金属表面与对照组无明显区别,10 000倍下相较对照组显得略微粗糙、凹凸不平,有一些可疑的腐蚀点。图3中,可见浸泡前镍基铸造合金试件在2 000、10 000倍下打磨痕迹连续。对照组溶液浸泡后表面未见明显变化。实验组溶液浸泡后,2 000倍下可见金属表面均匀散在凹坑,表面粗糙。10 000倍下可见打磨痕迹断续,有浅的凹坑,出现明显的腐蚀点隙。
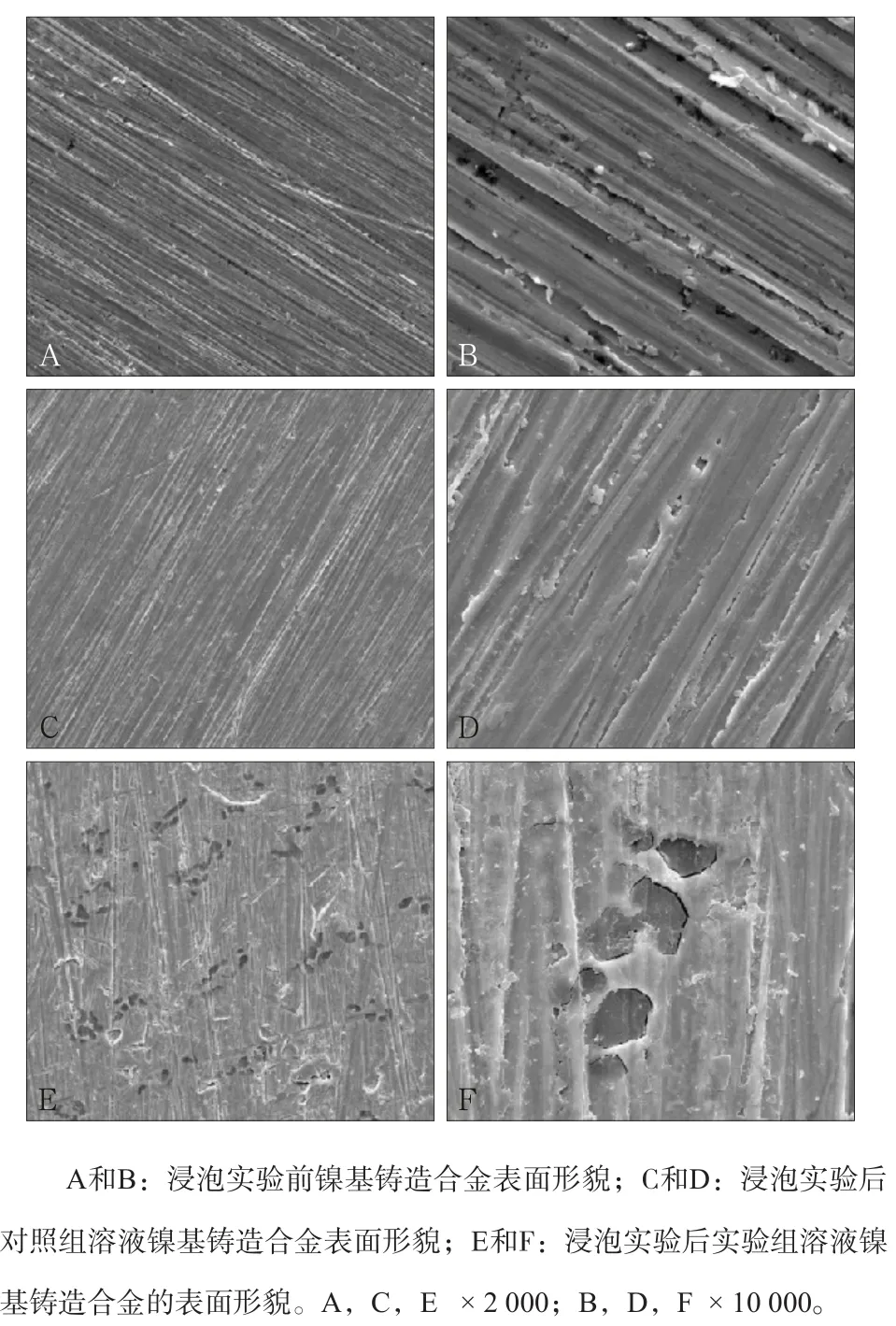
图2 浸泡实验前后镍基铸造合金扫描电子显微镜图片Fig2 The scanning results of nickel casting alloy as-received and after the immersion test
3 讨论
镍是机体生命活动所必需的微量元素,其生物学作用极为广泛[8]。镍离子本身的细胞毒性作用可对邻近组织甚至非邻近组织造成不同程度的损伤及改变。镍离子可通过修复体表面的菌斑而蓄积,达到较高浓度后可造成邻近组织的增生或炎症;镍基合金修复体在腐蚀过程中释放的镍离子可引发过敏已基本达成共识。研究[9-11]显示,镍基合金修复体可导致红斑、灼烧感、囊泡形成及味觉改变;此外,虽然没有报道将口腔修复用镍基合金和癌症联系起来,但是多种含Ni物质被认定为致癌物质。因此,避免镍基合金修复体发生腐蚀对于患者有一定临床价值。
口腔中金属材料腐蚀主要为电化学腐蚀[12]。当氢离子在阴极发生还原反应时,阳极金属溶解产生电子,从而促进电化学腐蚀的进展。故当口腔内pH降低时,口内修复体金属去极化加强,更易发生腐蚀而析出离子[13]。Mutlu-Sagesen等[14]发现几种常用烤瓷合金的离子析出与溶液pH有相关性。本研究中测得漱口水pH值为4.23,远低于正常唾液平均pH值6.8,故金属在其中更易产生离子的析出。
除低pH以外,氟化物也能增加镍离子的析出量。本研究选用的两种合金均以铬为主要成分之一,铬能在合金表面形成一层致密、稳定且能与基体结合紧密的氧化铬薄膜,使金属钝化[15],在腐蚀过程中能阻止镍的析出。但卤素阴离子可通过破坏金属表面钝化膜的方式加速合金元素的释放。有研究表明,在含氟0.05%人工唾液中浸泡后,钴铬合金和纯钛表面粗糙度较浸泡前有统计学差异。Knutson等[16]发现,暴露于含氟的液体环境对于多种正畸微种植体是不利的。在离体实验中有观察到在酸性人工唾液中加入氟化物确实增加了合金的镍离子析出。因此,可以认为漱口水中0.022%的氟化钠有促进镍离子析出的作用。
无论在对照组溶液还是含有漱口水的实验组溶液中,镍基铸造合金的镍离子析出均大于镍铬烤瓷合金。且在实验组溶液中,镍基铸造合金的镍离子析出几乎是镍铬烤瓷合金的16倍,其最大的原因可能是因为后者含有较高含量的钼。钼能不断地快速修补破坏的钝化膜,从而提高了金属的耐腐蚀性,降低了镍铬烤瓷合金中镍的析出。
离子析出的结果从扫描电子显微镜图像中可得到验证。在对照组溶液中浸泡后的两种金属表面形貌和浸泡实验前无明显区别,但经过实验组溶液浸泡的金属,其表面形貌均产生了不同程度的变化。其中,镍基铸造合金试件经过实验组溶液浸泡后,表面产生了明显的腐蚀孔隙。结合离子析出结果可认为,含有此种漱口水的溶液环境对两种镍基合金的腐蚀均有促进作用,其中又以镍基铸造合金为甚。
现实中漱口水为间断性使用,而本实验使用的是连续浸泡的方法。有文献报道,在动态pH值变化的体外实验中,两种含镍合金在酸性人工唾液浸泡后的镍离子析出均显著大于正常人工唾液浸泡的析出,且两种合金酸性加氟人工唾液浸泡的析出量均大于不加氟的酸性人工唾液浸泡组,TILITE P合金在pH值为4的人工唾液中的镍离子析出量可达正常pH人工唾液析出量的800倍左右。此外,在实际使用中,鼓漱的漱口水会对修复体表面产生冲击,并影响龈沟液中镍离子的浓度,可能会进一步影响镍离子的析出。但是,漱口水作为口腔保健用品,每天与口内修复体接触时间不超过2 min,无法确定这种动态变化的实际意义。有研究表明,使用含镍金属制作修复冠的患者口腔唾液镍离子的质量浓度在戴冠1周后有增加,但6个月后可恢复到戴冠前的水平。故在实际情况中使用漱口水对镍离子的析出有多大影响还有待更长时间深入的研究。
本研究使用以酸刺激状态下动态唾液总流率为参考配制变量严格控制的实验溶液,并使用检出限较高的ICP-OES进行析出离子的测定,探寻了一种牙科金属材料浸泡实验的方法。从实验结果可看出,在实验组混合溶液中,析出镍离子浓度均有不同程度升高,尤其是镍基铸造合金,经过浸泡实验后,其在含有漱口水的实验组溶液中镍离子浓度已是其对照组溶液镍离子浓度的30倍左右。扫描电镜观察到的结果和离子析出的结果一致。其差异可能由镍铬烤瓷合金中含有的钼造成。但是引入酸刺激增加唾液流速来配制实验溶液的新方法与传统方法是否有差异,实际生活中此类漱口水的使用对口内含镍合金修复体镍离子的析出究竟有多大影响还有待进一步探究。
4 参考文献
[1]Wataha JC,Drury JL,Chung WO.Nickel alloys in the oral environment[J].Expert Rev Med Devices,2013,10(4):519-539.
[2]Muris J,Goossens A,Gonçalo M,et al.Sensitization to palladium and nickel in Europe and the relationship with oral disease and dental alloys[J].Contact Derm,2015,72(5):286-296.
[3]Büyüköztürk S,Gelincik A,Ünal D,et al.Oral nickel exposure may induce TypeⅠ hypersensitivity reaction in nickel-sensitized subjects[J].Int Immunopharmacol,2015,26(1):92-96.
[4]Pazzini CA,Marques LS,Ramos-Jorge ML,et al.Longitudinal assessment of periodontal status inpatients with nickel allergy treated with conventional and nickel-free braces[J].Angle Orthod,2012,82(4):653-657.
[5]Iijima M,Yuasa T,Endo K,et al.Corrosion behavior of ion implanted nickel-titanium orthodontic wire in fluoride mouth rinse solutions[J].Dent Mater J,2010,29(1):53-58.
[6]Robin A,Meirelis JP.Influence of fluoride concentration and pH on corrosion behavior of Ti-6Al-4V and Ti-23Ta alloys in artificial saliva[J].Mater Corrosion,2007(3):173-180.
[7]Aung EE,Ueno M,Zaitsu T,et al.Effectiveness of three oral hygiene regimens on oral malodor reduction: a randomized clinical trial[J].Trials,2015,16:31.
[8]Ragsdale SW.Nickel biochemistry[J].Curr Opin Chem Biol,1998,2(2):208-215.
[9]Wataha JC,O’Dell NL,Singh BB,et al.Relating nickel-induced tissue inflammation to nickel release in vivo[J].J Biomed Mater Res,2001,58(5):537-544.
[10]Elshahawy WM,Watanabe I,Kramer P.In vitro cytotoxicity evaluation of elemental ions released from different prosthodontic materials[J].Dent Mater,2009,25(12):1551-1555.
[11]Thyssen JP,Menné T.Metal allergy—a review on exposures,penetration,genetics,prevalence,and clinical implications[J].Chem Res Toxicol,2010,23 (2):309-318.
[12]Loch J,Łukaszczyk A,Augustyn-Pieniążek J,et al.Electrochemical behaviour of Co-Cr and Ni-Cr dental alloys[J].Solid State Phenomena,2015(227):451-454.
[13]Esquivel-Upshaw JF,Dieng FY,Clark AE,et al.Surface degradation of dental ceramics as a function of environmental pH[J].J Dent Res,2013,92(5):467-471.
[14]Mutlu-Sagesen L,Ergun G,Karabulut E.Ion release from metal-ceramic alloys in three different media[J].Dent Mater J,2011,30(5):598-610.
[15]Benyahia H,Ebntouhami M,Forsal I,et al.Corrosion resistance of NiTi in fluoride and acid environments[J].Int Orthod,2009,7(4):322-334.
[16]Knutson KJ,Berzins DW.Corrosion of orthodontic temporary anchorage devices[J].Eur J Orthod,2013,35(4):500-506.
(本文编辑骆筱秋)
Comparative study on nickel release of two dental nickel alloys in mouth wash
Tian Taoran,Zhang Yanggen,Huang Xinqi,Li Longbiao,Zhang Xinxi,Zhu Zhuoli.(State Key Laboratory of Oral Diseases,West China Hospital of Stomatology,Sichuan University,Chengdu 610041,China)
This study was supported by the Science Foudation of Sichuan Medical Association(S15061).
[Abstract]ObjectiveThis study aims to investigate the release of nickel from two nickel alloy specimens for dental prosthesis in a commercial mouth wash through a constant immersion experiment.Methods Standard samples were casted from two different alloys and ground to achieve the same roughness.For our experimental group,one-half of the samples are immersed in a solution composed of artificial saliva and commercial mouthwash.For our control group,the other half of the samples are placed in a solution containing artificial saliva and distilled water.This procedure is performed at (37± 1) °C for 96 h.The amount of Ni ion released after the 96 h immersion test and the changes in the surfaces of the alloys asreceived and upon immersion are then determined by using an inductively coupled plasma optical emission spectrometer (ICP-OES) and a scanning electron microscope.Results The amount of released Ni ion is below the minimum detection limit of ICP-OES in the blank solution without the alloys.More ions are released from the Ni-casted alloy than from the Ni-Cr porcelain fused to a metal in the experimental group and the control group.The ions released from each alloy are also significantly different in the two solutions.Conclusion The tested commercial mouthwash accelerates the release of Ni ion from the two nickel alloys.This phenomenon is more significant in the nickel-casted alloy than in the other alloy type.
[Key words]mouth wash;dental alloy;immersion;nickel
[收稿日期]2015-12-01;[修回日期]2016-02-13
[基金项目]四川省医学会科研课题(S15061)
[作者简介]田陶然,硕士,Email:tiantrcd@163.com
[通信作者]朱卓立,讲师,博士,Email:zzl7505@126.com
[中图分类号]R 783
[文献标志码]A[doi] 10.7518/gjkq.2016.03.006

