胶体金核壳型沙丁胺醇分子印迹聚合物的光谱特征分析
任慧鹏,管毓渝,戴荣华,刘国艳,柴春彦
上海交通大学农业与生物学院, 上海 200240
胶体金核壳型沙丁胺醇分子印迹聚合物的光谱特征分析
任慧鹏,管毓渝,戴荣华,刘国艳,柴春彦*
上海交通大学农业与生物学院, 上海 200240

沙丁胺醇; 核壳型分子印迹物; 红外光谱; 扫描电镜; 快速检测
引 言
沙丁胺醇(salbutamol, SAL), 是众多非天然β-受体激动剂中的一种,促进动物肌肉组织的生长,进而提高瘦肉率[1]。自2002年起农业部严令禁止在动物养殖过程中使用SAL, 但仍有一些企业将SAL作为盐酸克伦特罗的替代品违法使用。滥用SAL会造成其在畜禽产品中残留过量,进而对消费者的安全和健康造成很大的威胁。建立完善的检测方法是控制SAL滥用的关键环节之一。目前,检测SAL的方法主要有HPLC[2],LC-MS[3]以及GC-MS[4]等色谱分析技术,也有基于免疫学技术的ELISA方法等[5]。其中GC-MS是检测SAL的确证性方法,应用最为普遍[6]。色谱法和免疫学技术均需要对样品进行繁琐的前处理,检测时间长,需要专门的仪器设备和专业分析人员才能完成。目前,食品安全控制机构需要检测的SAL样品数量庞大,亟需高效并适合于现场快速检测的新技术和新方法。而将传感技术与分子印迹技术结合,有望实现SAL的快速现场检测[7-8]。本工作采用沉淀聚合的方法合成常规SAL-MIPs,并以胶体金粒子为引发核制备核壳型SAL-MIPs。通过紫外和红外光谱等技术来分析它们的光谱学特征,以评价两种印迹物对目标分子的特异性识别能力,以期为建立基于分子印迹技术快速检测SAL的传感方法奠定基础。
1 实验部分
1.1 试剂与仪器
试剂: 沙丁胺醇标准品(SAL)购于中国检验检疫研究院; 氯金酸、柠檬酸钠、二甲基丙烯酸乙二醇酯(EGDMA)、甲基丙烯酸(MAA)、偶氮二异丁腈(AIBN)、二甲亚砜(DMSO)等试剂均为分析纯,购于中国医药集团; 实验用水为双蒸水。
仪器: EQUINOX-55 傅里叶变换红外光谱仪(Nicolet6700,ThermoFishe, American), 色散型显微拉曼光谱仪(SENTEARA R200, Bruker, Germany),UV1800PC紫外-可见分光光度计( Shimadzu, Japan), XMTD-204 电热恒温水浴锅(上海一恒实验设备有限公司), RS-120 超声波仪(上海瑞胜仪器仪表有限公司),索氏提取器( 泰州市科创实验设备有限公司)。
1.2 常规沙丁胺醇分子印迹聚合物(MIPs)和非印迹聚合物(NIPs)的制备
取SAL 0.239 3 g、MAA 0.258 3 g溶于2.34 mL DMSO中超声15 min并放置4 h进行预聚合。加入EGDMA 3.772 0 g, AIBN 0.032 8 g, 超声混合均匀。混合液进行氮吹排氧15 min, 完全密封后80 ℃ 水浴24 h, 得白色坚硬致密聚合物。将该聚合物置于研钵充分研磨, 用丙酮冲洗沉降,过滤得到粒径均匀的粉末状物质。将粉末中丙酮蒸干,放置于索氏提取器底部, 在下端固定在水浴锅中的烧瓶里加入体积比为9∶1的甲醇-乙酸溶液洗脱48 h。用甲醇洗去乙酸, 60 ℃干燥后得到MIPs。
制备NIPs时不加入作为模板分子的SAL, 其他步骤与制备MIPs相同。
1.3 胶体金核壳型沙丁胺醇分子印迹聚合物(MIPs)和非印迹聚合物(NIPs)的制备
1.3.1 金溶胶的制备
将1 mL质量分数为1%的氯金酸和25 mL蒸馏水加入圆底烧瓶,烧瓶加热并在上面连接冷凝装置。待烧瓶中液体沸腾时加入质量分数1%的柠檬酸溶液2.85 mL,继续加热。自溶液从黑色变为透明的红色时开始计时。计时15 min后取下烧瓶。将最终得到红色透明的金溶胶溶液置于4 ℃冰箱中保存备用。
1.3.2 胶体金核壳型SAL分子印迹聚合物的制备
取119 mL金溶胶于圆底烧瓶, 加入适量酒精再加入24 mg SAL, 室温震荡30 min。再加入25.8 mg MAA,234 μL DMSO,将上述混合物超声30 min使分散均匀, 放置4 h进行预聚合。在预聚合液中加入396.4 mg EGDMA, 3.28 mg AIBN。超声混合至溶液分布均一后, 充氮排氧15 min。将圆底烧瓶密闭,置于60 ℃水浴锅中24 h得浅蓝色絮状悬浊液。将液体过滤后获得的絮状沉淀烘干。用滤纸将烘干后的物质包封严实, 置于索氏提取器底部, 以甲醇∶乙酸(V∶V=9∶1)在提取器中80 ℃洗脱48 h。取出洗脱后的粉末,用甲醇洗涤除去乙酸,再次烘干即得胶体金核壳型SAL-MIPs,将该印迹物放在4 ℃冰箱保存。
非胶体金核壳型SAL-MIPs制备除了不加SAL外,其他操作与胶体金核壳型沙丁胺醇印迹聚合物完全相同。
1.4 两种沙丁胺醇印迹聚合物的形貌表征
用低真空超高分辨率扫描电镜(LV-SEM)分别分析两种印迹物的微观形貌。扫描电压: 5.0 kV; 放大倍数: 10 000 倍,扫描模式: vCD。
1.5 紫外吸收光谱分析
1.5.1 SAL(模板分子)与MAA(功能单体)预聚合液的紫外吸收光谱分析
各取1 mL浓度为0.1 mmol·L-1SAL-二甲亚砜溶液,置于编号为1~4的PVC管中。在1,2,3,4号管中分别加入浓度为的0, 0.2, 0.6和1.0 mmol·L-1的MAA-二甲亚砜溶液各1 mL。超声处理使溶液混合充分, 静置预聚合4 h。对SAL-MAA混合溶液进行紫外吸收测定,参比溶液未加SAL,其他处理相同。
1.5.2 金溶胶的紫外光谱分析
取1 mL制备成功的金溶胶,以蒸馏水为参照测定其紫外吸收图谱。
1.6 两种印迹物的傅里叶红外光谱分析
确认样品均完全干燥后,参照KBr压片法,分别取5 mg MIPs,NIPs和胶体金核壳型MIPs进行样品前处理, 在400~4 200 cm- 1范围测定红外光谱。
1.7 两种印迹物拉曼光谱分析
取10 mg洗脱后的MIPs和NIPs及胶体金核壳型MIPs, 在0~3 500 cm- 1范围内,785 nm激发波长处进行共聚焦拉曼检测。

Fig.1 Scanning electron microscopy (SEM) images of NIPs (a) and MIPs (b), ×10 000

Fig.2 Scanning electron microscopy (SEM) images of karyotype of colloidal gold MIPs without eluting (a) and eluted karyotype of colloidal gold MIPs (b), ×10 000
2 结果与讨论
2.1 沙丁胺醇印迹聚合物的形貌表征
沙丁胺醇印迹聚合物的形貌表征如图1和图2所示。
2.2 沙丁胺醇与甲基丙烯酸预聚合液的紫外吸收光谱特征
沙丁胺醇(模板分子)与甲基丙烯酸(功能单体)预聚合液的紫外吸收光谱如图3所示。
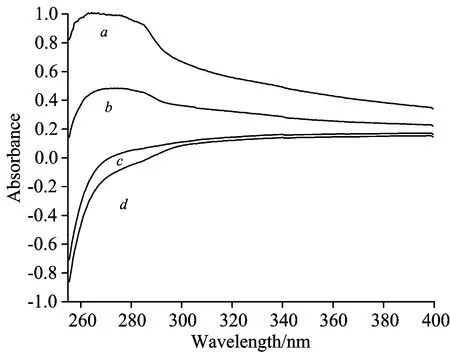
Fig.3 UV adsorption spectra of salbutamol (template molecule) and MAA (functional monomers)system in DMSO solution
a0(sal)=0.1 mmol·L-1;
b0(MA)/mmol·L-1=a: 1.0;b: 0.6;c: 0.2;d: 0
SAL分子是由带羟基、羟甲基的苯环和叔丁氨基组成的醇类, 其共轭系统的特征吸收峰在275 nm附近。从紫外吸收光谱的特征分析SAL与MAA的相互作用, 计算SAL和MAA形成的主客体配合物的配位比和结合常数。由图3可见, 当溶剂中MAA浓度逐渐升高时, SAL分子的吸收波长也随之出现红移现象,最大吸收波长数值不断增大,在图中表现为吸收峰向长波长方向平移。出现此现象的原因可能是MAA作为质子供体,跟SAL的生色基团发生作用形成氢键。SAL的最大吸收波长变化产生部分能量损失,这些能量损失参与氢键形成。

Fig.4 UV adsorption spectra of colloidal gold
设主体SAL的浓度为a0, 客体MAA浓度为b0, 化学配位比为n, 则结合反应如下
sal+nMAA=sal[MAA]n
(1)
K={sal[MAA]n}/[sal][MAA]n
(2)
根据物料平衡[sal]+{sal[MAA]n}=a0
[MAA]+{sal[MAA]n}=b0
(3)
因为b0远大于a0, 可忽略{sal[MAA]n}, 所以
[MAA]≈b0
(4)
将式(3)和式(4)代入式(2)得
(5)
假设溶液中发生吸收的物质只有sal与sal[MAA]n, 将SAL和配合物的摩尔吸收系数分别设为ε1和ε2, 由Lamber-Beer定律可知总吸光度为
A=ε1l[sal]+ε2l{sal[MAA]n}
=ε1l(a0-{sal[MAA]n}) +ε2l{sal[MAA]n}
=(ε2-ε1)l{sal[MAA]n}+ε1la0
(6)
令A0=ε1la0, 则吸光度的变化为
ΔA=A-A0=(ε2-ε1)l{sal[MAA]n}=Δεl{sal[MAA]n}
(7)
将式(7)代入式(5)得
(8)

从图4胶体金的紫外吸收光谱可以看到,金原子的紫外特征吸收峰非常明显,在512 nm附近。可知金原子具有稳定优良的光谱学特征,适合做引发核来制备更疏松、吸附能力更好的核壳型分子印迹物。
2.3 印迹聚合物及相关物质化学基团的红外光谱特征

Fig.5 IR spectra of salbutamol

Fig.6 IR spectra of MIP without eluting a and salbutamol b
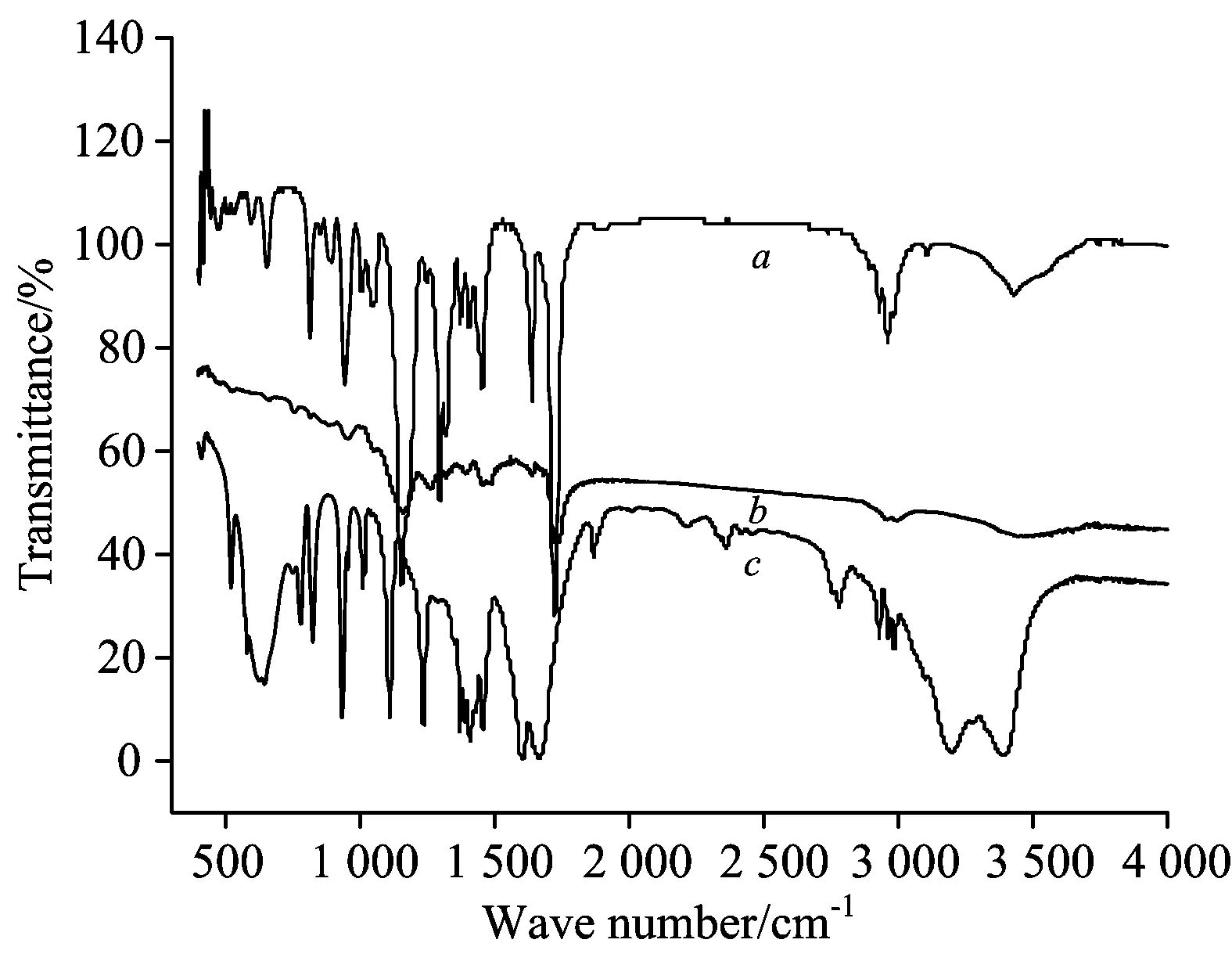
Fig.7 IR spectra of EGDMA a,MIPs without eluting b, MA c
2.4 MIPS和NIPS拉曼光谱特征


Fig.8 IR spectra of eluted MIPs a and NIPs b

Fig.9 IR spectra of karyotype of colloidal gold MIPs without eluting a and eluted MIPs b
图11为已洗脱和未洗脱胶体金核壳型MIPs的拉曼光谱,可以看到它们之间存在明显差异。未洗脱的核壳型MIPs中振动模增加,使几乎所有的特征峰峰宽都显著增加,最终叠加为图中所示。当把SAL去除掉以后,各化学键恢复正常,峰型和峰宽也与红外光谱峰对应。由此可知合成胶体金核壳型MIPs的过程与合成普通MIPs的过程相比,前者中各化合物在形成网状结构时大部分化学键发生了显著变形,这也是最终形成松散结构的另一影响因素。
在实验中使用本体聚合技术,顺利合成SAL-MIPs。此方法操作方便,易于普及。此外,SAL洗脱简单, 表明预聚合液中SAL与MA形成容易洗脱的1∶1型氢键主客体配合物,而结合常数K=-0.245×106L2·mol-2又说明它们以相对稳定的非共价方式结合, 这也验证了相关报道中的结论[11]。

Fig.11 Raman spectrum of karyotype of colloidal gold MIPs without elutingaand eluted karyotype of colloidal gold MIPsb
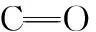
拉曼光谱图10中MIPs和NIPs中峰型基本相同但强度不同,是因为两者均存在吸收峰比较明显的相似官能团。但是,SAL分子中叔丁氨基的N原子通过氢键与MAA的羧基结合,进而产生识别位点。待SAL与交联剂EGDMA、引发剂AIBN按特定比例混合后, 聚合物中就会出现一些被交联固定的具有特异性识别作用的位点[12]。在印迹聚合物加热洗脱的过程中,作为模板分子的SAL被洗脱,在印迹聚合物中留下了一定尺寸的空穴结构,这些空穴的大小形状、化学结构、产生作用的位置等都可与SAL匹配,这是该印迹聚合物对SAL有特异选择性的原因之一[13]。另外, 印迹聚合物洗脱后形成的孔穴中,一部分分布在其中的官能团排列比较特异,这些官能团与SAL之间存在氢键非共价结合作用,产生特异识别SAL的作用位点[14]。氢键产生的作用力比静电产生的作用力更强,因此具有较强的结合能力; 而相对于共价键,氢键的结合能力又比较弱,所以模板分子更容易被去除,分子印迹聚合物的选择作用也因而提高。以氢键等非共价类型结合的MIP适应范围比较广泛[15],生物相容性也比较好,选择性优良,其识别性能也具有较大的应用潜力。
胶体金的生化性质和物化性质都较为独特, 其中的金原子很容易使化合物以它为核包绕络合形成分子印迹物。由于此类金核的存在,分子印迹物不断向外延展生长,最后形成松散、表面均一、空穴较多的结构。在这种结构的基础上,再结合普通分子印迹物的生物相容性和选择性等优点,胶体金核壳型分子印迹物将在生物传感检测方面具有更广阔的应用前景。
3 结 论
对SAL的分子印迹物(MIPs)进行光谱分析结果表明SAL和MAA生成的聚合物为主客体配合物类型,结合方式为氢键键合。将MIPs洗脱模板分子后留下含有特定类型官能团,化学结构及空间分布均与SAL高度匹配的空穴结构, 可与待测液中的目标分子SAL发生特异识别和专一结合作用。以金溶胶中的纳米金为核形成的胶体金核型分子印迹物不但具有普通分子印迹物的各种优点,其本身也有更加疏松的结构和更多产生特异识别作用的空穴。这样的疏松结构在吸附时能够提供更大的接触面积,更有利于目标分子与空穴中对应的官能团结合,从而弥补了普通分子印迹物在高浓度样品溶液中结合能力有限的问题,因而其具有更优良的检测效能。这也为建立基于分子印迹技术的快速检测SAL新方法奠定了理论和实践基础。
[1] JIANG Chen-lu,LI Lin(姜琛璐,李 林). Modern Preventive Medicine(现代预防医学),2013, 2: 227.
[2] LI Wei-hong, DAI Ting-can, XIONG Yan(李伟红, 戴廷灿, 熊 艳). Acta Agriculturae Jiangxi(江西农业学报), 2007, 19(3): 102.
[3] Lee H B, Sarafin K, Peart T E. J. Chromatogr. A, 2007, 1148: 158.
[4] Bocca B, Fiori M, Cartoni C, et al. Journal of AOAC International, 2003, 86: 8
[5] SUN Hai-xin, LING Hong-li, WANG Lei, et al(孙海新,凌红丽,王 雷,等). Chinese Journal of Animal Quarantine(中国动物检疫),2009, 12: 44.
[6] CHEN Xiao-shui, HOU Hong-wei, BIAN Zhao-yang, et al(陈晓水,侯宏卫,边照阳,等). Journal of Chinese Mass Spectrometry Society(质谱学报),2013, 34(5): 308.
[7] QI Yu-bing,LIU Ying,SONG Qi-jun(齐玉冰,刘 瑛,宋启军,等). Chinese Journal of Analytical Chemistry(分析化学),2011, 39: 1053.
[8] Xu Z X, Fang G Z, Wang S. Food Chemistry, 2010, 119(2): 845.
[9] Yang J, Zhu X L, Cai J B, et al. Anal. Bioanal. Chem., 2006, 384(3): 761.
[10] WEN Li-rong,LI Ming,ZHAO Gui-long(文丽荣,李 明,赵桂龙). Chinese Journal of Spectroscopy Laboratory(光谱实验室),2004, 21(2): 244.
[11] Qi Liang-deng,Yan Li-li, LI Hua-zhang, et al. Chinese Chemical Letters, 2011, 24: 1351.
[12] ZHANG Jin, XU Lan, WANG Ya-qiong, et al(张 进,徐 岚,王亚琼,等). Chinese Journal of Analytical Chemistry(分析化学),2009,37(7): 1041.
[13] GAO Xia, FAN Jing, WANG Xiao-long,et al(高 霞,樊 静,王小龙,等). Acta Chimica Sinica(化学学报),2013, 71: 1411.
[14] WANG Ying,LI Nan(王 颖,李 楠). Chemical Industry and Engineering Progress(化工进展), 2010, 29(12): 2315.
[15] Mayes A G, Whitcombe M J. Advanced Drug Delivery Reviews, 2005,57: 1742.
Spectroscopic Study of Salbutamol Molecularly Imprinted Polymers
REN Hui-peng, GUAN Yu-yu, DAI Rong-hua, LIU Guo-yan, CHAI Chun-yan*
School of Agriculture and Biology, Shanghai Jiao Tong University, Shanghai 200240, China

Salbutamol; Core-shell molecularly imprinted polymers; Infrared spectra; Scanning electron microscopy; Rapid detection
Nov. 24, 2014; accepted Mar. 28, 2015)
2014-11-24,
2015-03-28
国家自然科学基金项目(31372344)资助
任慧鹏,女,1990年生,上海交通大学农业与生物学院硕士研究生 e-mail: 826665647@qq.com *通讯联系人 e-mail: cychai88@hotmail.com
O657.3
A
10.3964/j.issn.1000-0593(2016)02-0372-07
*Corresponding author

