贯叶连翘引种驯化过程中生理生化特性、活性物质含量及抗氧化能力的变化
康霞,葛莉,栗孟飞*,甘延太*,李京耀,王克鹏
(1.甘肃农业大学农学院,甘肃 兰州730070;2.甘肃省干旱生境作物学重点实验室,甘肃农业大学生命科学与技术学院,甘肃 兰州730070;
3.甘肃省康县中药材技术指导站,甘肃 康县746500;4.甘肃农业大学资源与环境学院,甘肃 兰州730070)
贯叶连翘引种驯化过程中生理生化特性、活性物质含量及抗氧化能力的变化
康霞1,葛莉2,栗孟飞2*,甘延太1*,李京耀3,王克鹏4
(1.甘肃农业大学农学院,甘肃 兰州730070;2.甘肃省干旱生境作物学重点实验室,甘肃农业大学生命科学与技术学院,甘肃 兰州730070;
3.甘肃省康县中药材技术指导站,甘肃 康县746500;4.甘肃农业大学资源与环境学院,甘肃 兰州730070)
摘要:为了探明贯叶连翘引种驯化过程中生长适应能力以及活性物质的变化,以野生和栽培盛花期植株为材料,分别对生理生化特性、活性物质含量以及抗氧化能力进行了测定与分析,结果表明,栽培贯叶连翘的净光合速率、蒸腾速率、气孔导度、叶绿素含量和根系活力均高于野生植株,尤其是其盛花期和地上部分干重分别较野生植株提前了7 d和提高了16.67%。总黄酮和金丝桃素含量在栽培和野生植株同一器官中无显著差异;总酚类在野生花中的含量显著高于栽培花,而叶中的含量则相反;野生和栽培植株各器官中,总黄酮和酚类化合物含量在叶和花中的含量显著大于茎,而金丝桃素的含量表现为花>叶>茎。野生和栽培各器官抗氧化能力为叶>花>茎,其中,野生和栽培叶、茎提取液的抗氧化能力无显著差异,而栽培花的抗氧化能力显著大于野生花。以上研究结果表明,贯叶连翘野生转栽培后,不仅具有较好的生长适应能力,而且主要活性物质的积累量及抗氧化能力并未显著降低。该研究结果将对贯叶连翘种植栽培以及保护野生资源具有重要的参考价值和实践意义。
关键词:贯叶连翘;野生和栽培;生理生化特性;总黄酮和酚类;金丝桃素;抗氧化能力
贯叶连翘(Hypericumperforatum),又名贯叶金丝桃、圣·约翰草(St. John’s wort),为藤黄科(Guttiferae)金丝桃属(Hypericum)多年生草本植物,主要分布于我国甘肃、陕西、新疆、四川等地,株高20~100 cm,根系发达;茎直立,多分枝;叶无柄,披针形或长椭圆形;聚伞花序,生于茎及分枝顶端;蒴果卵珠状,种子黑褐色;花期5-7月,果期7-9月。传统中医认为,贯叶连翘具有抗菌消炎、收敛止血、调经活血、消肿止痛之功效,主要集中于镇静、抗炎、伤口愈合等方面[1]。现代药理学研究表明,贯叶连翘具有抗抑郁、抗癌、抗病毒、抗氧化、镇痛等作用[2-4]。由于贯叶连翘独特的药理学作用,目前已成为全球研究开发的热点草药之一[1,5]。
到目前为止,金丝桃素主要从野生贯叶连翘植株中提取分离,随着市场对金丝桃素需求的逐渐增加,使得野生贯叶连翘资源过度被采挖[6-7]。报道称,贯叶连翘除了含有金丝桃素外,还含有苯丙烷类、黄酮类、花青素、间苯三酚、挥发油等活性物质[8-9]。为了满足市场对金丝桃素的需求,很多学者从原料采集时期、提取分离效率、细胞组织培养等方面进行了大量研究[10-12];更为重要的是,为了解决活性物质提取原料问题,贯叶连翘的野生转栽培技术研究势在必行[13],在这一方面,很多学者开展了贯叶连翘引种驯化栽培、快速繁殖等方面的研究[14-15];但在引种驯化栽培过程中,生理生化特性以及活性物质变化方面的研究国内外报道甚少。杭悦宇等[13]报道称,栽培贯叶连翘的生物量、开花的一致性和生长的适应性等明显优于野生贯叶连翘,且金丝桃素含量亦达到野生贯叶连翘的水平。为了进一步探明贯叶连翘野生转栽培后的生长适应能力以及活性物质的变化,本研究就贯叶连翘引种驯化过程中生理生化特性(光合特性、叶绿素含量、根系活力等)、主要活性物质(黄酮类、酚类、金丝桃素)含量以及抗氧化能力进行了测定与分析,旨在为加快贯叶连翘种植栽培及推广以及保护野生资源提供理论基础和技术参考。
1材料与方法
1.1实验材料
野生贯叶连翘采自甘肃省陇南市康县岸门口镇中节村附近山林及沟边,栽培贯叶连翘采自甘肃省陇南市康县岸门口镇中节村甘肃省中药材野生贯叶连翘引种驯化示范区,实验材料于贯叶连翘盛花期采集,主要有植株上半部分茎、叶、花3个器官以及地下生长旺盛的根系组织,采集后立即带回实验室;地上部分阴干后保存备用,根系部分立刻进行活性测定。实验在甘肃农业大学干旱生境作物学重点实验室进行。
1.2实验方法
1.2.1生理生化指标的测定参考孙位等[16]光合指标测定方法,挑取生长基本一致的野生和栽培贯叶连翘20株,从上至下第5~6片叶,于2015年5月30日(无风晴天)上午9:00-11:00,进行光合指标的测定,当时光照强度为1280~1330 lx,大气温度为23~25℃。光合指标的测定使用便携式光合荧光系统测定仪(LI-6400XT,美国),测定光合指标包括净光合速率、蒸腾速率、气孔导度和胞间CO2浓度。叶绿素含量的测定采用乙醇-丙酮-水混合液提取测定的方法,根系活力的测定采用TTC法[17]。
1.2.2提取液的制备取阴干的材料,研碎后过178 μm筛,准确称取3.0 g粉末,置于70 mL 70%无水乙醇具塞三角瓶中,室温、黑暗、120 r/min旋转振荡提取7 d;然后在4℃、5000 r/min条件下离心10 min;上清液在80℃条件下减压蒸发浓缩至小体积;浓缩液用90%甲醇溶解并定容至50 mL,置于4℃冰箱中保存,备用。
1.2.3总黄酮含量的测定采用亚硝酸钠—硝酸铝—氢氧化钠法测定总黄酮化合物的含量,参考Ma等[18]的方法测定。具体步骤为:吸取1.2.2中提取液400 μL置于试管中,依次加入2.0 mL ddH2O和0.3 mL 5% NaNO2,混合振荡5 min后,加入0.3 mL 10% AlCl3,混合振荡1 min后,加入2.0 mL 1 mol/L NaOH,充分混合后,在 510 nm下测定反应液的吸光值A,以不加样品溶液的为空白对照,重复3次。总黄酮化合物的含量以儿茶素(catechin, CE)为标准品标定,计算公式为:
总黄酮含量(CE, mg/g DW)=C×V/M
标准曲线方程C(CE, mg/mL)=1.600A+0.070(R2=0.953)
式中,C为儿茶素的浓度(mg/mL),V为提取液的体积(mL),A为样品的吸光值,M为贯叶连翘材料的干物质重量(g)。
1.2.4总酚类含量的测定采用福林酚(Folin-Ciocalteu)试剂法测定总酚类化合物的含量,参考Beato等[19]的方法测定。具体步骤为:吸取1.2.2中提取液400 μL置于试管中,依次加入2.0 mL 10% Folin-Ciocalteu和1.0 mL 7.5% Na2CO3,混合振荡5 min后,置于水浴锅中37℃下避光反应1 h,取出在760 nm下测定反应液的吸光值A,以不加样品溶液的为空白对照,重复3次。总酚类化合物的含量以没食子酸(gallic acid, GAE)为标准品标定,计算公式为:
总酚含量(GAE, mg/g DW)=C×V/M
标准曲线方程C(GAE, mg/mL)=0.437A-0.043(R2=0.992)
式中,C为没食子酸的浓度(mg/mL),V为提取液的体积(mL),A为样品的吸光值,M为贯叶连翘材料的干物质重量(g)。
1.2.5金丝桃素含量的测定采用HPLC法测定材料中金丝桃素的含量,参考吴畏等[20]的方法测定。具体步骤为:将1.2.2中提取液用0.22 μm有机滤膜过滤,色谱柱为C18(150 mm×4.6 mm, 5 μm),流动相为甲醇∶水(85∶15,氨水调pH 9.5),流速1.0 mL/min,柱温35℃,检测波长588 nm,进样量20.0 μL。每个实验重复3次。以金丝桃素(sigma,纯度>95%,HPLC,货号56690)为对照品。首先,用90%甲醇配制10.0 μg/mL的金丝桃素溶液;然后,采用梯度浓度稀释法分别获得5.0,2.0,1.0,0.5,0.25 μg/mL的低浓度溶液;以峰面积(Y)对检测浓度(C, μg/mL)进行回归计算,得到标准品金丝桃素的标准方程分别为Y=48246C+1071 (R2=0.994),说明金丝桃素在0.25~10.0 μg/mL范围内与峰面积积分值呈线性关系。样品中金丝桃素的含量计算公式为:
金丝桃素含量(mg/g DW)=(C×V)/(M×1000)
式中,C为金丝桃素的浓度(μg/mL),V为提取液的体积(mL),M为贯叶连翘材料的干物质重量(g)。
1.2.6抗氧化能力的测定采用铁离子还原/氧化能力(ferric reducing/antioxidant power, FRAP)法测定有机活性物质总抗氧化能力,参考Benzie和Strain[21]及Li等[22]的方法测定。具体步骤为:吸取1.2.2中提取液100 μL加到提前制备好的3000 μL FRAP 溶液中(要求现配现用,配制方法为:取10倍体积的乙酸盐缓冲液,pH 3.6;1体积 10 mmol/L 2,4,6-三(2-吡啶基)三嗪[2,4,6-tris (2-pyridyl)-s-triazine, TPTZ]的40 mmol/L HCl溶解液,1体积的20 mmol/L FeCl3·6H2O,三者混合均匀),水浴锅中37℃反应4 min后,取出在593 nm下测定反应液的吸光值A(以不加样品溶液为参比对照,吸光值A0;以70%无水乙醇为空白对照),以500 μmol/L抗坏血酸90%甲醇溶液为阳性对照。每个实验重复3次,样品溶液的抗氧化能力以500 μmol/L Fe2+(FeSO4·7H2O) 为参比基础,计算公式为:
FRAP值(μmol/L)=[(A样品-A参比)/ (AFeSO4·7H2O-A参比)]×500(μmol/L)
1.3统计与分析
每个实验重复3次,采用Microsoft Office Excel 2007和SPSS 11.5软件进行数据处理与统计分析。
2结果与分析
2.1野生和栽培贯叶连翘的生理生化特性
由表1可知,栽培贯叶连翘的净光合速率、蒸腾速率和气孔导度分别较野生植株高9.85%,87.13%和8.33%;而胞间CO2浓度则相反,栽培植株相对于野生植株降低了6.49%。栽培植株的叶绿素含量和根系活力均高于野生植株,分别提高了18.88%和24.77%。栽培植株的盛花期为5月30日,而野生植株的盛花期为6月6日,前者的盛花期较后者提前了7 d。而且相同的生长条件下,贯叶连翘的生物量也明显提高,栽培植株的地上部干重较野生植株提高了16.67%。
2.2野生和栽培贯叶连翘不同器官中总黄酮化合物含量
由图1可知,在野生和栽培茎、叶和花3个器官中,叶和花中总黄酮化合物的含量均显著高于茎,而叶与花二者之间无显著性差异(P<0.05)。此外,同一器官中总黄酮化合物含量在野生和栽培植株之间并无显著性差异。
2.3野生和栽培贯叶连翘不同器官中总酚类化合物含量
由图2可知,在野生植株的茎、叶和花3个器官中,总酚类化合物的含量大小依次为花>叶>茎,且差异显著;在栽培植株中,叶和花中总酚类化合物的含量均显著高于茎,而叶与花二者之间无显著性差异(P<0.05)。尽管栽培植株茎中总酚类化合物的含量与野生植株间无显著差异,但其叶中比野生植株显著高出22%,而花中则显著降低,仅为野生植株的80.91%。

表1 野生和栽培贯叶连翘生理生化特性的比较
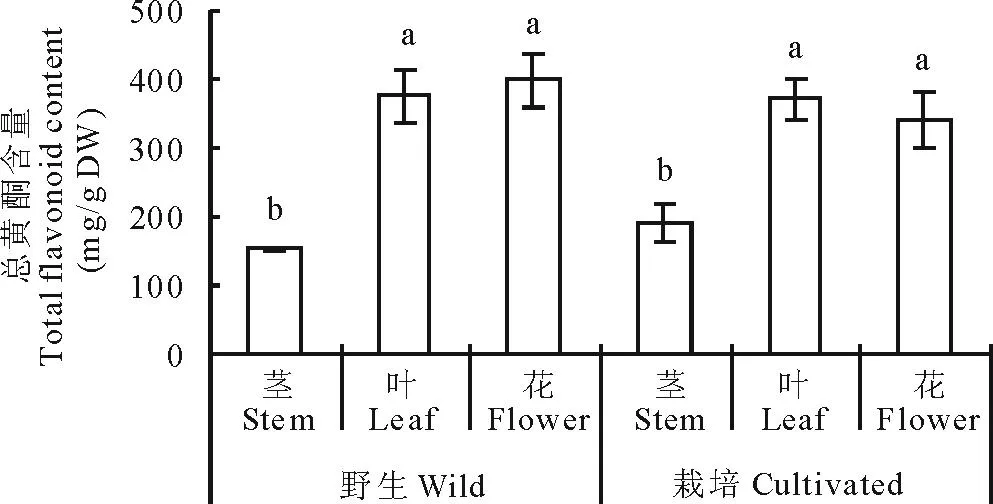
图1 野生和栽培贯叶连翘不同器官中总黄酮化合物的含量Fig.1 Total flavonoid content in different organs of wild and cultivated H. perforatum

图2 野生和栽培贯叶连翘不同器官中总酚类化合物的含量Fig.2 Total phenolic content in different organs of wild and cultivated H. perforatum
不同小写字母表示在P<0.05水平下达到显著性差异,下同。Different lowercases indicate significant differences atP<0.05 level, the same below.
2.4野生和栽培贯叶连翘不同器官中金丝桃素含量
由图3可知,在野生和栽培茎、叶和花3个器官中,金丝桃素的含量大小依次为花>叶>茎,且差异显著;野生和栽培花中金丝桃素含量分别为各自叶、茎的2.69,16.17倍和3.18,20.10倍;野生和栽培同一器官中无显著差异。
2.5野生和栽培贯叶连翘不同器官提取液的抗氧化能力
由图4可知,野生和栽培各器官提取液抗氧化能力均显著高于阳性对照抗坏血酸,抗氧化能力大小依次为叶>花>茎;栽培植株各器官差异显著,而野生叶抗氧化能力显著大于花和茎,但花和茎二者之间无显著差异;野生和栽培茎、叶的抗氧化能力无显著性差异,而栽培花抗氧化能力显著高出野生花的19.72%。
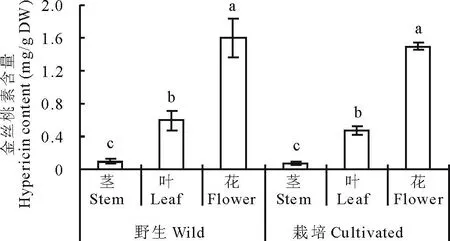
图3 野生和栽培贯叶连翘不同器官中金丝桃素的含量Fig.3 Hypericin content in different organs of wild and cultivated H. perforatum

图4 野生和栽培贯叶连翘不同器官提取液的抗氧化能力Fig.4 Antioxidant capacity of extracts from different organs of wild and cultivated H. perforatum
3讨论与结论
植物引种驯化(introduction and acclimatization)与人类的生活息息相关,有着悠久的历史,其给人类带来的利益是多方面的,比如,增加新的资源种类、以良种代替劣种、扩大栽培范围和保护珍稀濒危植物等[23]。郭巧生[24]提出,从经济原则来看,引进的药用植物无论是采用有性还是无性方式繁殖,只要通过栽培能正常生长并保持其原有的经济性状,即被称为引种栽培成功。本研究通过将甘肃省康县岸门口镇中节村附近山林及沟边的野生贯叶连翘栽培到附近的向阳、坡度平缓、土层深厚、疏松的砂质壤土地块,通过对其生理生化特性测定后发现,栽培贯叶连翘植株的净光合速率、蒸腾速率和气孔导度均高于野生植株,呈现为较强的光合效率,叶绿素含量和根系活力也均高于野生植株,加之栽培环境优越(比如向阳和土层深厚),最终使得盛花期较野生植株提前了7 d,地上部分干重(茎、叶和花)较野生植株提高了16.67%。以上结果初步说明本研究贯叶连翘引种驯化栽培取得成功。
李艳等[25]报道称,贯叶连翘植株中活性物质组分较为丰富,其中包括萘骈二蒽酮类(金丝桃素、伪金丝桃素、原金丝桃素等)、间苯三酚类(贯叶金丝桃素、加贯叶金丝桃素)、黄酮类(金丝桃苷、槲皮素、槲皮苷等)和其他类成分(挥发油、鞣质、原花青素等)。很多研究报道称,天然抗氧化剂越来越受人们的重视,尤其是黄酮类和酚类化合物,其在防治一些与自由基损伤相关的疾病以及在抗衰老过程中起着很重要的作用(比如癌症、冠心病、糖尿病等)[26-27]。本研究通过对野生和栽培贯叶连翘不同器官(茎、叶和花)中总黄酮、酚类化合物以及特有的化合物——金丝桃素进行了含量与抗氧化能力测定,结果发现,尽管野生植株花中总酚类的含量显著高于栽培花,而栽培叶中的含量却高于野生叶;同时,栽培和野生植株中总黄酮和金丝桃素含量在同一器官之间无显著差异;最终使得野生和栽培叶和茎提取液的抗氧化能力无显著差异,而栽培花的抗氧化能力反而显著大于野生花。朱慧芬等[23]报道称,植物引种驯化成败与否其关键要从内因(基因型)和外因(生态因子)两个方面,其中影响较大的生态因子主要有:温度、光照、湿度、土壤等。王莉等[28]报道称,植物次生代谢是植物在长期进化过程中与环境相互作用的结果,次生物质的代谢与积累易受到生长环境的影响和调控。因此,由于野生和栽培贯叶连翘在光照和土壤方面的差异,使得酚类物质含量以及抗氧化能力在某些器官中存在显著差异。
综上所述,贯叶连翘野生转栽培后,在向阳、坡度平缓、土层深厚、疏松的砂质壤土地块的生长环境条件下,植株具有较好的生长适应能力,生物量得到充分积累,而且茎、叶和花中主要活性物质总黄酮、酚类化合物以及金丝桃素的积累量并未显著降低,且花中的抗氧化能力有显著的增加。本实验只对野生和栽培贯叶连翘盛花期生理生化特性、活性物质(总黄酮、酚类化合物以及金丝桃素)积累量以及抗氧化能力进行了研究, 而对于野生和栽培过程中其他活性物质组分与含量以及不同生长期的变化,还需要进一步的研究和分析。该研究结果将对加快贯叶连翘种植栽培及推广,为金丝桃素的提取提供丰富的原材料,保护贯叶连翘野生资源具有重要的参考价值和实践意义。
References:
[1]Ouyang H, Xie L Y, Huang X F,etal. Progress and prospect of chemical composition and pharmacological research ofHypericumperforatum. Jiangxi Journal of Traditional Chinese Medicine, 2010, 41(7): 78-80.
[2]Group H D T S. Effect ofHypericumperforatum(St John’s wort) in major depressive disorder: a randomized controlled trial. Jama, 2002, 287(14): 1807-1814.
[3]Martarelli D, Martarelli B, Pediconi D.Hypericumperforatummethanolic extract inhibits growth of human prostatic carcinoma cell line orthotopically implanted in nude mice. Cancer Letters, 2004, 210(1): 27-33.
[4]Rezaei A, Pashazadeh M, Pashazadeh M,etal. Comparative study of sedative and anxiolytic effects of herbal extracts ofHypericumperforatumwith nardostachys jatamansi in rats. Zahedan Journal of Research in Medical Sciences, 2014, 16(3): 40-43.
[5]Özdemir E, Alplnar K. An ethnobotanical survey of medicinal plants in western part of central Taurus Mountains: Aladaglar (Nigde-Turkey). Journal of Ethnopharmacology, 2015, 166: 53-65.
[6]Durán N, Song P S. Hypericin and its photodynamic action. Photochemistry and Photobiology, 1986, 43(6): 677-680.
[7]Wölfle U, Seelinger G, Schempp C M. Topical application of St. John’s wort (Hypericumperforatum). Planta Medica, 2014, 80(2-3): 109-120.
[8]Nahrstedt A, Butterweck V. Biologically active and other chemical constituents of the herb ofHypericumperforatumL. Pharmacopsychiatry, 1997, 30(suppl. 2): 129-134.
[9]Jürgenliemk G, Nahrstedt A. Dissolution, solubility and cooperativity of phenolic compounds fromHypericumperforatumL. in aqueous systems. Pharmazie, 2003, 58(3): 200-203.
[10]Southwell I A, Bourke C A. Seasonal variation in hypericin content ofHypericumperforatumL. (St. John’s Wort). Phytochemistry, 2001, 56(5): 437-441.
[10]Karakashov B, Grigorakis S, Loupassaki S,etal. Optimisation of polyphenol extraction fromHypericumperforatum(St. John’s Wort) using aqueous glycerol and response surface methodology. Journal of Applied Research on Medicinal & Aromatic Plants, 2015, 2: 1-8.
[12]Wang J, Qian J, Yao L,etal. Enhanced production of flavonoids by methyl jasmonate elicitation in cell suspension culture ofHypericumperforatum. Bioresources & Bioprocessing, 2015, 2: 1-9.
[13]Hang Y Y, Lv Y, Zhou Y F,etal. The biological characteristics and property of wild and cultivated plants ofHypericumperforatumL. Journal of Plant Resources and Environment, 2002, 11(3): 20-23.
[14]Farshchi H S K, Arani M A, Nemati S H. Phytochemical and morphological attributes of St. John’s Wort (Hypericumperforatum) affected by organic and inorganic fertilizers; humic acid and potassium sulphate. Notulae Scientia Biologicae, 2014, 6(3): 326-330.
[15]Ding R X, Xu T F, Zhang H M. Tissue culture and rapid regeneration ofHypericumperforatum. Academic Journal of Second Military Medical University, 2000, 21(10): 904-906.
[16]Sun W, Pan Y Z, Qin L L. Effects of GA3and CEPA on photosynthetic characteristics and antioxidant enzymes in the flowering phase and the flowering response ofLiliumcasablanca. Acta Prataculturae Sinica, 2015, 24(8): 73-84.
[17]Li H S. Plant Physiological and Biochemical Principles and Techniques[M]. Beijing: Higher Education Press, 2001.
[18]Ma M L, Karsani S A, Mohajer S,etal. Phytochemical constituents, nutritional values, phenolics, flavonols, flavonoids, antioxidant and cytotoxicity studies onPhaleriamacrocarpa(Scheff.) Boerl fruits. BMC Complementary & Alternative Medicine, 2014, 14(8): 1187-1198.
[19]Beato V M, Orgaz F, Mansilla F,etal. Changes in phenolic compounds in garlic (AlliumsativumL.) owing to the cultivar and location of growth. Plant Foods for Human Nutrition, 2011, 66(3): 218-223.
[20]Wu W, Meng D S, Fu R Q,etal. Determination of hypericin in different parts ofHypericumperforatumfrom different habitats by HPLC. China Pharmacy, 2010, 21(11): 1020-1022.
[21]Benzie I F F, Strain J J. The ferric reducing ability of plasma (FRAP) as a measure of “antioxidant power”: the FRAP assay. Analytical Biochemistry, 1996, 239(1): 70-76.
[22]Li M F, Zhou L L, Yang D L,etal. Biochemical composition and antioxidant capacity of extracts fromPodophyllumhexandrumrhizome. BMC Complementary & Alternative Medicine, 2012, 12(1): 166-169.
[23]Zhu H F, Zhang C Q, Gong X. A summary on plant introduction and acclimatization research. Guihaia, 2003, 23(1): 52-60.
[24]Guo Q S. Medicinal Plant Resources[M]. Beijing: Higher Education Press, 2007.
[25]Li Y, Cao X L, Fu P. Introduction of chemical components ofHypericumperforatumL. and method of their separation and purification. Journal of Beijing Technology and Business University (Natural Science Edition), 2007, 25(6): 6-10.
[26]Kandaswami C C, Jr M E. Flavonoids as antioxidants. Natural Antioxidants Chemistry, 2000, 31(42): 1035-1042.
[27]Shahidi F, Wanasundara P K. Phenolic antioxidants. Critical Reviews in Food Science and Nutrition, 1992, 32(1): 67-103.
[28]Wang L, Shi L L, Zhang Y X,etal. Biosynthesis and regulation of the secondary metabolites in plants. Journal of Wuhan Botanical Research, 2007, 25(5): 500-508.
参考文献:
[1]欧阳辉, 谢丽艳, 黄小方, 等. 贯叶连翘的化学成分与药理研究进展及前景展望. 江西中医药, 2010, 41(7): 78-80.
[13]杭悦宇, 吕晔, 周义锋, 等. 贯叶连翘野生转家化前后生物学性状特征观察. 植物资源与环境学报, 2002, 11(3): 20-23.
[15]丁如贤, 许铁峰, 张汉明. 贯叶连翘的组织培养和快速繁殖. 第二军医大学学报, 2000, 21(10): 904-906.
[16]孙位, 潘远智, 覃琳岚. GA3和CEPA对香水百合开花期光合生理和抗氧化酶活性的影响及其花期响应研究.草业学报, 2015, 24(8): 73-84.
[17]李合生. 植物生理生化实验原理和技术[M]. 北京: 高等教育出版社, 2001.
[20]吴畏, 孟德胜, 傅若秋, 等. HPLC法测定不同产地贯叶连翘不同部位中金丝桃素的含量. 中国药房, 2010, 21(11): 1020-1022.
[23]朱慧芬, 张长芹, 龚洵. 植物引种驯化研究概述. 广西植物, 2003, 23(1): 52-60.
[24]郭巧生. 药用植物资源学[M]. 北京: 高等教育出版社, 2007.
[25]李艳, 曹学丽, 付鹏. 贯叶连翘的化学成分及其提取方法研究进展. 北京工商大学学报(自然科学版), 2007, 25(6): 6-10.
[28]王莉, 史玲玲, 张艳霞, 等. 植物次生代谢物途径及其研究进展. 武汉植物学研究, 2007, 25(5): 500-508.
Changes in physiological and biochemical characteristics, contents of bioactive compounds, and antioxidant capacity ofHypericumperforatumduring introduction and acclimatization
KANG Xia1, GE Li2, LI Meng-Fei2*, GAN Yan-Tai1*, LI Jing-Yao3, WANG Ke-Peng4
1.AgronomyCollege,GansuAgriculturalUniversity,Lanzhou730070,China; 2.CollegeofLifeScienceandTechnology,GansuProvincialKeyLabofAridlandCropScience,GansuAgriculturalUniversity,Lanzhou730070,China; 3.GuidancestationofherbscultivationofKangxian,Kangxian746500,China; 4.CollegeofResourceandEnvironmentalSciences,GansuAgriculturalUniversity,Lanzhou730070,China
Abstract:In this study, we investigated the changes in bioactive compounds in wild and cultivated Hypericum perforatum during introduction and acclimatization. Physiological and biochemical characteristics, bioactive compound contents, and antioxidant capacity were evaluated for H. perforatum plants at the flowering stage. The net photosynthetic rate, transpiration rate, stomatal conductance, chlorophyll content, and root activity were higher in cultivated plants than in wild plants. The flowering date was 7 days earlier in the cultivated plants than in the wild plants, and the dry weight of aboveground parts was 16.67% higher in cultivated plants than in wild plants. The total flavonoid and hypericin contents in the same organ did not differ significantly between the wild and cultivated plants. The total phenolic contents in flowers were higher in wild plants than in cultivated plants, while the opposite trend was observed for total phenolic contents in the leaves. Both wild and cultivated plants had higher total flavonoid and phenolic contents in the flowers and leaves than in the stem, while the highest hypericin content was in the flowers, followed by leaves, and then stems. The antioxidant capacity of the wild and cultivated plants was highest in the flowers followed by leaves, and then stems. There was no difference in the antioxidant capacity of leaf and stem extracts between wild and cultivated plants, while the antioxidant capacity of flower extracts was significantly stronger in cultivated plants than in wild plants. These results indicate that the cultivated plants not only showed strong acclimatization abilities, but also had bioactive compound contents and an antioxidant capacity similar to those of wild plants.
Key words:Hypericum perforatum; wild and cultivated; physiological and biochemical characteristics; total flavonoid and phenolic; hypericin; antioxidant capacity
*通信作者
Corresponding author. E-mail:lmf@gsau.edu.cn
作者简介:康霞(1977-),女,甘肃渭源人,在读博士。E-mail:kangxia007@163.com
基金项目:国家自然科学基金(31360148),甘肃省中药材产业科技攻关(GYC14-03)和甘肃农业大学SRTP(20150801)资助。
*收稿日期:2015-08-31;改回日期:2015-12-10
DOI:10.11686/cyxb2015385
http://cyxb.lzu.edu.cn
康霞, 葛莉, 栗孟飞, 甘延太, 李京耀, 王克鹏. 贯叶连翘引种驯化过程中生理生化特性、活性物质含量及抗氧化能力的变化.草业学报, 2016, 25(4): 104-110.
KANG Xia, GE Li, LI Meng-Fei, GAN Yan-Tai, LI Jing-Yao, WANG Ke-Peng. Changes in physiological and biochemical characteristics, contents of bioactive compounds, and antioxidant capacity ofHypericumperforatumduring introduction and acclimatization. Acta Prataculturae Sinica, 2016, 25(4): 104-110.

