鼠疫菌素的克隆表达与活性分析
王 婷,刘文华,邹 玲,张 灿,任慧英(青岛农业大学动物科技学院,山东青岛266109)
鼠疫菌素的克隆表达与活性分析
王婷,刘文华,邹玲,张灿,任慧英
(青岛农业大学动物科技学院,山东青岛266109)
摘要:为了研究鼠疫菌素的抑菌作用,PCR扩增并克隆鼠疫菌素(pst)基因,构建鼠疫菌素原核重组表达质粒pET28a-pst,在大肠杆菌BL21中表达。经His标签蛋白纯化柱纯化获得重组鼠疫菌素蛋白,并检测表达蛋白的抑菌活性。结果表明,鼠疫菌素基因长1 074 bp,重组鼠疫菌素为44 kD,以包涵体形式表达。纯化的鼠疫菌素对金黄色葡萄球菌ATCC25923和大肠杆菌O78具有一定的抑菌作用。研究结果将为进一步研究鼠疫菌素的应用奠定基础。
关键词:鼠疫菌素;克隆;原核表达;抑菌活性
Expression and Antibacterial Activity Analysis of Pesticin WANG Ting,LIU Wen-hua,ZOU Ling,ZHANG Can,REN Hui-ying
(College of Animal Science and Technology,Qingdao Agricultural University,Qingdao 266109,China)
Abstract:In order to investigate the antibacterial activity of pesticin(pst),pesticin gene was amplified by PCR and cloned into the prokaryotic expression plasmid pET28a-pst and expressed in BL21.The recombinant pesticin was purified with His-Tagged Protein Purification Kit and the antibacterial activity was analyzed .Our results showed that the full length of pesticin gene was 1 074 bp,and the recombinant pesticin was 44 kD.The antibacterial test results showed that purified pesticin had antibacterial activities against Staphylococcus aureu25923 and Escherichia.coli O78.
Key words:pesticin;cloning;prokaryotic expression;antibacterial activity
Corresponding authors:REN Hui-ying;ZHANG Can
细菌耐药性以及耐药菌感染是人医和兽医临床共同面临的一大难题。以大肠杆菌为例,全球每年因产肠毒素大肠杆菌(ETEC)引起的感染超过6.5亿例,并导致约80万例病人死亡[1]。据王占华报道[2],分离自医院的854株大肠杆菌对氨苄西林的耐药率高达87%,对庆大霉素和美络西林的耐药率超过70%,对头孢哌酮和头孢噻吩的耐药率均超过50%。大肠杆菌引起的初生仔猪腹泻、鸡大肠杆菌性败血症是动物养殖中的常见病,其发病率在细菌病中居首位。从华北地区分离的鸡源大肠杆菌中84.76%对四环素耐药,70.12%对多西环素耐药[3];猪肉中大肠杆菌可耐受的药物种类达8~11种,鸡肉中大肠杆菌对7~8种药物耐药[4]。尽管阿米卡星未被批准为兽药,但鸡肉源大肠杆菌对阿米卡星的耐药率达16.5%。细菌的广泛耐药性使抗生素治疗越来越困难,因此开发能有效规避细菌耐药性的抗生素替代品乃当务之急。
鼠疫菌素由鼠疫耶尔森菌产生,是具有溶菌酶活性的细菌素,可裂解细菌细胞壁中的肽聚糖,从而发挥杀菌作用。除可直接作用于革兰阳性菌外,鼠疫菌素还可以杀死亲缘关系较近的革兰阴性菌。研究发现[5],鼠疫菌素能特异靶向致病性大肠杆菌表面的FyuA蛋白,从而对大肠杆菌产生杀伤作用。FyuA是耶尔森菌强毒力岛中fyuA基因编码产物,大部分致病性大肠杆菌携带fyuA基因[6],从而成为鼠疫菌素的靶细胞。国内外对鼠疫菌素的杀菌作用鲜有报道,为了进一步研究鼠疫菌素的杀菌效果,本研究对鼠疫菌素基因进行克隆表达,并对其进行活性分析,以期为人和动物细菌病的控制提供新型的抗生素替代品。
1 材料与方法
1.1质粒与菌株克隆载体pMD19-T,购自TaKaRa公司;表达载体pET28a、大肠杆菌DH5α和BL21均为本实验室保存,鼠疫菌素DNA模板由云南省地方病防治所提供,金黄色葡萄球菌ATCC- 25923及O78型大肠杆菌分离株均为本实验室保存。
1.2引物与主要试剂限制性内切酶、PCR产物回收试剂盒和T4 DNA连接酶,均购自TaKaRa公司;质粒提取试剂盒、胶回收试剂盒、Ni-Agarose His标签蛋白纯化试剂盒及BCA蛋白浓度测定试剂盒,均购自北京康为世纪生物科技有限公司。上游引物pstF:5′-CCGGAATTCATGTCAGATACAA TG-3′,下游引物pstR:5′-CGCGTCGACTTATTTTAACAATC-3′,酶切位点用下划线表示,由上海生工生物工程技术服务有限公司合成。庆大霉素及林可霉素药敏纸片为杭州天和微生物试剂有限公司产品。
1.3鼠疫菌素基因的克隆及重组表达载体的构建以鼠疫菌素DNA为模板,PCR扩增鼠疫菌素基因。将目的基因连接到pMD19-T载体上,获得质粒pst/T,测序并进行序列分析。将鼠疫菌素基因进一步克隆到pET28a表达质粒,对重组质粒进行PCR及双酶切鉴定、测序。将测序正确的表达质粒转化BL21感受态细胞,获得表达鼠疫菌素pst的重组菌pET28a-pst/ BL21。
1.4重组蛋白pst的表达及条件优化将重组表达菌接入含有100 μg/mL卡那霉素的LB培养基中,37℃培养至菌液OD值为0.6,加入不同浓度的IPTG进行诱导,在不同时间分别取样,SDSPAGE检测重组蛋白的表达情况,分析不同诱导剂浓度和诱导时间对重组蛋白表达量的影响,确定最佳诱导表达条件。
1.5重组蛋白pst的可溶性检测及Western-Blot鉴定离心收集经IPTG在最佳条件下诱导表达后的菌体,PBS重悬后在冰浴条件下进行超声波裂解,裂解条件为:冰浴间歇超声,超声3 s,间歇1 s,待菌液较清亮时,约30 min停止超声,12 000 r/min (4℃)离心5 min,将上清和沉淀(PBS重悬)分别加入1×SDS上样缓冲液,煮沸后进行SDS-PAGE电泳,分析重组蛋白的表达形式。参照文献[7]进行Western-Blot分析。鼠抗His标签为首抗(1∶1 500),HRP标记羊抗鼠IgG为二抗(1∶3 000),DAB显色。1.6重组蛋白pst的纯化将重组表达菌进行超声破碎,离心收集沉淀。将包涵体蛋白经洗涤后变性溶解,对包涵体粗提取物进行透析与复性,4℃条件下进行尿素梯度透析复性(6、4、2、1、0 mol/L各12 h)。将复性的pst蛋白溶液用Ni-Agarose His标签蛋白纯化试剂盒纯化,收集目的蛋白峰后进行SDS-PAGE分析蛋白纯度。以BCA蛋白浓度测定试剂盒测定蛋白浓度。
1.7重组蛋白pst的抑菌试验将金黄色葡萄球菌ATCC25923和大肠杆菌O78菌株分别经液体培养至对数期(菌液浓度达108CFU/mL),取200 μL菌液在普通琼脂平板表面均匀涂布,将灭菌牛津杯(直径8 mm)放置于培养基的表面,在其中加入200 μL浓度为1 mg/mL的纯化蛋白,庆大霉素和林可霉素为抗生素对照,37℃温箱中培养18 h左右,测量抑菌圈大小。
1.8重组蛋白pst的溶菌活性复苏金黄色葡萄球菌ATCC25923和大肠杆菌O78首株,分别进行液体培养,37℃培养8 h,用LB肉汤依次倍比稀释到10-5,将蛋白与菌液相互作用,同时设PBS对照,作用2 h后,取出100 μL,用LB肉汤依次倍比稀释到10-3和10-2,取400 μL加至无菌平皿中,倒入约50℃的培养基,充分摇匀,每个稀释度重复2次,凝固后倒置培养24 h,进行计数。
2 结果与分析
2.1鼠疫菌素基因的克隆及测序用pst引物对扩增鼠疫菌素基因,并克隆入pMD19-T载体。将重组质粒进行PCR扩增,得到与预期1 074 bp大小一致的条带(图1)。经测序比对分析,克隆基因与鼠疫菌素pst基因(GenBank号为NC-017159.1)的同源性为100%。
2.2pst重组表达载体pET28a-pst的构建将质粒pst/T经双酶切后回收目的条带,插入pET28a,构建pET28a-pst重组表达质粒。PCR及酶切分析均得到与预期大小相当的条带,重组质粒的测序分析表明插入的片段正确(图2)。
2.3pst表达条件的优化将重组质粒转化至BL21,IPTG诱导表达后进行SDS-PAGE分析。与空质粒相比,出现与预期44 kD一致的蛋白条带。蛋白诱导优化分析结果显示0.8 mmol/LIPTG,诱导6 h效果最佳(图3、4)。

图1 pst基因的PCR扩增M:DNA标准分子质量;1:pst基因的PCR产物

图2 pET28a- pst的双酶切结果M:DNA标准分子质量;1:pET28a-pst的双酶切;2:pET28a-pst
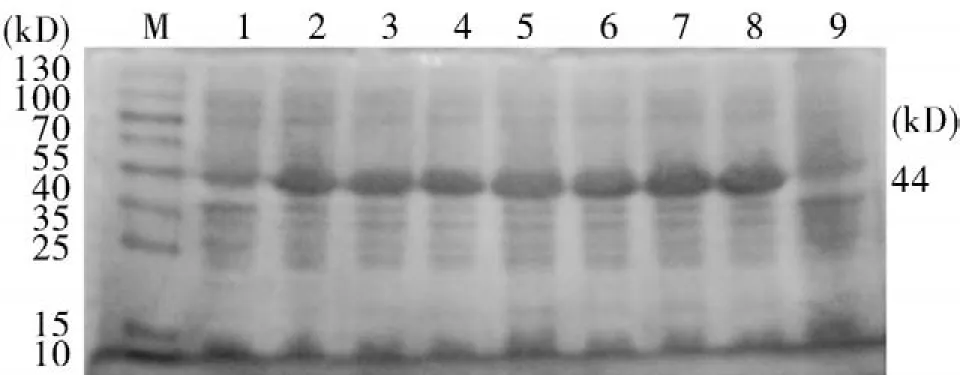
图3 IPTG浓度对pst表达的影响M:标准蛋白分子质量;1~8:重组菌分别用0、0.2、0.4、0.6、0.8、1.0、1.2、1.4 mmol/L的IPTG进行诱导;9:空质粒表达菌
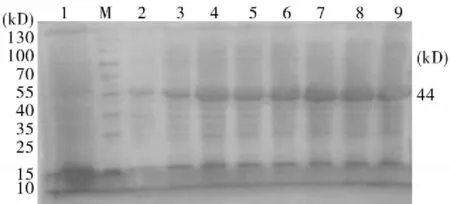
图4 诱导时间对pst表达的影响M:标准蛋白分子质量;1:空质粒表达菌;2~9:重组菌分别诱导1、2、3、4、5、6、7、8 h
2.4重组蛋白pst的可溶性检测及Western-Blot鉴定将诱导表达的菌体经超声裂解,分别取上清与沉淀进行SDS-PAGE电泳。结果表明,沉淀中有大量的目的蛋白条带,而上清中仅有少量的蛋白条带,因此pst重组蛋白主要以包涵体的形式存在(图5)。将经IPTG诱导的重组菌pET28apst/BL21经SDS-PAGE电泳后进行Western-Blot鉴定。结果表明,重组蛋白能与抗His的单克隆抗体结合,且符合44 kD的预期大小。
2.5重组蛋白pst的纯化与鉴定将重组表达菌的包涵体蛋白经变性与透析复性后进行蛋白纯化。纯化蛋白经SDS-PAGE分析,证明与预期的44 kD大小相符。
2.6重组蛋白pst的抑菌试验平板抑菌试验结果表明,重组蛋白pst能够对金黄色葡萄球菌ATCC 25923和O78型大肠杆菌产生抑菌效果,抑菌圈大小分别为16 mm和12 mm。
2.7重组蛋白pst的溶菌活性通过蛋白与菌液相互作用后,与PBS对照组相比,金黄色葡萄球菌细菌数下降22%,大肠杆菌O78细菌数下降14%。

图5 目的蛋白pst的可溶性鉴定M:标准蛋白分子质量;1:菌体裂解上清;2:菌体裂解沉淀
3 讨论
细菌素是细菌产生的一种具有杀菌作用的蛋白质,通常认为,细菌素只能作用于与它同种不同菌株的细菌以及与它亲缘关系相近的细菌[8]。细菌素可抑制多种病原菌,但抑菌谱的宽窄差异较大。如乳球菌素仅能抑制其他乳球菌,而戊糖片球菌产生的细菌素对绿脓杆菌、克雷伯菌及李斯特菌具有抑制作用[9]。细菌素的作用机制多种多样,主要分能量依赖性和非能量依赖性两种。鼠疫菌素是比较独特的细菌素,具有溶菌酶活性,能水解肽聚糖成分。肽聚糖是细菌细胞壁特有的成分,细菌细胞壁的结构存在差异,革兰阴性菌的肽聚糖层有外膜包裹,而革兰阳性菌肽聚糖层暴露在表面,因此理论上鼠疫菌素可对革兰阳性菌产生直接杀伤作用。文献报道,鼠疫菌素对革兰阴性的杀伤作用需要依赖于目标细菌表面特定的外膜蛋白FyuA,FyuA是耶尔森菌强毒力岛中fyuA基因的编码产物,大部分致病性大肠杆菌携带fyuA基因[3,10],从而成为鼠疫菌素的靶细胞。理论上鼠疫菌素对革兰阳性菌,如金黄色葡萄球菌、溶壁微球菌及大部分致病性大肠杆菌具有裂解作用。
本研究发现,人工表达的鼠疫菌素对金黄色葡萄球菌ATCC25923和大肠杆菌O78具有抑菌作用,对鼠疫菌素作用机理的深入研究将为开发治疗细菌病的抗生素替代品奠定基础。
参考文献:
[1] Qadri F,Svennerholm A M,Faruque A S,et al . Enterotoxigenic Escherichia coli in developing countries:epidemiology,microbiology,clinical features,treatment,and prevention[J].Clin Microbiol Rev,2005,18(3):465-483.
[2]王占华.医院感染大肠埃希氏菌的发生率及耐药监测[D].泰安:泰山医学院,2013.
[3] Zhang T,Wang C G,Lv J C,et al . Survey on tetracycline resistance and antibiotic-resistant genotype of avian Escherichia coli in North China[J].Poult Sci,2012,91:2774-2777.
[4]刘书亮,张晓利,韩新锋,等.动物性食品源大肠杆菌耐药性研究[J].中国食品学报,2011,11(7):163-168.
[5] Patzer S I,Albrecht R,Braun V,et al.Structural and mechanisic studies of pesticin,a bacterial homolog of phage lysozymes[J] . J Biol Chem,2012,287(28):23381-23396.
[6]吕殿红,魏文康,黄忠,等.105株携带耶尔森菌强毒力岛大肠杆菌的毒力基因型和部分菌株毒力因子序列研究[J].中国预防兽医学报,2012,34(1):71-73.
[7]萨姆布鲁克J,弗里奇E F,曼尼阿蒂斯T.分子克隆实验指南[M].金冬雁,黎孟枫,侯云德,等译.2版.北京:科学出版社,1998:880-898.
[8]陆承平,兽医微生物学[M].北京:中国农业出版社,2007.
[9] Svetoslav D,Todorov,Leon M T.Bacteriocin production by Pedi-OCOCCUS pentosaceus isolated from marula(Scerocarya birrea)[J]. International Journal of Food Microbiology,2009,132:117-126.
[10] Tadesse D A,Zhao S,Tong E,et al . Antimicrobial drug resistance in Escherichia coli from humans and food animals,United States,1950-2002[J].Emerg Infect Dis,2012,18(5):741-749.
通讯作者:任慧英,E-mail:renren0228@sina.com;张灿,E-mail:cleverflame@163.com
作者简介:王婷(1990-),女,硕士生,主要从事兽医微生物与免疫学方向的研究,E-mail:wangting900603@163.com
基金项目:山东省自然科学基金(ZR2009DM009);山东省自然科学基金(ZR2013CQ024)
收稿日期:2014-10-27
中图分类号:R 516.8
文献标志码:A
文章编号:0529- 6005(2016)01- 0006- 03

