伤科消肿颗粒处方提取工艺优选*
李海英,刘 武,刘吉成
(1.广西中医药大学第一附属医院,广西 南宁 530023; 2.广西壮族自治区玉林食品药品检验所,广西 玉林 537000)
伤科消肿颗粒处方提取工艺优选*
李海英1,刘 武1,刘吉成2
(1.广西中医药大学第一附属医院,广西 南宁 530023; 2.广西壮族自治区玉林食品药品检验所,广西 玉林 537000)
目的 优选伤科消肿颗粒的提取工艺条件。方法 以挥发油的提取量、干膏量、芍药苷和绿原酸含量为综合指标,采用正交试验优选最佳提取条件。结果 先取薄荷用水提取,挥发油提取率为75.3%;再取薄荷药渣及药液与其他14味药材,加水煎煮2次,芍药苷和绿原酸提取率为79.8%和83.3%;干膏量为每张处方16.49 g;浓缩水提液至相对密度1.15,加乙醇至60%(g/g),冷藏静置12 h,减压浓缩上清液,芍药苷和绿原酸的转移保留率为80%和74%,干膏量为每张处方10.01 g。结论 优选的提取工艺简单、稳定、可行,为伤科消肿颗粒处方提取工艺条件提供了科学依据。
伤科消肿颗粒;正交试验;提取工艺
伤科消肿颗粒是在广西中医药大学第一附属医院骨科多年临床应用经验处方基础上生产的颗粒剂型医院制剂,主要由土鳖虫、赤芍、泽兰、金银花、粉防己、连翘等15味中药材经提取加工等步骤制成,具有活血止痛、利水消肿之功效[1-2],临床主要用于外伤或车祸患者骨折术。中药颗粒剂给药方便,既可吞服又可混悬或溶解在水中服用,且吸收好、起效快、不良反应小、携带方便[3]。本试验中是在临床应用的经验处方基础上[1-2],对方中有效成分进行提取、纯化而制成医院制剂,以在疗效、成本、不良反应、患者服药顺应性等诸多方面综合衡量,对此方进一步优化成颗粒剂,研制新的中成药制剂,为更好地发挥伤科消肿颗粒疗效提供参考。
1 仪器与试药
Agilent 1200型高效液相色谱议(美国安捷伦科技有限公司,配DAD检测器);Millipore Simplicity-UV型超纯水机(美国密里博公司);SB2200-T型超声波清洗器(上海必能信公司);BZF-30型电热真空干燥箱(上海博迅实业有限医疗设备厂);RE-52AA型旋转蒸发仪(上海亚荣生化仪器厂);BT224S型电子天平(北京赛多利斯仪器系统有限公司);MA100型水分测定仪(中国赛多利斯仪器系统有限公司);CP225D1/10万电子天平(中国赛多利斯仪器系统有限公司);GM-0.33Ⅱ隔膜真空泵(天津津腾实验设备有限公司);SHB-Ⅱ循环式多用真空泵(郑州长城科工贸易有限公司);OS101-2AB型电热干燥箱(重庆银河试验仪器有限公司)。乙醇(分析纯)、乙腈(色谱纯)、磷酸(分析纯),均购自西陇化工股份有限公司;淀粉、糊精、蔗糖、乳糖为辅料。芍药苷对照品(批号为 110736-201337,含量94.9%),绿原酸对照品(批号为110753~201314,含量96.6%),均由中国食品药品检定研究院提供。试验所用各药材购于广西玉林中药材市场,经广西玉林食品药品检验所中药室刘吉成鉴定为正品,详见表1。

表1 伤科消肿颗粒中15味中药材一览表
2 方法与结果
2.1 指标成分的测定
伤科消肿颗粒方中薄荷需单独提取,故以挥发油收集量作为薄荷提取的考察指标;赤芍和金银花中的主要有效成分别为芍药苷和绿原酸[4],与本方的功能主治有一定相关性,故将芍药苷和绿原酸作为伤科消肿颗粒提取工艺筛选时含量测定的指标性成分。为更有效地提取伤科消肿颗粒中的成分,另将与本方中药材提取得到的干膏量作为工艺筛选指标。各指标成分检测方法为芍药苷和绿原酸,用高效液相色谱(HPLC)法测量,波长分别为230 nm和327 nm;挥发油和干膏用重量法测量。
2.2 含量测定方法学考察
色谱条件:色谱柱为菲罗门Gemini C18柱(250 mm× 4.6 mm,5 μm);流动相为乙腈-0.1%磷酸溶液(14∶86);流速为1.0 mL/min;柱温为30℃;检测波长芍药苷为230 nm,绿原酸为327 nm;进样量为10 μL。在此条件下,理论板数以芍药苷峰计算应不低于3 000。芍药苷在进样溶液质量浓度为2.754~275.4 μg/mL时,与峰面积线性关系为 Y=10.93 X+7.795(r=0.999 4),平均回收率为98.3%,RSD为1.4%;绿原酸进样溶液质量浓度为4.343~434.3 μg/mL时与峰面积线性关系为 Y=20.55 X-5.15(r=0.999 6),平均回收率为111.4%,RSD为2.6%。
2.3 提取工艺正交试验
2.3.1 挥发油提取预试验
处方中薄荷的挥发油为药理活性成分之一,属轻质油。称取薄荷100 g,加入药材8倍量水,浸泡20 min,水蒸气蒸馏至挥发油的量不再增加,记录各时间点挥发油的收集量。结果提取0.5,1,1.5,2,2.5,3 h时挥发油收集量分别为0.3,0.5,0.67,0.75,0.76,0.76 mL,结果表明,在2.5 h以后油收集量变化不大,故选择1.5,2,2.5 h为考察提取时间的3个水平。
2.3.2 挥发油提取正交试验优选
浸泡时间:称取薄荷药材3份每份100 g,分别加水浸泡20,30,40 min,用水蒸气蒸馏,测量挥发油的收集量。
加水量:称取薄荷药材3份,每份100 g,分别加6,8,10倍水浸泡,用水蒸气蒸馏,测量挥发油的收集量。
以浸泡时间(A)、加水量(B)、煎煮时间(C)作为挥发油提取正交试验的考察因素,每个因素取3个水平。采用 L9(34)正交试验法进行试验,优选挥发油的最佳提取工艺。正交试验水平因素见表2。
2.3.3 水提工艺正交试验优选
提取时间:取薄荷药渣及药液与土鳖虫、赤芍、金银花、益母草等其他14味药材3份煎煮提取,分别提取2,3,4 h,滤过,以干膏重、芍药苷含量、绿原酸含量综合评价分析作为考察指标,优选最佳水提取工艺。
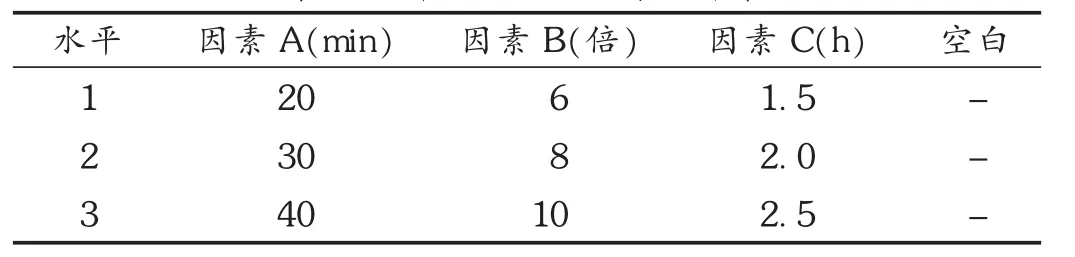
表2 挥发油提取因素水平表
提取次数:取薄荷药渣及药液与土鳖虫、赤芍、金银花、益母草等其他14味药材3份煎煮提取,分别提取1,2,3次,滤过,以干膏重、芍药苷含量、绿原酸含量综合评价分析作为考察指标,优选最佳水提取工艺。
加水量:取薄荷药渣及药液与土鳖虫、赤芍、金银花、益母草等其他14味药材3份煎煮提取,分别加6,8,10倍水,滤过,以干膏量、芍药苷含量、绿原酸含量综合评价分析作为考察指标,优选最佳水提取工艺。
本方临床使用均为水提取,根据一般水提取以提取时间(A)、提取次数(B)、加水量(C)作为考察因素,本方轻质和重质药材各半,吸水率较大的药材粉防己、茯苓等占20%左右,故选择加水量6,8,10倍。每个因素取3个水平,采用 L9(34)正交试验法安排试验,以干膏重、芍药苷含量、绿原酸含量综合评价分析作为考察指标,优选最佳水提取工艺。正交试验水平因素表见表3。

表3 水提试验因素水平表
2.3.4 醇沉工艺正交试验
相对密度:取水提液分别浓缩相对密度至1.10,1.15,1.20,再用一定浓度的乙醇醇沉,静置一定时间后以固体减少率、芍药苷和绿原酸的含量综合评价分析作为考察指标,优选最佳醇沉工艺。
醇沉浓度:分别取浓缩至一定密度的提取液3份,再分别用50%,60%,70%乙醇醇沉,静置一定时间后以固体减少率、芍药苷和绿原酸的含量综合评价分析作为考察指标,优选最佳醇沉工艺。
醇沉浓度:分别取浓缩至一定密度的提取液3份,再用一定浓度的乙醇醇沉,分别静置12,24,48 h后以固体减少率、芍药苷和绿原酸的含量综合评价分析作为考察指标,优选最佳醇沉工艺。
水提时药材所含鞣制、淀粉等无效成分溶出,为了进一步去除无效成分,改善制剂状况减少服用量,保证制剂的溶化性,加入一定量乙醇,使提取液达到适当乙醇浓度来除去杂质,对醇沉的工艺条件进行筛选,考察浓缩相对密度(A)、醇沉浓度(B)、醇沉时间(C)因素。浓缩液1.05时过稀量大,不利于沉淀出无效成分且需要大量乙醇增加生产成本,浓缩液1.25时过稠且加入乙醇后总体积小,沉淀易被浓缩液包裹,不易过滤造成浓缩液残留在沉淀物中,故浓缩液相对密度考察选择1.10,1.15,1.20。醇沉浓度也是根据一般制备颗粒剂的醇沉浓度50%~70%,故选取50%,60%,70%浓度的乙醇醇沉。每个因素取3个水平,采用 L9(34)正交试验法安排进行试验,以固体减少率、芍药苷和绿原酸的含量综合评价分析作为考察指标,优选最佳醇沉工艺。正交试验水平因素表见表4。

表4 醇沉试验因素表
2.4 供试品溶液的制备与测定
挥发油样品的制备及测定:称取100 g薄荷药材9份,分别置挥发油提取器中,按各挥发油提取工艺制备,分别记录各工艺的挥发油收集量。
水提取样品的制备及测定:称取9份单个处方量的薄荷药材备用,将薄荷按挥发油项下提取挥发油后,药渣及药液与其他土鳖虫、赤芍、金银花、益母草等其他14味药材合并,按水提工艺制备,得到提取液浓缩,干燥记录干膏重,然后取干膏约0.5 g,精密称定,置25 mL容量瓶中,用70%甲醇稀释至刻度,过滤,取续滤液用0.45 μm微孔滤膜过滤。精密吸取供试品溶液10 μL注入高效液相色谱仪,测定并采用外标一点法计算芍药苷和绿原酸的含量。
醇提取样品的制备及测定:取已得到的浓缩液,按各醇沉工艺制备,得到醇沉液浓缩,干燥记录干膏重,然后取干膏约0.5 g,精密称定,置25 mL容量瓶中,用70%甲醇稀释至刻度,过滤,取续滤液用0.45 μm微孔滤膜过滤。精密吸取供试品溶液10 μL,注入高效液相色谱仪,测定并采用外标一点法计算芍药苷和绿原酸的提取率。测定结果见表5至表10。
以挥发油得量为评价指标,通过上述挥发油提取正交试验及方差分析,结果表明,浸泡时间(因素A)无差异 FA<F1-0.10(2,2),从生产周期方面考虑,选 A1,即浸泡时间为20 min;加水量(因素B)有差异,F1-0.10(2,2)<FB<F1-0.05(2,2),应选B3水平,但从极差上看,B2和B3接近,故选B2,即加8倍量水;提取时间(因素C),有显著性差异 F1-0.05(2,2)<FC<F1-0.01(2,2),应选 C3即提取2.5 h,最优组合确定为A1B2C3,即加入8倍量水,浸泡20 min,水蒸汽蒸馏保持微沸提取2.5 h。
通过考察干膏得量、芍药苷、绿原酸3个指标,权重法计算所得综合评分为评价指标,正交试验方差分析结果表明,提取时间(因素A)无差异 FA<F1-0.10(2,2),从直观结果和生产周期方面考虑,选 A1,即提取时间为 2 h;提取次数(因素 B)有差异 F1-0.10(2,2)<FB<F1-0.05(2,2),应选 B3水平,但从极差上看,B2和 B3接近,故选B2,即提取2次;加水量(因素C),有显著性差异 F1-0.05(2,2)<FC<F1-0.01(2,2),应选 C3,即加水量为10倍量,最优组合确定为A1B2C3,即加10倍量水煎煮2次,每次2 h。

表5 挥发油提取工艺正交设计及指标测定结果
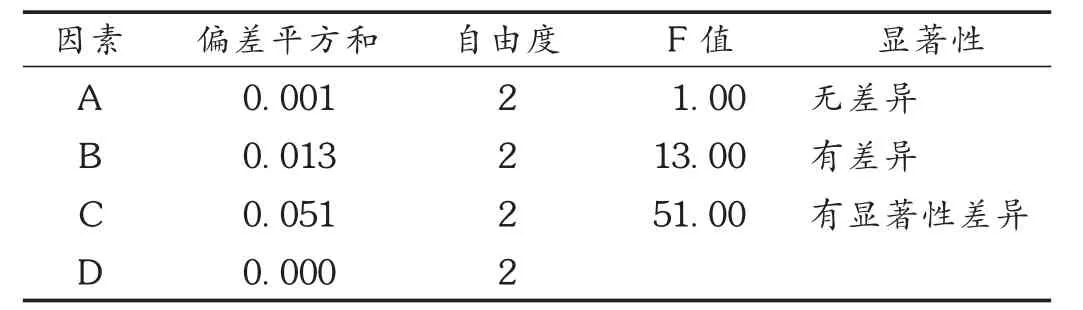
表6 挥发油提取工艺正交试验方差分析表
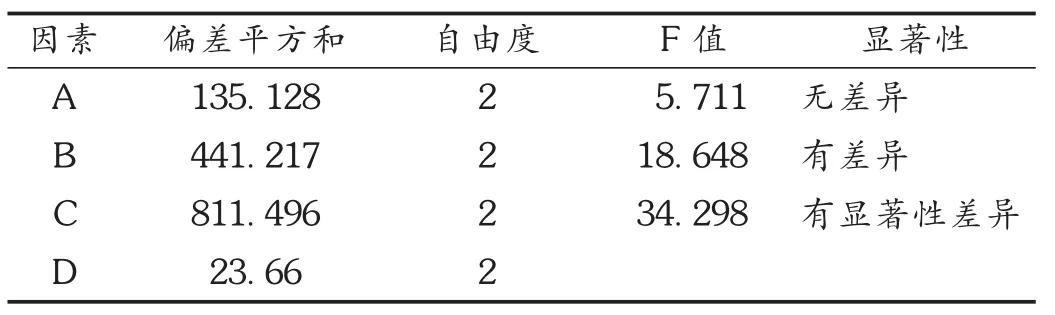
表8 综合评分的方差分析
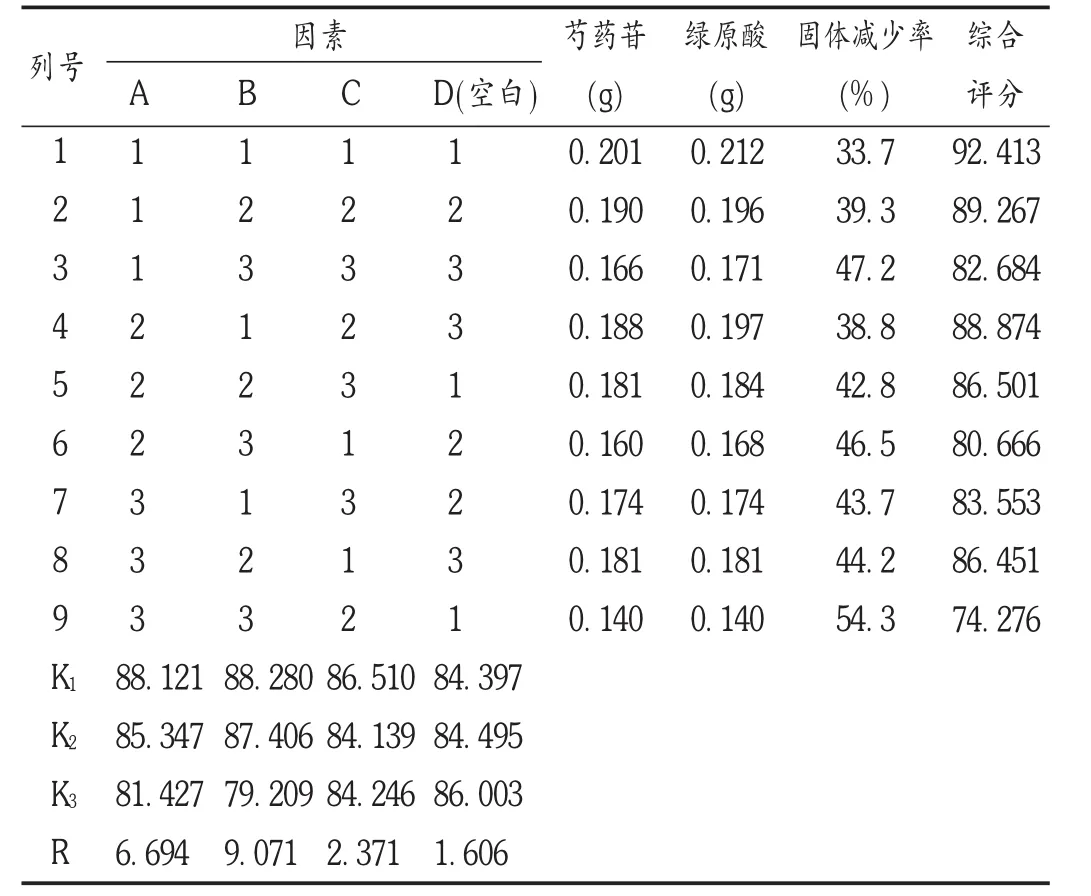
表9 醇沉工艺正交试验设计及结果分析
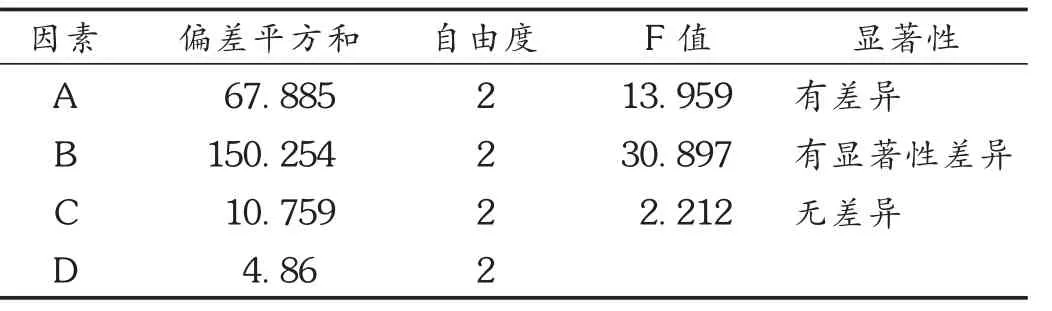
表10 综合评分的方差分析
通过考察固体减少率、芍药苷、绿原酸3个指标,权重法计算所得综合评分为评价指标,正交试验方差分析结果表明,浓缩相对密度(因素A)有差异 F1-0.10(2,2)<FA<F1-0.05(2,2),应选A1水平,考虑相对密度A1清膏量大醇沉需使用较大量的乙醇,后续浓缩耗能也大,从经济角度出发权衡利弊选择A2,即浓缩相对密度为1.15;醇沉浓度(因素B),有显著性差异 F1-0.05(2,2)<FB<F1-0.01(2,2),从直观结果上分析,B1和B2很接近,结合生产经验,醇沉浓度60%的澄清度会明显比50%的好,故选择B2,即醇沉浓度为60%;静置时间(因素C)无差异 FC<F1-0.10(2,2),从直观结果和生产周期成本考虑,选 C1,即静置时间为 12 h。理论上最优组合为A1B1C1,结合实际考虑确定最优组合A2B2C。即取浓缩至约1.15(80℃)的清膏,加乙醇使含醇量为60%(g/g),顺同一方向充分搅拌后冷藏静置12 h。
2.5 优选工艺验证试验
按上述确定的最佳挥发油、水提、醇沉试验条件分别平行提取3份,计算得到挥发油提取率为75.3%,RSD为0.77%(n=3),水提取的芍药苷、绿原酸提取率为79.8%,83.3%,干膏量为每张处方16.49 g,RSD分别为3.71%,2.90%,1.16%(n=3),醇沉后的芍药苷转移保留率为80%,绿原酸转移保留率为74%,固体减少率为43.37%,干膏量为每张处方10.01 g,RSD分别为1.95%,3.16%,1.93%,1.76%(n=3),表明该工艺合理、稳定、可行。
3 讨论
在剂型选择方面,参照文献可选择注射剂、胶囊、膏药、酊剂等剂型,但考虑到中药注射剂输液反应多[5-6],生物制剂药物研发的新兴领域,研发周期长、失败率较高[7]。因毒胶囊猖獗市场,贴剂、酊剂等存在刺激性大、吸收慢且污染衣物等缺点,最终选择可吞服又可混悬或溶解在水中服用、吸收好、起效快、不良反应小、携带方便的颗粒剂。薄荷挥发油提取时蒸馏要控制微沸状态,否则沸腾过猛形成的油珠不易聚集,且部分挥发油可能会逸出,影响读数的准确性,故在提取时需控制蒸馏温度。根据原方汤剂采用水提可以提取出有效药效成分,由于水提后干膏得量约每张处方16.5 g,若直接干燥制粒则单方服用量太大,考虑方中金银花、泽兰、茯苓、粉防己等药材所含淀粉等无效成分溶出,为了进一步去除无效成分,改善制剂状况减少服用量,保证制剂的溶化性进行醇沉除杂,在醇沉工艺研究过程中发现,乙醇应边搅拌边缓缓加入,否则提取液局部浓度过高,会快速出现蓬松的絮状沉淀并包裹部分提取液,给过滤带来困难,并影响醇沉效果。处方中药物提取的干膏量越多表明提取效率越好,在醇沉中干膏量越少表明提取醇沉出的杂质越多。
[1]刘 武,米 琨,王 斌,等.活血利水法治疗四肢骨折术后肿胀疗效观察[J].新中医杂志,2011,43(9):59.
[2]刘 武,米 琨,伏春华,等.活血利水法治疗骨折术后肢体肿胀 320例的临床回顾性研究[J].广西中医学院学报,2011,14(3):18.
[3]陶 晶.浅谈中草药制成颗粒剂的优点[J].中国现代药物应用,2009,3(17):183.
[4]陆小华,马 骁,王 建,等.赤芍的化学成分和药理作用研究进展[J].中草药,2015,46(4):595-596.
[5]丁 红,赵俊苹.浅谈中药注射剂的不良反应发生原因[J].医药与保健,2014,17(1):128-129.
[6]陈婉玲,李宇清,杨肖敏,等.49例中药注射剂输液反应原因分析及应对策略[J].中华全科医学,2010,8(2):204-205.
[7]田 军,郝博济.抗高血压药物靶标及剂型的研发进展[J].中国药房,2013,24(9):852-855.
Optimization Study on Extracting Technology of Shangkexiaozhong Granules
Li Haiying1,Liu Wu1,Liu Jicheng2
(1.First Affiliated Hospital of Guangxi University of Chinese Medicine,Nanning,Guangxi,China 530023; 2.Guangxi YuLin Institute for Food and Drug Control,Yulin,Guangxi,China 537000)
Objective To optimize the extracting technology conditions of shangkexiaozhong Granules.M ethods Orthogonal design was used to optimize the extraction conditions,with the content of multi-target ingredients such as the extraction of volatile oil,total solid, content of paeoniflorin and chlorogenic acid as comprehensive evaluation indexes.Results The optimum extraction conditions were as follows:take a certain amount of mint extract with water;the volatile oil content was 75.3% by this way;take the mint medical and the other 14 medicinal materials extracted with water for 2 times,the extraction percentage of Paeoniflorin and chlorogenic acid were 79.8% and 83.3%;the quantity of dry paste was 16.49 g per formula;then concentrated water-decocted liquid to be 1.15 on relative density;added ethanol to 60% (g/g);then kept them to be in cold storage and standing by 12 h;reduced pressure and concentrated the supernatant,with the rate of transfer-remaining were 80% and 74%,and the quantity of dry paste was 10.01 g per formula.Conclusion The Optimization of extraction process is simple,stable and feasible.The results provide the scientific experimental basis for determining the technology conditions of Shangkexiaozhong Granules.
Shangkexiaozhong Granules;Orthogonal Test;extracting process
TQ461;R284.1;R286.0
A
1006-4931(2016)01-0013-05
李海英(1979-),女,汉族,主管药师,主要从事药理学研究,(电子信箱)841733449@qq.com;刘武(1964-),男,汉族,博士研究生,教授,主要从事中医骨伤临床研究,本文通讯作者,(电子信箱)dawu6465@126.com。
2015-07-28)
*2013年广西壮族自治区卫生厅中壮瑶药制剂研发类课题,项目编号:GZZJ13-07。

