常温下H2O2氧化高浓度苯酚水溶液制备苯二酚
席 涛, 马红蕾, 张颖杰, 陈 强, 孔 岩
(南京工业大学 化学化工学院 材料化学工程国家重点实验室, 江苏 南京 210009)
常温下H2O2氧化高浓度苯酚水溶液制备苯二酚
席涛, 马红蕾, 张颖杰, 陈强, 孔岩
(南京工业大学 化学化工学院 材料化学工程国家重点实验室, 江苏 南京 210009)
摘要:以表面活性剂为苯酚增溶剂,水为溶剂,H2O2为氧化剂,0.5B-0.5Cr-4Fe-MCM-41为催化剂,催化苯酚羟基化反应合成苯二酚,考察了表面活性剂种类、苯酚在水中的质量分数(m(Phenol)/(m(Phenol)+m(H2O)))、苯酚与H2O2的摩尔比(n(Phenol)/n(H2O2))、反应温度对该反应的影响。结果表明,在以十二烷基磺酸钠为增溶剂、m(Phenol)/(m(Phenol)+m(H2O))=0.30、n(Phenol)/n(H2O2)=3、反应温度25℃、反应时间2 h的条件下,苯酚羟基化反应的苯酚转化率达到24.2%,苯二酚的选择性达到94.8%,且0.5B-0.5Cr-4Fe-MCM-41催化剂具有良好的重复使用性能,基本满足工业化要求。
关键词:介孔分子筛;苯酚羟基化;高浓度;表面活性剂;常温
苯二酚(DBHs),特别是邻苯二酚(CAT) 和对苯二酚(HQ) 作为重要的化工原料,广泛应用于香料、染料、医药、橡胶等领域[1-3]。由于具有合成路线短、条件温和、原子经济性高、有利于大规模工业化生产、符合绿色化学理念等优点,苯酚H2O2氧化法已成为合成DBHs最重要的方法[4]。目前,工业上主要以TS-1为催化剂,其弊端在于催化剂价格昂贵,同时催化过程以丙酮为溶剂,造成环境污染[5],而常温下以水为溶剂可以避免这些问题。
美国Mobil公司首次合成的M41s系列介孔分子筛填补了大孔与微孔分子筛材料领域的空白[6-7],规整的孔道、可调变的孔径、较大的比表面积等突出特点使其成为潜在的催化剂载体。由于纯硅介孔分子筛骨架中缺少活性位,迄今已成功将Fe[8-11]、Cu[12]、V[13]、Co[14-15]、Cr[16]、W[17]、Al[18]、Mn[19]、Ti[20]等金属掺杂到介孔分子筛中。Jiang等[8]以及Wu等[10]研究发现,过渡金属Fe在以水为溶剂的苯酚羟基化反应中表现出较高的催化活性,因而含Fe介孔分子筛被认为是苯酚羟基化反应的一种高效催化剂[8-11]。为了进一步提高催化活性,研究者也致力于研究助剂掺杂对催化性能的影响[21-24]。
苯酚制备苯二酚反应大都是在较高温度下进行,介孔分子筛水热稳定性较差,过高的反应温度严重限制了催化剂的循环再生。常温下进行反应具有提高催化剂的稳定性、减少反应能耗、避免产物过度氧化等优势。然而,常温下苯酚水溶性较差,使苯酚制备苯二酚反应只能在低浓度下进行,在工业生产中分离的能耗较大,增加了分离成本。
笔者在前期工作基础上,采用加入表面活性剂的方式来提高室温下苯酚水溶液浓度,以0.5B-0.5Cr-4Fe-MCM-41为催化剂,进行苯酚制备苯二酚反应,考察了表面活性剂种类、反应条件等对反应的影响,同时考察了催化剂再生效果。
1实验部分
1.1 试剂
偏硅酸钠(Na2SiO3·9H2O)、十六烷基三甲基溴化铵(CTAB)、硝酸铁(Fe(NO3)3·9H2O)、四硼酸钠(Na2B4O7·10H2O)、硝酸铬(Cr(NO3)3·9H2O)、酒石酸(TA)、十二烷基三甲基溴化铵(DTAB)、十二烷基氯化吡啶(DPC)、十二烷基磺酸钠(SDS)、十二烷基硫酸钠(SLS)、十二胺(DL)、十二酸(DA)、过氧化氢(H2O2,质量分数为30%)、苯酚(C6H5OH),均为分析纯,购于上海国药集团化学试剂有限公司。
1.2 催化剂制备
将5.7 g偏硅酸钠(Na2SiO3·9H2O)和1.8 g十六烷基三甲基溴化铵(CTAB)溶于50 mL去离子水中,搅拌至澄清,记为A溶液。分别称取4.5 g的硝酸铁(Fe(NO3)3·9H2O)、3.8 g四硼酸钠(Na2B4O7·10H2O)、4.0 g硝酸铬(Cr(NO3)3·9H2O),溶于10 mL去离子水中,待溶解后,记为B溶液。将B溶液缓慢加到A溶液中,室温下搅拌2 h,再向其中加入0.7 g酒石酸,搅拌5 min,用1 mol/L的H2SO4调节溶液pH=11.0。将所得溶液转移至聚四氟乙烯内衬的不锈钢反应釜中,于100℃下水热120 h。所得样品经洗涤、离心、干燥,并于马福炉中空气气氛下,550℃焙烧5 h,得到n(B)∶n(Cr)∶n(Fe)∶n(Si)=0.5∶0.5∶4∶1的催化剂,标记为0.5B-0.5Cr-4Fe-MCM-41。
1.3 催化剂表征
采用Rigaku D/Max-RA型X射线衍射仪测定催化剂的XRD谱, CuKα射线,Ni滤波片,管电压为40 kV,管电流40 mA,2θ范围1.5°~8°。采用Jarrell-Ash 1100型光谱仪(电感耦合等离子体原子发射光谱ICP)测定催化剂的活性组分(Fe、B、Cr)的含量。
1.4 表面活性剂对苯酚增溶作用的测定
常温下,称取6份4.29 g苯酚,分别加至10 mL去离子水中,再分别加入6种表面活性剂作增溶剂,通过测定加入的增溶剂质量得到该增溶剂的增溶效果。这6种增溶剂为十二烷基三甲基溴化铵(DTAB)、十二烷基氯化吡啶(DPC)、十二烷基磺酸钠(SDS)、十二烷基硫酸钠(SLS)、十二胺(DL)、十二酸(DA)。
1.5 苯酚羟基化反应实验步骤
在配有磁力搅拌、恒温水浴和三口烧瓶的装置中进行苯酚羟基化反应。将计量的苯酚、表面活性剂及催化剂溶于10 mL去离子水中,搅拌加热到指定温度,再滴加一定量的H2O2,反应2 h。取出反应液,冷却至室温,离心分离。采用外标法以Agilent 1100高效液相色谱仪分析产物组成,根据式(1)~式(4)计算苯酚羟基化反应的苯酚转化率和各产物选择性。
(1)
(2)
(3)
s(Diphenol)=s(Catechol)+s(Hydroquinone)
(4)
式(1)~式(4)中,n0为苯酚初始物质的量,mol;n1为已转化的苯酚物质的量,mol;n2为生成邻苯二酚的物质的量,mol;n3为生成对苯二酚的物质的量,mol;x(Phenol)为苯酚转化率,%;s(Catechol)为邻苯二酚的选择性,%;s(Hydroquinone)为对苯二酚的选择性,%;s(Diphenol)为苯二酚的选择性,%。
2结果与讨论
2.1 表面活性剂种类对室温下苯酚增溶作用及苯酚羟基化反应的影响
表1为6种表面活性剂对苯酚在水中的增溶作用。由表1可见,表面活性剂的种类对苯酚在水中的溶解度有较大的影响。加入少量DTAB、DPC、SDS,以及SLS后苯酚全部溶解于水,且增溶效果由强到弱的顺序为DPC、DTAB、SLS、SDS;而加入较多量DL和DA,苯酚也无法全部在水中溶解。常温下,非离子表面活性剂DL和DA本身水溶性较差,对苯酚的增溶作用不明显。离子型表面活性剂较易溶于水,其分子中的非离子基团(亲油基)对苯酚分子中的“苯环”部分具有较强的亲和力,从而增加了苯酚在水中的溶解作用;同时由于苯酚为强极性弱酸性物质,而离子型表面活性剂溶于水后,能电离生成离子,其产生的盐效应也会进一步增加苯酚的溶解度。
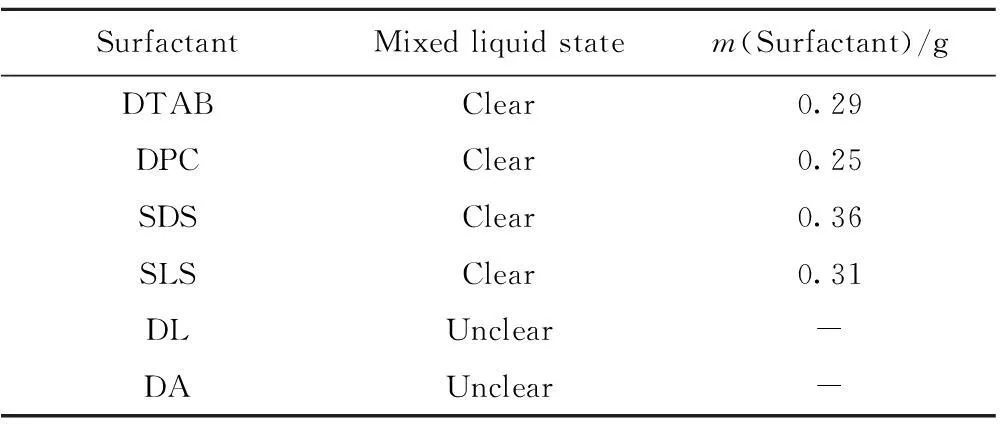
表1 6种表面活性剂对苯酚在水中的增溶作用
Experiment conditions:T=25℃;m(Phenol)=4.29 g;V(H2O)=10 mL
由表1还可知,阳离子表面活性剂对苯酚的增溶效果大于阴离子型表面活性剂的,这可能是阳离子型表面活性剂的有机基团带有正电荷,与苯酚电离出的苯氧阴离子的静电引力促使苯酚进一步电离溶解。DPC对苯酚具有最优的增溶效果可能是因为其分子中含有一个类似“苯环”的吡啶环,根据“相似相溶性”原理,苯酚更易溶于DPC所形成的胶团中。
选择对苯酚具有较好增溶作用的表面活性剂十二烷基磺酸钠(SDS)、十二烷基三甲基溴化铵(DTAB)和十二烷基氯化吡啶(DPC)作为增溶剂用于苯酚羟基化反应,室温下的反应结果列于表2。

表2 增溶剂的种类对苯酚羟基化反应的影响
Reaction conditions:n(Phenol)/n(H2O2)=3;T=25℃;t=2 h;m(Phenol)/(m(Phenol)+m(H2O))=0.30
由表2可知,采用的表面活性剂对苯酚的增溶效果越好,苯酚羟基化反应的转化率越低。这可能由于增溶效果较好的表面活性剂分子中的有机基团对苯酚的吸附作用较强,导致溶液中游离苯酚的浓度降低,与催化剂表面接触的苯酚量减少,从而使得苯酚转化率降低。考虑到SDS对苯酚的增溶效果较好,且便宜易得,由它作为苯酚羟基化反应的转化率较高,故选其为增溶剂考察反应条件对0.5B-0.5Cr-4Fe-MCM-41催化苯酚羟基化反应的影响。
2.2 0.5B-0.5Cr-4Fe-MCM-41催化苯酚羟基化反应的影响因素
2.2.1苯酚在水中质量分数的影响
在n(Phenol)/n(H2O2)=3、T=25℃、t=2 h的条件下,考察苯酚在水中质量分数m(Phenol)/(m(Phenol)+m(H2O))对苯酚羟基化反应的影响,结果列于表3。由表3可知,随着m(Phenol)/(m(Phenol)+m(H2O))的增加,所需表面活性剂的量也相应增加,随之苯酚转化率增加,苯二酚选择性则减小。m(Phenol)/(m(Phenol)+m(H2O))越高,该反应速率也就越快,即相同时间内苯酚转化率也就越大。从苯二酚收率考虑,适宜的m(Phenol)/(m(Phenol)+m(H2O))为0.30。
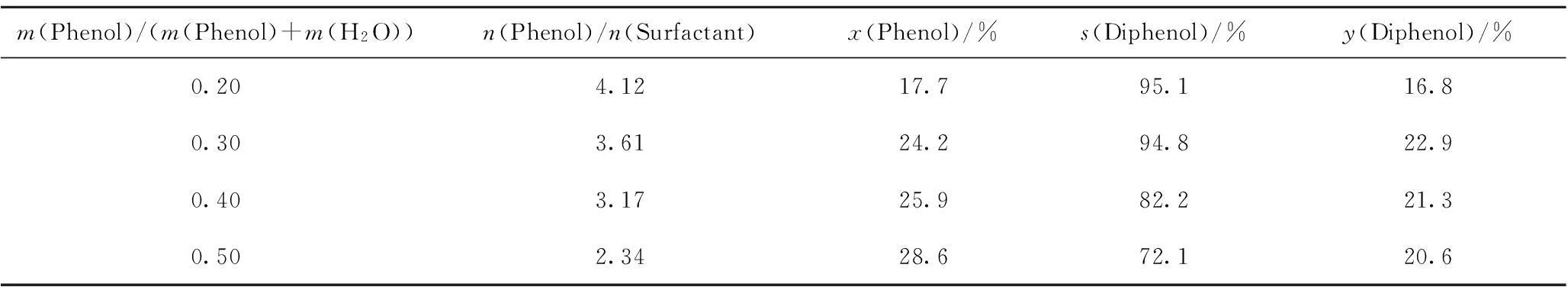
表3 m(Phenol)/(m(Phenol)+m(H2O))对苯酚羟基化反应的影响
n(Phenol)/n(H2O2)=3;T=25℃;t=2 h
2.2.2n(Phenol)/n(H2O2)的影响
在m(Phenol)/(m(Phenol)+m(H2O))=0.30、T=25℃、t=2 h的条件下,考察n(Phenol)/n(H2O2)对苯酚羟基化反应的影响,结果列于表4。由表4可见,随着n(Phenol)/n(H2O2)的减少,苯酚转化率相应地增加,苯二酚选择性则减小。这可能是H2O2的增加导致 H2O2快速分解,溶液中出现大量的OH·自由基。此外,过多的H2O2同时也会与苯二酚进一步反应,生成焦油及醌类物质,使其选择性下降。结果表明,在该催化体系中,H2O2用量不宜过多,适宜的n(Phenol)/n(H2O2)为 3。
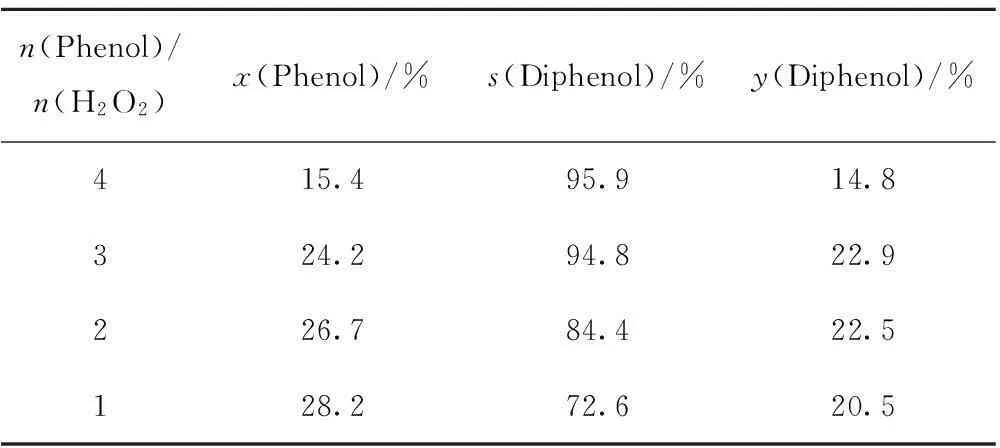
表4 n(Phenol)/n(H2O2)对苯酚羟基化反应的影响
T=25℃;t=2 h;m(Phenol)/(m(Phenol)+m(H2O))=0.30
2.2.3反应温度的影响
表5为不同反应温度下苯酚羟基化反应的转化率和产物选择性。由表5可见,随着反应温度的升高,苯酚转化率增加,苯二酚的选择性下降。当反应温度较低时,催化剂不能有效活化H2O2,苯酚转化率明显较低;而反应温度较高时,催化剂能有效活化H2O2,转化率增加。当温度较高时,苯二酚易过度氧化,因而选择性下降。因此,选择适宜的反应温度为25℃。
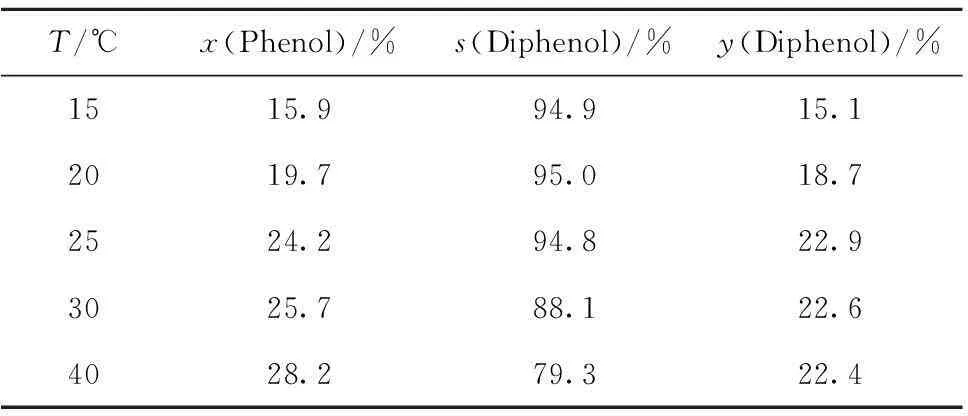
表5 反应温度对苯酚羟基化反应的影响
n(Phenol)/n(H2O2)=3;t=2 h;m(Phenol)/(m(Phenol)+m(H2O))=0.30
2.3 0.5B-0.5Cr-4Fe-MCM-41催化剂的重复使用性能
将每次反应后的催化剂过滤洗涤后于100℃下干燥1 h,再于550℃焙烧3 h,重复使用,考察催化剂的重复使用性能,结果示于图1。反应前以及5次重复使用后0.5B-0.5Cr-4Fe-MCM-41催化剂的XRD谱示于图2,二者的金属及助剂元素含量列于表6。
由图 1 可见,采用新鲜0.5B-0.5Cr-4Fe-MCM-41催化剂时,苯酚的转化率为24.2%,苯二酚的选择性达到94.8%;随着催化剂使用次数的增加,苯酚的转化率和苯二酚的选择性基本保持不变,重复使用至第 5 次时,苯酚转化率保持 20%以上,苯二酚的选择性仍在90%以上。这一结果表明,该催化剂在催化苯酚羟基化反应中具有良好的重复使用性能。
由图2可知,新鲜和重复使用5次后的0.5B-0.5Cr-4Fe-MCM-41催化剂的XRD谱衍射峰形状与位置基本相同,表明其介孔结构基本保持不变。
由表6可知,重复使用5次后,0.5B-0.5Cr-4Fe-MCM-41催化剂的活性组分Fe及助剂B、Cr的含量略有所下降,说明活性组分不易洗脱。因而,在该反应条件下,催化剂的稳定性较好,具有很好的工业应用前景。
目前,工业上主要以TS-1作为合成苯二酚的催化剂,将笔者研发的0.5B-0.5Cr-4Fe-MCM-41催化剂与TS-1[25]作对比,结果列于表7。由表7可知,0.5B-0.5Cr-4Fe-MCM-41与TS-1的催化活性相当。0.5B-0.5Cr-4Fe-MCM-41催化苯酚羟基化反应在室温下进行,以水为溶剂,节能环保,符合绿色化学的理念,为工业化生产打下良好的基础。

图1 0.5B-0.5Cr-4Fe-MCM-41催化苯酚羟基化反应
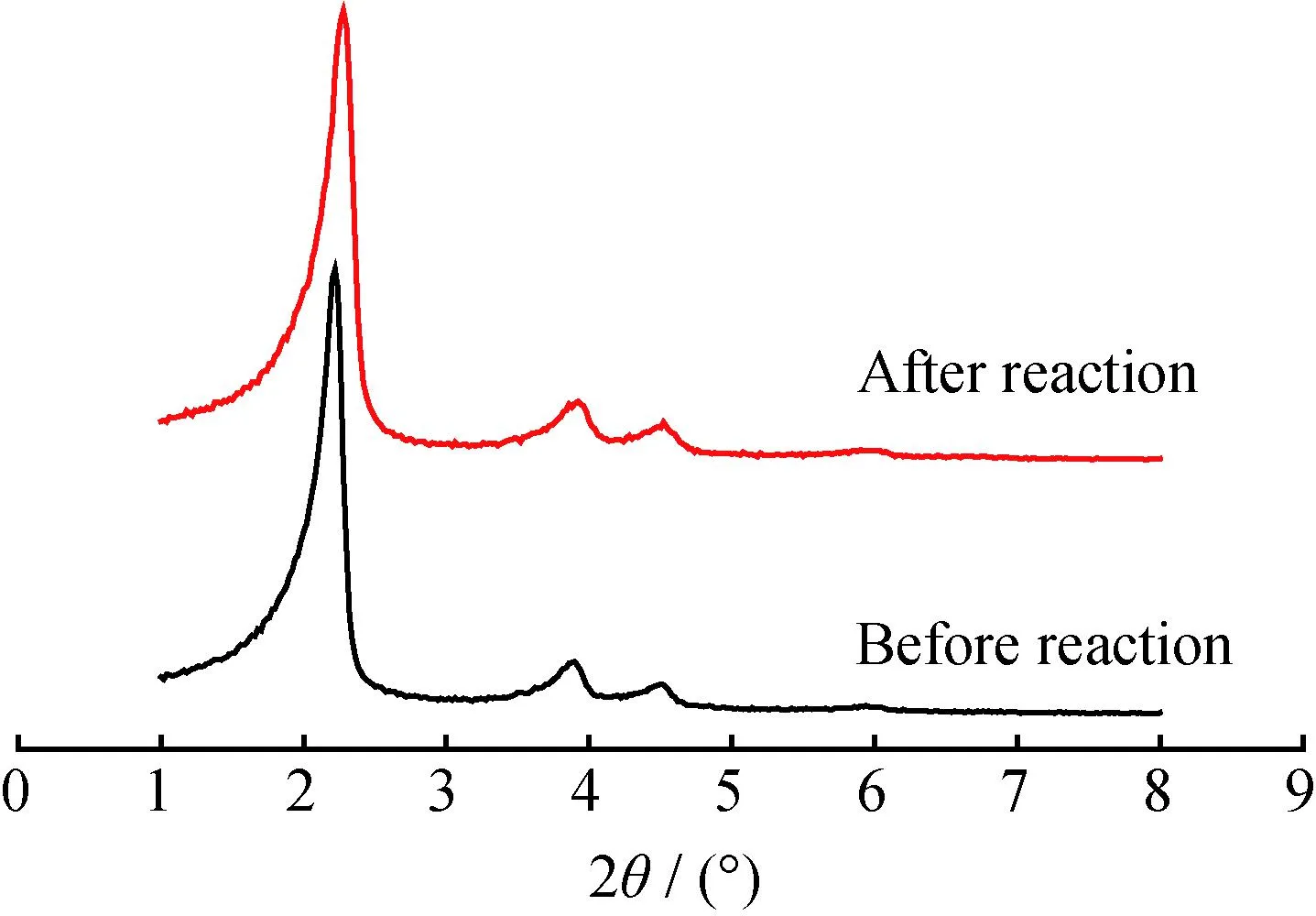
图2 新鲜和催化苯酚羟基化反应5次后

0.5B-0.5Cr-4Fe-MCM-41nFe/nSinB/nSinCr/nSiFresh4.020.470.44Afterfivereactions3.950.440.39
ICP result
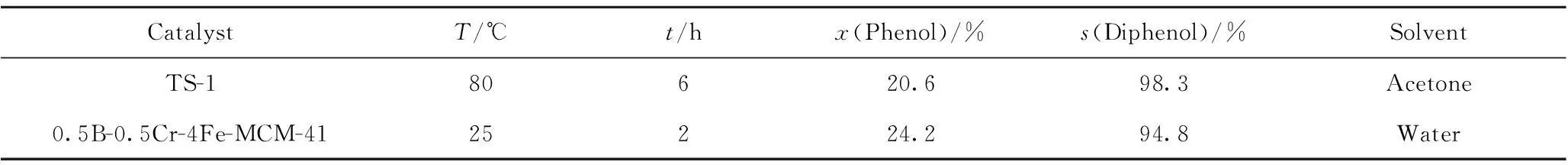
表7 TS-1与0.5B-0.5Cr-4Fe-MCM-41催化苯酚羟基化性能对比
3结论
(1) 在苯酚羟基化催化反应体系中加入阴离子表面活性剂十二烷基磺酸钠,可提高室温下苯酚的水溶性,也可促使催化剂活性中心分散,提高催化性能,使该反应能够在较高浓度下进行。反应以水为溶剂,节能环保,符合绿色化学理念。
(2) 以0.5B-0.5Cr-4Fe-MCM-41为催化剂,十二烷基磺酸钠为苯酚增溶剂,苯酚羟基化反应的最佳反应条件为m(Phenol)/(m(Phenol)+m(H2O))=0.30、n(Phenol)/n(H2O2)=3、反应温度25℃、反应时间2 h;在此条件下,苯酚的转化率达到24.2%,苯二酚的选择性达到94.8%。
参考文献
[1] LIANG Xiuli, YANG Ruiguang, LI Guiying, et al. Phenol hydroxylation over Fe-incorporated mesoporous materials prepared by coprecipitation[J]. Microporous and Mesoporous Materials, 2013, 182: 62-67.
[2] 郑亚清, 陶文波, 丁克鸿. 苯酚选择性氧化制对苯二酚催化剂的合成及性能研究[J]. 工业催化, 2014, 22(4): 287-292. (ZHENG Yaqing, TAO Wenbo, DING Kehong. Synthesis and catalytic properties of catalyst Cd-MOF-cat for selective oxidation of phenol to hydroquinone[J]. Industrial Catalysis, 2014, 22(4): 287-292.)
[3] 卢长娟, 陈日志, 金万勤, 等. TS-1催化苯酚羟基化制苯二酚的本征动力学研究[J]. 化学工程, 2008, 36(6): 38-41. (LU Changjuan, CHEN Rizhi, JIN Wanqin, et al. Intrinsic kinetics of hydroxylation of phenol to catechol with TS-1 peroxide catalyst[J]. Chemical Engineering, 2008, 36(6): 38-41.)
[4] CHEN Rizhi, BAO Yaohui, XING Weihong, et al. Enhanced phenol hydroxylation with oxygen using a ceramic membrane distributor[J]. Chinese Journal of Catalysis, 2013, 34(1): 200-208.
[5] 张海娇, 姚明恺, 刘月明, 等. TS-1 分子筛的无机法合成及其催化苯酚羟基化性能[J]. 催化学报, 2007, 28(10): 895-899. (ZHANG Haijiao, YAO Mingkai, LIU Yueming, et al. Synthesis of TS-1 using inorganic SiO2-TiO2precursor and its catalytic performance for hydroxylation of phenol[J]. Chinese Journal of Catalysis, 2007, 28(10): 895-899.)
[6] BECK J, VARTULI J, ROTH W. A new family of mesoporous molecular sieves prepared with liquid crystal templates[J]. Journal of the American Chemical Society, 1992, 114(27): 10834-10843.
[7] KRESGE C, LEONOWICZ M, ROTH W. Ordered mesoporous molecular sieves synthesized by a liquid-crystal template mechanism[J]. Nature, 1992, 359(6397):710-712.
[8] JIANG Yanqiu, LIN Kaifeng, ZHANG Yining, et al. Fe-MCM-41 nanoparticles as versatile catalysts for phenol hydroxylation and for Friedel-Crafts alkylation[J]. Applied Catalysis A:General, 2012, 445: 172-179.
[9] 陈强, 马红蕾, 孔岩, 等. 苯酚羟基化制备苯二酚介孔分子筛催化剂的合成与改性[J]. 石油学报(石油加工), 2014, 30(1): 134-139. (CHEN Qiang, MA Honglei, KONG Yan, et al. Synthesis and modification of mesoporous molecular sieve catalyst used for phenol hydroxylation[J]. Acta Petrolei Sinica (Petroleum Processing Section), 2014, 30(1): 134-139.)
[10] WU Cheng, KONG Yan, WANG Jun, et al. Synthesis, characterization and catalytic performance for phenol hydroxylation of Fe-MCM-41 with high iron content[J]. Microporous and Mesoporous Materials, 2008, 113(1-3): 163-170.
[11] 李新柱, 张记市. 铁掺杂介孔磷铝分子筛催化苯酚羟基化反应性能[J]. 石油学报(石油加工), 2010, 26 (4): 525-530. (LI Xinzhu, ZHANG Jishi. Catalytic performance of Fe-substituted mesoporous aluminophosphate molecular sieves for phenol hydroxylation[J]. Acta Petrolei Sinica (Petroleum Processing Section), 2010, 26(4): 525-530.)
[12] MA Xinbin, CHI Hanwen, YUE Hairong, et al. Hydrogenation of dimethyl oxalate to ethylene glycol over mesoporous Cu-MCM-41 catalysts[J]. AIChE Journal, 2013, 59(7):2530-2539.
[13] ZHAO Nan, GAO Haixia, KONG Yan, et al. Synthesis, characterization and catalytic activity of nano-spherical MCM-41 modified with vanadium[J]. Journal of Nanoscience and Nanotechnology, 2014, 14(9): 7300-7306.
[14] HAN Bing, WANG Haiqing, KONG Yan, et al. Improvement on the mesostructural ordering and catalytic activity of Co-MCM-41 with ascorbic acid as auxiliary[J]. Materials Letters, 2013, 100: 159-162.
[15] 孙庆林, 杨渊, 孔岩, 等. 高钴含量MCM-41合成、催化性能及钴形态的化学分析方法[J]. 无机化学学报, 2011, 27(12): 2346-2352. (SUN Qinglin, YANG Yuan, KONG Yan, et al. Synthesis, catalytic activity and chemical analysis method for Co-MCM-41 with high cobalt content[J]. Chinese Journal of Inorganic Chemistry, 2011, 27(12): 2346-2352.)
[16] KILICARSLAN S, DOGAN M, DOGU T. Cr incorporated MCM-41 type catalysts for isobutane dehydrogenation and deactivation mechanism[J]. Industrial & Engineering Chemistry Research, 2013, 52(10): 3674-3682.
[17] THATSHANAMOORTHY V, NARAYANAN V. Synthesis, characterization and electrochemical sensing property of W-MCM-41[J]. Asian Journal of Chemistry, 2013, 25(11): 6083-6086.
[18] ELHAM Z, FAEZEH F, JIM S. Synthesis, crystal structure and catalytic activity of a new Mo Schiff base complex with Mo histidine immobilized on Al-MCM-41 for oxidation of sulfides[J]. Inorganica Chimica Acta, 2014, 414: 63-70.
[19] QI Ben, LOU Lanlan, WANG Yanbing, et al. Comparison of different prepared Mn-MCM-41 catalysts in the catalytic epoxidation of alkenes with 30% H2O2[J]. Microporous and Mesoporous Materials, 2014, 190: 275-283.
[20] WANG Shengping, MA Changqing, SHI Yun, et al. TI incorporation in MCM-41 mesoporous molecular sieves using hydrothermal synthesis[J]. Frontiers of Chemical Science and Engineering, 2014, 8(1): 95-103.
[21] MANUEL G, PATRICIA B, GIUSEPPE F, et al. Preparation of Pd/Cu MCM-41 catalysts for hydrodechlorination: Influence of the synthesis procedure[J]. Microporous and Mesoporous Materials, 2014, 190: 1-9.
[22] WU Yong, ZHANG Yinjie, KONG Yan, et al. Synthesis, characterization and catalytic activity of binary metallic titaniumand iron containing mesoporous silica[J]. Microporous and Mesoporous Materials, 2012, 162: 51-59.
[23] MUTHURAJ E, LEENA P, THIRIPURANTHAGAN S, et al. Room temperature efficacious synthesis of diphenylmethane over Fe/Al-MCM-41 catalysts[J]. Catalysis Communications, 2010, 11(10): 876-879.
[24] 孔岩, 徐鑫杰, 王军, 等. 助剂种类对Cu-MCM-41在苯羟基化反应中催化性能的影响[J]. 催化学报, 2008, 29(4): 385-390. (KONG Yan, XU Xinjie, WANG Jun, et al. Effect of promoters on the catalytic activity of MCM-41 with high copper content in benzene hydroxylation[J]. Chinese Journal of Catalysis, 2008, 29(4): 385-390.)
[25] 张海娇, 谢伟, 刘月明. 低成本TS-1分子筛的制备及其苯酚羟基化性能研究[J]. 工业催化, 2007, 15(5): 60-63. (ZHANG Haijiao, XIE Wei, LIU Yueming. Preparation of low cost TS-1 zeolite and its catalytic properties for hydroxylation of phenol[J]. Industrial Catalysis, 2007, 15(5): 60-63.)
Oxidation of Phenol With High Concentration in Aqueous Solution to Diphenol by H2O2Under Room Temperature
XI Tao, MA Honglei, ZHANG Yingjie, CHEN Qiang, KONG Yan
(StateKeyLaboratoryofMaterials-OrientedChemicalEngineering,CollegeofChemistryScienceandEngineering,
NanjingUniversityofTechnology,Nanjing210009,China)
Abstract:With surfactants as solubilizer, water as solvent, H2O2as oxidizer, 0.5B-0.5Cr-4Fe-MCM-41 as catalyst, catechol and hydroquinone were synthesized from phenol. The effects of the surfactant kinds, mass fraction of phenol in water (m(Phenol)/(m(Phenol)+m(H2O))), molar ratio of phenol to H2O2(n(Phenol)/n(H2O2)), reaction temperature on the hydroxylation of phenol were investigated. Under the optimal reaction conditions, i.e., SDS as solubilizer, m(Phenol)/(m(Phenol)+m(H2O))=0.30, n(Phenol)/n(H2O2)=3, 24.2% conversion of phenol and 94.8% selectivity of diphenol were achieved after reacted at 25℃ for 2 h. The reusability of 0.5B-0.5Cr-4Fe-MCM-41 catalyst was excellent, meaning that this technology can fully match the industrial application.
Key words:mesoporous molecular sieves; hydroxylation of phenol; high concentration; surfactant; room temperature
中图分类号:TQ426.6; O643.36; TQ032.4
文献标识码:A
doi:10.3969/j.issn.1001-8719.2016.01.028
文章编号:1001-8719(2016)01-0201-06
基金项目:国家自然科学基金(21276125、21476108)和江苏省高校研究生科研创新计划(CXLX13_430)项目资助
收稿日期:2014-11-13
第一作者: 席涛,男,硕士研究生,从事工业催化氧化研究
通讯联系人: 孔岩,男,教授,博士,从事多孔催化剂的工业应用研究;Tel:025-83587860; E-mail:kongy36@njut.edu.cn

