芦丁在Nafion/纳米金@石墨烯修饰碳糊电极上的电化学行为及测定
匡云飞 ,邹建陵,李 薇,杨颖群,许金生,冯泳兰,李玉明
(衡阳师范学院 化学与材料科学学院,湖南 衡阳 421008)
芦丁在Nafion/纳米金@石墨烯修饰碳糊电极上的电化学行为及测定
匡云飞 ,邹建陵,李 薇,杨颖群,许金生,冯泳兰,李玉明
(衡阳师范学院 化学与材料科学学院,湖南 衡阳 421008)
用滴涂法制备了Nafion/纳米金@石墨烯修饰碳糊电极(Nafion/ AuNPs@GS/CPE),研究了芦丁在该修饰电极上的电化学行为,探讨了微分脉冲溶出伏安法(DPSV)测定芦丁的最佳实验条件。结果表明,在含一定量的芦丁的柠檬酸-柠檬酸钠缓冲溶液(pH 3.4)中,发现在约0.3 V左右处芦丁产生一灵敏的氧化峰,其氧化峰电流Ipa与其浓度c在0.5~10 μmol/L 和10~200 μmol/L范围内呈良好的线性关系(R分别为0.995 6和0.996 0),检出限(S/N=3)为0.3 μmol/L。该修饰电极具有良好的选择性、稳定性和重现性,将其用于实际样品中芦丁含量的检测,结果满意。
芦丁;微分脉冲溶出伏安法;纳米金;石墨烯;修饰碳糊电极
芦丁(Rutin,RT),也叫芸香苷、维生素P,是一种来源于植物的天然黄酮类化合物,属维生素药类。它不仅可以作为治疗药物,还可以作为保健品。研究发现,芦丁有许多药理作用[1~5],如抗自由基活性、体外抗菌、抗脂质过氧化、降低血糖、血管舒张、抑制血小板活化因子、抗急性胰腺炎等。因此,探求新的检测植物和药物中芦丁的含量具有十分重要的社会意义和应用价值。
目前对芦丁的检测研究常用方法有高效液相色谱法[6]、化学发光法[7]、毛细管电泳法[8]、紫外分光光度法[9]、流动注射法[10]等,但是这些方法成本较高、操作过程复杂、检测时间长,而电化学检测方法[11~15]能快速检测,且成本较低、易于操作,因此电化学检测方法得到了广泛的应用。
本文以石墨烯[16]和纳米金[17](均为自制)、Nafion为修饰剂,组装了一种新型的、高灵敏的检测实际样品中芦丁含量的电化学传感器——Nafion/纳米金@石墨烯修饰碳糊电极(Nafion/AuNPs@GS/CPE),可用于实际样品中芦丁检测。
1 实验部分
1.1 仪器与试剂
EC550电化学工作站(武汉高仕睿联科技有限公司),PL203电子分析天平(梅特勒-托利多仪器(上海)有限公司),SB-3200DTN超声波清洗机(宁波新芝生物科技股份有限公司),DHG-9036A恒温鼓风干燥箱(上海精宏实验设备有限公司)等。
芦丁(BR)、氯金酸(AR)、石墨粉(CP)购于国药集团化学试剂有限公司,铁氰化钾(AR)、N,N-二甲基甲酰胺(AR)购于天津市大茂化学试剂厂,其它试剂均为AR,试验用水为高纯去离子水。
1.2 修饰电极的制备
以1∶3质量比称取一定量的液体石蜡和石墨粉于研钵中混合均匀至糊状,再填入到聚四氟乙烯碳糊电极空腔中并压实,在光滑称量纸上磨光,即为裸碳糊电极(CPE)。再将其置于0.5 mol/L H2SO4中,在-0.1V~0.7V电位范围内以100 mV/s循环伏安扫描至曲线趋于稳定,取出,水洗,晾干,备用。
按2:1:1(体积比)取已超声分散好的石墨烯(GS,1 mg/mL)、纳米金(AuNPs,1 mg/mL)溶胶和Nafion溶液(w = 0.1 %)混合,再超声得到Nafion/AuNPs@GS均匀的修饰液。用微量移液器移取适量修饰液滴涂在CPE的表面,用红外灯烘干成膜,即得到Nafion/AuNPs@GS/CPE。为了对比,将石墨烯溶胶(1 mg/mL)和Nafion溶液(w=0.1 %)按2:1的体积比,纳米金(1 mg/mL)溶液和Nafion溶液(0.1 %)按1:1的体积比分别混合超声,采用上述方法分别得到Nafion/GS/CPE和Nafion/AuNPs/CPE。
1.3 实验方法
在含一定量芦丁的pH 3.4的柠檬酸-柠檬酸钠缓冲溶液中,以Nafion/AuNPs@GS/CPE电极为工作电极,饱和甘汞电极(SCE)为参比电极,铂电极为辅助电极,在-0.2 V处搅拌富集150 s,平衡15 s,在脉冲高度PH 0.04 V,阶梯高度SH 0.004 V,脉冲宽度PW 0.05 s,阶梯时间ST 0.2 s的脉冲条件下,静止5 s,在0.1 V~0.9 V范围内采用微分脉冲溶出伏安法(DPSV)扫描,并记录0.32 V左右处氧化峰电流,以峰电流为横坐标,芦丁浓度为纵坐标,绘制工作曲线,同时采用标准加入法测量样品中芦丁的含量。
2 结果与讨论
2.1 以铁氰化钾为探针表征修饰电极
在5×10-3mol/L K3Fe(CN)6和1 mol/L KNO3溶液中,分别以CPE(a)、Nafion/AuNPs/CPE(b)、Nafion/GS/CPE(c)和Nafion/AuNPs@GS/CPE (d)为工作电极,-0.1~0.7 V范围内以50 mV/s扫速进行循环伏安扫描(如图1)。

图1 5×10-3 mol/L铁氰化钾和1 mol/L KNO3溶液的CV图a:CPE,b:Nafion/AuNs/CPE ,c:Nafion/GS/CPE,d:Nafion/GS@AuNs/CPE
实验表明,Fe(CN)63-/4-在CPE上的氧化峰电位(Epa)为0.330 V,还原峰电位(Epc)为0.241 V,峰电位差(ΔEp)为0.089 V,Ipa/Ipc约为2.4;在Nafion/AuNPs/CPE上Epa为0.325 V,Epc为0.237 V,ΔEp为0.088 V,Ipa/Ipc约为2.2;在Nafion/GS/CPE上的Epa为0.319 V,Epc为0.237 V,ΔEp为0.082 V,Ipa/Ipc约为1.5;而在Nafion/ AuNPs @ GS/CPE上的Epa为0.314 V,Epc为0.233 V,ΔEp为0.081 V,Ipa/Ipc约为1.1。经过比较,探针Fe(CN)63-/4-在Nafion/ AuNPs @ GS/CPE上产生的电流最大,且ΔEp最小,表明由于GS和AuNPs具有优良的导电性、大的比表面积及强吸附等特性,利用两种纳米材料的协同作用,使Nafion/AuNPs@GS膜能有效地提高电极的导电效率和电极反应的可逆性,加快了电极表面的电子传递。
2.2 芦丁在Nafion/AuNPs@GS/CPE上的电化学行为
2.2.1 循环伏安行为
于-0.2~0.6 V电位范围内,以0.1 V/s的扫描速度,研究了芦丁在修饰电极上的循环伏安行为(如图2)。实验发现:在含1.00×10-4mol/L芦丁的pH=3.4的柠檬酸-柠檬酸钠缓冲溶液中,芦丁在CPE上的Epa为0.316 V,Epc为0.234 V,ΔEp为0.082 V。在Nafion/AuNPs/CPE上,Epa为0.313 V,Epc为0.233 V,ΔEp为0.080 V。在Nafion/GS/CPE上,Epa为0.309 V,Epc为0.232 V,ΔEp0.077 V。在Nafion/AuNPs@GS/CPE上,Epa为0.304 V,Epc为0.230 V,ΔEp0.074 V。同时还比较了芦丁在不同电极上的峰电流大小, 复合修饰电极上的Ipa和Ipc最大,ΔEp最小。由此说明,因GS和AuNPs的引入,使电极的有效表面积增大,亦即使其与芦丁结合的反应位点增多;同时电极的导电性增强,加快了芦丁与电极之间的电子传递,提高了修饰电极对芦丁的电催化活性,增强了电极反应的可逆性,提高了测定方法的灵敏度。
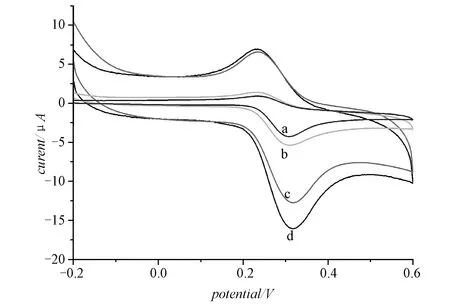
图2 1.00×10-4 mol/L芦丁在各电极上的CV图a:CPE,b:Nafion/AuNs/CPE ,c:Nafion/GS/CPE,d:Nafion/GS@AuNs/CPE
2.2.2 微分脉冲溶出伏安行为
在-0.2~0.6 V电位范围内,以pH=3.4的柠檬酸-柠檬酸钠缓冲溶液为底液,分别以CPE,Nafion/AuNPsCPE,Nafion/GS/CPE,Nafion/AuNPs@GS/CPE为工作电极对1.00×10-4mol/L芦丁的进行DPSV扫描(如图3)。
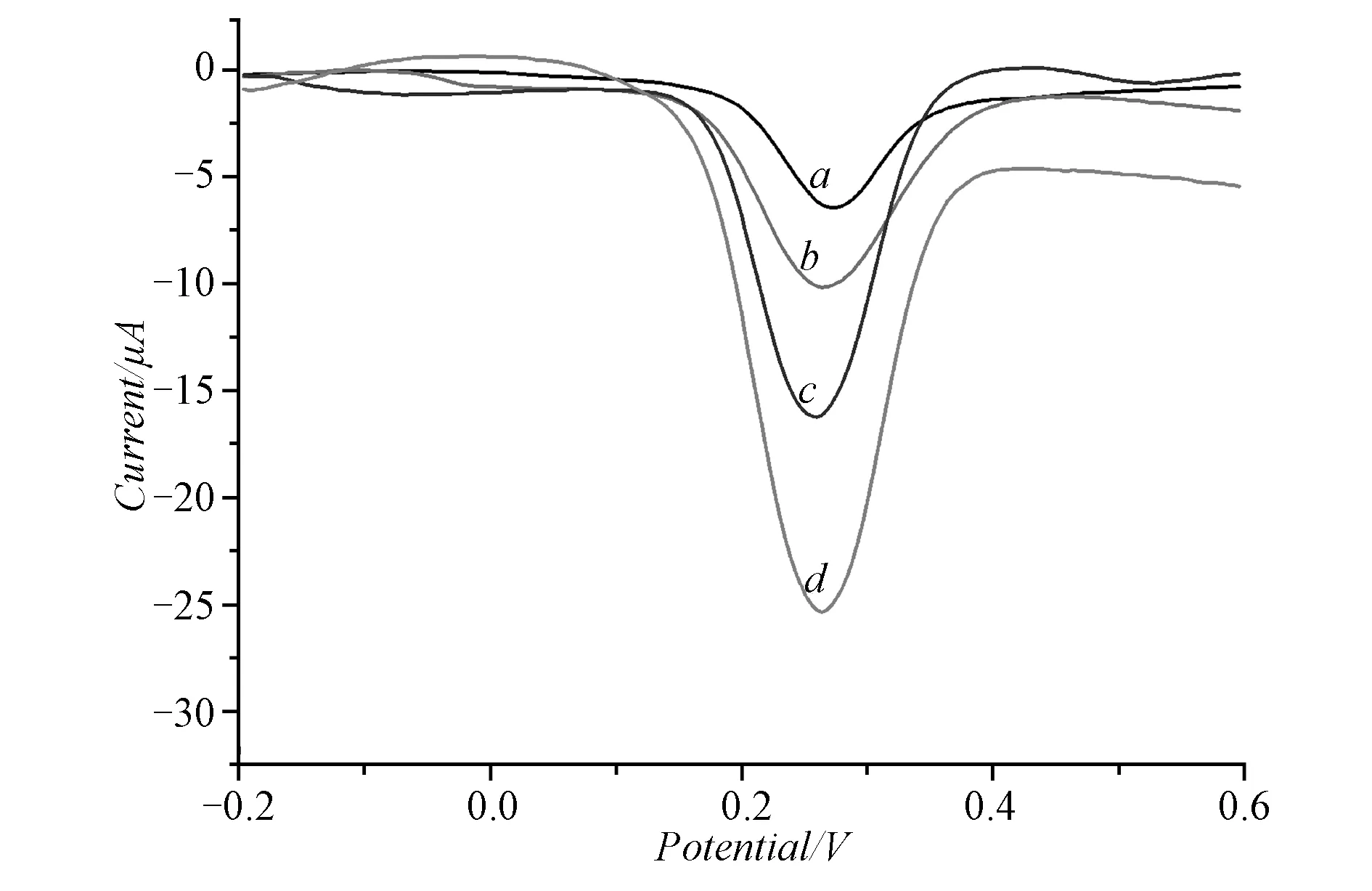
图3 1.00×10-4 mol/L芦丁的DPSV图a:CPE,b:Nafion/AuNs/CPE ,c:Nafion/GS/CPE,d:Nafion/GS@AuNs/CPE
实验发现,从a到d氧化峰电流逐渐增加,氧化峰电位逐渐负移。与CPE电极相比,芦丁在Nafion/AuNPs/CPE,Nafion/GS/CPE,Nafion/AuNPs@GS/CPE上的Ipa分别约为CPE电极的1.821,2.936,4.735倍。氧化峰电位分别负移了0.004,0.008,0.012 V。进一步说明复合修饰电极充分发挥了GS和AuNPs的协同效应,使得复合修饰电极具有更高的灵敏度和选择性。
2.3 制备电极条件的优化
采用DPSV,在-0.2~0.6 V内,以pH=3.4的柠檬酸-柠檬酸钠缓冲溶液为底液,分别以GS和AuNPs分散液(浓度均为1 mg/mL)、Nafion(w=0.1 %)按不同体积比超声混合后制备修饰电极,然后以其为工作电极对1.00×10-4mol/L芦丁的进行DPSV扫描。实验发现,当体积比为2∶1∶1时制备的修饰电极,其氧化峰电流最大,因此, GS分散液、AuNPs分散液、Nafion三者的最佳配比为2∶1∶1。
同时考察了修饰剂用量的影响,当修饰剂用量在2 μL~12 μL范围内时,实验发现,随着修饰液量的增加,芦丁的Ipa也逐渐增加;修饰液量为8 μL时,Ipa达到最大值,随后缓慢下降。这是因为随着修饰量的增加,电极的表观表面积增加,芦丁在电极上的吸附量也随之增多,电化学响应增强,当修饰液达到8 μL后继续增加修饰液量时,由于电极表面修饰材料过厚,导致其导电能力下降,使得Ipa也下降。因此本实验选用8 μL为最佳修饰液用量。
2.4 底液种类和溶液pH的选择
采用DPSV,在0.1~0.9 V范围内分别考察了1.00×10-4mol/L芦丁在KCl-HCl(pH1.7)、KHC8H4O4-HCl(pH 3.6) 、CHCOOH-CH3COONa(pH 3.8)、KHC8H4O4-NaOH (pH 4.8)、Na2HPO4-柠檬酸(pH 5.2)、柠檬酸-柠檬酸钠(pH 6.4)、Na2HPO4-NaH2PO4(pH 7.0)、NH4Cl-NH3(pH 9.1)、H3BO3-KCl-NaOH(pH 10.0)、Na2CO3-NaHCO3(pH 10.1)、Na2HPO4-NaOH (pH 12.0)、KCl-NaOH(pH 13.0)等缓冲溶液中的响应情况,结果表明,芦丁在柠檬酸-柠檬酸钠缓冲溶液中Ipa最大,峰形窄而尖锐且对称。故本实验选取柠檬酸-柠檬酸钠缓冲溶液作为最佳底液。
同时考察了芦丁在不同pH(3.0~6.6)缓冲液中的响应。结果显示,当缓冲液的pH为3.4时,Ipa达到最大值,故本实验选取pH为3.4的柠檬酸-柠檬酸钠缓冲液为最佳实验条件。且芦丁的Epa随pH的增大而逐渐负移,线性关系为:Epa(V)=0.719 0-0.057 9pH (R=0.995 1),斜率为-0.057 9,与电化学反应理论值-0.059 2非常接近,证明芦丁在Nafion/AuNPs@GS /CPE电极上发生的氧化还原反应为等质子等电子过程。
2.5 扫描速度的影响
采用CV在25~500 mV/s范围内对含1.00×10-4mol/L芦丁以不同扫描速度进行扫描(图4)。
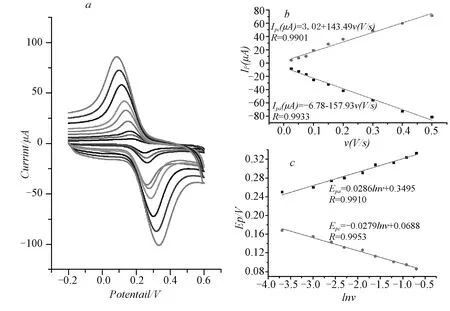
图4 扫描速度影响图(b)Ip与v的关系图;(c)Ep与lnv的关系图
实验表明,氧化还原峰电流均随扫速的增大而增加,Ipa和Ipc与扫速v均呈良好的线性关系(图4(b)),即:Ipa(μA) = 3.02+ 143.49v(V/s) (R=0.990 1)和Ipc(μA) = -6.78 -157.93v(V/s) (R=0.993 3)。这说明芦丁在Nafion/AuNPs@GS/CPE上的氧化还原过程受吸附控制。同时还发现,Epa和Epc与lnv亦呈良好的线性关系(图4(c)),即:Epa(V) = 0.349 5+0.028 6lnv(R=0.9910)和Epc(V) = -0.027 9-0.027 9lnv(R=0.995 3)。这说明随着扫速的增加,氧化还原峰电位之差也逐渐增大,可逆性逐渐变小。
2.6 DPSV测定最佳实验条件的优化
采用DPSV法,以Nafion/AuNPs@GS /CPE为工作电极,以pH为3.4柠檬酸-柠檬酸钠缓冲溶液为底液,测定1.00×10-4mol/L的芦丁。经过反复试验,最后得出的最佳实验富集电位、富集时间、平衡时间、静置时间分别为:-0.2 V、150 s、15 s、5 s。
2.7 线性范围和检出限
在最佳实验条件下,采用DPSV测定了不同浓度的芦丁溶液(见图5)。实验发现,在0.5~10 μmol/L及10~200 μmol/L浓度范围内,芦丁浓度与氧化峰电流成良好的线性关系,线性回归方程分别为:Ipa(μA)=2.432c(μmol/L)+ 4.673 (R=0.995 6)和Ipa(μA)=0.1922c (μmol/L) + 23.85 (R=0.996 0),检出限(S/N=3)为0.3 μmol/L。
2.8 选择性试验
在最佳实验条件下,采用DPSV测定了几种常见物质对1.00×10-4mol/L芦丁测定的影响,实验表明,100倍的Zn2+、Fe3+、Mn2+、Cu2+、淀粉、葡萄糖;200倍的谷氨酸、抗坏血酸对芦丁的测定没有影响。这说明Nafion/AuNPs@GS/CPE对芦丁具有较好的选择性。
2.9 电极的重现性和稳定性
在最佳实验条件下,采用DPSV在用同一支电极对1.00×10-4mol/L芦丁溶液连续测定11次,所得Ipa的RSD为2.0 %。按修饰电极的制备方法制备同一批次5根修饰电极,采用相同的方法对1.00×10-4mol/L芦丁溶液中测定,其Ipa的RSD为4.9 %。同时采用相同的方法,对同一电极在不同时间进行测定,发现该修饰电极在放置15天后其氧化峰电流降低了9.4 %。实验结果说明了该Nafion/AuNPs@GS/CPE具有良好的稳定性和重现性。
2.10 样品分析
在最佳实验条件下,采用DPSV用Nafion/AuNPs@GS/CPE对芦丁样品进行测定。样品芦丁片是由山西云鹏制药有限公司生产,产品批号为A121201,每片芦丁片含量为20 mg。将5片芦丁片放在研钵中磨碎,用无水乙醇定容至100 mL,作为样品溶液,取5份1 mL该样品溶液分别于编号为1、2、3、4、5的10 mL比色管中,然后从2号开始依次加入芦丁1.00×10-3mmol/L标准液1 mL、2 mL、3 mL、4 mL,再用pH=3.4柠檬酸-柠檬酸钠缓冲溶液定容至刻度,转移到小电解杯中进行DPSV测定,重复测定5次,由标准加入法求出芦丁的浓度(5次)分别为159.4,159.1,158.7,159.8,159.5 μmol/L,平均值为159.3 μmol/L,RSD为4.2 %。
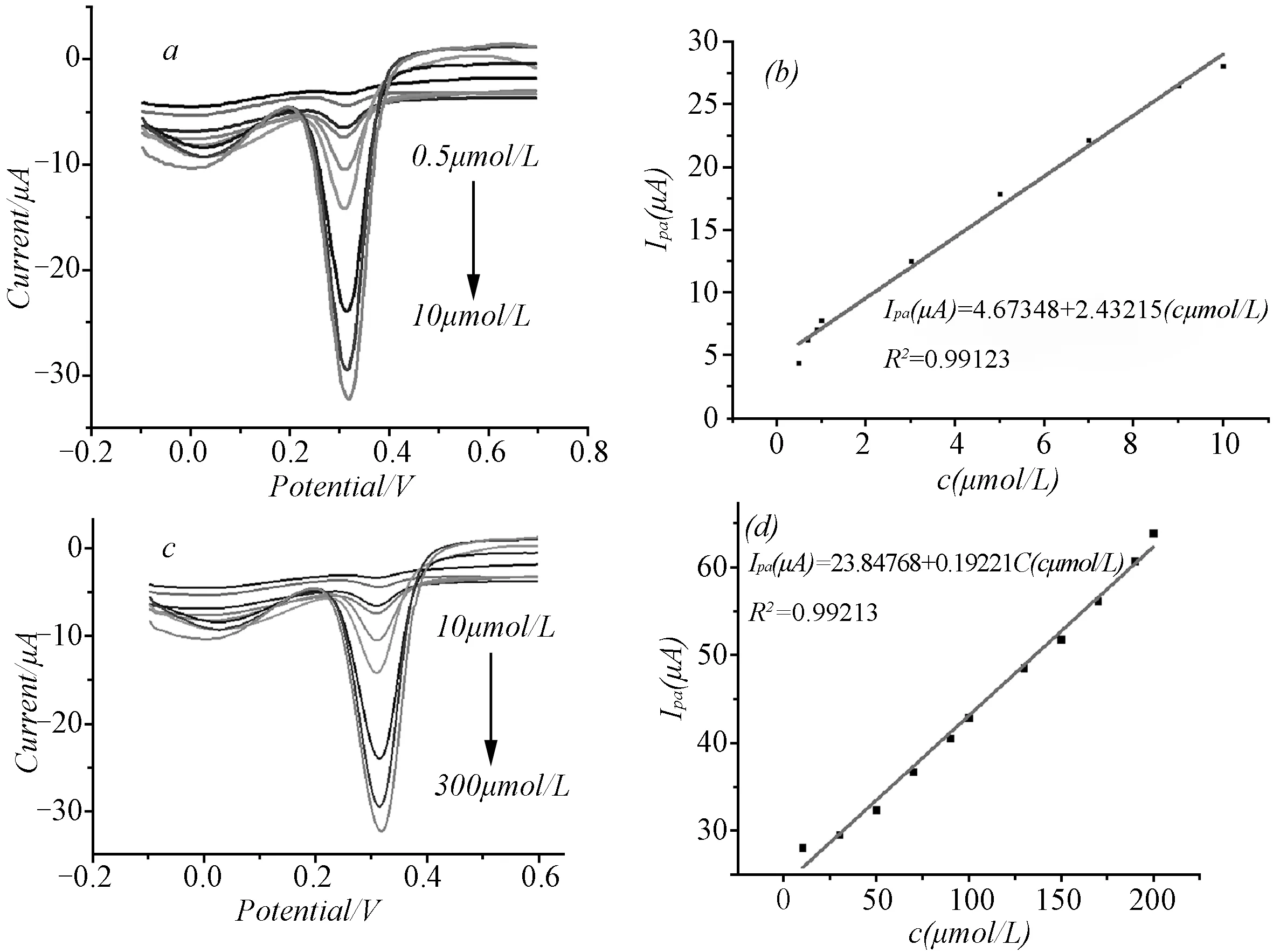
图5 线性范围和工作曲线(a)(b)0.5~10 μmol/L;(c)(d)10~200 μmol/L
采用标准加入法测定样品的回收率,结果见表2,回收率在97.0 %~101.5 %,结果比较满意。

表1 芦丁样品回收率测定
[1] 黄金珠.芦丁对大鼠肠缺血再灌注损伤的保护作用[J].中国现代药物应用,2012,6(16):131-132.
[2] 姚萍,葛新,董小青,等.芸香苷的体外抑菌作用[J].中国卫生检验杂志,2013,23(2):335-337.
[3] 黄建东,王建中,孟阿会,等.芦丁铬的合成及其辅助降血糖作用观察[J].食品工业科技营养与保健,2011,6(11):376-383.
[4] 王斯慧,黄琬凌,陈庆松,等.芦丁、槲皮素对α-淀粉酶抑制活性研究[J].食品与发酵科技, 2012,48(3):34-37.
[5] 陈爱华,赵维中.芸香苷对急性胰腺炎大鼠胰腺毛细血管通透性的影响[J].军医进修学院学报,2010,31(4):358-362.
[6] SHEN Y. P, YIN H. W, CHEN B, et al. Validated reversed phase-high performance liquid chromatographydiode array detector method for the quantitation of rutin, a natural immnnostimulant for improving survival in aquacukure practice,in toonea sinensis folium [J].Pharmacogn. Mag,2012,29(8): 49-53.
[8] SHI QIANG, SUI LU ZHI, LU YUAN QI. Research on flavonoids contents in Fructus Sophorae with capillary zone electrophoresis[J].Pakistan Journal of Pharmaceutical Sciences,2013,26(6): 1131-1136.
[9] OBMSNN ASTRID, PUREVSUREN, SODNOMTSEREN, et al. HPLC determination of flavonoid glycosides in Mongolian dianthus versicolor fisch (caryophllaceae) compared with quantification by UV spectrophotometry[J]. Phytochemical Analysis,2012,23(3):254-259.
[10] 孙伟,王丹,张媛媛,等. 电化学沉积纳米金和石墨烯修饰离子液体碳糊电极检测芦丁的研究[J].分析化学, 2013, 41(5):709-713.
[11] 刘坤平,李惠茗,何钢,等. 芦丁在石墨烯修饰电极上的电化学行为及其灵敏检测[J].安徽农业科学,2013,41(10):4238-4242.
[12] 刘振平,翟海云,何建英,等.芦丁在杂化纳米材料修饰电极上的电化学行为及其应用[J].广东药学院学报,2015,31(1):36-42.
[13] SUN W, YANG M X, LI Y Z, et al. Electrochemical behavior and determination of rutin on a pyridinium-based ionic liquid modified carbon paste electrode[J].Journal of Pharmaceutical and Biomedical Analysis,2008,48(5):1326-1331.
[14] 张亚,杜芳艳,严彪,等.芦丁在纳米金修饰玻碳电极上的电化学行为及其测定[J].分析实验室,2012,31(1):68-71.
[15] 岳莹,梁卿,郭勇,等.介孔碳纳米纤维修饰电极用于黄酮类化合物芦丁的电化学测定[J].分析测试学报,2012,31(8):915-921.
[16] 匡云飞,邹建陵,李薇,等. 双酚A 在壳聚糖石墨烯复合膜电化学传感器上的电化学行为及测定[J]. 分析试验室, 2013,32(3): 33-37.
[17] 匡云飞,邹建陵,李薇,等. 扑热息痛在Nafion-石墨烯-纳米金复合膜修饰电极上的电化学行为[J]. 分析试验室, 2013,32(4): 30-35.
(编校 陈志敏)
Electrochemical Behavior and Determination of Rutin in the Nafion/Gold Nanoparticles @ Graphene Film Modified Carbon Paste Electrode
KUANGYun-fei*,ZOUJian-ling,LIWei,YANGYing-qun,XUJin-sheng,FENGYong-lan,LiYu-ming
(College of Chemistry and Materials Science,Hengyang Normal University,Hengyong Hunan 421008,China)
In this paper,the Nafion/gold nanoparticles@graphene film modified carbon paste electrode(Nafion/AuNs@GS/CPE)was prepared by drop coating method,and the electrochemical behavior of Rutin was studied.The optimal experimental conditions for the determination of Rutin by differential pulse stripping voltammetry were investigated.The results show that in the Citric acid sodium citrate buffer solution (pH 3.4) buffer solution,It is found that 0.3 V produces a sensitive oxidation peak at about RT.The oxidation peak current of Ipahas good linear relationship with the concentration of C in the range of 0.5~10 μmol/L and 10~200 μmol/L (R is 0.995 6 and 0.996 0 respectively).The detection limit (S/N = 3) is 0.3 μmol/L.The modified electrode has good selectivity,stability and reproducibility,for the detection of Rutin in real samples with satisfactory results.
Rutin; differential pulse voltammetry; gold nanoparticles; graphene; modified carbon paste electrode
2016-08-16
湖南省科技计划重点项目( 2012FJ2002)
匡云飞(1963-):男,汉族,湖南祁东人,教授,主要从事电化学分析和配合物合成的研究。
O623.42
A
1673-0313(2016)06-0054-06

