高效液相色谱法测定羊奶中五种氟喹诺酮类药物残留量的研究
李丹,张玉洁,孙志文,王鹤佳,李倩,仲锋*
(1、中国兽医药品监察所,北京 100081;2、北京市兽药监察所,北京102629)
高效液相色谱法测定羊奶中五种氟喹诺酮类药物残留量的研究
李丹1,张玉洁1,孙志文2,王鹤佳1,李倩1,仲锋1*
(1、中国兽医药品监察所,北京 100081;2、北京市兽药监察所,北京102629)
建立了一种可同时检测羊奶中五种氟喹诺酮类药物(环丙沙星、达氟沙星、恩诺沙星、沙拉沙星、二氟沙星)残留的高效液相色谱—荧光检测法。羊奶样品经乙腈提取,正己烷去脂肪,C18柱净化。以0.05 mol/L磷酸三乙胺溶液和乙腈溶液为流动相,流速为0.8 mL/min,激发波长280 nm,发射波长450 nm。结果表明环丙沙星、恩诺沙星、沙拉沙星、二氟沙星在10~200 ng/mL,达氟沙星在2~40 ng/mL呈良好的线性关系,R2均大于0.999。环丙沙星、恩诺沙星、沙拉沙星、二氟沙星的最低定量限为30 μg/kg,达氟沙星的最低定量限为6 μg/kg。环丙沙星、恩诺沙星、沙拉沙星、二氟沙星在30~200 μg/kg的浓度添加水平上,达氟沙星在6~40 μg/kg的浓度添加水平上其回收率均在70~100 %,批内、批间的相对标准偏差小于20 %。该方法简单快速、灵敏度高、重复性好,适用于羊奶中五种氟喹诺酮类药物残留检测。
高效液相色谱法;氟喹诺酮类药物;残留;羊奶
环丙沙星、达氟沙星、恩诺沙星、沙拉沙星和二氟沙星均属于氟喹诺酮类抗菌药物,该类药物具有高效、广谱、低毒等特点,在畜牧业养殖业中广泛用于预防与治疗动物疾病[1]。随着喹诺酮类药物在人医和兽医应用的增加,其各种毒副作用也逐渐显现出来,美国自20世纪80年代中期至今已使用1亿人次以上,氟喹诺酮类药物的严重不良反应年发生率约1/3500。日本对氟喹诺酮的开发研究中,副作用发生率为1.6%~4.8%[2]。因此通过有效的技术手段,对动物性食品中的有关氟喹诺酮类药物残留进行检测,以确保人类对动物性食品消费的安全,具有十分重要的意义。为加强兽药残留监控工作,保证动物性食品卫生安全,农业部于2002年发布第235号公告《动物性食品中兽药最高残留限量》中规定达氟沙星在羊奶中的最高残留限量(MRL)为30 μg/kg;恩诺沙星和环丙沙星在羊奶中的最高残留限量(MRL)为100 μg/kg[3]。
目前,有关FQs多残留在动物组织中的检测方法,国内外已有诸多报道。主要是通过高效液相色谱法,液相色谱串联质谱法及荧光检测器检测[4-6],但是采用高效液相色谱法同时检测羊奶中环丙沙星、达氟沙星、恩诺沙星、沙拉沙星和二氟沙星残留的方法尚未见报道。本研究旨在建立一种操作步骤简单,并可满足同时检测羊奶中五种氟喹诺酮类药物的多残留分析方法。
1 材料与方法
1.1 标准品、主要试剂及其配制 环丙沙星、达氟沙星、恩诺沙星、二氟沙星对照品,中国兽医药品监察所,含量≥99.0%;沙拉沙星对照品,中国兽医药品监察所,含量≥95.0%。乙腈(色谱纯)、正己烷(色谱纯)、正丙醇(色谱纯),美国Fisher公司;磷酸二氢钾(分析纯)、磷酸(分析纯)、三乙胺(分析纯),国药集团化学试剂有限公司;C18固相萃取柱:100 mg/mL;水,美国Millipore超纯水仪制备,符合GB/T 6682-1992规定的一级水。
环丙沙星、达氟沙星、恩诺沙星、沙拉沙星和二氟沙星标准储备液:分别称取环丙沙星、恩诺沙星、沙拉沙星和二氟沙星对照品约50 mg,达氟沙星约10 mg,精密称定,于50 mL量瓶中,用0.03 mol/L氢氧化钠溶解并稀释成含达氟沙星0.2 mg/mL、含环丙沙星、恩诺沙星、沙拉沙星和二氟沙星1 mg/mL的标准储备液。
环丙沙星、达氟沙星、恩诺沙星、沙拉沙星和二氟沙星标准工作液:准确量取适量标准储备液,用乙腈溶解并稀释成浓度为2 μg/mL的标准工作液(达氟沙星浓度为0.4 μg/mL)。
1.2 主要仪器 Agilent 1100高效液相色谱仪(配荧光检测器)美国安捷伦公司;AE 240型分析天平; Biofuge Stratos高速冷冻离心机德国贺利氏公司;IKEA涡动混合仪;IKA-WERKE振荡器。
1.3 方法
1.3.1 样品的提取 称取(2±0.05) g试料,置50 mL离心管中,乙腈5 mL,正己烷8 mL,涡旋混匀,中速振荡5 min,10000 r/min离心10 min,上清液转入50 mL鸡心瓶中,残渣再用乙腈5 mL提取一遍,合并两次提取液,加正丙醇3 mL,于55 ℃水浴下旋转蒸发至干,加pH7.0磷酸盐缓冲液10 mL溶解,备用。
1.3.2 样品的净化 C18柱用甲醇2 mL、水2 mL预洗。取备用液3.0 mL过柱,用水1 mL洗,挤干。流动相1.0 mL洗脱,混匀,过滤膜,供高效液相色谱法测定。
1.3.3 色谱操作条件及参数 色谱柱: Hypersil C18(250 mm×4.6 mm,i.d ),粒径5 μm,或相当者;流动相为0.05 mol/L磷酸三乙胺溶液—乙腈液(82∶18,v/v);流速: 0.8 mL/min;检测波长: 激发波长280 nm,发射波长450 nm;柱温:30 ℃,进样量: 20 μL。1.3.4 标准曲线的制备 准确量取适量的环丙沙星等五种标准工作液,用流动相稀释成含环丙沙星、恩诺沙星、沙拉沙星和二氟沙星浓度分别为10、20、60、100、150、200 ng/mL,达氟沙星浓度分别为2、4、12、20、30、40 ng/mL的系列混合标准溶液,进样分析绘制标准曲线,并计算回归方程及相关系数。
1.3.5 回收率及精密度的测定 采用标准添加法,称取羊奶样品,置于50 mL离心管中,添加适宜浓度的环丙沙星等五种标准工作液,环丙沙星、恩诺沙星、沙拉沙星和二氟沙星在羊奶中的药物浓度为30、100、200 ug/kg;达氟沙星在羊奶中的药物浓度为6、20、40 ug/kg。每种浓度5个样品,重复3批次,按照1.3.1和1.3.2的方法处理后,供HPLC测定,外标法定量,计算回收率、批内、批间变异系数。
1.3.6 检测限和定量限的测定 对环丙沙星等五种标准工作液,进行HPLC分析,并逐渐降低浓度,以溶液检测时的信噪比(S/N)分别大于等于3和10作为药物的检测限和定量限。并计算定量限浓度点的回收率及批内、批间相对标准偏差,验证其可靠性[7]。
2 结果与分析
2.1 色谱分离 在优化的色谱条件下,测得羊奶中环丙沙星、达氟沙星、恩诺沙星、沙拉沙星和二氟沙星色谱峰峰形好,峰间隔时间较长,且均达到基线分离。空白组织样品在上述时间无干扰峰出现,色谱图见图1。
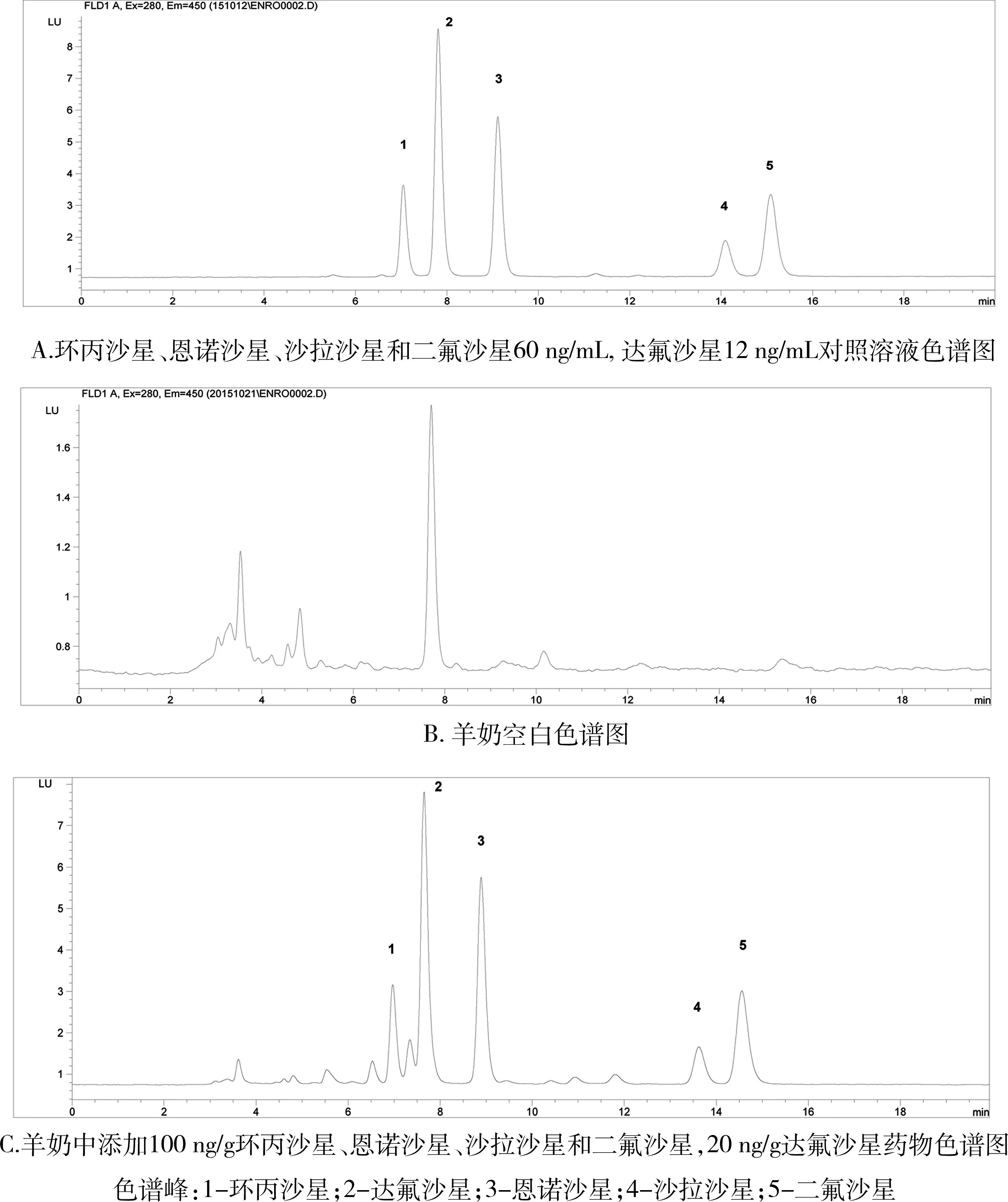
图1 羊奶中环丙沙星、达氟沙星、恩诺沙星、沙拉沙星和二氟沙星的高效液相色谱图
2.2 标准曲线 分别以环丙沙星、达氟沙星、恩诺沙星、沙拉沙星和二氟沙星的色谱峰面积与其对应的对照溶液的质量浓度作图,得到相应的标准曲线。环丙沙星、恩诺沙星、沙拉沙星和二氟沙星在30~200 μg/kg的质量浓度范围内,达氟沙星在6~40 μg/kg的质量浓度范围内,色谱峰面积与浓度呈良好的线性关系。线性回归方程、相关系数见表1。

表1 环丙沙星、达氟沙星、恩诺沙星、沙拉沙星、二氟沙星的回归方程、相关系数和线性范围
2.3 样品的回收率及精密度
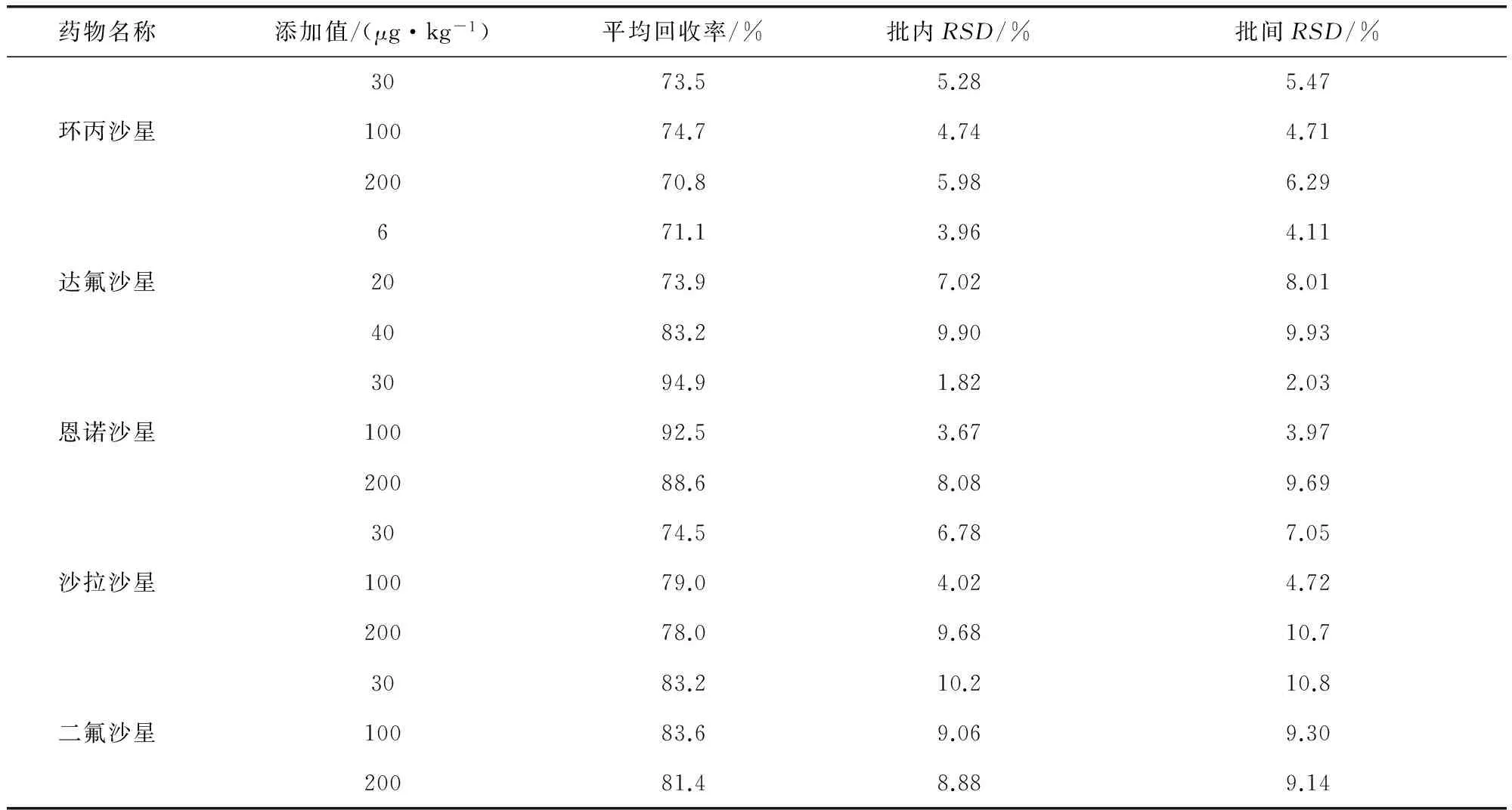
表2 环丙沙星、达氟沙星、恩诺沙星、沙拉沙星、二氟沙星在羊奶中的回收率(n=5)
由表2可以看出羊奶中环丙沙星、恩诺沙星、沙拉沙星、二氟沙星添加浓度水平分别为30、100、200 μg/kg时,平均回收率分别在70.8%~74.7%,88.6%~94.9%,74.5%~79.0%,81.4%~83.6%范围内,批内、批间的RSD分别低于5.98%、6.29%;8.08%、9.69%;9.68%、10.7%;10.2%、10.8%;达氟沙星添加浓度水平分别为6、20、40 μg/kg时,平均回收率分别在71.1%~83.2%范围内,批内、批间的RSD分别低于9.90%、9.93%。结果表明该方法可靠,重复性高。
2.4 灵敏度 应用本试验建立的检测方法,测得羊奶中环丙沙星、恩诺沙星、沙拉沙星、二氟沙星的检测限、定量限分别为9 μg/kg(S/N≥3)、30 μg/kg(S/N≥10),达氟沙星的检测限、定量限分别为1.8 μg/kg(S/N≥3)、6 μg/kg(S/N≥10)。由表2可见,添加浓度为30 μg/kg时,环丙沙星、达氟沙星(添加浓度为6 μg/kg)、恩诺沙星、沙拉沙星、二氟沙星在羊奶中的平均回收率均大于71.1 %,批内、批间的RSD分别低于10.2%、10.8%。表明该方法在定量限水平的可靠性好,且灵敏度高,完全满足环丙沙星、达氟沙星、恩诺沙星、沙拉沙星、二氟沙星在羊奶中残留检测的需要。
3 讨论与小结
3.1 色谱条件的选择 参考国内外有关资料,经过反复试验摸索,氟喹诺酮类药物在酸性条件下,具有较强的荧光吸收。因此,确立用高效液相色谱仪荧光检测器,激发波长为280 nm;发射波长为450 nm;流动相为0.05 mol/L磷酸/三乙胺—乙腈液。为达到分离度要求,在试验过程中调整流动相中有机相浓度比例,最后确立0.05 mol/L磷酸/三乙胺—乙腈液(82∶18)等度洗脱。
3.2 样品提取与净化方法的优化 在方法的提取研究过程中,对样品的提取液进行了实验摸索,采用酸性乙腈、碱性乙腈及纯乙腈溶液进行提取实验,结果发现,纯乙腈提取效果非常理想,对不同浓度的添加实验其回收率均高于70%,达到了残留检测的要求,因此,确立乙腈作为提取液。在去脂过程中,对正己烷、异辛烷的去脂效果进行了对比研究,结果表明正己烷的去脂效果优于异辛烷,同时对于正己烷的用量进行了优化选择,结果表明8 mL正己烷的加入去脂效果最好。此外,在样品提取过程中,对离心机使用的转速和时间进行了对比试验,发现两次离心过程中,离心机转速为10000 r/min,离心时间为10 min的样品除杂效果明显优于离心机转速为10000 r/min,离心时间为5 min及转速为5000 r/min,离心时间为5 min或10 min。
在方法的净化研究过程中,提取液经旋转蒸发浓缩至干后,用流动相溶解,过滤膜直接进样分析,发现样品基质干扰特别严重,达不到基本分离的要求,因此确定采用固相萃取技术进行样品的净化。实验过程中,对HLB,C18等固相萃取柱及不同柱规格进行了摸索和比较研究,最终发现C18,100 mg/mL规格的萃取柱对样品的净化效果最好,最大程度地降低了样品基质对有效成分的干扰,使得环丙沙星、达氟沙星、恩诺沙星、沙拉沙星、二氟沙星在羊奶中的残留检测技术参数(灵敏度、精密度、准确度)均达到了兽药残留检测方法的要求。
3.3 方法的回收率及灵敏度 本试验中环丙沙星、恩诺沙星、沙拉沙星、二氟沙星的添加浓度范围为30~200 μg/kg时,回收率在70.8%~94.9%范围内,批内和批间RSD分别低于10.2%、10.8%,达氟沙星的添加浓度范围为6~40 μg/kg时,回收率在71.1%~83.2%范围内,批内和批间RSD分别低于9.90%、9.93%,符合农业部对兽药残留试验规范中的要求[8]。通过添加定量限浓度点对其可靠性进行验证,结果发现环丙沙星、达氟沙星、恩诺沙星、沙拉沙星、二氟沙星在羊奶中的回收率均大于71.1%,批内、批间的RSD分别低于10.2%、10.8%。表明该方法在定量限水平的可靠性好,且灵敏度高,完全满足环丙沙星、达氟沙星、恩诺沙星、沙拉沙星、二氟沙星在羊奶中残留检测的需要。
本研究建立了一种同时检测羊奶中五种氟喹诺酮类药物的多残留分析方法。本试验条件下,表明该方法灵敏可靠,完全满足羊奶中环丙沙星、达氟沙星、恩诺沙星、沙拉沙星、二氟沙星的残留检测要求。
[1] 陈杖榴. 兽医药理学(第二版) [M]. 北京:中国农业出版社,2002: 282.
[2] 吴永宁,邵兵,沈建忠.兽药残留检测与监控技术[M].北京,化学工业出版社,2007:402.
[3] 中华人民共和国农业部.动物性食品中兽药最高残留限量[S].
[4] 董志远,赵晓凤,宫秀杰等. 牛奶中氟喹诺酮类药物残留量检测方法研究[J]. 北京:中国兽药杂志,2008(10): 14-16.
[5] 孙雷,朱馨乐,张骊,等. 牛奶中七种氟喹诺酮类药物残留检测高效液相色谱-串联质谱法研究[J]. 北京:中国兽药杂志,2008(11): 16-19.
[6] 李丹,张玉洁,仲锋等. 鸡蛋中氟喹诺酮类药物残留量检测方法研究[J]. 北京:中国兽药杂志,2010(6): 1-4.
[7] 李俊锁,邱月明,王超.兽药残留分析[M].上海:上海科学技术出版社,2002:40.
[8] 中华人民共和国农业部.关于发布《兽药残留试验技术规范(试行)》的通知[S].
(编辑:陈希)
Study on Detection Method Quinolones Residues in Sheep Milk by HPLC
LI Dan1, ZHANG Yu-jie1, SUN Zhi-wen2, WANG He-jia1, LI Qian1, ZHONG Feng1*
(1.ChinaInstituteofVerterinaryDrugControl,Beijing,100081;2.BeijingveterinarydrugmonitoringInstitute,Beijing,102629)
A method for determination of quinolones residues in sheep milk with HPLC by FLD detection was established. Ciprofloxacin、danofloxacin 、enrofloxacin、sarafloxacin and difloxacin were extracted from sheep milk with acetonitrile and degreased in hexane, dissolved with pH7.0 phosphate solution after evaporation, then the solution was purified with C18 column. The mobile phase were 0.05 mol/L triethylammonium phosphate solution and acetonitrile, the flow rate was 0.8 mL/min .Fluorescence detection was carried out at excitation and emission wavelengths of 280 nm and 450 nm . A good linearity of the calibration curve was obtained with the range of 10~200 ng/mL for ciprofloxacin、enrofloxacin、sarafloxacin and difloxacin, and 2~40 ng/mL for danofloxacin(R2>0.999). The limit of quantification of ciprofloxacin、enrofloxacin、sarafloxacin and difloxacin was 30 μg/kg, and danofloxacin was 6 μg/kg. The average recoveries of quinolones residues from spiked sheep milk at the three concentrations of 30、100、200 μg/kg(ciprofloxacin、enrofloxacin、sarafloxacin and difloxacin)and 6、20、40 μg/kg(danofloxacin)ranged from 70-100 %(n=5) respectively. In day-between days batch variation coefficients were both less than 20 %.This method can be applied for the determination of quinolones residues in sheep milk.
HPLC;quinolones ;residues;sheep milk
李丹,硕士,从事兽药残留方法学研究及残留检测工作。
2015-12-02
A
1002-1280 (2016) 01-0031-05
S859.84

