高效液相色谱法测定缬沙坦胶囊的溶出度
杨 静,徐轶飞,苗爱东,尹娜娜, 王文习
[作者单位] 100071北京,北京军区联勤部药品仪器检验所(杨静、徐轶飞、苗爱东),266101山东 青岛,青岛市黄海制药有限责任公司(尹娜娜), 050081 石家庄,白求恩国际和平医院药剂科(王文习)
高效液相色谱法测定缬沙坦胶囊的溶出度
杨静,徐轶飞,苗爱东,尹娜娜, 王文习

[作者单位]100071北京,北京军区联勤部药品仪器检验所(杨静、徐轶飞、苗爱东),266101山东 青岛,青岛市黄海制药有限责任公司(尹娜娜), 050081 石家庄,白求恩国际和平医院药剂科(王文习)
[摘要]目的建立高效液相色谱法(HPLC)测定缬沙坦胶囊溶出度的方法。方法采用《中国药典》2010年版中缬沙坦胶囊溶出度测定条件,以磷酸盐缓冲液(调节pH 6.8)1000 ml为溶出介质,100 r/min,30 min取样。液相色谱柱为Extend C18(4.6 mm×250 mm,5 μm), 以乙腈-水-冰醋酸(500:500:1)(v/v)为流动相,检测波长:230 nm,流速:1.0 ml/min,柱温:30℃。结果缬沙坦在0.004~0.06 mg/ml范围内线性关系良好,线性方程为Y=28.771X-28.145(r=0.9997,n=8),平均回收率为101.27%(RSD=1.07%,n=9)。HPLC与紫外-可见分光光度法(UV)溶出度测定结果有一致性。结论高效液相色谱法测定缬沙坦胶囊溶出度的方法准确度高、简便、快速,适用于该制剂的质量控制。
[关键词]缬沙坦胶囊;溶出度;高效液相色谱法
缬沙坦胶囊是一种特异性血管紧张素Ⅱ受体拮抗剂,用于治疗各类轻至中度高血压。缬沙坦的主要剂型有胶囊、片剂和分散片,胶囊剂最为常用。《中国药典》收载的对其溶出度的检查方法为紫外分光光度法[1],而含量测定、有关物质采用的均是高效液相色谱法(HPLC),目前已见其它药物采用HPLC测定溶出度的报道[2-7],本文采用HPLC不需稀释,仅通过调节进样量,对6个不同厂家、2个不同规格的缬沙坦胶囊进行了溶出度测定,并与紫外分光光度法测定溶出度的结果进行了比较,结果基本一致。
1仪器和试药
Agilent1200高效液相色谱仪和化学工作站(美国Agilent公司),UDT-812GS溶出仪(镇江禄根仪器有限公司),UV-2450型紫外可见分光光度计(日本岛津公司),MettLerAG285型电子天平(瑞士梅特勒公司)。缬沙坦对照品(批号:100651-201203,含量:99.8%,中国食品药品检定研究院生产);缬沙坦胶囊(6个不同厂家的产品批号分别是:A厂:1411023;B厂:140406;C厂:140104;D厂:141001;E厂:X1766;F厂:20141229。其中A、B、C、D、E厂的产品规格均为80 mg,F厂产品规格为40 mg);乙腈(Fish公司,色谱纯);水为自制超纯水;磷酸二氢钾、氢氧化钠、冰醋酸均为分析纯。
2方法与结果
2.1溶液的制备对照品溶液的制备:精密称取60℃减压干燥2 h的缬沙坦对照品0.02004 g于50 ml量瓶中,用磷酸盐缓冲液溶解并定容,即得浓度为400 μg/ml的对照品储备液。准确量取5 ml于50 ml量瓶中,用磷酸盐缓冲液定容得到每1 ml含40.08 μg的对照品溶液。供试品溶液的制备:取供试品6粒,分别投入6个溶出杯中,按照《中国药典》2010年版中缬沙坦胶囊溶出度测定条件,以磷酸盐缓冲液(调节pH 6.8)1000 ml为溶出介质,转速100 r/min,温度(37±0.5)℃,分别于5、10、15、20、25、30 min时,取溶出液10 ml(同时补充10 ml 37℃的溶出介质),过滤,去除初滤液2 ml,取续滤液即得供试品溶液。6个不同厂家的供试品分别依法操作。
2.2色谱条件与系统适应性实验色谱柱:Agilent Extend C18(4.6 mm×250 mm);流动相:乙腈-水-冰醋酸(500:500:1)(v/v);流速:1.0 ml/min;检测波长230 nm;柱温:30℃;进样20 μl(A、B、C、D、E厂规格为80 mg的产品:进样10 μl)。理论板数按缬沙坦峰计算应不低于4000。取“2.1”项下对照品溶液和供试品溶液进样分析,见色谱图1。
2.3方法验证
2.3.1线性关系考察:分别准确移取“2.1”项下对照品储备液0.1、0.2、0.4、0.5、0.75、1.0、1.25、1.5 ml至10 ml量瓶,用溶出介质稀释至刻度,摇匀,得到浓度分别为4、8、16、20、30、40、50、60 μg/ml的系列对照溶液,按“2.2”项下色谱条件进行测定,以缬沙坦对照品浓度为横坐标,峰面积为纵坐标作标准曲线。回归方程为Y=28.771X-28.145,r=0.9997。表明缬沙坦浓度在4~60 μg/ml范围内与峰面积线性关系良好。
2.3.2精密度试验:取缬沙坦线性考察系列溶液中浓度为40 μg/ml的对照品溶液,按上述色谱条件,进样20 μl,连续进样6次,测得的峰面积的RSD为0.44%。
2.3.3稳定性试验:取浓度为40 μg/ml的对照品溶液,室温放置,分别于制备后的0、2、4、6、8、10、12 h按上述色谱条件进样测定,计算结果RSD为0.53%。表明在此浓度下缬沙坦在12 h内稳定。

图1 缬沙坦液相色谱图A为对照品,B为供试品,1为缬沙坦峰
2.3.4回收率试验:按照“2.4.1”项下方法,对供试品B进行溶出度检查,于30 min时,取9份理论浓度为80 μg/ml的溶出液5 ml于10 ml量瓶中,平均分为3组,每组分别精密加入对照品储备液0.6、1.0、1.4 ml,用溶出介质稀释至刻度,摇匀,过0.45 μm滤膜,取续滤液按上述色谱条件进样10 μl进行测定,计算对照溶液的实际加入量及回收率。低、中、高3种浓度的回收率结果见表1。
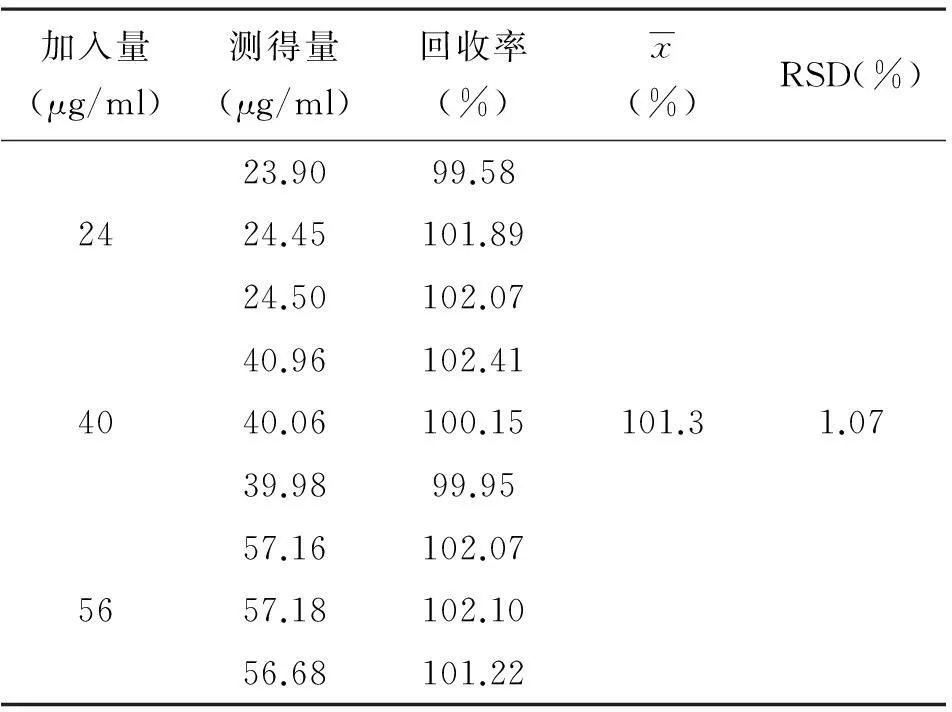
表1 不同浓度下供试品溶出度回收率测定结果
2.4两法测定溶出度结果及溶出曲线比较
2.4.1溶出度检查:按《中国药典》[1]方法,以磷酸盐缓冲液(调节pH6.8)1000 ml为溶出介质,温度37℃,转速100 r/min,分别于5、10、15、20、25、30 min时,取溶出液10 ml,过滤,去除初滤液2 ml,取续滤液5 ml至25 ml量瓶,用溶出介质稀释至刻度,摇匀,即得供试品溶液。准确移取对照品储备液4 ml至100 ml量瓶,用溶出介质稀释至刻度,摇匀,得到浓度为16 μg/ml对照溶液,照紫外-可见分光光度法,在250 nm的波长处测定吸光度,分别计算在6个不同取样时间点的溶出量。另取“2.1”制备的供试品溶液,按照“2.2”色谱条件进样测定,以缬沙坦峰面积按外标法计算6个不同取样时间点的溶出量。6个不同厂家的供试品分别同法测定。
2.4.2两法的溶出参数比较:HPLC与紫外-可见分光光度法(UV)溶出度测定结果见表2,经t检验,两种方法获得的溶出参数差异无统计学意义(t=0.313,P=0.7558)。

表2 两种方法测定缬沙坦胶囊溶出度结果比较(%)
2.4.3两法溶出曲线考察情况见图2。
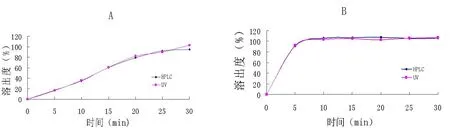
图2 6个厂家缬沙坦胶囊HPLC和UV法的溶出曲线HPLC为高效液相色谱法,UV为紫外-可见分光光度法
3讨论
6厂家产品均为国产,溶出过程中胶囊壳全部溶解无残留,虽溶出曲线存在差异,但30 min时溶出值均达到80%,符合药典规定。B、C、E、F厂产品溶出迅速,5 min内溶出值即达到90%以上,从试验结果可看出,两种方法获得的溶出度值基本一致,HPLC获得的溶出曲线更加平稳。方法学验证结果表明:采用HPLC测定缬沙坦胶囊的溶出度结果准确、科学可靠,不需稀释,取样滤过后直接进样,不仅简化了操作过程,定量也更为准确,测定结果的精密度更高[8-13],缬沙坦在本文的色谱条件下峰型较好,数据信息也更加完整、真实,本法中的溶液浓度与药典中含量测定的浓度一致,可与含量测定同时检测,既可提高效率、降低成本,对于缬沙坦胶囊的制剂工艺、药品质量控制也具有重要的意义。
[参考文献]
[1]中华人民共和国国家药典委员会.中国药典[M].二部.北京:中国医药科技出版社,2010:1137.
[2]方韵,田杰.头孢克肟分散片溶出度HPLC法与UV分光光度法测定结果的比较[J].抗感染药学,2013,10(3):200-202.
[3]范松华.高效液相色谱法测定阿托伐他汀钙片的溶出度[J].上海医药,2013,5,34(1):53-56.
[4]李月秋,赵艳艳,韩媛媛,等.高效液相色谱法测定氟康唑胶囊的溶出度[J].河北大学学报,2009,29(4):403-406.
[5]杨林,何丹.高效液相色谱法测定吗替麦考酚酯胶囊的溶出度[J].药物分析杂志,2008,28(7):1177-1179.
[6]王昕,唐素芳.吲达帕胺片体外溶出度试验与体内药代动力学的相关性[J].药物分析杂志,2013,33(5):755-762.
[7]伏圣青,陈华,南楠,等.艾司唑仑片溶出度检测方法的建立以及溶出曲线评价[J].药物分析杂志,2013,33(5):885-888.
[8]李卿.羥苯磺酸钙胶囊的溶出度研究[J].右江民族医学院学报,2014,36(4):628-630.
[9]成文昭,方灿,杨芳芳,等.国产格列本脲片的溶出度对比分析[J].贵阳医学院学报,2010,35(4):370-373.
[10]马慧萍,任俊,何蕾,等.抗高原缺氧药雪莲黄酮胶囊的质量控制标准[J].解放军医药杂志,2014,26(10):90-93.
[11]马晓东,章文斌,周定标,等.BCUN-PLGA缓释可降解微球的制备与特征[J].中华神经医学杂志,2006,5(7):692-695.
[12]杨水泉,李玲,黄如训,等.脑出血患者血清兴奋性氨基酸水平与功能恢复的关系[J].中国综合临床,2005,21(2):120-122.
[13]杨倩,郭福庆,曹晓云,等.国产盐酸环丙沙星片及胶囊溶出度比较[J].药物分析杂志,2010,30(8):1578-1581.
(收稿时间:2015-09-22修回时间:2015-10-24)
综述
·论著·
High Performance Liquid Chromatography in Determination of Dissolution of Valsartan Capsules
YANG Jing1, XU Yi-fei1, MIAO Ai-dong1, YIN Na-na2, WANG Wen-xi3(1. Institute for Drug and Instrument Control, Combined Logistic Department of Beijing Military Area Command,Beijing 100071,China; 2. Qingdao Huanghai Pharmaceutical Co., Ltd., Qingdao, Shandong 266101, China; 3. Department of Pharmacy, Bethune International Peace Hospital of PLA, Shijiazhuang 050000, China)
[Abstract]ObjectiveTo establish a high performance liquid chromatography (HPLC) method to detect dissolution of Valsartan capsules. MethodsBased on detection conditions in the Chinese Pharmacopoeia (2010 edition), the dissolution of Valsartan capsules was detected by phosphate buffer (pH 6.8) 1000ml as the dissolution medium with 100 r/min, and samples were obtained after treatment for 30 min. Liquid chromatographic column was Extend C18 (4.6 mm×250 mm, 5 μm), mobile phase was composed of acetonitrile, water and glacial acetic acid [500∶500∶1 (V/V)], and the wavelength was 230 nm. The flow rate was 1.0 ml/min with 30℃ column temperature. ResultsValsartan showed good linear correlation in the range of 0.004-0.06 mg/ml, and the linear equation was Y=28.771X-28.145 (r=0.9997, n=8), and the average recovery was 101.27% [relative standard deviation (RSD)=1.07%, n=9]. The HPLC had concordance with ultraviolet and visible spectrophotometry (UV) in detection of the dissolution. ConclusionHPLC method in determination of the dissolution of Valsartan capsule is accurate, simple and quick, and it can be applied to the quality control of the preparation.
[Key words]Valsartan capsules; Dissolution; High performance liquid chromatography
[DOI]10.3969/j.issn.2095-140X.2015.12.025
[文献标志码][中国图书资料分类号]R446.1A
[文章编号]2095-140X(2015)12-0109-04
[通讯作者]王文习:E-mail:64462039@qq.com

