肌内注射黄体酮引起人工性脂膜炎一例A case of factitial panniculitis caused by intramuscular progesterone
赵珊珊,姚志远,郑占才
肌内注射黄体酮引起人工性脂膜炎一例
A case of factitial panniculitis caused by intramuscular progesterone
赵珊珊,姚志远,郑占才
[关键词]脂膜炎,人工性;黄体酮
[中图分类号]R759.73
[文献标识码]B
[文章编号]1674-1293(2015)05-0390-02
DOI:10.11786/sypfbxzz.1674-1293.20150526
作者简介:赵珊珊,女,在读硕士研究生,研究方向:真菌感染,E-mail: zheng88483@163.com
通讯作者:郑占才,E-mail: zhengzhancai@sina.com
收稿日期(2015-05-08 修回日期 2015-08-26)
临床资料
患者,女,42岁。主因双侧臀部出现红色硬结15 d,于2014年12月2日就诊。患者15 d前于外院妇产科行辅助受孕,予黄体酮臀部肌内注射40 mg/d (10 mg/ml),共15 d(积累注射量600 mg),期间双侧臀部注射部位周围逐渐出现局部红肿、硬结,渐加重,有轻度压痛。患者自发病以来无发热、咳嗽、关节痛等。既往体健,否认有结核、肝炎等传染病史,否认手术史、外伤史,药物、食物过敏史,家族中无类似疾病患者。体格检查:发育正常,营养中等,各系统检查未见异常。皮肤科检查:双侧臀部各见一6 cm×4 cm大红色斑块,边界不清,表面无破溃,皮温正常,质硬,有轻度压痛(图1a)。实验室检查未见异常。于右侧臀部斑块中央切取皮损,组织病理检查示:表皮轻度角化过度,基底层色素轻度增多,真皮浅深层血管周围、附属器周围单一核细胞浸润,皮下脂肪以小叶为主的淋巴细胞、组织细胞及多核巨细胞浸润,可见嗜脂性脂肪坏死及微囊性脂肪坏死,组织病理改变符合脂膜炎(小叶性为主)(图2a-2c)。免疫组化染色示:KP-1散在阳性,Ki-67阳性率<2%(图2d,2e)。苏木精-伊红(HE)切片偏振光检查未发现异物。诊断:人工性脂膜炎。治疗:停止肌内注射黄体酮,清热散结胶囊 5粒,每日3次口服,嘱患者自行局部按摩、热敷。患者服用清热散结胶囊2周后自行停药,1.5个月后复诊,硬结消退约80%,局部留有轻微色素沉着(图1b)。2个月后电话随访,臀部硬结及局部色素沉着均已完全消退。
讨论
人工性脂膜炎是人为因素造成的脂膜炎,常发生于注射矿物油(如石蜡油)和液体硅酮后[1]。注射引起的人工性脂膜炎皮损发生位置视注射部位而定,常见于臀部。注射黄体酮进行黄体功能支持是体外受精时胚胎移植诱发超排卵的常规治疗。长期大剂量肌内注射黄体酮,有时会在注射部位出现红肿、硬结,
作者单位:100029北京,中日友好医院皮肤病与性病科(赵珊珊,姚志远,郑占才)
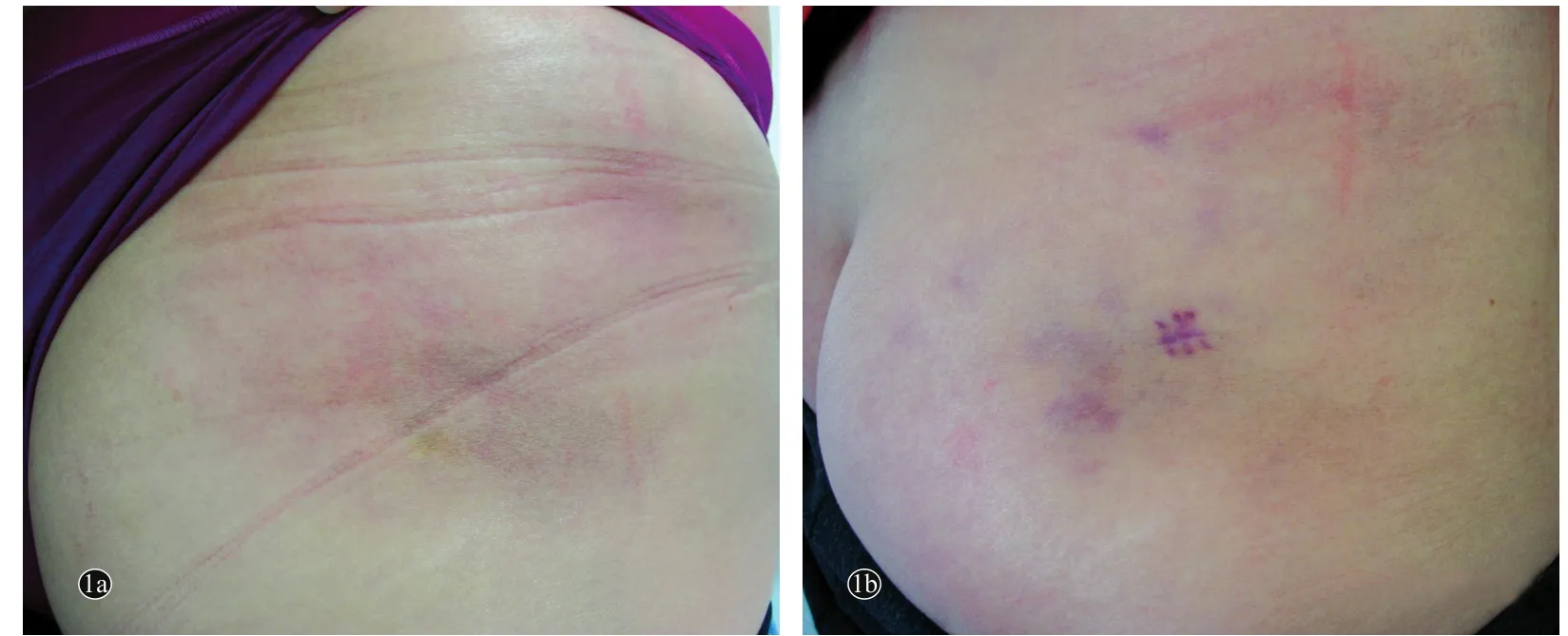
图1 肌内注射黄体酮引起人工性脂膜炎患者臀部皮损
甚至人工性脂膜炎。原因可能是黄体酮属油剂,不溶于水,油剂本身易引起药物吸收不良,导致药物局部蓄积,刺激脂肪组织产生炎症。另外,长期大量同一部位注射,易出现注射阻力增大,当注射深度未达到肌肉层时,药液常停留在皮下组织,药物不易被吸收,进而促进了硬结的产生。研究表明,黄体酮每次6支(10 mg/ml)比每次3支(20 mg/ml)出现人工性脂膜炎比例更高,可能与黄体酮溶媒量或溶媒质量相关[2]。肌内注射黄体酮除引起人工性脂膜炎外,还可引起非肌注部位的皮肤反应性病变。有文献报道1 例33岁女性在辅助生殖时臀部肌内注射黄体酮4周后,双侧膝部出现结节性红斑,组织病理表现为间隔性脂膜炎,停药2 d后皮损消退[3]。这种结节性红斑是一种反应性病变,而非真正的人工性脂膜炎。
人工性脂膜炎的组织病理学表现通常无特异性[1],部分患者为急性小叶性炎症伴脂肪坏死和中性粒细胞浸润,炎症中央区脂肪细胞完全消失,边缘部有组织细胞和巨细胞。后期成纤维细胞增生,发生纤维化,可见钙化灶。也可只有肉芽肿性反应。某些患者,炎症也可累及脂肪间隔,组织病理学上类似结节性红斑。采用偏振光显微镜观察发现双折射物质有助于本病诊断。本例患者主要以小叶性肉芽肿性炎症为主,伴有嗜脂性脂肪坏死及微囊性脂肪坏死。结合患者黄体酮注射史、临床表现、血常规、组织病理学表现,可以明确诊断为人工性脂膜炎(黄体酮所致可能性大)。本病需与狼疮性脂膜炎相鉴别,后者主要见于中年女性,皮损表现为疼痛性皮下结节和斑块,常见于颊部、臀部、臂部,其次为股部、胸部,约30%的患者抗核抗体(ANA)、类风湿因子(+),免疫球蛋白升高。组织病理表现为小叶或小叶/间隔混合性脂膜炎;黏蛋白沉积;脂肪小叶透明坏死;淋巴细胞和浆细胞浸润;淋巴细胞团块状聚集或形成滤泡[4]。
本病的治疗应首先停用注射液,可改变用药途径,如黄体酮缓释凝胶阴道置药或黄体酮阴道环等。硬结部位可适度按摩、热敷或理疗,以促进炎症吸收、消散。也可辅以中药活血化淤、清热散结。另外,肌内注射黄体酮时应选择粗长的注射针头,注射速度宜慢,两侧臀大肌交替注射,深达肌层,这些方法可能有助于预防本病的发生。

图2 肌内注射黄体酮引起人工性脂膜炎患者皮损组织病理与免疫组化
【参 考 文 献】
[1]赵辨. 中国临床皮肤病学 [M]. 南京: 江苏科学技术出版社, 2009: 1151.
[2]孙青苗, 金彦, 陈捷, 等. 肌肉注射黄体酮致局部不良反应相关因素分析 [J]. 中国药物与检测中国药物应用与监测, 2009, 6(5):301.
[3]Jeon HC, Choi M, Paik SH, et al. A case of assisted reproductive therapy-induced erythema nodosum [J]. Ann Dermatol, 2011, 23(3): 362-364.
[4]朱学骏, 王宝玺, 孙建方. 皮肤病学 [M]. 2版. 北京: 北京大学医学出版社, 2014:1862.
(本文编辑 祝贺)
- 实用皮肤病学杂志的其它文章
- 急性荨麻疹95例实验室相关指标检测及分析
- 阿维A治疗18例儿童泛发性脓疱性银屑病疗效及安全性分析
- 种痘样水疱样EB病毒感染相关淋巴细胞增生性疾病一例Hydroavacciniforme-like Epstein-Barr Virus-associated lymphoproliferative disorders:a case report and literature review
- Merkel细胞癌一例A case report of skin Merkel cell carcinoma
- 肢端角化性类弹性纤维病一例Acrokeratoelastoidosis: a case report
- 光动力疗法治疗鲍恩病一例Successful treatment of a case of Bowen's disease with photodynamic therapy

