胡芦巴胶降解工艺研究
·实验研究·
胡芦巴胶降解工艺研究
贺少龙1,冯军1,洪彤彤1,隋宏1,2,王文苹1,2,3
(1.宁夏医科大学药学院,宁夏 银川 750001;2.宁夏回药现代化工程技术研究中心,宁夏 银川 750004;
3.回医药现代化省部共建教育部重点实验室,宁夏 银川 750004)
摘要:目的优选胡芦巴胶的降解方法及工艺,获得质量稳定可控的低分子量多糖。方法 以总糖和还原糖含量以及黏度为评价指标,比较酸水解、超声辅助、酶解等工艺,优选最佳条件。并依据紫外、红外及差示扫描热图谱对产物进行初步评价。结果不同降解工艺所得还原糖得率分别为酶解52.41%、超声辅助42.19%、酸解24.59%;以纤维素酶用量10 U·mg-1、50 ℃处理150 min时,降解效果最佳。重复实验表明该工艺稳定可控, 紫外、红外及DSC图谱无明显差异,峰位基本不变。结论酶法降解胡芦巴制备低分子量多糖,方法简便、高效、易于控制。
关键词:胡芦巴胶;酶法降解;黏均分子量;低分子量多糖
基金项目:国家自然科学
作者简介:贺少龙,男,研究方向:新型载药材料及给药系统研究,E-mail:15296907978@163.com
通讯作者:王文苹,女,博士研究生,教授,研究方向:新型载药材料及给药系统研究,Tel:0951-6880581,E-mail:wangwenpingg@sina.com
中图分类号:R284.2文献标识码:A
Study on degradation process of fenugreek gum
HEShao-long1,FENGJun1,HONGTong-tong1,SUIHong1,2,WANGWen-ping1,2,3
(1.SchoolofPharmacy,NingxiaMedicalUniversity,Yinchuan750001,China;2.NingxiaEngineering&
TechnologyResearchCenterForModernizationofHuiMedicine,Yinchuan750004,China;
3.KeyLabofHuiEthnicMedicineModernization,MinistryofEducation,Yinchuan750004,China)
Abstract:ObjectiveTo optimize the degradation process of fenugreek gum and to obtain low-molecular-weight polysaccharide with stable and controllable quality.Methods Taking total sugar,reducing sugar content and viscosity parameter as evaluating index,degradation methods of traditional acid hydrolysis,ultrasound-aided acid hydrolysis and enzymatic degradation were compared and the process conditions were further optimized. The fenugreek gum and its degradation products were characterized by UV,IR and DSC spectrometry respectively.Results The reducing sugar content of different degradation methods were 52.41% for enzymatic degradation,42.19% for ultrasound-aided acid hydrolysis and 24.59% for traditional acid hydrolysis. The optimum process was as follows:Fenugreek gum solution was treated with 10 U cellulose at 50 ℃ for 150 min.Repeated experiments showed that the degradation process was stable and controllable.No significant differences were found in the UV,IR or DSC spectrums between fenugreek gum and its degradation products.Conclusion Enzymatic degradation of fenugreek gum turned was an efficient,simple and controllable method.
Key words:Fenugreek gum;Enzymatic degradation;Viscosity-average molecular weight;Low-molecular-weight polysaccharide
胡芦巴胶(Fenugreek gum,以下简称FG)源于胡芦巴种子内胚乳部分,属中性黏多糖,主要成分为半乳甘露聚糖,以β-D-1,4糖苷键链接形成主链[1]。国内现多将胡芦巴胶用作工业增稠剂,食品级增稠性、保水性添加剂等[2],但对胡芦巴胶作为生物医药材料的相关研究较少。近年来发现不仅天然多糖自身具有食用或医药价值,且其低分子量多糖也具有独特的药理活性。例如有学者对3种不同天然来源的半乳甘露聚糖进行比较,结果表明半乳糖基的比例越高,其降血糖和降血脂的作用就愈强[3~5]。低分子量多糖具有良好的生理功能,在食品、饲料、医药等行业有着广泛的应用[6],受到研究者的普遍关注。因此,本文拟对胡芦巴胶进行降解、制备低分子量多糖,优选方法和工艺,以期为胡芦巴胶相关新产品的开发和应用奠定基础。
1材料和方法
1.1仪器与设备DF-101s恒温培养摇床(上海恒科学仪器);TDL-40B离心机(上海安亭);UV-2450紫外分光光度计(日本岛津);DV-III流变仪(美国博勒飞);乌氏黏度计(上海亚太技术玻璃公司,91683501);TENSOR37傅立叶红外光谱仪(德国布鲁克公司);UV-2450紫外分光光度计(日本岛津);TGA/DSC同步热分析仪(南京大展机电技术研究所)。
1.2材料与试剂胡芦巴种子(亳州蜀中药业有限公司,批号:20110205);纤维素酶(上海源叶生物科技有限公司,酶活力≥35 U·mg-1);果胶酶(北京索莱宝公司,酶活力≥40 U·mg-1);甘露聚糖酶(江苏锐阳生物,酶活力≥60 000 U·mg-1);葡萄糖标准品(中国药品生物制品检定所,含量≥98%,批号:MUST-12122601);无水乙醇(天津北联试剂公司,批号:20130620);盐酸(白银银环化学制剂厂,批号:20100203);氢氧化钠(天津市大茂化学试剂厂,批号:20100527);柠檬酸(北京化工厂,批号:890815);亚硫酸钠(天津市福晨化学试剂厂,批号:20040906);酒石酸钾钠(天津市风船化学试剂科技有限公司,批号:20101220),所用水均为蒸馏水,由宁夏医科大学动力中心提供。
1.3总糖及还原糖含量方法[7,8]总糖含量的测定:取待测品100 mg精密称定,置于带塞烧瓶中,再各加入10 mL 6 moL·L-1HCl溶液和15 mL蒸馏水混匀,在沸水浴中密封加热30 min后。以流水冷却后,加入酚酞指示剂2滴,用10%NaOH溶液中和至溶液呈淡红色,转移至100 mL容量瓶中加水定容,过滤取续滤液待测。
还原糖的测定:取待测样品溶液1.0 mL置 25 mL比色管中,加入1.5 mL蒸馏水、3.0 mL DNS试剂混匀,于沸水浴中煮沸10 min,取出立即用冰水浴冷却至室温,加水至刻度,摇匀、待测。
DNS法测定波长的确定:分别取葡糖糖标准液(1 mg·mL-1)0.0、0.2、0.4、0.6、0.8、1.0、1.2、1.4 mL于比色管中,加水至2.5 mL,再精密加入DNS试剂3.0 mL,混匀,于100 ℃水浴10 min,流水冷却,加水至刻度、摇匀,于200~800 nm处进行扫描,结果空白样品和对照品均在 490 nm 有最大吸收,故确定490 nm为检测时所用波长。
上述样品分别在490 nm波长处测吸光度值,并按下式(1)计算样品中总糖或还原糖的含量。所得结果按式(2)计算还原糖得率。
含量(%)=(a×C×D)/W×100
(1)
还原糖得率=还原糖含量(mg)/总糖含量(mg)×100%
(2)
式中a=0.9,为校正系数;C为样品浓度;D为稀释倍数;W为样品重量(mg)。
以葡萄糖为标准品制得工作曲线为:A=20.177C-0.091 9,相关系数R2=0.998 1,结果显示,在0~40 μg·mL-1范围内,总糖与还原糖的含量同吸光度成正比,且相关性良好。
1.4黏均分子量的测定取100 mg 降解产物精密称定,加0.2 mol·L-1NaCl 水溶液配制浓度在1.1~1.5 g·cm-3的范围内的系列溶液。取10 mL 该溶液置乌氏黏度计中,在30 ℃水浴恒温的条件下,用秒表测定下落的时间,根据Mark-Houwink经验式(3)[9,10]计算黏均分子质量。
(3)
其中,η 为溶液黏度,Mη为黏均分子质量,K=7.5×10-2,α=0.662。
1.5黏度的测定将样品配制成1%的溶液,选用DV-III流变仪(4号转子,60 rpm)室温下测定黏度。
1.6降解方法及工艺的选择分别采用酸解、超声辅助酸解、酶解等方法降解胡芦巴胶,以还原糖得率以及黏均分子量为评价指标,优选最佳降解方法和合成工艺。
1.6.1酸解方法取2%的胡芦巴胶糖溶液,加入10 mL 10%盐酸溶液,置于50 ℃水浴上恒温水解4 h后,冷却并调pH至中性,取1 mL用DNS法测定还原糖的含量,将剩余降解液用90%的乙醇沉淀,放置烘箱干燥备用。
1.6.2超声辅助酸解方法超声辅助酸解方法同上,在加入10%盐酸溶液后,置于超声提取器中超声处理。其他处理与传统酸解均相同。
1.6.3酶解方法配制2%的胡芦巴胶糖溶液,加入酶液后,于50 ℃下降解一定时间,煮沸5 min灭活酶,放冷备用[11]。分别考察酶的种类、酶质量浓度、时间等因素对样品还原糖含量等指标的影响(n=3)。
1.6.4结构分析分别利用紫外、红外及DSC扫描胡芦巴胶及降解产物,比较所得图谱,对降解产物进行初步评价。
2结果与分析
2.1不同降解方法的考察将各种工艺降解后的低分子量多糖用90%的醇沉,干燥后复溶,分别测吸光度值并按“1.3”项下公式(1)、(2)计算总糖和还原糖含量、还原糖得率。根据“1.4”项下的方法,计算FG多糖及各工艺降解后低分子量多糖的黏均分子量,结果见表1。

表 1 不同降解工艺所得还原糖得率及黏均分子量( n=3)
注:-表示未计算得出
由表1可知,不同方法降解产物还原糖得率分别为:52.41%、42.19%、24.59%,酶解>超声辅助>酸解;黏均分子量为:纤维素酶(50 885.59 Da)> 酸解(4 131.56 Da)。推测其原因可能是,盐酸水解条件强烈、降解完全,但易破坏糖的结构,因此所得产物黏均分子量较小;而超声辅助酸解破坏糖的结构更彻底,工艺重现性较差,使得溶液在乌式黏度计中下落时间存在很大差异,不能有效计算出黏均分子量。酶解方法简便、省时,且还原糖得率最高。因此选择酶解的方法。
2.2酶种类的优选
2.2.1不同酶的选择考察不同酶种类对产物还原糖含量的影响,结果如图 1 。
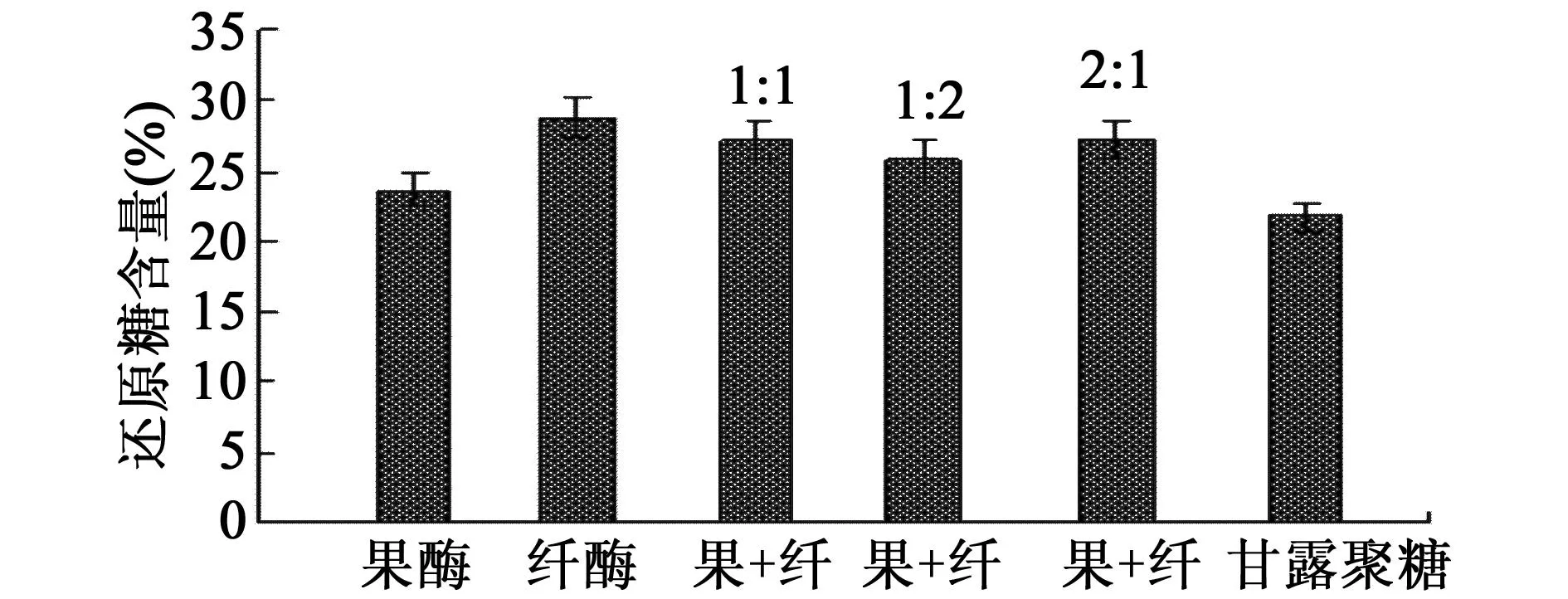
图1 酶种类对还原糖含量的影响
结果表明,当采用单一酶时,所得还原糖含量依次为:纤维素酶>果胶酶>甘露聚糖酶;当采用果胶酶及纤维素酶和果胶酶的混合酶时,所得产物还原糖含量差异不显著,且均低于纤维素单一酶。推测可能是因为酶的作用活性具有高度的专一性。果胶酶本质上是聚半乳糖醛酸水解酶,降解多糖后主要生成的是β-半乳糖醛酸,所以单糖的量少;甘露聚糖酶水解α-半乳糖残基在主链中的位置、含量、酯酰化的程度有关,若完全水解甘露聚糖,需要与其他酶协同作用[9]。而纤维素酶恰是分解β-1,4-结合的葡萄糖苷键的纤维素物质[12]。因此,选择纤维素酶进一步的考察。
2.2.2纤维素酶用量的考察取2% FG溶液,分别加入不同体积的纤维素酶液,考察酶用量对所得产物还原糖含量的影响,结果见图 2 。

图2 酶用量对还原糖含量的影响
结果表明,还原糖含量随着酶用量的增加而升高,当加入2 mL(100 U·mL-1)的纤维素酶溶液时,产物还原糖含量最高、基本达到平衡。因此选用加入酶量10 U·mg-1作进一步的考察。
2.2.3酶解时间的考察结果见图3。
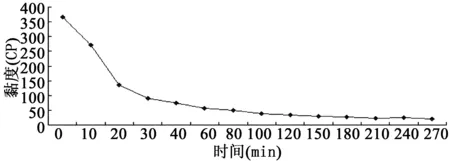
图3 不同时间点降解液的黏度
如图3所示,酶解过程中体系黏度值随酶解时间的延长而迅速降低,30 min后,黏度值变化趋于平缓,150 min后体系黏度值几乎不再变化,这一现象可能是由于对纤维素酶敏感的β-1,4糖苷键首先在酶的作用下迅速发生断裂,分子量降低,导致黏度值下降。而其余机团对酶的敏感性较弱,因此降解过程后期黏度变化较小[13]。综合考虑降解效率确定最佳酶解时间为150 min。
2.3胡芦巴胶及其酶解产物结构初步分析胡芦巴胶与降解低分子量多糖紫外、红外及差示扫描热扫描结果如图4所示,各图谱无明显差异,峰位基本不变,表明降解后结构未发生本质变化。其中,紫外光谱扫描图相似,均在260 nm和280 nm有吸收峰,说明各组分仍含有微量核酸与蛋白质。IR图谱显示胡芦芭胶与降解低分子量多糖均在3 436、2 925、1 746、1 645、1 541、1 152、1 076、1 023 cm-1处有较强的吸收峰[14],低分子量多糖的红外谱图与原胡芦巴胶的极为相似,只是1 746、1 541 cm-1处的特征吸收峰变强,说明酶解后胡芦巴胶单元基本结构没有发生明显变化,只是糖苷键断裂,-OH增多;DSC显示胡芦巴胶 (图4中a) 在90~150 ℃之间出现一个较明显放热峰,峰顶温度为125 ℃,在125 ℃两侧出现两个吸热峰。纤维素酶降解产物(图4中b)与胡芦巴胶峰形基本相同,峰强均减弱,在270 ℃放热峰消失。可见随着分子量降低,胡芦巴胶的聚集状态发生了改变,规整性减弱,分子结构的结晶区受到一定程度的破坏,结晶度降低,样品分解时放热峰峰强减弱。
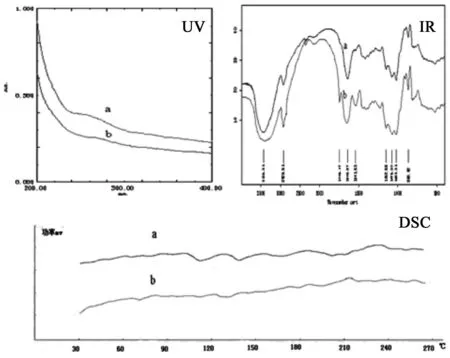
图 4 UV、IR及DSC扫描图 a.胡芦芭胶;b.低分子量多糖
3讨论
3.1目前大分子多糖主要采取化学降解法、酶降解法和物理降解法3种方法水解[15]。化学降解一般应用硫酸降解、稀盐酸法等,化学降解的原理是酸性溶液能引起多糖中糖苷键的断裂,使多糖降解为低分子片段,但相对而言,化学降解条件不易控制,易引起多糖结构破坏。超声波也可引起多糖解聚,多糖经控制性超声波处理,部分解聚,分子量降低,同时黏度下降,基本重复结构不变,保持了原有活性。但超声波辐射的结果表明,无论辐射时间长短,解聚物具有相当窄的分子量分布,不利于推广应用。酶降解反应因其高度的专一性、高效性以及降解条件及过程易于控制、无副反应等,在多糖降解中已逐渐受到重视。本文考察了酸解、超声辅助、酶解的方法对降解产物的影响,最终优选了酶法降解。

3.3还原糖指含有游离醛基、酮基和半缩醛、羟基而具有还原作用的单糖和双糖[19],而3,5-二硝基水杨酸(DNS)法是测定还原糖含量的常用方法。本文采用DNS测定降解产物中还原糖含量时,为了降低部分二糖等还原性糖对测定结果的影响,在测定过程中,重复测量3次,计算回收率,结果显示,平均回收率为97.84%,RSD=0.96%,表明用DNS法测定降解产物还原糖含量准确、可靠。
4结论与展望
本文以还原糖含量以及黏均分子量为指标,结合黏度,综合考察了不同降解方法和工艺条件对所得产物的影响,优选制备胡芦巴胶低聚糖最佳条件,其最佳酶解温度50 ℃,时间150 min,用量10 U·mg-1。初步结构分析表明,分子量显著下降,但结构图谱说明酶解后其结构没有发生显著改变。酶法简便,可控、高效,所得胡芦巴胶低分子量多糖可用于进一步活性评价,有利于胡芦巴胶相关新产品的开发和利用。
参考文献:
[1]汤凤霞,王忠敏.胡芦巴胶溶液流变特性研究[J].食品科学,2004,25(5):46-52.
[2]杨永利,郭守军,张继,等.冷水溶胡卢巴胶的流变性研究[J].食品科学,1999,6:23-25.
[3]Sharma RD,Raghuram TC.Hypoglycaemic effect of fenugreek seeds in non-insulin dependent diabetic subjects[J].Nutr Res,1990,10(7):731-739.
[4]Madar Z,Abel R,Samish S,et al.Glucose-lowering effect of fenugreek in non-insulin dependent diabetics[J].Eur J Clin Nutr,1988,42(1):51-54.
[5]Prasanna M.Hypolipidemic effect of fenugreek:A clinical study[J].Inf J Phamacol,2000,32(1):34-36.
[6]张雪云.功能性低聚糖的研究开发[J].饮料工业,2013,16(1):5-8.
[7]喻玲玲,邹坤.鄂产魔芋中葡甘露聚糖的含量测定[J].时珍国医国药,2008,19(3):680-682.
[8]李卫彬,阳文辉,黄锁义,等.当归总糖、还原糖和多糖的含量测定方法探讨[J].微量元素与健康研究,2008,25(3):46-47.
[9]韩哲文.高分子科学实验[M].上海:华东理工大学出版社,2005:55-61.
[10]王丽伟,卢拥军,单文文,等.瓜尔胶低分子量化降解条件研究[J].油田化学,2006,23(1):33-35.
[11]王在贵,黄世霞,张永跃,等.酶法降解茯苓多糖技术初步研究[J].中国饲料,2008,8:41-43.
[12]Manning K,Wood DA.Production and regulation of extracellular endocellulase by Agaricus bisporus[J].Microbiol,1983,129(6):1839-1847.
[13]Cai J,Zhao L,Zhang D.Chemical constituents from bletilla ochracea schltr.[J].Chem Res Chin Univ,2007,23(6):705-707.
[14]张黎明,王玲玲,孙茜,等.胡芦巴胶半乳甘露聚糖的酶法改性及其产物表征[J].食品科学,2009,30(1):195-199.
[15]赖萍,林跃鑫.天然多糖分子修饰研究进展[J].生命的化学,2003,23(3):183-187.
[16]史大华,刘玮炜,刘永江,等.低分子量海带岩藻多糖的制备及其抗肿瘤活性研究[J].时珍国医国药,2012,23(1):53-55.
[17]刘慧燕,赵谋明.江蓠低分子量多糖的提取以及抗氧化活性研究[J].食品工业科技,2005,26(3):67-69.
[18]杨春瑜,薛海晶,夏文水,等.黑木耳超微粉多糖分子量分布及降血脂功能研究[A].中国食品科学技术学会第五届年会暨第四届东西方食品业高层论坛论文摘要集[C].2007:398.
[19]邢其毅,裴伟伟,徐瑞秋,等.基础有机化学[M].第3版.北京:高等教育出版社,2005:980-984.

