肺动静脉瘘所致隐源性卒中病例分析及初筛方法研究
董培,隗冬梅,白亚秋,黄可飞,胡建科,杨曦晨
肺动静脉瘘(pulmonary arteriovenous fistula,PAVF)又称肺动静脉畸形,属临床少见病。近年随着PAVF导致脑梗死病例不断报道,其与隐源性卒中的关系被逐渐注意到,其机制是反常性栓塞。本文总结近年于本院确诊的PAVF所致脑梗死2例,分析患者临床表现、影像学特点,比较各种诊断方法特点。
1 资料与方法
1.1 一般临床资料
病例1:女,26岁,主因“突发右侧肢体无力伴言语不能2个月”于2015年8月入院。现病史:入院前2个月与家人争吵后出现右侧肢体无力,伴言语不能,但能理解他人讲话,口角向左歪斜,双眼视物模糊,于卧床休息30 min后出现意识丧失,无肢体抽搐,无二便失禁。4 h后症状缓解。当地头磁共振成像(magnetic resonance imaging,MRI)提示左侧大脑中动脉供血区大面积新发梗死灶。既往史:活动后气促8年。间断性头痛6年,每于劳累后出现,发作前双眼闪光持续2 min左右出现头钝痛,卧床休息约30 min可缓解,不影响正常活动。无反复鼻出血、齿龈出血、咯血、便血史。否认吸烟饮酒、高血压、高脂血症、糖尿病史。家族史:父母体健。查体:血压102/81 mmHg,轻度构音障碍,右侧面部针刺觉减退,右侧肢体针刺觉及音叉振动觉减退。一般内科检查及神经系统检查未见异常。辅助检查:头MRI(发病2个月)左侧颞顶叶皮层梗死灶。血常规:血红蛋白(hemoglobin,Hb)112 g/L,红细胞(red blood cell,RBC)4.11×1012/L,血细胞比容(hematocrit,HCT)Hct 36.1%。类风湿因子、凝血功能、CYP2C19基因型检测、超敏C反应蛋白、血清同型半胱氨酸、生化全项、补体C3C4、心磷脂抗体、免疫全套、抗中性粒细胞胞浆抗体、颈部血管超声、双下肢动静脉超声、弓上计算机断层扫描血管造影(computed tomography angiography,CTA)、头MRA、经颅多普勒、动态心电图未见异常。外院行血气分析提示缺氧,具体数值不详。
病例2:女,44岁,主因“发作性右侧肢体无力伴言语不清18 d”于2015年2月入院。现病史:入院前18 d晨起后突发右侧肢体无力,继而出现言语不清、吐字费力,但能理解他人讲话,伴右侧肢体麻木感。数小时后症状完全缓解。发病4 d后当地头MRI提示左侧基底节区新发梗死灶。既往史:活动后气促史10余年。自诉月经期经量较多,诊断“子宫腺肌症”。幼年反复鼻出血史,诊断为“干燥性鼻炎”,已愈。孕期曾患有“一过性血糖升高”,已愈。否认吸烟饮酒、高血压史。家族史:母亲患糖尿病,其父体健。查体:血压126/80 mmHg,一般内科检查及神经系统检查未见异常。辅助检查:头MRI(发病第20天)左侧基底节放射冠区伴渗出,右尾状核头、右侧脑室室旁梗死软化灶,脑内散在点状缺血改变。血常规Hb 110 g/L,RBC 4.14×1012/L,Hct 34.5%。室内空气下桡动脉血气分析:pH 7.407,PCO238.6 mmHg,PO284.9 mmHg,SO296%。动态心动图:窦性心律不齐,偶发房性期前收缩,阵发ST-T改变。胸部X线:两肺纹理稍重;右肺尖硬结节灶可能。生化全项、血清同型半胱氨酸、类风湿因子、凝血功能、免疫全套、抗中性粒细胞胞浆抗体、肿瘤标志物、主动脉弓超声、颈部超声、双下肢动静脉超声、头MRA、经颅多普勒、腹部超声未见异常。
1.2 方法 行cTCD、TEE检查。cTCD:准备两支10 ml注射器,一支混合盐水(9 ml生理盐水+1 ml空气+少量静脉血),另一支空管,经三通管连接,将两支注射器来回推注10次,经右侧肘正中静脉弹丸式注射,采用德国DWL经颅多普勒仪2 MHz探头监测双侧大脑中动脉。按文献[1]要求,需完成两次检查,第一次于平静呼吸状态下推注,第二次于推注后5 s行VM并持续10 s,两次检查间隔10 min。观察内容包括大脑中动脉栓子出现时间(潜伏期)、数量、持续时间,及与VM关系。依据栓子数量分级:0;1~10个栓子;>10个但无雨帘状;雨帘状(雨帘状指栓子数量多,以至于不能分辨单个栓子)[1]。有效VM判定方法:大脑中动脉血流速度减慢,之后反应性充血,血流速度增快。
2 结果
两例分别为青、中年女性,急性起病,速达高峰,头MRI提示缺血性卒中,例1为流域性梗死,例2皮层下梗死(图1、2),例1既往无脑血管病危险因素,虽然例2孕期曾患有“一过性血糖升高”,母亲患糖尿病,但两例均缺乏颅内、外大动脉粥样硬化性病变证据。动态心电图、TTE正常排除严重心律失常及瓣膜病等常见心源性原因;无引起急性脑梗死灶的其他原因,如炎症、凝血系统疾病、肿瘤等。两例TEE未见异常,右心声学造影示右房右室顺序显影,嘱患者行VM约5个心动周期后左房内肺静脉开口处见陆续大量微泡,考虑PAVF可能性大。cTCD(图1、2):两例第一次检查于平静呼吸状态下,分别于约第12个、第11个心动周期,探及雨帘状栓子信号,持续时间>50个心动周期。第二次检查VM后第7个、第6个心动周期出现栓子信号,栓子数量无明显变化,且于VM作用消失后(大脑中动脉血流速度回复后)仍有大量栓子信号。两例经肺部DSA确诊为PAVF,例1右肺中叶PAVF;例2右肺中叶、左肺舌叶PAVF。例1胸部增强CT与血管造影结果符合,例2未行胸部增强计算机断层扫描(computed tomography,CT)。例1于外院行经皮肺动静脉瘘栓塞术治疗,出院6个月随访活动后气促、头痛减轻,未再出现脑血管病事件。例2于外院行左肺舌叶封堵术,出院12个月随访活动后气促减轻,未再出现脑血管事件。
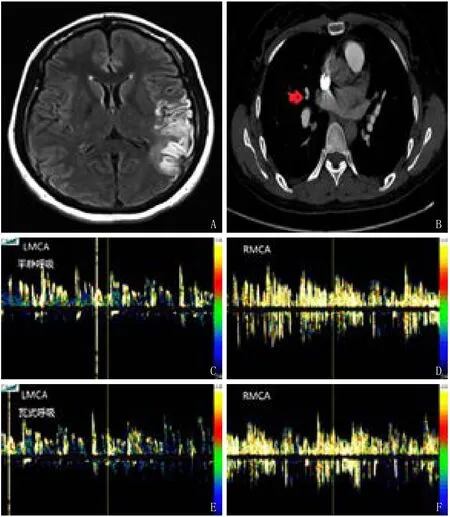
图1 例1头MRI及cTCD
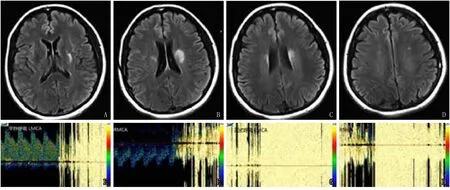
图2 例2头MRI及cTCD
3 讨论
3.1 临床表现
3.1.1 肺内表现 PAVF大多为先天性,系因胚胎发育异常导致肺动脉或体循环动脉与肺静脉直接相通,并在肺动脉压力下血管壁形成瘘管或瘤样病变,发病率仅2/100 000~3/100 000[2]。超过50%的PAVF患者无临床症状[3],症状性PAVF在儿童期无症状,随着分流不断增加,于成人期出现一系列低氧表现,如活动后呼吸困难、头晕、易疲劳等,体格检查可以发现发绀、杵状指(趾)、胸部连续性杂音。或仅表现为动脉血气分析异常。两例患者缺氧表现不明显,追问病史时方述活动后气促,例2患者DSA术前检查时动脉血气分析提示缺氧,提示动脉血气分析可能是PAVF唯一的肺内表现。另外PAVF有遗传倾向,约70%合并遗传性出血性毛细血管扩张症(hereditary hemorrhagic telangiectasia,HHT)[4]。但本文例1患者及国内已报道的部分病例仅存在肺部血管畸形,缺乏反复自发性鼻出血、皮肤毛细血管扩张及家族史,不符合HHT诊断标准,例2患者幼年反复鼻出血史,尚不能排除HHT诊断。提示对于隐源性卒中患者,动脉血气分析低氧表现可提供PAVF证据。
3.1.2 神经系统表现及影像学特点 缺血性卒中是PAVF最常见的肺外表现,其中短暂性脑缺血发作37%,脑梗死18%[5],机制为反常性栓塞。推测栓子可能源于:①双下肢、盆腔等周围静脉系统血栓形成;②未经肺毛细血管滤过的细菌、气栓;③原位血栓形成[6];④缺氧导致红细胞增多,血液黏稠度增加,形成小血栓。本文两例无颅内感染证据,不符合红细胞增多症诊断,考虑静脉统及原位血栓形成可能性大。两例患者仅行双下肢静脉检查未发现血栓,可能原因是:①检查时间过晚于发病时间;②静脉栓子不稳定,易溶解。提示如怀疑反常栓塞,应尽早完善静脉系统检查,包括盆腔、双下肢。目前认为PAVF发生缺血性卒中的影响因素有:①供血动脉直径:直径>3 mm发生缺血性卒中;②PAVF数量:多发较单发PAVF发生缺血性卒中概率高[7-8]。解释了例2头MRI病灶较例1多,除了位于皮层下的新发梗死灶外,皮层及皮层下多发陈旧灶。但应注意供血动脉直径不能等同于瘘口大小。PAVF合并偏头痛概率较高[9],例1患者头痛虽不符合偏头痛诊断标准,但经肺动静脉瘘栓塞术后头痛程度减轻,推测头痛也是PAVF神经系统表现之一。其他神经系统表现包括脑脓肿(5%~9%)[5],虽然发生率较低,既往脑脓肿病史患者发生隐源性卒中时,应考虑存在PAVF可能。
3.2 诊断方法
3.2.1 肺影像学检查 肺结构学检查是PAVF确诊方法。虽然胸部X线是肺部疾病常规检查手段,但因组织重叠投影,易漏诊,例2胸部X线未发现病灶。肺部DSA是诊断PAVF的金标准,可以观察PAVF瘘口、供血动脉、引流静脉等情况,但DSA是一种有创检查,不适于单纯诊断。肺部CTA是非侵入性的血管成像技术,是PAVF首选诊断方法,可以显示病灶整体情况,测量供血动脉直径。但患者需注入造影剂,且有一定辐射。
3.2.2 超声检查 虽然是间接诊断方法,但无创无辐射,且有助于与心内分流相鉴别。TEE可以直观显示房间隔等心脏解剖结构,两例CDFI未发现卵圆孔未闭,右心声学造影显示微泡经肺静脉到达左心房,且到达时间较晚(VM后5个心动周期),卵圆孔未闭多在3个或3个以下心动周期到达[10]。由于TEE部分有创性,患者不易配合完成VM,可能出现假阴性结果,且有0.9%并发症风险[1]。cTCD目前已广泛用于右向左分流的筛查,是一种无创性检查,操作简便,患者易于配合,可以实时动态观察进入颅内动脉栓子及脑血流变化情况。两例cTCD栓子信号特点:数量多(雨帘样);时程长(>50个心动周期);不受VM影响(平静呼吸时即见栓子信号,VM后栓子数量无变化,且在VM作用消失后仍有大量栓子信号)。房间隔缺损、合并肺动脉高压的PFO患者也可出现持续性大量分流,二者差别在于分流量是否受VM影响。VM造成右房左房压力差,卵圆孔孔径增大,分流量增加,VM作用消失后分流消失或减少。PAVF患者栓子经由肺动-静脉通路进入左房,即使VM作用消失后分流量不受影响。
总结,PAVF虽然是临床少见病,但作为主要的心外分流途径不容忽视。对于怀疑隐源性卒中患者,cTCD结合动脉血气分析有助于PAVF初筛,且适于疗效评价及随访。
1 Jauss M,Zanette E.Detection of right-to-left shunt with ultrasound contrast agent and transcranial Doppler sonography[J].Cerebravasc Dis,2000,10:490-496.
2 Hodgson CH,Kaye RL.Pulmonary arteriovenous fistula and hereditary hemorrhagic telangiectasia:a review and report of 35 cases of fistula[J].Dis Chest,1963,43:449-455.
3 Sands A,Dalzell E,Craig B,et al.Multiple intrapulmonary arteriovenous fistulas in childhood[J].Pediatr Cardiol,2000,21:493-496.
4 Shovlin C,Letarte M.Hereditary hemorrhagic telangiectasia and pulmonary arteriovenous malformations:issues in clinical management and review of pathologic mechanisms[J].Thorax,1999,54:714-729.
5 White RI Jr,Lynch-Nyhan A,Terry P,et al.Pulmonary arteriovenous malformations:techniques and long-term outcome of embolotherapy[J].Radiology,1988,169:663-669.
6 Yeung M,Khan KA,Antecol DH,et al.Transcranial Doppler ultrasonography and transesophageal echocardiography in the investigation of pulmonary arteriovenous malformation in a patient with hereditary hemorrhagic telangiectasia presenting with stroke[J].Stroke,1995,26:1941-1944.
7 Gossage JR,Kanj G.Pulmonary arteriovenous malformations.A state of the art review[J].Am J Respir Crit Care Med,1998,158:643-661.
8 Moussouttas M,Fayad P,Rosenblatt M,et al.Pulmonary ateriovenous malformations:cerebral ischemia and neurologic manifestations[J].Neurology,2000,55:959-964.
9 Thenganatt J,Schneiderman J,Hyland RH,et al.Migraines linked to intrapulmonary right-to-left shunt[J].Headache,2006,46:439-443.
10 Chessa M,Drago M,Krantunkov P,et al.Differential diagnosis between patent foramen ovale and pulmonary arteriovenous fistula in two patients with previous cryptogenic stroke caused by presumed paradoxical embolism[J].J Am Soc Echocardiogr,2002,15:845-846.

