对T2DM合并IR患者进行综合治疗及为其选择降血糖药物的方案
王宇阳 徐 梅⋆ 刘丹彤 秦亚玮
(1.徐州医科大学附属医院药学部 江苏 徐州 221006; 2.徐州医科大学药学院 江苏 徐州 221004)
患者罹患2型糖尿病(Type 2 diabetes mellitus,T2DM)的主要原因是其发生了胰岛素分泌缺陷和胰岛素抵抗(insulin resistance,IR)。IR是指在多种因素的作用下胰岛素促进人体摄取和利用葡萄糖的效率下降,进而使人体代偿性地分泌过多的胰岛素,以维持血糖稳定的一种现象。IR的主要表现是胰岛素的靶器官或靶组织对胰岛素的敏感性降低。T2DM患者IR的发生率为85%左右。在发生IR后,T2DM患者心血管疾病的发生率可显著增高[1]。因此,改善IR在治疗T2DM的过程中具有极其重要的地位。
1 对T2DM1合并IR患者进行饮食治疗与运动治疗的方案
营养过剩可引起脂代谢紊乱、腹型肥胖、高血压、心脏病等一系列胰岛素抵抗综合征(MS)。MS的发病与IR密切相关,而改善IR的一线疗法是饮食疗法和运动疗法。进行饮食治疗是治疗T2DM的首选方法。进行运动治疗可增加T2DM患者外周组织中胰岛素的敏感性。动物实验证明,进行饮食治疗与运动治疗可显著降低IR大鼠的FPG及空腹胰岛素(FINS)的水平,提高其机体的胰岛素敏感指数(ISI)[2]。临床实践证实,进行饮食控制和运动锻炼能增强人体对葡萄糖的摄取和利用功能,提高其外周组织对胰岛素的敏感性,进而可减轻其IR。
1.1 对T2DM合并IR患者进行饮食治疗的方案 医学营养疗法(Medical Nutrition Therapy, MNT)是糖尿病的基础疗法。MNT主要包括个体化营养评估、营养诊断、制定营养计划、实施营养计划及营养监测等。此法在防治糖尿病及其并发症、帮助糖尿病患者进行自我病情管理及对患者进行糖尿病教育等方面均可起到重要的作用。据报道,早期T2DM患者在进行3个月的强化饮食治疗后其糖化血红蛋白(HbA1C)值可下降2%,其糖尿病微血管和大血管并发症的发生率也可显著降低[3]。我们在参考中国2型糖尿病防治指南(2013版)的基础上,制定了对T2DM患者进行饮食治疗的目标及路线图,详情见图1。

图1 对T2DM患者进行饮食治疗的目标及路线图[4]
糖尿病患者每日摄入的总能量需根据三大营养素的比例进行分配,其膳食中由脂肪提供的能量不应超过总能量的30%(饱和脂肪酸的摄入量不应超过总能量的7%),由碳水化合物提供的能量应占总能量的50%-60%。肾功能正常的糖尿病患者,蛋白质的摄入量应为10%-15%(优质蛋白的摄入量应超过50%)。有显性蛋白尿的糖尿病患者,其蛋白质的摄入量宜限制在0.8g/kg/d以下,其食盐的摄入量应限制在每天6g以内。合并高血压的此病患者应严格地限制食盐的摄入量[4]。
1.2 对T2DM合并IR患者进行运动治疗的方案 运动疗法在T2DM的综合治疗方案中占有重要的地位。进行有规律的运动可增加T2DM合并IR患者胰岛素受体的亲和力和胰岛素受体的数目,提高其外周组织对胰岛素的敏感性,从而可改善IR。研究表明,此类患者进行长期有规律的运动不仅能改善糖代谢,有效预防糖尿病的并发症,还能防治血脂异常、肥胖症及高血压。T2DM患者在进行运动治疗后其甘油三酯、总胆固醇的指标均可显著降低[5]。需要注意的是,T2DM患者在进行运动前要进行必要的心肺功能及运动功能评估,若其不适合进行运动应待其病情得到改善后再开始进行有规律的运动。
1.2.1 对T2DM合并IR患者进行运动治疗的方式 T2DM合并IR患者进行运动的方式要与其年龄、病情及身体的承受能力相符。在对此类患者进行运动治疗期间应定期评估其上述情况,及时调整其运动计划。此类患者若无进行抗阻运动的禁忌症,最好每周进行2次轻度或中度的抗阻运动,并重点锻炼肌肉的力量和耐力。联合进行抗阻运动和有氧运动是T2DM合并IR患者较好的运动方式。
1.2.2 对T2DM合并IR患者进行运动治疗的强度 T2DM合并IR患者在进行运动时需重点考虑运动项目的安全性与有效性。美国糖尿病协会(ADA)指出,T2DM合并IR患者在进行运动时其摄氧量应达到其最大摄氧量的60%,即应进行中等强度的运动。中等强度的运动主要包括快走、打太极拳、骑车、打乒乓球、打羽毛球和打高尔夫球等。
1.2.3 对T2DM合并IR患者进行运动治疗的时间和频率T2DM合并IR患者的运动时间一般应在餐后的1-2个小时内。研究发现,此类患者在餐后的90min内进行运动可取得最好的降血糖效果。此类患者进行运动的频率一般应达到每周3-5次,每次进行运动的时间至少为20-30min,其运动的间歇期不宜超过3-4天,否则可使已经增高的胰岛素敏感性明显降低。此类患者进行运动的持续时间应从最初的5-10min/次逐渐增加至40-60min/次,但最长不应超过60min/次,以免发生关节和肌肉损伤。
2 T2DM合并IR患者进行药物治疗的方案
2.1 T2DM合并IR患者宜选用的降血糖药物
2.1.1 噻唑烷二酮类药物(TZDs) TZDs为强效过氧化物酶体增生物激活受体γ(PPAR-γ)的选择性激动剂。TZDs不会促使人体分泌胰岛素,但能增强胰岛素靶细胞对胰岛素的敏感性,从而降低血糖,改善胰岛β细胞的功能及IR。目前,在我国上市的TZDs主要为罗格列酮和吡格列酮。为T2DM患者单用TZDs进行治疗不会导致低血糖。为此病患者联用TZDs与其他的降血糖药物(如磺酰脲类药物、二甲双胍)可增强降血糖的作用,但也可增加患者低血糖的发生率。TZDs经常引发的不良反应为体重增加和水肿。
2.1.2 二甲双胍 二甲双胍是T2DM患者控制血糖的一线用药和进行联合用药时的基本用药。此药主要通过减少肝脏葡萄糖的输出和改善外周IR来降低血糖。二甲双胍可改善IR的机制主要包括以下两个方面:1)此药可加强人体内葡萄糖的无氧酵解及氧化代谢,抑制肝糖原的异生。2)此药可抑制人体内高浓度的葡萄糖和TNF-α所导致的脂肪分解,降低游离脂肪酸的含量及血脂的水平、改善IR。UKPDS的研究结果证明,二甲双胍可降低肥胖的T2DM患者心血管事件的发生率及其死亡率[4]。在临床上,二甲双胍主要用于对肥胖的T2DM患者进行治疗。肥胖的T2DM合并IR患者在使用此药进行治疗后可取得降低血糖、改善IR及减少体重的作用。单用二甲双胍治疗T2DM不会导致低血糖。肝肾功能不全、低血容量性休克及心力衰竭患者应禁用此药,老年患者应慎用此药。研究发现,与单用TZDs或二甲双胍相比,联用TZDs和二甲双胍治疗T2DM的效果较优,可更有效地降低患者的血糖值和HbA1c值,改善其胰岛β细胞的功能和IR[6]。
2.1.3 DPP-4抑制剂 DPP-4抑制剂可抑制DPP-4的活性、减少GLP-1的代谢,从而可使内源性GLP-1的浓度升高。GLP-1可同时作用于胰岛α细胞和胰岛β细胞,促进胰岛β细胞分泌胰岛素,同时抑制胰岛α细胞释放胰高血糖素,减少肝糖的输出,增加肌肉、脂肪组织对糖的摄取,提高肝脏、肌肉等组织对胰岛素的敏感性,从而降低血糖。研究发现,DPP-4抑制剂可增高胰岛素的水平,显著改善IR,但其改善IR的效果弱于二甲双胍[7]。脂肪组织可分泌多种因子(如脂联素、瘦素等),其中脂联素能改善IR并增加胰岛素的敏感性。研究发现,为T2DM合并IR患者应用DPP-4抑制剂进行治疗可明显增加其脂联素的水平,进而可改善IR[8]。
2.1.4 GLP-1受体激动剂 GLP-1是一种重要的肠促胰岛素。GLP-1受体激动剂可作用于胰岛α细胞和胰岛β细胞,增加胰岛素的分泌量,抑制胰高血糖素的分泌,改善糖毒性。GLP-1受体激动剂能延缓患者的胃排空,抑制其摄食中枢的功能,减少其食物的摄入量,从而减轻其体重,改善其IR的症状。此外,GLP-1受体激动剂还可作用于肝脏和脂肪组织,升高血浆及肝组织中脂联素的水平,抑制肝糖原的异生,降低内源性葡萄糖的水平、促进脂肪组织(特别是内脏脂肪)的分解,从而可间接地改善IR。综上所述,GLP-1受体激动剂可通过改善血糖、血脂、减轻体重等多种生物学效应发挥保护胰岛β细胞、改善IR和保护心血管等重要的作用。
2.2 T2DM合并IR患者在合并有其他疾病时宜选择的药物 T2DM合并严重IR的患者若同时患有高血压或血脂异常,应选用具有改善IR的降压药物或调脂药物。
2.2.1 ACEI/ARB类药物 ACEI具有增加骨骼肌的血流量、改善血管内皮的功能、促进胰腺的血循环、增加胰岛素的分泌量、改善IR等作用。发生低钾血症会持续损伤患者胰岛的功能。发生低镁血症可显著减少患者胰岛素的分泌量。ACEI可抑制血管紧张素醛固酮系统(RAS)的功能,阻断醛固酮的分泌,保存细胞内的钾和镁,从而可保护胰岛的功能,改善IR。此外,ACEI还可增高人体内激肽的水平,调节葡萄糖的转运和摄取。
2.2.2 他汀类药物 T2DM合并IR患者可因发生炎症因子介导的炎症反应而使血管内皮受到损伤,引起血管内皮细胞的结构和功能异常,使胰岛素不能发挥作用而引发IR。他汀类药物不仅具有调脂的作用,还具有潜在的抗炎作用,能减少人体内炎症介质的产生,改善血管内皮的功能,增加骨骼肌的血流量,提高胰岛素的敏感性,进而可改善IR。
3 T2DM合并IR患者治疗IR的路线图
T2DM是一种终身缓慢进展性疾病,常与IR同时发生。随着病程的进展,T2DM合并IR患者胰岛的功能可逐渐下降,并逐渐出现多种并发症。因此,T2DM合并IR患者需进行饮食治疗、运动治疗及药物治疗等综合治疗,而且在选用药物时应重点考虑其是否具有改善IR的作用。我们参考“中国2型糖尿病防治指南”,为T2DM合并IR患者制定了治疗IR的路线图。详见图2。
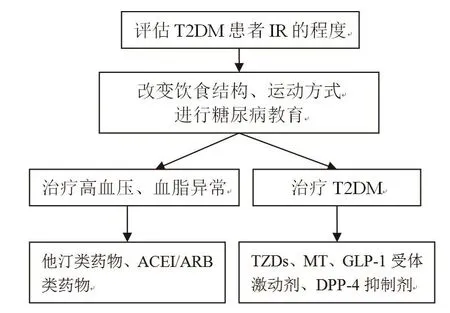
图2 T2DM合并IR患者治疗IR的路线图
4 案例分析
4.1 案例分析 1.某女性患者,52岁,其BMI值为32.4Kg/m2,因“血糖偏高1年”在我院接受住院治疗。1年前,该患者在进行体检时发现血糖升高,其FPG值为12.7mmol/L。该患者曾服用二甲双胍缓释片及瑞格列奈进行治疗,并间断性地使用胰岛素进行治疗,但未规律地监测血糖,未控制饮食,平时其血糖值在12-15mmol/L之间波动。在1个月前,该患者在进行体检时发现FPG值为15.8mmol/L,进行尿糖检测的结果为“++++”。在该患者入院后对其进行相关的检查,确诊其患有T2DM、高血压。该患者有10年的高血压病史,其血压控制尚可。该患者的T2DM初次得到确诊,其腹围为105.2cm,其体型肥胖,其HbA1c 值为9.50%,其血糖控制差,其空腹胰岛素(FINS)值为290.70pmol/L,其合并高血压且存在IR。在对该患者进行降血糖治疗时应重视改善其IR的症状,并对其进行降血压、减轻体重等综合治疗。该患者最初联用沙格列汀与格列喹酮进行降血糖治疗,但其空腹及餐后血糖均控制不佳。此后,该患者联用沙格列汀、格列吡嗪缓释片与阿卡波糖进行降血糖治疗,其血糖控制仍不理想。该患者的FPG 值为12.56mmol/L,其HbA1c值为 9.50%。根据《中国2型糖尿病防治指南》2013版中提供的意见,新确诊的T2DM患者,在HbA1c值>9.0%或FPG值>11.1mmol/L时口服降血糖药物很难在短期内使血糖得到理想的控制。此类患者应采用短期胰岛素强化疗法进行治疗,待血糖得到控制后再使用能改善IR的降血糖药物进行治疗。本例患者的BMI值为32.4Kg/m2,且体型肥胖、肝肾功能良好,在对其进行短期的胰岛素强化治疗后应使用二甲双胍和GLP-1受体激动剂对其进行治疗。这两种药物均具有改善IR和减轻体重的作用。GLP-1受体激动剂可延缓胃排空并抑制进食,因此易导致胃肠道的不良反应。患者在使用此药进行治疗1周内可出现腹胀、腹痛、嗳气及便秘等一系列症状,但一般不需停药其不适的症状即可自行缓解。研究发现,与单用二甲双胍、TZDs相比,联用这两种药物治疗T2DM可有效降低患者的FPG值、餐后血糖(PPG)值及HbA1c值,改善其胰岛β细胞的功能和IR。另一项研究发现,联用GLP-1受体激动剂与二甲双胍治疗IR的效果较好。在对本例患者进行治疗时,我们建议联合使用GLP-1受体激动剂、二甲双胍和TZDs三种不同机制的降血糖药物,以改善其IR。该患者有10年的高血压病史,曾服用厄贝沙坦氢氯噻嗪片进行治疗。患者若长期使用氢氯噻嗪片进行治疗会对其血糖产生影响。因此,我们建议该患者改用ACEI或ARB类药物进行治疗,以有效地控制血压,同时治疗IR(这两种药物均能改善IR)。在对该患者进行治疗期间,我们对其进行了系统的糖尿病知识宣教,嘱其长期保持规律的饮食习惯及进行适当的运动,以便增强其机体对葡萄糖的摄取和利用能力,提高其外周组织对胰岛素的敏感性,进而改善其IR的症状。该患者在进行系统的治疗后其病情得到了理想的控制。
4.2 案例分析 2.某男性患者,74岁,其BMI值为31.23Kg/m2,因“血糖值升高14年,发生水肿伴视物模糊1个月”在我院接受住院治疗。该患者在发病初期曾服用二甲双胍进行治疗,但其血糖控制欠佳,其FPG值为10mmol/L。1年前,该患者出现双下肢可凹性水肿,其尿蛋白值为121.00mg/L。该患者改用门冬胰岛素30进行治疗(早餐前皮下注射22u的此药,晚上皮下注射14u的此药),在用药期间未监测血糖。近1个月,该患者双下肢水肿的症状加重,其血Cr 值为132μmol/L,其BUN值为 10.50mmol/L。为此,该患者改用门冬胰岛素30(早餐前皮下注射20u的此药,晚上皮下注射16u的此药)、阿卡波糖(50mg,tid po)与米格列奈钙(5mg,bid po)进行治疗。该患者有1年的高血压病史,其血压值最高可达160/100mmHg,其血压控制不佳。该患者的病情被诊断为:T2DM、糖尿病肾病、2级高血压、脑梗塞。该患者的体型肥胖,其FINS值为 2980.00pmol/L,其HbA1c值为 6.60%,其血糖控制差,且存在IR。为该患者长期使用胰岛素进行治疗会增加其体重,而体重的增加又会进一步升高其血糖和血脂,加重其IR,形成恶性循环。因此,在对该患者进行治疗时应选择能改善IR、减轻体重的降血糖药物。二甲双胍是治疗T2DM的一线用药。该药不仅可有效改善IR,还可减轻肥胖患者的体重。但是,二甲双胍禁用于肝肾功能不全的患者。本例患者的年龄偏高且存在肾功能不全,不适合使用二甲双胍进行治疗。该患者使用的降血糖药物包括门冬胰岛素30(早晨皮下注射20u)、阿卡波糖(50mg, tid po)和米格列奈钙(5mg,bid po)。米格列奈钙属于餐时胰岛素促泌剂。将此药与胰岛素联合使用时可增加患者低血糖的发生率。本例患者在进行治疗的过程中多次出现低血糖、进食糖块后血糖上升的情况。我们建议该患者停用米格列奈钙,将使用门冬胰岛素的方案调整为早晨皮下注射18u、晚上皮下注射16u,但其血糖仍未得到理想的控制。该患者的胰岛功能受损且合并有IR。因此,我们建议该患者使用GLP-1受体激动剂利拉鲁肽进行治疗。该患者在应用利拉鲁肽进行治疗后其病情得到了有效的控制。GLP-1受体激动剂具有改善血糖、血脂、减轻体重、保护胰岛β细胞、改善IR和保护心血管等作用。本例患者的血Cr值为 132μmol/L。利拉鲁肽在进入人体后,其99%的药物成分可与血浆蛋白相结合,而且不经过肾脏清除,不会对肾功能造成损害。GLP-1受体激动剂可延缓胃排空并抑制进食,因此易导致腹胀、腹痛、嗳气、便秘等胃肠道的不良反应。患者在使用此药进行治疗期间若发生上述的不良反应一般不需停药,只需放慢进食的速度其不适的症状即可自行缓解。
5 结论
在对T2DM合并IR患者进行降血糖治疗时,首先应评估其发生IR的严重程度,然后对其进行有针对性的减轻体重、降血压、调脂、降血糖(选用具有改善IR作用的降血糖药)等常规治疗,同时应对其进行糖尿病知识的宣教、运动治疗与饮食治疗。临床药师应结合T2DM合并IR患者病情的特点及临床医生的意见为患者设计合理的降血糖用药方案,从而更有效地控制其血糖,改善其IR。
[1] Hsu CH. Different impacts of metabolic syndrome compon ents on insulin resistance in type 2 diabetes[J]. Int J Endocrinol, 2013, 2013:1-7.
[2] 陈丹, 毕会民. 饮食、运动对胰岛素抵抗大鼠骨骼肌中GSK-3表达的影响[J].中国现代医学杂,2009,19(22): 3421-3424.
[3] 胡一宇, 黄丽华. 糖尿病患者饮食教育的研究现状[J].中华护理杂志, 2013, 48(6):555-557.
[4] 中华医学会糖尿病学分会. 中国糖尿病防治指南(2010版)[S].北京:北京大学医学出版社,2011:18-20.
[5] 孙莉敏, 胡永善, 吴毅. 运动锻炼对2型糖尿病患者血脂与体质指标的影响[J].中国运动医学杂志,2002, 21(1):51-53.
[6] 庞晓瑜, 郭卉. 胰岛素增敏剂与ACEI类药物治疗胰岛素抵抗的研究进展[J].中国医药科学, 2013, 3(6):34-36.
[7] 吕珊珊, 潘天荣, 钟兴, 等. 西格列汀联合二甲双胍对2型糖尿病患者胰岛素抵抗、血脂和血压的影响[J].安徽医科大学学报, 2014, 6(49):107-109
[8] 王丹彤. 西格列汀联合二甲双胍对2型糖尿病胰岛素抵抗及脂联素的影响[J].药物研究, 2015, 24(16):54-55.

