siRNA沉默Bmi-1表达对肺腺癌A549细胞侵袭能力的影响
siRNA 沉默Bmi-1表达对肺腺癌A549细胞侵袭能力的影响
刘丹丹郑翔宇1,2刘奔刘纯青1王艺芳1赵宝霞1孟秀香1
(大连医科大学诊断学实验中心,辽宁大连116044)
摘要〔〕目的观察Bmi-1基因沉默对A549细胞增殖和侵袭影响并初步探讨其机制。方法根据四条针对Bmi-1的小干扰RNA(siRNA)序列,将其瞬时转染到A549细胞中,选择最有效的一条链并构建到逆转录病毒真核表达载体pSUPERretro-Neo中,形成重组载体,然后将其稳定转染至A549细胞中,构建了稳定转染Bmi-1-shRNA的A549细胞。应用MTT实验检测Bmi-1-siRNA对A549细胞体外增殖的影响;Transwell小室观察其对A549侵袭能力的影响;RT-PCR和明胶酶谱法分别观察siRNA对A549细胞MMP-2/MMP-9表达及活性的影响。结果Bmi-1 siRNA能够抑制A549细胞的增殖能力和侵袭能力,Bmi-1 siRNA能够抑制A549细胞MMP-2/MMP-9的表达和活性。结论Bmi-1 siRNA对A549细胞侵袭能力的抑制和MMP-2/MMP-9的活性降低有关。
关键词〔〕肺腺癌;siRNA;Bmi-1基因;侵袭
中图分类号〔〕R734〔文献标识码〕A〔
基金项目:辽宁省自然科学
通讯作者:孟秀香(1965-),女,教授,博士,硕士生导师,主要从事肿瘤细胞生物学研究。
1大连医科大学检验医学院2河南省中医院检验科
第一作者:刘丹丹(1964-),女,实验师,主要从事肿瘤细胞生物学研究。
目前对肺腺癌发生发展确切机制的了解仍较为贫乏,因此研究肺癌侵袭、转移的发生机制具有重要的临床意义。Bmi-1最初作为原癌基因被Van Lohuizen等人〔1〕发现,Bmi-1与c-myc基因协同使得B淋巴细胞发生改变从而导致了鼠淋巴白血病〔2〕。近年研究表明,Bmi-1基因在人类一些常见的恶性肿瘤如鼻咽癌、乳腺癌、大肠癌、胃癌等肿瘤中都存在高表达情况〔3~6〕,与肿瘤的增殖和淋巴结转移密切相关。有关Bmi-1在肺癌中的表达已有报道,非小细胞肺癌(NSCLC)中Bmi-1表达较正常肺组织相比明显增高〔7〕。并且Bmi-1在肺癌的晚期较肺癌早期表达明显增高〔8〕,这说明Bmi-1参与了肺癌的发生发展机制。以往研究中,针对Bmi-1基因设计4对发夹式Bmi-1 siRNA质粒,均能抑制子宫颈癌Hela细胞的体内外增殖能力〔9〕。本文研究沉默Bmi-1基因的表达对A549细胞迁移和侵袭的影响。
1材料和方法
1.1细胞培养A549细胞用含10%胎牛血清的RPMI-1640培养基在37℃、5% CO2的CO2培养箱中培养。未转染的细胞命名为A549-wt,转染PSUPER-retro-neo-Bmi-1和自由序列的分别命名为A549-siRNA-Bmi-1和A549-ctr。
1.2RT-PCR总RNA用Trizol试剂提取,然后按照TaKaRa的RT-PCR试剂盒说明书进行操作。MMP-2基因上游引物:5′-TGGCAGTGCAATACCTGAAC-3′,MMP-2基因下游引物:5′-CCGTACTTGCCATCCTTCTC-3′;MMP-9基因上游引物:5′-AGTGGCACCACCACA ACA T-3′,MMP-9基因下游引物:5′-TCCTGGGTGTAGAGTCTCTCG-3′;GAPDH上游引物:5′-GAAGGTGAAGGTCGGAGTC-3′,GAPDH下游引物:5′-GAAGATGGTGATGGGATTTC-3′。扩增产物在含0.5%溴乙啶的1%琼脂糖凝胶电泳中分离。
1.3四甲基偶氮唑蓝比色法(MTT)法检测细胞增殖能力取对数生长期的三组细胞消化后按每孔细胞数为2×103单细胞悬液接种于96孔板中,设5个复孔,1 d后各组分别取5孔进行实验,连续测5 d。检测时每孔加入MTT 10 μl,4 h后小心吸去孔内的液体,加入150 μl DMSO,震荡15 min,使结晶物完全溶解,酶标仪490 nm测定吸光度。
1.4细胞侵袭试验按照BD BioCoatTMMatrigelTMInvasion Chamber试剂盒说明书要求进行操作。大致如下:将无血清培养基加入小室,然后置于37℃、5%CO2培养箱内2 h。除去培养基,加入浓度为1×105/ml的细胞悬液0.5 ml(无血清)。下室加含10%胎牛血清的培养基0.75 ml。在37℃、5%CO2培养箱内48 h。用棉签将残留在上室内表面的细胞拭去。用10%甲醛固定迁移至小室外表面的细胞,0.25%结晶紫染色后在显微镜下计数细胞,取5个视野(×400)细胞计数的平均值。
1.5明胶酶谱分析取等量的三组细胞接种在6孔板上,待80%融合时换无血清的1640培养基继续培养72 h收集上清液。1 000 r/min离心5 min,分装,-80℃保存。制胶结束后(分离胶含0.1%明胶的),自冰箱中拿出细胞上清液,加入无β-巯基乙醇的5×上样缓冲液后进行上样、电泳。取出PAGE胶,在含2.5%TritonX-100洗脱液震荡洗涤15 min×4次,加入明胶酶缓冲液,37℃孵育48 h。再进行脱色直至出现清晰条带。凝胶成像,图像分析软件进行定量分析。
1.6统计学方法采用SPSS13.0统计软件行方差分析。
2结果
2.1Bmi-1 siRNA抑制A549细胞的体外增殖能力MTT法检测A549细胞每天的吸光度值,A549 Bmi-1 siRNA细胞在第三天及以后的时间OD值明显低于A549-ctr 和A549-wt两组细胞,生长速度明显受到抑制(P<0.05);而后两组细胞的生长数值在统计学上无差异(P>0.05)。见表1。
表1 沉默Bmi-1基因对A549细胞体外增值能力的
与A549-siRNA-Bmi-1比较:1)P<0.05
2.2Bmi-1 siRNA抑制A549细胞的侵袭能力Transwell方法检测沉默Bmi-1基因后对A549细胞侵袭能力的影响,A549-Bmi-1-siRNA细胞组的侵袭能力显著低于A549-wt和A549-ctr细胞组(P<0.01),而A549-wt和A549-ctr细胞组之间无显著性差异(P>0.05)。见图1。

图1 沉默Bmi-1基因对A549细胞侵袭能力的影响(×400)
2.3沉默Bmi-1表达对MMP-2/MMP-9表达及活性的影响
2.3.1RT-PCR检测三组细胞中MMP-2和MMP-9 mRNA表达结果A549-Bmi-1-siRNA细胞MMP-2、MMP-9 mRNA的表达比A549-wt和A549-ctr细胞中MMP-2、MMP-9表达明显降低(P<0.05)。见图2。
2.3.2明胶酶谱法检测沉默Bmi-1基因后对MMP-2和MMP-9活性的影响如图3所示,A549-Bmi-1 siRNA细胞组MMP-2
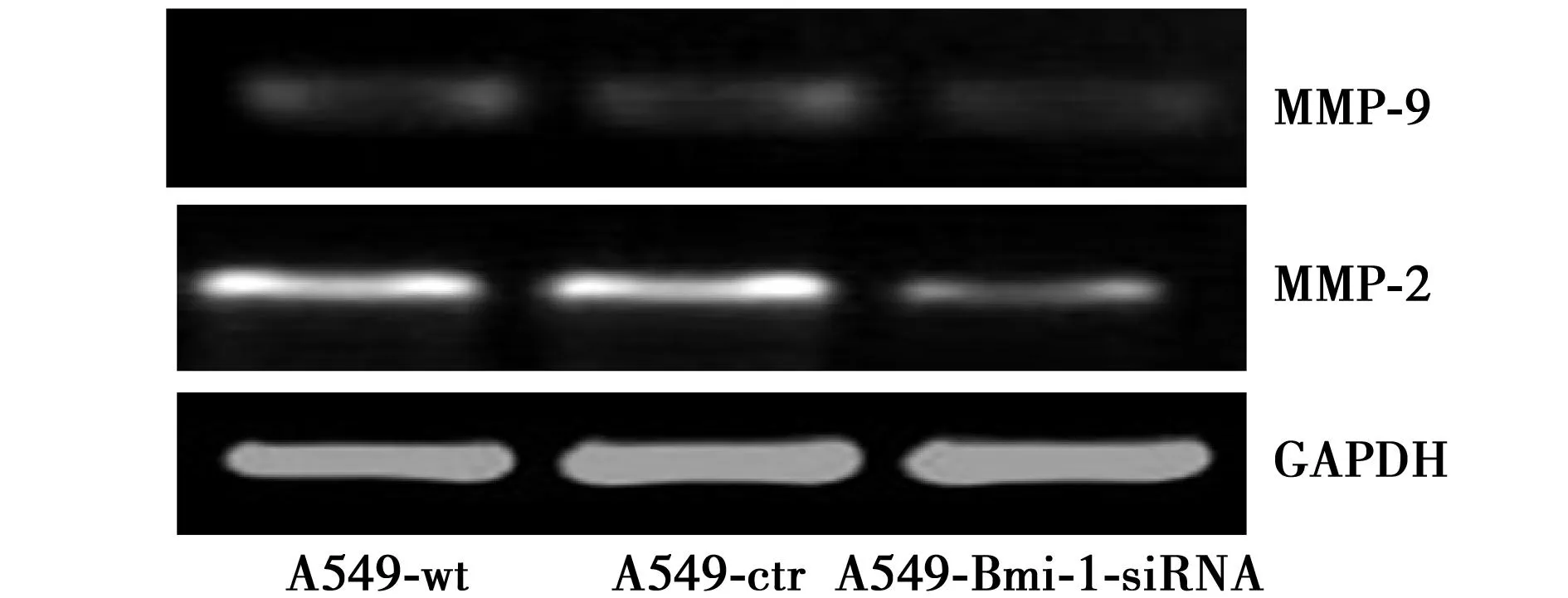
图2 RFT-PCR检测各组细胞MMP-2、MMP-9 mRNA表达
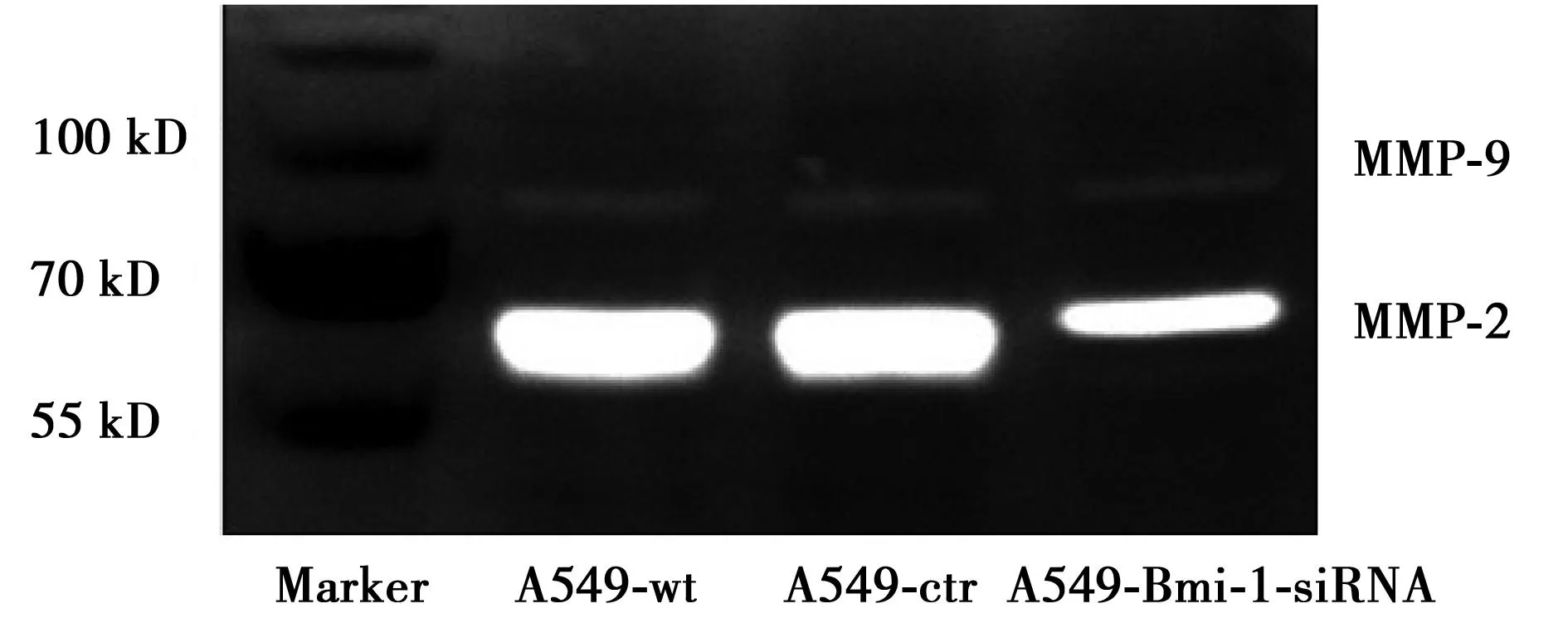
图3 沉默Bmi-1基因对A549细胞MMP-2/MMP-9 活性的影响
(active形式)和MMP-9(active形式)显著低于A549-wt和A549-ctr细胞组(P<0.05),而A549-wt和A549-ctr细胞组酶谱分析结果无显著差异(P>0.05)。
3讨论
本文结果表明沉默Bmi-1基因能够减弱A549细胞的体外增殖能力侵袭是恶性肿瘤也是最重要的恶性生物学特征。肿瘤细胞通过细胞膜表面特定的受体与细胞外基质或基底膜中的层黏连蛋白、Ⅳ型胶原和纤维连接蛋白的黏附在一起,然后通过释放一些蛋白水解酶类或激活基质中已经存在的酶原来促使基质成分发生降解,癌细胞才得以迁移至被水解的基质空隙中,通过这一方式癌细胞不断向基质深层侵袭,为下一步的转移打下了基础。铺有人工基底膜Transwell小室是目前检测癌细胞体外侵袭能力的简单而有效的方法。Transwell小室实验中采用的基质胶Matrigel是从EHS小鼠肿瘤中提取的基质成分,富含层黏连蛋白以及Ⅳ型胶原等成分。将基质胶Matrigel铺在侵袭小室的多孔滤膜上,能够形成和天然基底膜非常类似的基底膜结构,可以模拟体内的基质状况。小室下方的血清浓度高于上方,所以,具有侵袭能力的细胞就会朝向高血清浓度方向趋动,穿过人工基底膜和直径为 8 pm的聚碳酸微孔滤膜。本研究发现干扰组A549细胞成功穿过Matrigel膜和小室滤膜的细胞数较两个对照组明显减少,说明转染Bmi-1-shRNA能够使肺腺癌细胞侵袭能力明显降低。
Liotta等〔10〕提出侵袭转移三步学说:即黏附、降解和移动。其中血管基底膜的降解、破坏是肿瘤侵袭转移的重要步骤,基质膜是机体阻碍癌细胞侵袭和转移的重要屏障。当癌细胞脱离原发灶迁移到细胞外基质时,癌细胞能够通过分泌多种蛋白水解酶来降解细胞外基质,将基底膜这个阻碍癌细胞侵袭的屏障破坏。癌细胞从血管基底膜的破损处移出进入到血管中,进行血道转移。从中不难看出,肿瘤细胞侵袭能力是其进行转移的必需前提,因而非常重要。而达到侵袭目的的前提是其能分泌一些蛋白酶来降解细胞外基质。能降解细胞外基质的蛋白酶包括四种,其中基质金属蛋白酶(MMPs)是所有蛋白酶中最重要的一种。在癌细胞侵袭和转移的这一复杂过程中,MMPs起着非常重要的作用,是一类依赖锌离子的细胞外蛋白水解酶,可降解细胞外基质,能促进恶性肿瘤细胞的侵袭和转移〔11,12〕。根据其作用底物的类型不同,可将金属蛋白酶分为五大类,即胶原酶、明胶酶、基质溶解酶、巨噬细胞弹性蛋白酶、膜型基质金属蛋白酶。这些酶的主要功能是降解各种类型的胶原、明胶蛋白、纤连蛋白、层连蛋白等细胞外基质成分。在这些酶中,最为重要同时研究比较清楚的是明胶酶MMP-9和MMP-2〔13〕,二者可以催化水解细胞间基质成分,降解基膜的主要成分胶原,促进肿瘤细胞向周围正常组织浸润〔14〕。Suzuki等〔15〕发现在NSCLC中的MMP-2和MMP-9均有高表达,且MMP-2的表达明显强于MMP-9,故认为MMP-2在肺癌发生发展中发挥比MMP-9更加重要的作用。本实验结果显示高侵袭肺腺癌细胞株A549中,MMP-2的表达及活性也确实高于MMP-9。Bmi-1与肿瘤的侵袭转移密切相关,但它与MMPs是否有关及其介导通路尚未见报道。本研究结果表明,Bmi-1-shRNA抑制了A549细胞MMP-2/MMP-9 mRNA表达及MMP-2/MMP-9的活性,Bmi-1与肺腺癌的侵袭特性密切相关。
4参考文献
1Van Lohuizen M,Verbeek S,Scheijen B,etal.Identification of cooperating oncogenes in E mu-myc transgenic mice by provirus tagging〔J〕.Cell,1991;65(5):737-52.
2Haupt Y,Alexander WS,Barri G,etal.Novel zine finger gene implicated as myc collaborator by retrovirally accelerated lymphomagenesis E-myc transgenic mice〔J〕.Cell,1991;65(5):753-63.
3Kim JH,Yoon SY,Jeong SH,etal.Overexpression of Bmi-1 oncoprotein correlates with axillary lymph node metastases in invasive ductal breast cancer〔J〕.Breast,2004;13(5):383-8.
4黄开红,刘建化,李学先,等.Bmi-1基因过度表达与胃癌分化、转移及预后的关系〔J〕.南方医科大学学报,2007;27(7):973-5.
5Yonemitsu Y,Imazeki F,Chiba T,etal.Distinct expression of polycomb group proteins EZH2 and Bmi-1 in hepatocellular carcinoma〔J〕.Hum Pathol,2009;40(9):1304-11.
6林妙霞,文卓夫,冯智英,等.Bmi-1、Ki67在大肠肿瘤组织中的表达及其意义〔J〕.癌症,2008;27(12):1321-6.
7冯艳,宋立兵,郭宝红,等.Bmi-1在乳腺癌组织中的表达及意义〔J〕.癌症,2007;26(2):154-5.
8Vrzalikova K,Skarda J,Ehrmann J,etal.Prognostic value of Bmi-1 oncoprotein expression in NSCLC patients:a tissue microarray study〔J〕.J Cancer Res Clin Oncol,2008;134(9):1037-42.
9Yue Jiang,Benli Su,Xiuxiang Meng,etal.Effect of siRNA-mediated silencing of Bmi-1 gene expression on Hela cells〔J〕.Cancer Sci,2010;101(2):379-86.
10Liotta LA,Stetler Stevenson WG.Tumor invasion and metastasis:an imbalance of positive and negative regulation〔J〕.Cancer Res,1991;51(18 suppl):5054s-9s.
11Stetler-Stevenson WG,Hewitt R,Corcoran M.Matrix metalloproteinases and tumor invasion:from correlation and causality to the clinic〔J〕.Semin Cancer Biol,1996;7(3):147-54.
12Brinckerhoff CE,Matrisian LM.Matrixmetalloproteinases:a tail of a frog that became a prince〔J〕.Nat Rev Mol Cell Biol,2002;3(3):207-14.
13Parsons SL,Watson SA,Brown PD,etal.Matrix metalloproteinases〔J〕.Br J Surg,1997;84(2):160-6.
14Zeng ZS,Cohen AM,Guillem JG.Loss of basement membrane typeⅣ collagen is associated with increased expression of metal-leprotemases 2 and 9(MMP-2 and MMP-9)during human colorectal tumorigenesis〔J〕.Carcingenesis,1999;20(5):745-9.
15Suzuki M,Lizasa T,Fujisawa T,etal.Expression of matrixmetalloproteinases and tissue inhibitor of matrixmetalloproteinases in non-small cell lung cancer〔J〕.Invasion Metastasis,1998;18(3):134-41.
〔2014-03-17修回〕
(编辑安冉冉/曹梦园)

