基于CdTe量子点荧光增强测定结晶紫
李 云,衷明华
(1.韩山师范学院生命科学与食品科技学院,广东潮州 521041;2.韩山师范学院化学与环境工程学院,广东潮州 521041)
基于CdTe量子点荧光增强测定结晶紫
李 云1,衷明华2
(1.韩山师范学院生命科学与食品科技学院,广东潮州 521041;2.韩山师范学院化学与环境工程学院,广东潮州 521041)
以巯基乙酸为稳定剂,用水热法合成CdTe量子点(QDs),基于结晶紫对CdTe QDs的荧光增强作用,建立测定结晶紫含量的新方法.在优化实验条件下,结晶紫浓度在2.5~12.5 ng/mL范围内与CdTe QDs的荧光增强程度呈良好的线性关系,相关系数r=0.9954,检出限为0.35 ng/mL.该方法用于水样中结晶紫含量的测定,加标回收率为95.0%~102.3%.
CdTe量子点;结晶紫;荧光增强
近年来,量子点(QDs)以吸收光谱宽、发射光谱窄、光稳定性好等优势引起研究者的关注[4,5].量子点表面轻微的变化会引起其光学性能急剧的变化,因此以量子点为荧光探针建立的荧光检测方法,已广泛应用于金属离子[6,7]、兽药[8,9]、农药[10]等领域的分析检测.本文选用巯基乙酸作为稳定剂,以水溶液合成法合成了CdTe QDs并以其为荧光探针测定CV.
1 实验部分
1.1 主要仪器与试剂
RF-5301PC型荧光分光光度计(日本岛津公司);TU-1900双光束紫外可见分光光度计(北京普析公司),PHS-3C型精密pH计(上海雷磁公司);HD200-1可视氮气吹扫仪(杭州汇尔公司);85-2型恒温磁力加热搅拌器(金坛国瑞实验仪器厂);“希波氏Xiboshi”C18固相萃取小柱(天津富集科技有限公司);HX-1050恒温循环器(北京博医公司);Human PowerⅡ纯水器(北京普析公司代理).
高纯碲粉(Te粉,天津市光复精细化工研究所);硼氢化钾(KBH4,天津市大茂化学试剂厂);巯基乙酸(TGA,国药集团化学试剂有限公司);氯化镉(CdCl2·2.5H2O,上海亭新化工厂);结晶紫(CV,阿拉丁试剂公司);所用试剂除特别说明外均为分析纯;实验所用水为二次去离子水;高纯N2.
1.2 CdTe QDs的制备
准确称取0.048 g Te粉和0.12 g KBH4于反应瓶中,加入2.00 mL水,搅拌,于65℃水浴继续搅拌至黑色Te粉完全消失,得到紫红色透明的KHTe水溶液.在N2的保护下,于250 mL浓度为25 mmol/L CdCl2水溶液中,加入0.1 mL TGA,用1 mol/L NaOH溶液调节pH至9左右,继续通N2除氧30 min,在搅拌下滴入KHTe前驱体溶液,使n(Cd2+):n(HTe-)=3:4,于90℃下继续加热搅拌回流15 min,得到CdTe QDs溶液并置于冰箱中4℃保存备用.CdTe QDs浓度以溶液中Cd2+浓度表观计算.
1.3 测定方法
取10 mL比色管,依次加入2 mL pH=5.0 Britton-Robinson缓冲液、2.5 mL 5.0×10-5mol/L CdTe QDs溶液、适量的CV溶液,然后用水稀释至刻度,摇匀.在50℃水浴中加热10 min后,在RF-5301PC型荧光分光光度计上,用1 cm荧光皿,激发狭缝1.5 nm,发射狭缝3 nm,于λex=350 nm,λem=352 nm波长处测定相对荧光强度△F(△F=F-Fo,F为加入CV溶液所测得的荧光值,Fo为空白溶液).
新鲜豇豆:购于重庆市永川区双竹农贸市场;泡菜水:实验室自制;泡菜乳酸菌:北京川秀科技有限公司;半乳糖醛酸、咔唑、对氨基苯磺酸、盐酸萘乙二胺、抗坏血酸、2,6-二氯酚靛酚钠盐等:均为分析纯。
2 结果与讨论
2.1 CdTe QDs的荧光发射和紫外-可见吸收光谱表征
对CdTe QDs溶液分别进行荧光发射和紫外可见吸收光谱检测,其荧光发射光谱(曲线a)及紫外可见吸收光谱(曲线b)如图1所示.从吸收光谱可见,在482 nm处有较明显的第一激子吸收峰,根据公式[11]:D= (9.8127×10-7) λ3-(1.7147×10-3)λ2+(1.0064)λ-194.84,可计算出CdTe QDs的粒径.其中,D为量子点的粒径,λ为量子点的最大吸收波长.计算得出CdTe QDs的粒径为1.75 nm;由荧光光谱可知,CdTe QDs在352 nm波长处有一平滑尖锐且对称的荧光发射峰,其半峰宽不足4 nm,说明该量子点具有优良的光谱性能.CdTe QDs溶液中加入结晶紫后,考察不同浓度结晶紫溶液对CdTe QDs荧光光谱的影响,如图1 a中1→6曲线所示(CV浓度从1至6分别为:0 ng/mL、2.5 ng/mL、5.0 ng/mL、7.5 ng/mL、10.0 ng/mL、12.5 ng/mL),加入结晶紫溶液后,CdTe QDs荧光发射峰位置无明显变化,但荧光强度显著增强.实验选择352 nm作为荧光检测波长.
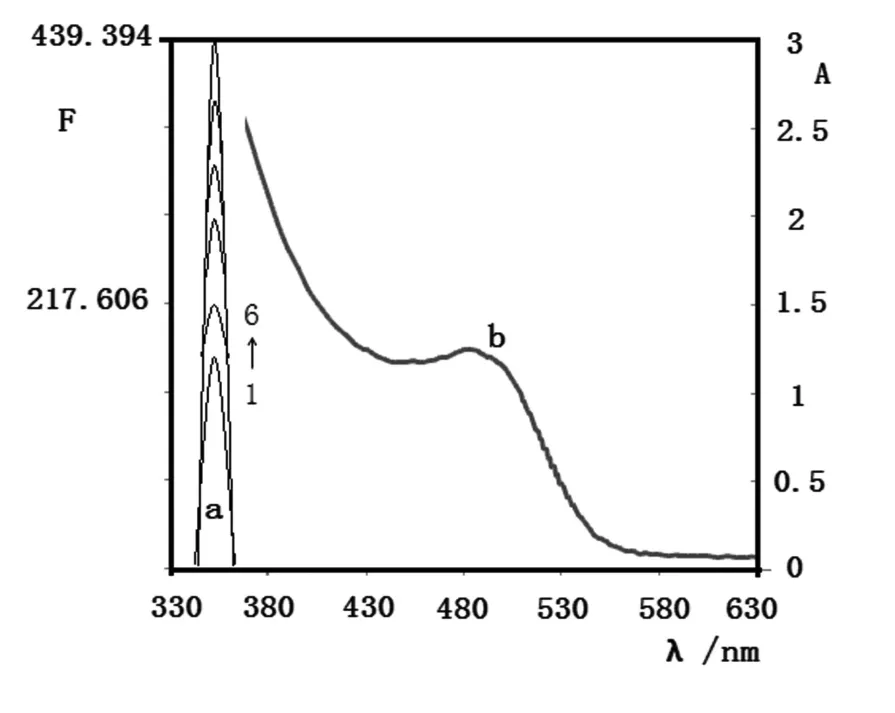
图1 CdTe QDs的紫外-可见吸收光谱(b)及不同CV浓度存在时CdTe QDs荧光发射光谱(a)的变化
2.2 实验条件的优化
2.2.1 酸度及缓冲介质的的影响
按实验方法,以Britton-Robinson缓冲溶液调节体系pH值,探讨了pH为2.0~6.0下的荧光强度,如图2所示[1:CdTe QDs2:CV-CdTe QDs3:△F=(2-1)],在pH=5.0时,体系的△F值最大;在pH=5.0时,考察了Britton-Robinson、Kolthoff、clark-lubs、HAc-NaAc及磷酸盐等缓冲介质对体系的影响,HAc-NaAc使荧光猝灭,Britton-Robinson、clark-lubs使荧光增强,其余缓冲介质对荧光影响不大.在荧光增强体系中,以Britton-Robinson缓冲溶液效果最优;故确定为2.0 mL pH=5.0 Britton-Robinson缓冲溶液来控制体系酸度.
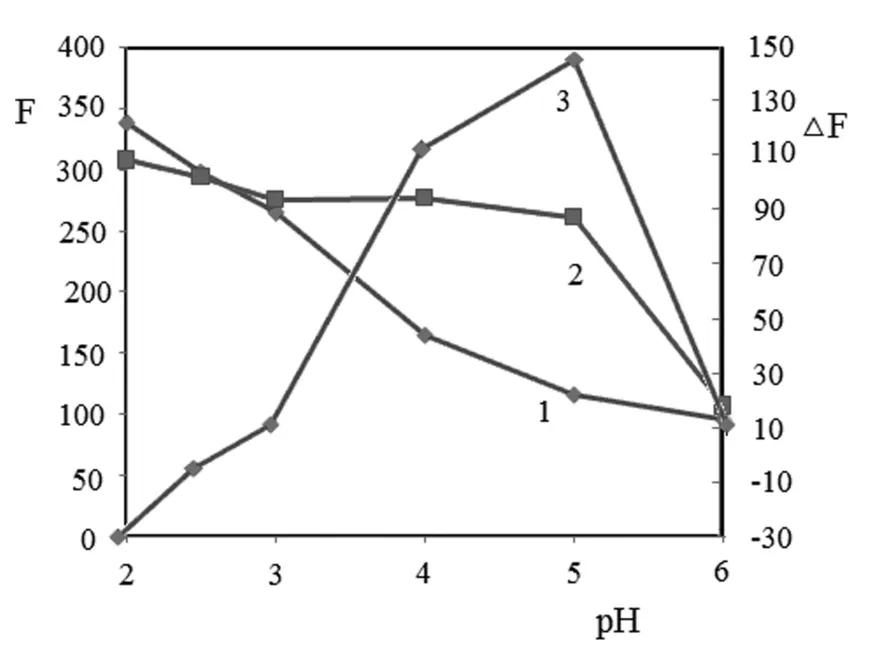
图2 不同pH值对体系的影响
2.2.2 CdTe QDs浓度的影响
CdTe QDs浓度太高或太低,在一定程度上会影响结晶紫测定的线性范围和灵敏度.考察CdTe QDs浓度对体系荧光增强强度的影响,如图3曲线1所示.由图3曲线1可知,CdTe QDs溶液中加入结晶紫后,随着CdTe QDs浓度的增大,体系△F逐渐增加,线性范围逐渐增大;但当CdTe QDs浓度大于12.5×10-6mol/L,△F反而逐渐降低,灵敏度逐渐降低;当CdTe QDs浓度为12.5×10-6mol/L时,△F达到最大.考虑到线性范围和灵敏度,实验选择CdTe QDs的最佳浓度为12.5×10-6mol/L.
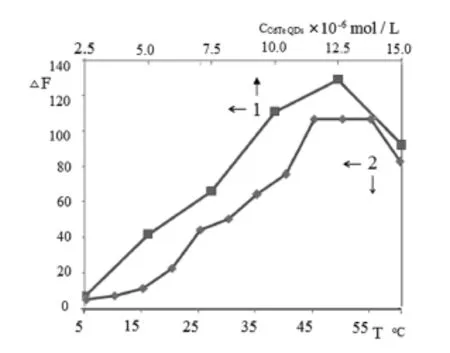
图3 CdTe QDs浓度对体系荧光强度增强影响
2.2.3 温度与时间的影响
实验考察了5~60℃的温度对体系△F的影响,如图3曲线2所示.由图3曲线2可知,温度过低反应速度慢,随着温度升高,粒子热运动加快,CdTe QDs与CV间作用力减弱,故选择水浴50.0℃下进行;水浴50.0℃下放置10 min体系△F达到稳定,且在120 min内保持不变.因此,实验选择水浴50.0℃下反应10 min后测定体系的荧光强度.
2.3 共存物质的影响
按照实验方法,CV浓度为10.0 ng/mL时,考察了常见离子对反应体系的干扰情况,结果见表1.

表1 共存物质的影响
2.4 方法的线性方程及检出限
在优化实验条件下,CV浓度在2.5~12.5 ng/mL范围内与体系荧光增强强度△F呈良好的线性关系,线性方程为:△F=13.06c(ng/mL)-11.81,相关系数r=0.995 4,检出限(以3σ计,n=11)为0.35 ng/mL.按上述方法重复11次测定2.5 ng/mL的CV溶液,相对标准偏差为0.42%,说明该方法具有较好的重现性和精密度.
2.5 实际水样测定
采集某养殖户水样立即用0.45 μm滤膜过滤,置4℃冰箱中备用;取100 mL并以5 mL/min流速通过预处理好的希波氏C18固相萃取小柱,小柱离心脱水后用3 mL甲醇洗脱;洗脱液用氮气吹扫仪吹至近干,转移至100 mL容量瓶中定容,按1.3测定方法测定水样中CV含量,同时进行加标回收试验,如表2所示.从表2可知,水样中未检出CV(低于检出限),加标回收率为95.0~102.3%,相对标准偏差(RSD)不高于4.87%,说明本方法可用于水样中CV含量的测定.
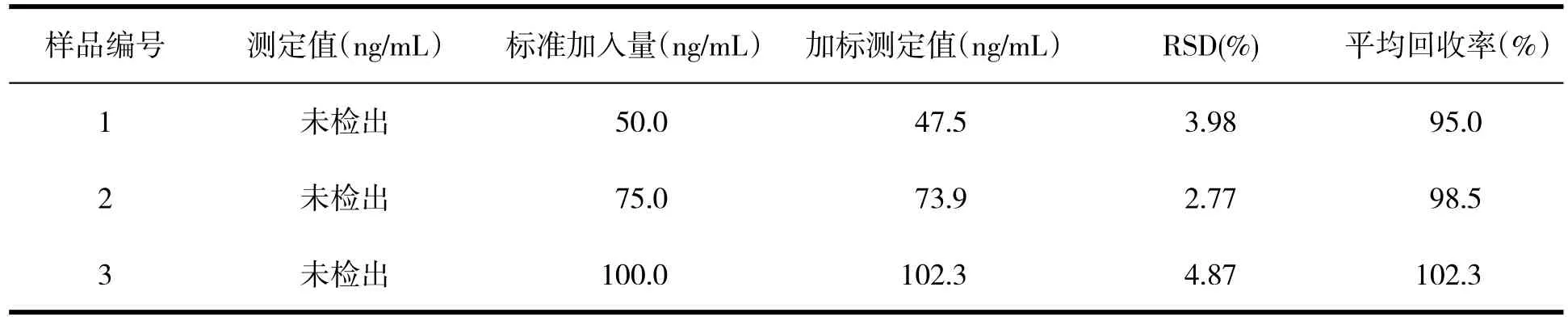
表2 水样中CV测定结果及回收试验(n=5)
[1]向仲朝,岳蕴瑶,张婷,等.水产品中孔雀石绿和结晶紫及其代谢产物的高效液相色谱测定法[J].中国卫生检验杂志,2014,24(6):788-790.
[2]朱慧敏,李贵荣,王永生,等.[PbI4]2--CV体系共振瑞利光散射法测定痕量结晶紫[J].应用化工,2012,41(6):1081-1084.
[3]陈兴会,吕昌银,严成艳,等.磷钼酸共振瑞利光散射法测定痕量结晶紫[J].中国卫生检验杂志,2008,18(6):1074-1076.
[4]阮康成.量子点荧光光谱学与生命科学[J].生命科学,2003,15(2):84-87.
[5]任国兰,柴宜民,卫洪青,等.量子点荧光探针的合成[J].山西师范大学学报(自然科学版),2003,17(1):60-62.
[6]李满秀,郝晓凤,王磊,等.碲化镉量子点荧光猝灭法测定镍[J].冶金分析,2015,35(6):49-52.
[7]孟元华,陶冠红.CdSe/CdS量子点荧光探针检测大米中的镉[J].中国卫生检验杂志,2014,24(2):180-182+193.
[8]魏宏,王云云,宋尔群.基于CdTe量子点测定烟酸诺氟沙星的新方法研究[J].化学学报,2011,69(17):2039-2046.
[9]彭金云,郑雅倩.硫代乙醇酸修饰CdS量子点荧光猝灭法测定呋喃西林[J].食品工业科技,2014,35(19):301-303+07.
[10]黄珊,马建强,肖琦,等.油溶性CdSe量子点荧光探针直接检测农药水胺硫磷[J].光谱学与光谱分析,2013,33(10):2853-2857.
[11]范萌,张林,刘巧玲,等.3-巯基丙酸修饰的CdTe量子点荧光探针用于碘酸根离子的检测[J].分析科学学报,2014,30(1):16-20.
Determination of Crystal Violet Based on Fluorescence Enhancing of CdTe Quantum Dots
LI Yun1,ZHONG Ming-hua2
(1.College of Life Sciences and Food Technology,Hanshan Normal University,Chaozhou,Guangdong,521041; 2.College of Chemistry and Environmental Engineering,Hanshan Normal University,Chaozhou,Guangdong,521041)
The water-soluble CdTe quantum dots(QDs)were synthesized using thioglycolic acid(TGA)as stabilizer agents.Based on the fluorescence enhancement of CdTe QDs caused by crystal violet(CV),a new method for the determination of CV was developed.Under the optimal conditions,the fluorescence enhancement intensity of CdTe QDs showed a good linearity over the concentration of CV in the range of 2.5-12.5 ng/mL.The correlation coefficient was 0.9954 and the limit of detection was 0.35 ng/mL.The proposed method was successfully applied in the determination of CV in water samples with spiked recoveries of 95.0%-102.3%.
CdTe quantum dots;Crystal Viole(tCV);fluoresence enhancement
O 657.3
A
1007-6883(2015)06-0040-04
责任编辑 朱本华
2015-11-09
李云(1977-),男,湖北宜昌人,韩山师范学院生命科学与食品科技学院讲师,博士.

