正丙醇/碳酸钠双水相体系提取发酵液中γ-聚谷氨酸的研究
张智维, 刘 婷, 韩 飞
(陕西科技大学 食品与生物工程学院, 陕西 西安 710021)
正丙醇/碳酸钠双水相体系提取发酵液中γ-聚谷氨酸的研究
张智维, 刘婷, 韩飞
(陕西科技大学 食品与生物工程学院, 陕西 西安710021)
摘要:为弥补传统提取方式成本高、连续性差等缺点,采用正丙醇/碳酸钠双水相体系,从发酵液中分离提取了γ-PGA,且γ-PGA富集在盐相.采用正交试验研究了正丙醇浓度、碳酸钠浓度、温度、pH等对γ-PGA提取率的影响.结果表明,选用正丙醇/碳酸钠双水相体系的最佳提取条件为:正丙醇浓度18%(质量分数)、碳酸钠浓度14%(质量分数)、温度40 ℃、pH 10.在此条件下,γ-PGA的提取率为98.07%,说明该方法可行.
关键词:双水相体系; 提取; γ-聚谷氨酸; 正交试验
0引言
γ-聚谷氨酸(γ-PGA)是由D型和L型谷氨酸单体通过α-氨基和γ-羧基组成的同源聚酰胺[1].γ-PGA具有水溶性、生物相容性、生物可降解性、可食用性、无毒等特点,故在工业应用中显示出了很大潜力[2].例如,在食品工业中可作为增稠剂和稳定剂,在废水处理中可作为生物絮凝剂,在医药中可作为药物载体和控释材料,在农业中可作为肥料,在化妆品中可作为保湿剂[3]等.
微生物发酵法是生产γ-PGA优先选择的方法[4,5].目前,提取γ-PGA的方法主要有:有机溶剂沉淀法、化学沉淀法和膜分离法[6,7]等.有机溶剂沉淀法是最常用的方法,但有机溶剂的用量太大,提取成本较高,限制了其在工业生产中的应用[8,9];化学沉淀法的后续脱盐步骤比较复杂[10];膜分离法容易堵塞、连续化程度低[11].
双水相萃取具有处理量大、萃取效率高、易于连续操作、易于工艺放大[12]等特点,可弥补传统γ-PGA提取方式的缺点.目前,双水相萃取技术已经广泛应用于提取蛋白质[13]、氨基酸[14]、酶[15]、抗生素[16]等领域.
本文采用正丙醇/碳酸钠双水相体系提取发酵液中的γ-PGA,主要是利用γ-PGA在两相中的选择性分配,实现与发酵液中其它杂质分离的目的.应用了正交试验优化双水相体系提取γ-PGA的系统组成以及操作条件,从而确定了提取的最佳工艺.
1材料与方法
1.1材料与试剂
无水乙醇、异丙醇、磷酸氢二钾、无水碳酸钠、无水硫酸钠(分析纯,天津市天利化学试剂有限公司);正丙醇(分析纯,天津市科密欧化学试剂有限公司);γ-聚谷氨酸发酵液(实验室发酵制得,发酵液中γ-PGA的含量为10.17 g/L).
1.2仪器与设备
紫外可见光分光光度计(上海美普达仪器有限公司);电子天平(福州华志科学仪器有限公司);pH计(上海仪电科学仪器股份有限公司);电热恒温水浴锅(天津市泰斯特仪器有限公司);快速混匀器(上海浦东物理光学仪器厂).
1.3实验方法
1.3.1绘制相图
配制浓度为20%(w/w)的有机溶剂溶液和12%(w/w)的无机盐溶液.向25 mL刻度试管中加入一定量的有机溶剂溶液,再逐滴加入盐溶液,直至溶液浑浊;然后逐滴加入水,直至溶液澄清,计算此时系统中有机溶剂和无机盐的浓度;再加入盐溶液使溶液浑浊,如此反复操作,直至溶液不出现浑浊或澄清.以盐浓度为横坐标、有机溶剂浓度为纵坐标,绘制双水相相图.
图1为不同有机溶剂/盐双水相体系的相图.
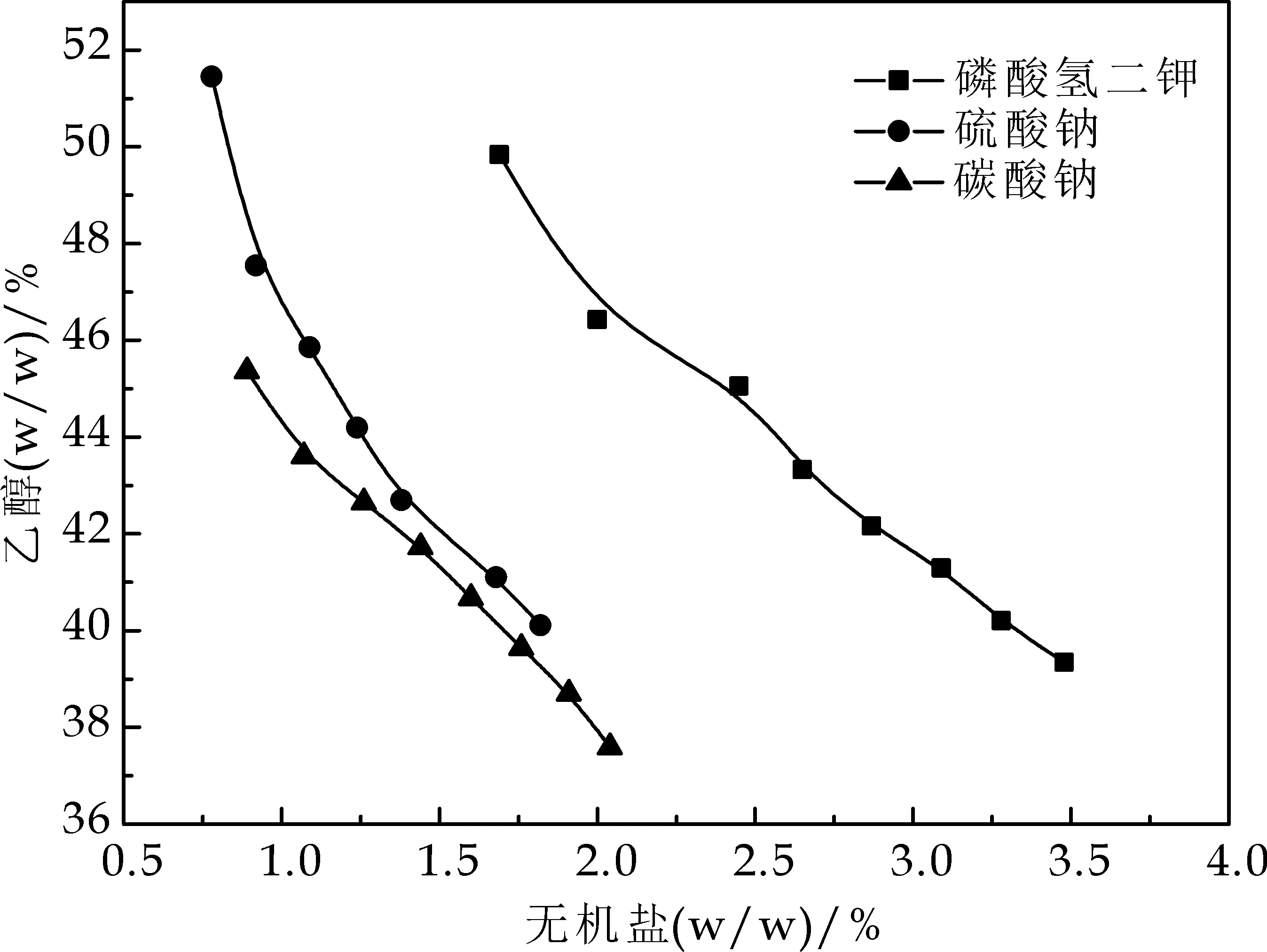
(a)乙醇/磷酸氢二钾(硫酸钠、碳酸钠)双水相系统相图

(b)正丙醇/磷酸氢二钾(硫酸钠、碳酸钠)双水相系统相图
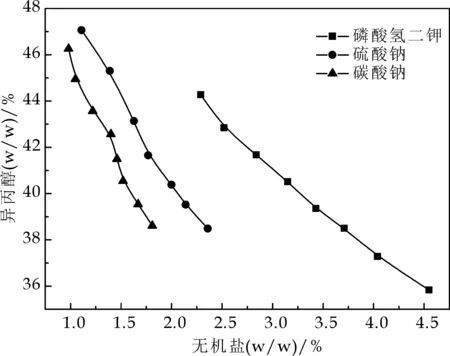
(c)异丙醇/磷酸氢二钾(硫酸钠、碳酸钠)双水相系统相图图1 不同有机溶剂/盐双水相系统相图
1.3.2双水相体系制备
根据相图,确定用于提取γ-PGA的双水相体系中两相的大致范围.在25 mL刻度试管中,按照计算量依次加入有机溶剂溶液、无机盐溶液、发酵液等,用蒸馏水补足至20 g,振荡混合,静置分相.
1.3.3单因素实验
采用正丙醇/碳酸钠双水相体系提取γ-PGA的目的是弥补传统提取方式的缺点.实验中以提取率作为考察指标(同时适当考虑分配系数),考察了各因素对γ-PGA提取效果的影响,应选择适宜的操作条件.
(1)不同双水相体系对γ-PGA提取率的影响
选择20%无水乙醇、正丙醇、异丙醇等和12%磷酸氢二钾、硫酸钠、碳酸钠等进行两两组合,组成9组双水相体系.静置分相后,测定上下相中γ-PGA的浓度,并计算提取率.
(2)正丙醇浓度对γ-PGA分配行为的影响
在碳酸钠浓度为12%(质量分数)、温度25 ℃、pH 9.5、分相时间2.5 h时,正丙醇的浓度依次为15%、18%、21%、24%、27%、30%、33%等,在此条件下进行实验,测定上下相中γ-PGA的浓度,计算提取率和分配系数,并选取适宜的正丙醇浓度.
(3)碳酸钠浓度对γ-PGA分配行为的影响
在正丙醇浓度为18%(质量分数)、温度25 ℃、pH 9.5、分相时间2.5 h时,碳酸钠的浓度依次为9%、10%、11%、12%、13%、14%、15%、16%、17%等,在此条件下进行实验,测定上下相中γ-PGA的浓度,计算提取率和分配系数,并选取适宜的碳酸钠浓度.
(4)温度对γ-PGA分配行为的影响
在正丙醇浓度为18%(质量分数)、碳酸钠浓度为14%、pH 9.5、分相时间2.5 h时,温度依次为30 ℃、35 ℃、40 ℃、45 ℃、50 ℃、55 ℃、60 ℃等,在此条件下进行实验,测定上下相中γ-PGA的浓度,计算提取率和分配系数,并选取适宜的温度.
(5)pH对γ-PGA分配行为的影响
在正丙醇浓度为18%(质量分数)、碳酸钠浓度为14%、温度40 ℃、分相时间2.5 h时,pH依次为9.5、10、10.5、11、11.5、12、12.5等,在此条件下进行实验,测定上下相中γ-PGA的浓度,计算提取率和分配系数,并选取适宜的pH值.
1.3.4正交试验
单因素实验选取实验因素和水平,再做正交试验以确定最佳组合,最终确定最佳系统组成和操作条件.
1.3.5分析方法
γ-聚谷氨酸的测定:CTAB浊度法[17].
1.3.6计算
(1)相比:R=Vt/Vb,其中Vt为上相体积(mL);Vb为下相体积(mL).
(2)分配系数:K=Ct/Cb,其中Ct为上相中γ-PGA的浓度(g/L);Cb为下相中γ-PGA的浓度(g/L).
(3)提取率:Y= 1 / (1+RK),其中K为分配系数.
2结果与讨论
2.1γ-PGA的标准曲线和回归方程
在235 nm处分别测定8μg/mL、16μg/mL、24μg/mL、32μg/mL、40μg/mL、48μg/mLγ-PGA标准液的吸光度,得到回归方程为Y= 0.017 75X+0.047 93,R2=0.997 49.
2.2不同双水相体系对γ-PGA提取率的影响
不同双水相体系对γ-PGA的提取率如图2所示.从图2可以看出,乙醇/碳酸钠体系不分相,乙醇/硫酸钠和乙醇/磷酸氢二钾体系的提取率相差不大,异丙醇和三种盐组成的体系提取率相差也不大,正丙醇/磷酸氢二钾体系的提取率最低,正丙醇/碳酸钠体系的提取率最高,达到96.3%.因此,选择正丙醇/碳酸钠体系进行下面的实验.

1.乙醇-碳酸钠;2.乙醇-硫酸钠;3.正丙醇-碳酸钠;4.正丙醇-硫酸钠;5.正丙醇-磷酸氢二钾;6.异丙醇-碳酸钠;7.异丙醇-硫酸钠;8.异丙醇-磷酸氢二钾图2 不同双水相系统对γ-PGA提取率的影响
2.3正丙醇浓度对γ-PGA分配行为的影响
正丙醇浓度对γ-PGA分配行为的影响如图3所示.由图3可知,总体上看提取率Y和分配系数K都随着正丙醇浓度的增加呈现减小的趋势,在正丙醇浓度为18%时体系的提取率达到最大.有机溶剂/盐双水相体系的分相过程是有机溶剂和无机盐争夺水分子的过程,随着正丙醇浓度的增加,上相中水的含量下降,γ-PGA更易分配于下相,因此分配系数K减小,但是由于相比一直增加,所以提取率Y呈现下降趋势.因此,确定正丙醇浓度为18%.
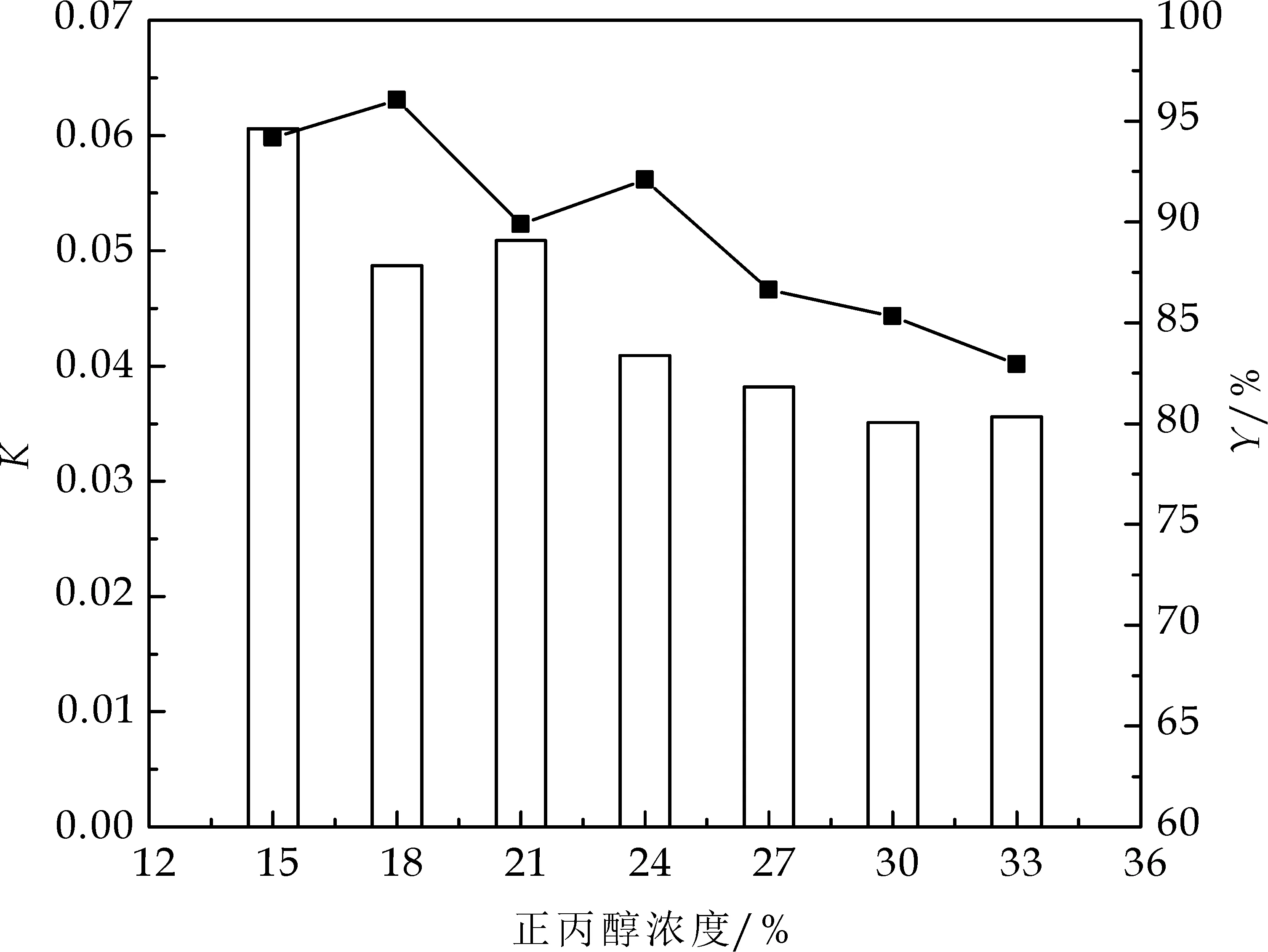
柱形图:分配系数K;折线图:提取率Y图3 正丙醇浓度对γ-PGA分配行为的影响
2.4碳酸钠浓度对γ-PGA分配行为的影响
碳酸钠浓度对γ-PGA分配行为的影响如图4所示.由图4可知,提取率随碳酸钠浓度变化的总体趋势是先增大后减小,在碳酸钠浓度为14%时,提取率最大.其原因是随着碳酸钠浓度的增加,水合能力增强,下相的含水量增大,γ-PGA更易分配于下相,分配系数减小,提取率增大.因此,可确定碳酸钠的浓度为14%.

柱形图:分配系数K;折线图:提取率Y图4 碳酸钠浓度对γ-PGA分配行为的影响
2.5温度对γ-PGA分配行为的影响
温度对γ-PGA分配行为的影响如图5所示.由图5可以看出,当温度大于40 ℃后,分配系数增加,提取率减小;在40 ℃时分配系数最小,提取率最大.这是因为温度增加使体系的黏度降低有利于分相,进而影响γ-PGA的分配.而且,温度还影响γ-PGA的溶解度,随着温度的升高,γ-PGA的溶解度增大,当温度大于40 ℃时,下相中γ-PGA已经达到饱和,浓度基本保持不变,所以提取率和分配系数变化的幅度较小.因此,选择温度为40 ℃.
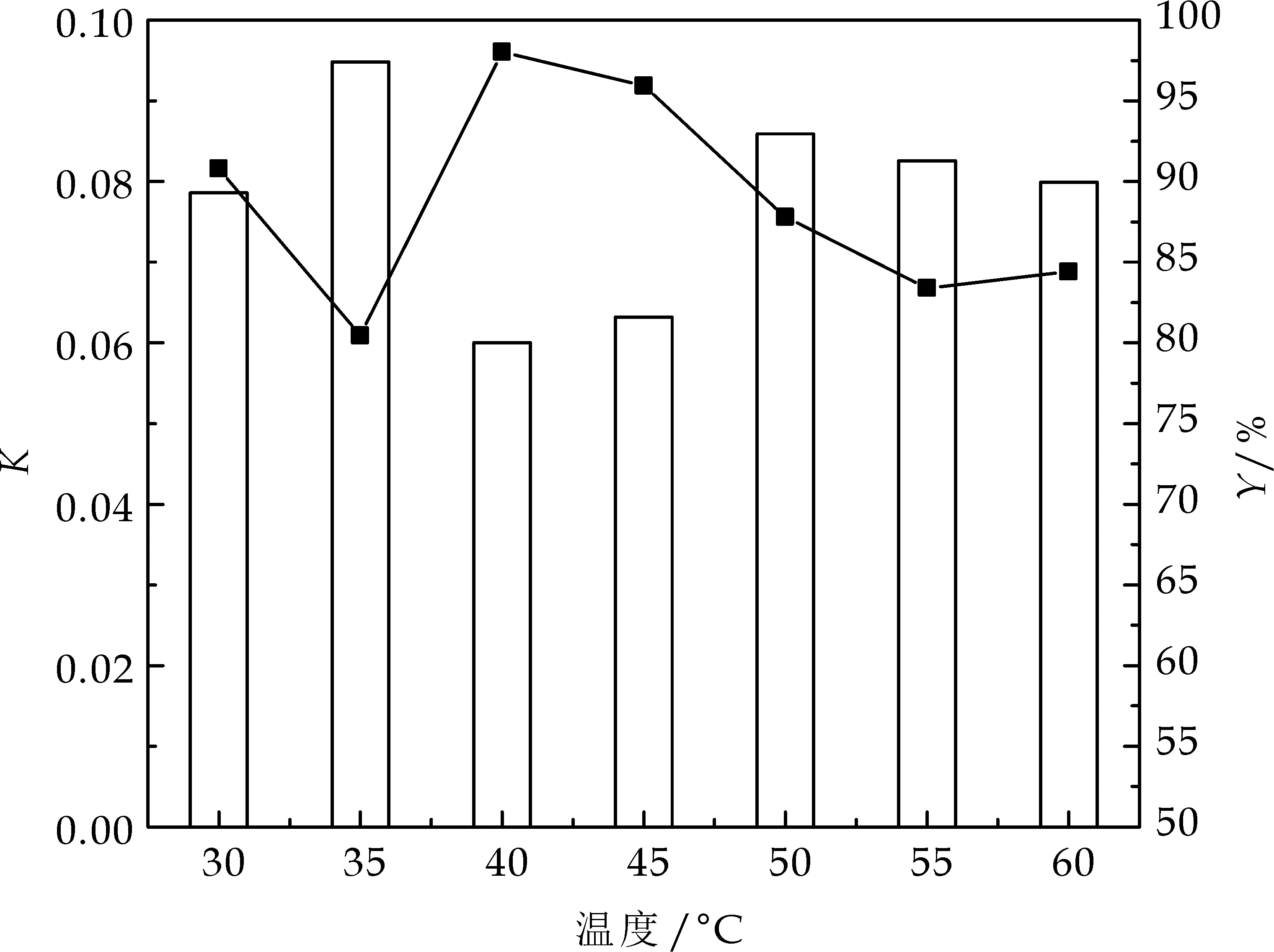
柱形图:分配系数K;折线图:提取率Y图5 温度对γ-PGA分配行为的影响
2.6pH对γ-PGA分配行为的影响
pH对γ-PGA分配行为的影响如图8所示.由图8可知,当pH>10时,体系的提取率显著降低.这是因为γ-PGA是由带负电荷的谷氨酸单体组成,溶液pH的改变将影响羧基的解离平衡,以及其与双水相体系的静电效应,从而影响γ-PGA的分配结果.在碱性环境下,γ-PGA带负电,且pH越高,γ-PGA解离为负二价状态存在的比例越高,从而使之更难分配到电位为负的下相,所以分配系数增加,萃取率减小;当pH减小时,负二价状态存在的比例减少,体系的相间电位差减小,提取率增大.因此,选择pH值为10.

柱形图:分配系数K;折线图:提取率Y图6 pH对γ-PGA分配行为的影响
2.7正交试验
根据以上单因素实验,确定正丙醇浓度、碳酸钠浓度、温度和pH四个因素,并分别选取相应的水平值进行正交试验,且以提取率作为主要的研究对象.正交试验的因素水平表如表1所示.
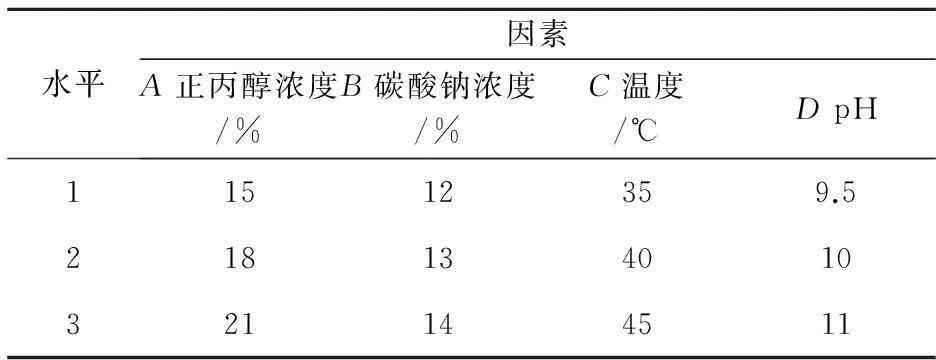
表1 因素水平表
表2为正交试验结果极差分析表.其实验结果表明,pH的极差最大,对γ-PGA提取率的影响最大,温度对γ-PGA提取率的影响显著性高于碳酸钠的影响,正丙醇浓度的影响最小.故各因素对试验指标影响的主次顺序依次为DCBA.因为正丙醇的极差最小,故以正丙醇浓度为误差,做方差分析,其结果如表3所示.
表3为正交试验方差分析表.由表3可知,在给定的置信度α= 0.05时,Fα(2,2)=19.只有pH的F比大于F临界值,表明只有pH对提取率有显著影响.影响γ-PGA提取率的正交试验各因素的最优组合为A2B3C2D2.

表2 正交试验结果极差分析表

表3 正交试验方差分析表
通过对试验数据进行直观分析可知,影响γ-PGA提取率的正交试验各因素水平的最佳组合为A2B3C2D2,即正丙醇浓度18%、碳酸钠浓度14%、温度40 ℃、pH10.表4为验证性试验结果.由表4可知,在最佳提取条件下,γ-PGA的提取率为98.07%,高于正交试验中所得的最优结果97.95%(见表2所示).因此,确定双水相体系的组成为:正丙醇浓度18%、碳酸钠浓度14%、温度40 ℃、pH10.

表4 验证性试验
3结论
本文实现了直接从发酵液中提取γ-PGA,菌体富集在上相,γ-PGA聚集在下相.通过正交试验得到了最佳提取条件为:双水相系统组成为正丙醇浓度18%(质量分数)、碳酸钠14%(质量分数)、温度40 ℃、pH10,其γ-PGA的提取率达98.07%.这一结果比正交试验中的最大值提高了1.22%,为γ-PGA的分离纯化提供了一种新方法.
参考文献
[1]BaiqiHuang,PeiyongQin,ZhiweiXu,etal.EffectofCaCl2on viscosity of culture broth,and on activities of enzymes around the 2-oxoglutarate branch,in Bacillus subtilisCGMCC2108producing[J].BioresourceTechnology,2011,102(3):3 595-3 598.
[2]FanZhu,JinCai,XiangtingWu,etal.Themainbyproductsandmetabolicfluxprofilingofγ-PGA-producingstrainB.subtilisZJU-7underdifferentpHvalues[J].JournalofBiotechnology,2013,164(1):67-74.
[3]HuiliZhang,JianzhongZhu,XiangchengZhu,etal.High-levelexogenousglutamicacid-independentproductionofpoly-(γ-glutamicacid)withorganicadditioninanewisolatedBacillus subtilisC10[J].BioresourceTechnology,2012,116:241-246.
[4]曹名锋,金映虹,解慧.γ-聚谷氨酸的微生物合成、相关基因及应用展望[J].微生物学通报, 2011,38(3):388-395.
[5]刘青芝.微生物发酵法生产γ-聚谷氨酸的研究[D].济南:山东大学,2010.
[6]王雷.双水相系统提取γ-聚谷氨酸的研究[D].天津:天津商业大学,2009.
[7]鞠蕾,马霞.γ-聚谷氨酸的提取方法改进[J].现代化工,2011,31(s1):267-270.
[8]曾庆东,李文杰,王志伟,等.甲醇-乙醇分步沉淀法提取γ-聚谷氨酸[J].食品与发酵工业,2014,40(5):222-228.
[9]李文婧.γ-聚谷氨酸发酵及提取工艺研究[D].济南:山东轻工业学院,2010.
[10]石冬霞.γ-聚谷氨酸的微生物合成、分离纯化及性质与应用研究[D].哈尔滨:哈尔滨商业大学,2010.
[11]赵兰坤,徐恒山,楼良旺.发酵产γ-聚谷氨酸的提取工艺研究现状[J].发酵科技通讯,2014,43(2):27-28.
[12]郭晶晶.双水相萃取技术进展[J].广州化工,2014,42(19):26-28.
[13]刘杨,王雪青,庞广昌,等.双水相萃取法富集分离螺旋藻藻蓝蛋白的研究[J].海洋科学,2008,32(7):30-37.
[14]李青云,袁凤梅,吴金英.聚乙二醇/硫酸钠双水相萃取懒氨酸[J].食品与发酵工业,2014,40(4):221-226.
[15]黎志德,蚁细苗,黄思鸿,等.聚乙二醇-硫酸铵双水相体系萃取α-葡聚糖酶[J].甘蔗糖业,2013(1):38-42.
[16]柴丽.二元小分子醇/盐双水相体系中抗生素的分离富集行为[D].西安:长安大学,2013.
[17]张庆庆,金鑫强,陈剑翔,等.发酵液中γ-聚谷氨酸含量快速测定方法研究[J].食品工业科技,2012(19):294-296.
Study on n-propanol/sodium carbonate aqueous two-phase
system to extract polyγ-glutamic acid from fermentation broth
ZHANG Zhi-wei, LIU Ting, HAN Fei
(College of Food and Biological Engineering, Shaanxi University of Science & Technology, Xi′an 710021, China)
Abstract:The work attempted to study and optimize the aqueous two-phase systems (n-propanol/sodium carbonate) to extract γ-PGA from fermentation broth,in which γ-PGA was enriched in salt phase,the effect of several parameters such as concentration of phase forming components (n-propanol and sodium carbonate),temperature and pH on the extraction rate and partition coefficient of γ-PGA were studied.Orthogonal experiment design was applied to determine the optimum technical conditions for extraction.The results showed that the optimum extraction condition of n-propanol/sodium carbonate aqueous two-phase system were 18%(w/w) n-propanol and 14%(w/w) sodium carbonate at 40 ℃ and pH=10.Under the optimal condition,the extraction rate was 98.07%.In conclusion, the method has good reliability.
Key words:aqueous two-phase system; extraction; poly γ-glutamic acid; orthogonal experiment design
中图分类号:TQ922+.1
文献标志码:A
文章编号:1000-5811(2015)05-0130-05
作者简介:张智维(1967-),女,陕西西安人,高级工程师,研究方向:食品微生物发酵
基金项目:陕西省科技厅自然科学基金项目(2009JM2005); 陕西省教育厅专项科研计划项目(09KJ373)
收稿日期:*2015-05-19

