淀粉制品中铝含量的测定
◎马艳秋,杨正慧,韩凤霞,夏春秋,张 琪
(吉林市产品质量检验院,吉林 吉林 132013)
面制品、膨化食品中铝的测定较为常见,检测方法一般参照国家标准[1],但实际操作时,发现效果并不理想。检测人员对此方法进行了诸多尝试:姚辉等人在GB/T 5009.182-2003方法的基础上,参考了卫生部水质中铝的测定方法,发现用乙二胺-盐酸缓冲液比乙酸-乙酸钠缓冲液效果更好,pH值控制在6.7~7.0,最佳波长选择630 nm[2];韦凤栖等人提出干法灰化较湿法消解的效果更佳[3];钱滢文等人对面制食品中铝的测定方法的改进,除采用干法消化外,缓冲液也变为pH6.7~7.0的乙二胺-盐酸缓冲体系,波长选择650 nm,并对干法、湿法处理的样品测定结果进行比较,认为硝酸-高氯酸湿法消解重现性相对较差,结果偏高[4];陈峰对湿法消解步骤进行了调整,与国标法有所不同,并将乙酸-乙酸钠缓冲溶液pH值确定为6.5[5];黄龙等人采用先碳化、再用550℃灰化的方法处理食品,也获得了干法灰化比湿法消解更具优势的结论[6];此外,王永平等提出了在显色反应体系中加入OP-10乳化剂,使显色灵敏、体系更稳定[7]。
拉皮,也称粉皮,属淀粉制品,具有价格便宜、美味可口的优点,是普通百姓餐桌上常见的时令小菜,在GB 2760《食品添加剂使用标准》中,淀粉制品并未被允许使用含铝添加剂。2014年国家卫生计生委等5部门联合发布了《关于调整含铝食品添加剂使用规定的公告》,限制并禁止含铝食品添加剂的使用,但从近年来曝光的新闻事件中不难看出,不仅目前市售面制食品、膨化食品中铝含量仍旧居高不下,甚至在粉皮这类禁止添加含铝添加剂的食品中,也依然“铝”见不鲜。
谷小伟等人用湿法消解、分光光度法测定了紫菜中的铝[8],而淀粉制品中铝的检测少见报道。本文力求建立一个针对淀粉制品的样品前处理、紫外分光光度检测方法,以应用于淀粉制品中铝含量的检测工作。
1 材料与方法
1.1 仪器
TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限公司),电子分析天平(沈阳龙腾电子有限公司),箱式电子炉(RJX-4-9 天津市华北实验电炉厂),pHS-3C数字式酸度计(上海瑞达仪器厂),电子万用炉1000W(北京市永光明医疗仪器有限公司)。
1.2 试剂
铝标准储备液(1mg/mL):精密称取1.0000g金属铝(纯度99.99%),加50mL 6mol/L盐酸溶液,加热溶解,冷却后,移入1000 mL容量瓶中,用水稀释至刻度。该溶液每毫升相当于1 mg铝。
铝标准使用液:吸取1.00 mL铝标准储备液,置于100 mL容量瓶中,用水稀释至刻度,再从中吸取5.00 mL于50 mL容量瓶中,稀释至刻度。该溶液每毫升相当于1 μg铝(使用液现用现配)。
硫酸试剂:10%及1%(体积分数)硫酸。
乙酸-乙酸钠溶液:称取34 g乙酸钠(NaAc.3H2O)溶于450 mL水中,加2.6 mL冰乙酸,调pH至5.5,用水稀释至500 mL。
0.5 g/ mL铬天青S溶液:称取50 mg铬天青S,用水溶解并稀释至100 mL。(现用现配)。
0.2 g/ L十六烷基三甲基溴化铵溶液:称取20 mg十六烷基三甲基溴化铵,用水溶解并稀释至100 mL。(现用现配)。
10 g/L抗坏血酸溶液:称取1.0 g抗坏血酸用水溶解并稀释至100 mL(现用现配)。
1.3 试验方法
1.3.1 样品的处理
称取粉皮1.500~2.000 g于瓷坩埚中,在电子万用炉小火碳化至无烟,冷却后移入箱式电子炉中,在550℃下灰化4h。如果灰化不完全,取出冷却后,加入几滴硝酸浸湿残渣,置于电子万用炉上小火蒸干,再移入箱式电子炉中灰化1~2 h,冷却后加入10 mL 10%硫酸溶液溶解灰分,将试样消化液过滤移入100 mL容量瓶中,用少量水多次洗涤坩埚,洗液合并于容量瓶中定容至刻度,摇匀备用同时作试剂空白(注意试样与空白所用坩埚新旧程度保持一致)。
1.3.2 标准曲线绘制
绘制标准曲线采用七点法:取1μg/ mL铝标准使用液0、0.2 mL、0.4 mL、 0.6 mL、0.8mL、1.0 mL、2.0 mL(相当于含铝0、0.2μg、0.4μg、0.6μg、0.8μg、1.0μg、2.0μg)于25mL比色管中,再分别加入1mL 1%硫酸溶液,依次加入8mL乙酸-乙酸钠溶液,1.0mL 10 g/L抗坏血酸溶液,混匀,加2.0mL0.2g/ L十六烷基三甲基溴化铵溶液,混匀,再加2.0 mL0.5g/ mL铬天青S溶液,摇匀后,用水稀释至刻度。室温放置20 min后,用1 ㎝比色皿,于分光光度计上,以0管调零点,于640nm波长处测定吸光度,绘制标准曲线。
1.3.3 样品测定
吸取1.0 mL试样消解液及试剂空白试液,置于25mL比色管中,以下依照1.3.2进行,根据标准曲线比较定量。按以下公式计算结果:

X—试样中铝的含量,单位为毫克每千克(mg/kg)。
C1——测定用试样中铝的质量,单位为微克(μg)。
C2——试剂空白液中铝的质量,单位为微克(μg)。
m——试样质量,单位为克(g)。
W——样品含水百分数。
V1——试样消化液总体积,单位为毫升(mL)。
V2——测定用试样消化液体积,单位为毫升(mL)。
2 结果和讨论
2.1 样品前处理优化
本次实验对比了湿样及烘干样品干法灰化处理的效果,发现直接对2 g左右的粉皮样品进行碳化、灰化,比烘干后称取2 g样品效果更佳。分析原因,粉皮样品水分较大,约80%左右,烘干后的2 g样品实际上已经相当于10 g左右湿样;此外,有可能在烘干过程中样品表面发生干结现象影响内部水分散失,因此碳化、灰化不易彻底。在预实验中发现,该粉皮样品铝含量较高,因此,称取2 g湿样完全可以满足检出限要求。同时,应保证测量样品及空白试剂所用坩埚新旧程度一致,以消除系统误差。
2.2 试剂配制
为保证显色体系稳定,实验用铬天青S溶液、十六烷基三甲基溴化铵溶液、抗坏血酸溶液采用“现用现配”的方式,避免由于某种试剂配制时间过长后,使显色反应受到影响,导致标准工作曲线精密度变差。
2.3 线性范围
标准曲线线性范围为0~2.0μg,曲线方程为Y=0.11958X-0.00167,相关系数为0.99928,结果表明,在0~2.0μg范围内,线性关系良好,见图1。
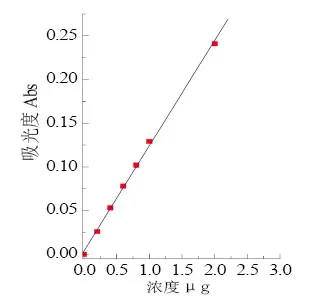
图1 标准工作曲线
2.4 pH及吸收波长
本次实验对比了pH5.5及pH6.0的乙酸-乙酸钠缓冲液,结果pH5.5的显色体系更稳定,线性更佳。吸取铝标准溶液2.0 mL,置于25mL比色管中,依照1.3.3步骤依次加入试剂,用1cm比色皿于紫外分光光度计500~700 nm范围内扫描光谱,发现640 nm处吸光度值最大,见图2。
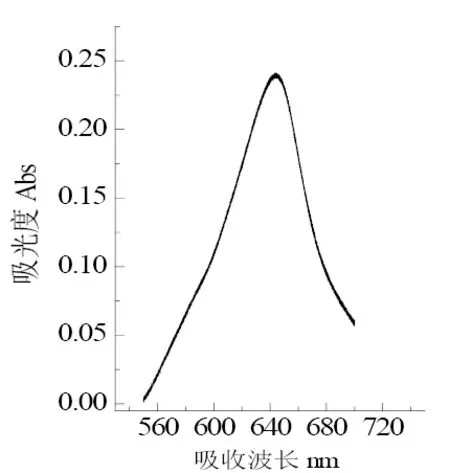
图2 最大吸收波长
2.5 样品分析
用干法灰化法测量某市售淀粉制品(粉皮)中铝含量,检测结果重现性良好,见表1。
3 结论
样品经干法消化后,在乙酸-乙酸钠缓冲溶液中,三价铝离子在十六烷基三甲基溴化铵阳离子表面活性存在下,与铬天青S形成三元体系配合物,利用紫外分光光度计测定淀粉制品中铝的含量。该法具有操作简单、抗干扰、重现性好等优点,相对标准偏差不超过6%,能满足淀粉制品中铝含量的检测要求,是一种可行的分析方法。

表1 某市售粉皮铝含量检测结果

[1]中华人民共和国卫生部.GB/T5009.182-2003面制食品中铝的测定[S].中国标准出版社出版,2004.
[2]姚辉,韩墨,姜春才,等.面制食品中铝测定方法的几点探讨[J].中国卫生检验杂志,2014(11).
[3]韦凤栖,谭壮志.面制食品中铝检测方法的改进[J].中国卫生检验杂志,2012(1).
[4]钱滢文,洪霞.面制食品中铝测定方法的改进[J].中国卫生检验杂志,2010(10).
[5]陈峰.铬天青S分光光度法测定膨化食品中的铝[J].中国卫生检验杂志,2006(8).
[6]黄龙,刘健,罗爱玲.干法灰化法测定食品中的铝含量[J].现代农业科技,2014(8).
[7]王永平,赖强,刘健康,等.面制品中铝测定方法的改进[J].中国卫生检验杂志,2011(10).
[8]谷小伟,张四银.分光光度计法测定紫菜中铝的含量[J].现代农业科技,2013(23).

