来曲唑和克罗米芬分别联合HMG 治疗多囊卵巢综合征疗效的系统评价
王沛丽,王芳,丁楠
(1.甘肃省监狱管理局兰州医院,兰州 730030;2.兰州大学第二医院生殖医学中心,兰州 730030)
多囊卵巢综合征(PCOS)是育龄期妇女常见的一种以排卵障碍为主要表现的生殖内分泌疾病,其发病率大约占育龄期妇女的5%~10%[1],占不孕人群的30%~40%,占不排卵性不孕的75%左右,其典型临床表现以高雄激素血症、月经失调、肥胖伴高胰岛素血症为主。促排卵是治疗PCOS不孕的关键,目前在临床工作及研究中虽已积累了较多行之有效的促排卵方案,但妇产科医生仍在努力追求一种理想的方案。现国内外对PCOS患者诱发排卵首选的一线药物仍为克罗米芬(CC),虽然它使用方便,排卵率高(73%~87%),但由于它有半衰期长、消耗雌激素受体、妊娠率低(10%~20%)等缺点[2],在临床上的使用受到一定程度的限制。除此之外,临床上对于CC治疗失败的患者可给予二线促排卵药物人绝经期促性腺激素(HMG),但它易出现多胎妊娠和卵巢过度刺激综合征(OHSS)的危险。自2001年Mohamed等[3]首次使用来曲唑(LE)促排卵并在临床上取得了良好疗效以来,国内外对其进行了大量的临床及基础研究,有研究认为来曲唑促排卵率高,并发症少,有望取代克罗米芬成为一线促排卵药物[4-5]。
早在1996 年Lu 等[6]就开始尝试着联合应用CC+HMG 用于诱导排卵,并将联合用药推广于临床,认为其是一种方便、有效、廉价的促排卵方式。随着人类辅助生殖技术的不断发展,诱导排卵的多样化越来越被人们所发现并了解。在对宫腔内人工授精的不孕患者行促排卵治疗的随机对照研究中[7-8]LE+HMG 有着与CC+HMG 相似的妊娠率,并且是一种安全、有效的促排卵方式。在临床诊疗多囊卵巢综合征不排卵引起的不孕患者中,我们也尝试着应用联合用药的促排卵方案,取得了较好的临床效果。本文通过系统评价此二种不同的联合用药促排卵方式,以了解PCOS患者有效的促排卵方法,为临床用药提供相对可靠的证据。
资料与方法
一、纳入与排除标准
1.研究设计:针对PCOS 不孕患者行LE+HMG 或CC+HMG 联合促排卵的随机对照研究(RCT)。
2.研究对象:(1)确诊的PCOS患者,其诊断标准严格按照鹿特丹修正的2003 年标准执行[9],即满足以下3项标准中的两项:①稀发排卵或无排卵;②高雄激素血症和(或)高雄激素的临床表现;③卵巢多囊样改变:超声提示一侧或双侧卵巢均有≥12个直径2~9 mm 的卵泡,和(或)卵巢体积≥10ml。排除其他高雄激素病因(如高泌乳素血症、先天性肾上腺皮质增生、库欣综合征、雄激素分泌性肿瘤等);(2)患者3个月内未使用激素类药物并且首次行促排卵治疗;(3)患者年龄均≤40岁;(4)患者不孕的年限及文献来源不限。
排除标准:①非随机对照试验;②文献中为联合促排卵用药与单一促排卵药物的比较;③文献中的研究对象为CC抵抗的PCOS患者或者掺杂有其他原因引起的不孕患者;④重复发表的或文献质量较差的论文;⑤未提供明确的原始数据或者原始数据不充分者;⑥文献为综述或者摘要;⑦失访率超过20%的研究。
3.干预措施:实验组采用LE+HMG(75~150U/d)促排卵,对照组采用CC+HMG(75~150U/d)促排卵。
4.观察指标:主要结局指标为周期妊娠率(周期妊娠率=临床妊娠周期数/总周期数×100%);次要结局指标为HMG 用量、HCG 日优势卵泡个数、流产率(流产率=流产病例数/总临床妊娠数)×100%、不良事件发生率[(多胎妊娠率+OHSS发生率)/总临床妊娠数];HCG 日子宫内膜厚度。
二、试验筛选
中文检索词“多囊卵巢综合征,来曲唑,芳香化酶抑制剂,克罗米芬,人绝经期促性腺激素,meta分析”;英 文 检 索 词 为“Polycystic ovary syndrome(PCOS)、letrozole(LE)、aromatase inhibitor、Clomiphene citrate、human menopausal gonadotropin(HMG)、menotropins、meta”。 计 算 机 检 索Pubmed、The cochrane library、Wanfang、CNKI、VIP、CBM 等中外数据库,检索年限不限制。此外,在图书馆手工检索2010年1月至2015年4月以来的相关杂志(中华妇产科杂志、实用妇产科杂志、中国实用妇科与产科杂志、现代妇产科进展等)并追溯已纳入文献的参考文献。
由两名评价者独立检索相关文献并评估研究文献的质量,有不同看法时双方协调达成一致,必要时请示上级人员进行相关方面的指导。严格按照上述标准,确定本研究的最终纳入的文献。
三、方法质量学评价
Meta分析是在原有研究结果基础上的再次分析,因此选取高质量的文献做统计分析非常重要。对纳入的研究进行质量评价,采用Cochrane系统手册5.1.0[10]推荐的RCT 的偏倚风险评估工具评价纳入研究的偏倚风险。
四、统计分析
选用RevMan5.3软件对所纳入的研究进行数据的处理与分析。对纳入的文献中周期妊娠率、流产率等以相对危险度(Relative Ratio,RR)作为统计分析量,不良事件发生率以危险差(risk difference,RD)作为统计分析量,HMG 用量、HCG 日优势卵泡数、HCG 日子宫内膜厚度以加权平均差(standard mean difference,SMD)作为统计分析量,并且分别计算其95%的可信区间(95%CI)(检验水平α=0.05);P<0.05表示差异有统计学意义。
利用RevMan5.3 提供的Mantel-Haenszel检验法对所纳入的研究进行异质性检验,以I2表示各文献之间的异质性。我们一般认为I2在0~40%时表示异质性可以忽略不计,30%~60%时表示存在一定程度的异质性,50%~90%时说明有较明显的异质性[11]。若异质性检验结果无统计学意义且I2≤50%,选用固定效应模型;当异质性检验具有统计学意义且I2>50%时采取随机效应模型。当纳入研究数量足够时,进行漏斗图分析观察是否存在发表偏倚。
结 果
一、检索结果
初检获得648篇相关文献,剔除重复发表和交叉的文献、不符合纳入标准的文献,共筛选出6 篇[12,13,14,15,16,17]相关的RCT文献。6篇纳入的文献均为随机对照研究,合计共有PCOS病例658例,其中LE+HMG 组病例数为321例,CC+HMG组病例数为337例。入选的文献基本情况见表1。
二、纳入研究的质量方法学评价
入选的6 篇文献中有4 篇提到了随机分配,2篇分配方式未提及,是否分配隐蔽及采用盲法均不清楚,6篇中均无失访和退出,均采用了ITT 分析。具体质量评价见表2。

表1 纳入研究的文献基本特征

表2 纳入研究的方法学质量评价
三、Meta分析结果
1.不同促排卵方案组HMG 用量:共有2篇文献[12-13]数据中包含有两种促排卵方案的HMG 用量,统计分析结果显示2 个研究异质性较高(P<0.01,I2=95%),故采用随机效应模型进行最终结果分析。结果显示两种促排卵方案之间HMG 用量无统计学差异[0.67,95%CI(-0.66,2.00),P=0.33](图1)。
2.HCG 日优势卵泡数:共有4篇文献[12-15]数据中有两种促排卵方案的HCG 日优势卵泡数,统计分析结果显示4个研究异质性较高(P<0.01,I2=86%),故采用随机效应模型进行最终结果分析。结果显示两种促排卵方案之间HCG 日优势卵泡数无统计学差异[-0.47,95%CI(-1.01,0.07),P=0.08](图2)。
采用RevMan 5.3软件自动生成的漏斗图,可看出4篇纳入文献的数据基本分布在中线的两侧,各文献间的偏倚不明显(图3)。

图1 LE+HMG 组与CC+HMG 组HMG 用量的比较
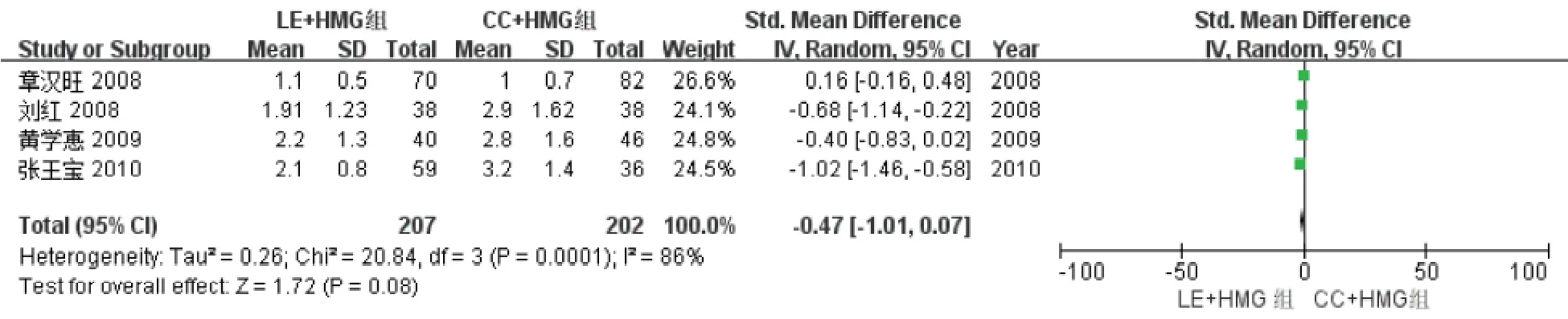
图2 LE+HMG 组与CC+HMG 组HCG 日优势卵泡数的比较
3.周期妊娠率:各纳入文献中均有两组周期妊娠率的比较,统计分析结果显示6个研究异质性较高(P=0.04,I2=57%),故采用随机效应模型进行最终结果分析。结果显示二组之间周期妊娠率无统计学差异[1.34,95% CI(0.88,2.04),P=0.17](图4)。漏斗图显示6篇纳入的文献基本分布在中线的两侧,各文献间的偏倚不明显(图5)。
4.流产率:共有2篇文献[13-14]数据中包含有两种促排卵方案的流产率,统计分析结果显示2个研究具有同质性(P=0.41,I2=0%),故采用固定效应模型进行最终结果分析。结果显示二组之间流产率无统计学差异[-0.11,95%CI(-0.38,0.16),P=0.43](图6)。
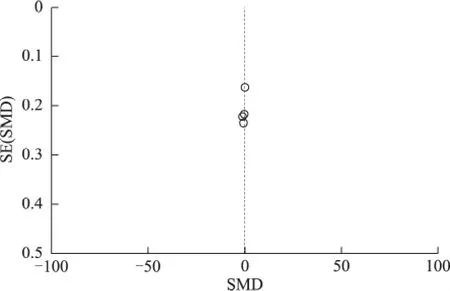
图3 LE+HMG 组与CC+HMG 组HCG 日优势卵泡数的漏斗图
5.不良事件发生率:共有5篇相关文献[12-15,17]中有两种促排卵方案不良事件发生率(多胎妊娠率和OHSS发生率之和)的比较,5个研究具有同质性(P=0.67,I2=0%),故采用采取固定效应模型进行最终结果分析。结果显示LE+HMG 组不良事件发生率较CC+HMG 组低,差异有统计学意义[-0.05,95%CI(-0.08,-0.01),P=0.007](图7)。漏斗图显示5篇纳入文献基本分布在中线的两侧,各文献间的偏倚不明显(图8)。
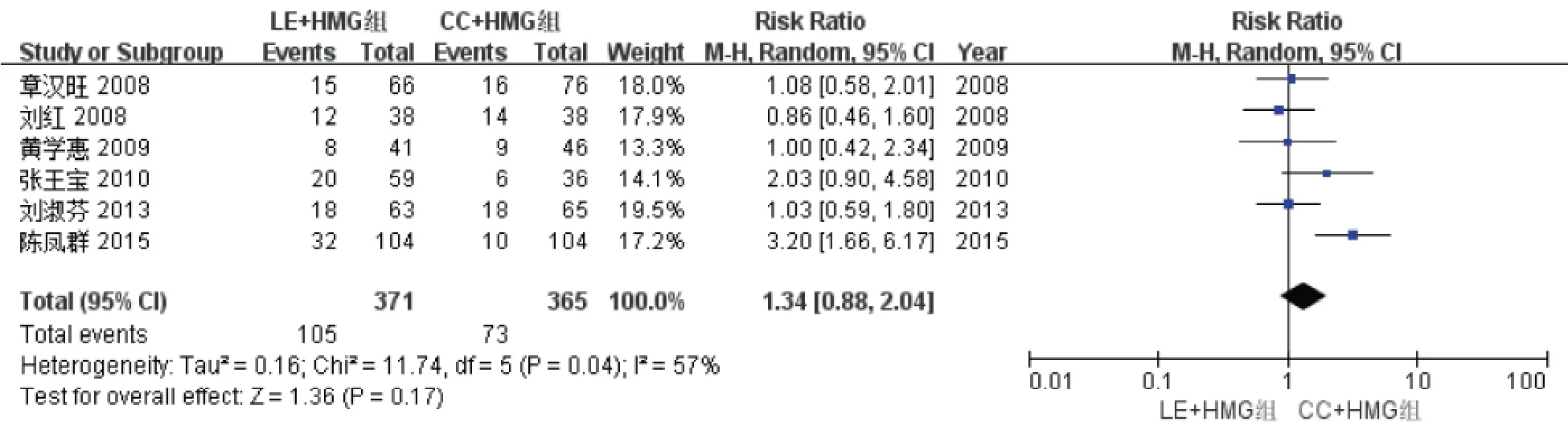
图4 LE+HMG 组与CC+HMG 组周期妊娠率的比较
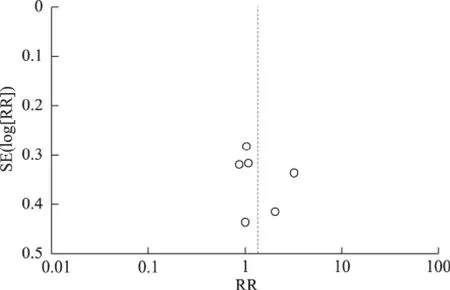
图5 LE+HMG 组与CC+HMG 组周期妊娠率的漏斗图
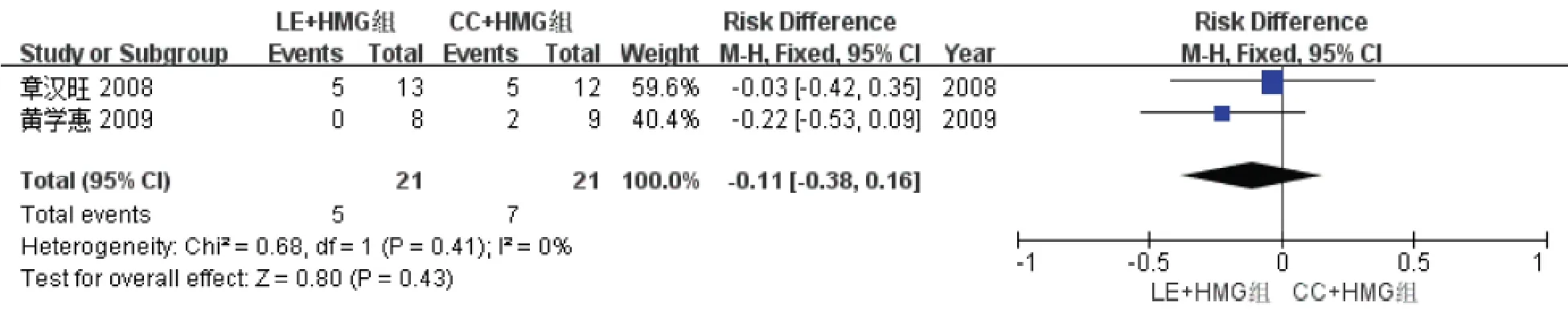
图6 LE+HMG 组与CC+HMG 组流产率的比较
6.HCG 日子宫内膜厚度:共有5 篇相关文献[12-16]中有两种促排卵方案HCG 日子宫内膜厚度的相关数据,统计分析结果显示5个研究异质性较高(P<0.01,I2=94%),故采用随机效应模型进行最终结果分析。结果显示二组之间HCG 日子宫内膜厚度无统计学差异[0.75,95%CI(-0.05,1.54),P=0.07](图9)。漏斗图显示五篇纳入的文献基本分布在中线的两侧,各文献间的偏倚不明显(图10)。

图7 LE+HMG 组与CC+HMG 组不良事件发生率比较

图8 LE+HMG 组与CC+HMG 组不良事件发生率的漏斗图

图9 LE+HMG 组与CC+HMG 组HCG 日子宫内膜厚度的比较
图10 LE+HMG 组与CC+HMG 组HCG 日子宫内膜厚度的漏斗图
讨 论
PCOS在WHO 排卵型障碍分型中属于II型,其特点为雌激素水平和促性腺激素水平在正常范围内[18],但黄体生成素(LH)和卵泡刺激素(FSH)比例失调,其病因繁多,现研究多认为其可能与某些遗传基因与环境相互作用而引起的下丘脑-垂体-卵巢轴功能的紊乱有关,最终导致卵巢持续不排卵。目前治疗手段仍以调节饮食结构、调整月经周期、控制高雄激素血症、调节胰岛素抵抗和促排卵治疗为主。
促排卵治疗作为有生育要求的患者中的关键治疗环节,目前国内外主张的首选治疗药物仍为克罗米芬(CC),但其治疗后的累积妊娠率较低,并且有20%~30%的患者对其抵抗[5],这部分患者虽然可经达英-35和二甲双胍预处理后再进行CC 促排卵,但有一部分患者仍然不能得到很好的疗效。对于CC治疗失败的PCOS 患者,在临床上一般推荐使用二线促排卵药物HMG,然而HMG 直接作用于卵巢,导致卵巢中的多个卵泡同时发育,增加了患者多胎妊娠及OHSS的发生率,并且HMG 价格相对昂贵,很多患者难以接受。
来曲唑(LE)是第三代芳香化酶抑制,其可以特异、可逆地抑制芳香化酶,阻断雄激素向雌激素的转化,使雌激素生成减少,解除雌激素对下丘脑的抑制作用,使FSH、LH 释放,卵泡募集增加。此外,和CC相比,LE的半衰期短,体内清除快,不抑制雌激素受体,对子宫内膜、宫颈粘液无不良影响。一项最新的系统评价LE 和CC 的随机对照试验显示,LE比CC 有着更高的排卵率和妊娠率,是PCOS患者促排卵治疗的较理想的选择方案之一[5]。但目前关于LE联合HMG 与CC 联合HMG 治疗PCOS的疗效,相关的系统评价相对较少。Jee等[19]的一项非随机对照试验研究显示HCG 日成熟卵泡数在LE+HMG 组更多,而两组间临床妊娠率及HCG日子宫内膜厚度无统计学差异;而刘红等[12]的研究显示HCG 日成熟卵泡数在CC+HMG 组更多。各个研究的结果不相一致。因此本研究搜集LE 和CC分别联合HMG 治疗PCOS的相关文献,系统评价不同促排卵方式的疗效,为临床用药提供一定的依据。
在本分析中,两种促排卵方式在HMG 用量方面无统计学差异,这与章汉旺等[13]的研究结果相一致,而与刘红等[12]的研究结果相反。考虑到含HMG 用量的相关文献偏少,文献中所含的病例数偏低,期待大样本随机对照研究进行更进一步的证实。
CC+HMG 组较LE+HMG 组HCG 日优势卵泡数多,但无统计学差异;LE+HMG 组的周期妊娠率高于CC+HMG 组,但无统计学差异。显示LE+HMG 在临床妊娠结局上与CC+HMG 有类似的效果。
Biljan等[20]通过比较LE 促排卵后出生的婴儿与正常分娩出生的婴儿后发现,二组总体先天异常发生率无统计学差异,但运动系统和心血管系统异常率在LE促排卵组高于对照组,所以最终认为LE存在潜在的胚胎毒性。但Mitwally等[21]通过不同促排卵方案的对比,发现LE 促排卵在流产率及多胎妊娠率方面低于其他组,他认为尚不能证明LE具有潜在的毒性。在本分析中,LE+HMG 与CC+HMG 两组之间流产率、妊娠率等方面均无统计学差异,亦不支持LE在促排卵中存在潜在的毒性,这可能与LE的半衰期较短,当促排卵妊娠成功后,已基本在体内清除,在胎儿发育时期已无药理作用。此外,LE+HMG 与CC+HMG 相比可显著降低多胎妊娠及OHSS 等不良事件的发生率,这可能与LE半衰期短,卵泡募集后E2分泌增加,抑制了FSH 的过量释放,得以使小卵泡闭锁,保证了单优势卵泡的生长有关[22]。
在HCG 日子宫内膜厚度方面,LE+HMG 组子宫内膜厚度较CC+HMG 组略厚,但差异无统计学意义。LE+HMG 组HCG 日子宫内膜厚度增加的原因可能为LE 阻碍雄激素向雌激素转化,虽在卵泡期早期可能会因为雌激素的减少引起子宫内膜暂时性的生长缓慢,但LE 不影响雌激素受体,当其半衰期过后,随着卵泡的生长,生成的雌激素逐渐增多,对子宫内膜无不良影响[23]。此外有研究显示,使用LE后,患者的子宫内膜血管供血增多,引起子宫内膜增厚[24-25],HCG 日较厚的子宫内膜有利于受精卵顺利着床。在这一点上,LE+HMG 相比于CC+HMG 有一定的优势。
综上所述,在临床上使用LE+HMG 促排卵与CC+HMG 有着相似的疗效,且在减少不良事件发生率方面有着较明显的优势,有一定的临床应用前景。
本Meta分析纳入文献的质量高低不同,且搜索到的相关文献数目、周期数偏少。因此,期待进行进一步的严谨设计、高质量的大样本研究,为临床工作提供更加坚实可靠的证据。
[1] 中华医学会妇产科学分会内分泌组.多囊卵巢综合征的诊断和治疗专家共识[J].中华妇产科杂志,2008,43:553-555.
[2] Homburg R.Clomiphene citrate-end of an era?A mini review[J].Hum Reprod,2005,20:2043-2051.
[3] Mohamed FM,Mitwally MD,Robert F.Use of an aromatase inhibitor for induction of ovulation in patients with an inadequate response to clomiphene citrate[J].Fertil Steril,2001,75:305-309.
[4] Legro RS,Brzyski RG,Diamond MP,et al.Letrozole versus clomiphene for infertility in the polycystic ovary syndrome[J].N Engl J Med,2014,371:119-129.
[5] Franik S,Kremer JA,Nelen WL,et al.Aromatase inhibitors for subfertile women with polycystic ovary syndrome:summary of a Cochrane review[J].Fertil Steril,2015,103:353-355.
[6] Lu PY,Chen AL,Atkinson EJ,et al.Minimal stimulation achieves pregnancy rates comparable to human menopausal gonadotropins in the treatment of infertility[J].Fertil Steril,1996,65:583-587.
[7] Akbari S,AYazi RM,Ayazi RF.Comparing of letrozole versus clomiphene citrate combined with gonadotropins in intrauterine insemination cycles[J].Iran J Reprod Med,2012,10:29-32.
[8] Yun BH,Chos SJ,Park JH,et al.Minimal stimulation using gonadotropin combined with clomiphene citrate or letrozole for intrauterine insemination[J].Yonsei Med J,2015,56:490-496.
[9] Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group.Revised 2003 consensus on diagnostic criteria and long-term health risk related to polycystic ovary syndrome[J].Hum Reprod,2004,19:41-47.
[10] Higgins JP,Green S.Cochrane Handbook for Systematic Reviews of Interventions(Version 5.1.0)[DB/OL].[cited 2012Jan 5].Available at:http://www.cochrane-handbook.org.
[11] 刘续保,王素萍.临床流行病学与循证医学[M].第4版.北京:人民卫生出版社,2013:126-132.
[12] 刘红,李媛,陈子江,等.人绝经期促性腺激素联合氯米芬或来曲唑用于多囊卵巢综合征患者促排卵疗效比较[J].中国妇产科临床杂志,2008,9:339-342.
[13] 章汉旺,饶群,艾继辉,等.来曲唑联合HMG 对多囊卵巢综合征 患 者 促 排 卵 的 临 床 研 究[J].医 药 导 报,2008,27:647-650.
[14] 黄学惠,廖翌,马方.两种促排卵方案在多囊卵巢综合征不孕患者中的临床观察[J].中国医药导报,2009,18:9-11.
[15] 张王宝.来曲唑联合人绝经期促性腺激素对多囊卵巢综合征伴不育的疗效观察[J].生殖医学杂志,2010,19:152-153.
[16] 刘淑芬.97例多囊卵巢综合征不孕症患者促排卵治疗的临床观察[J].中国医药指南,2013,11:270-271.
[17] 陈凤群.来曲唑、HMG、曲普瑞林联合促排卵治疗多囊卵巢综合 征 不 孕 患 者 的 疗 效 观 察[J].河 北 医 药,2015,37:900-901.
[18] 陈新娜.无排卵性不孕妇女的药物治疗[M].北京:人民卫生出版社,2006:127.
[19] Jee BC,Ku SY,Suh CS,et al.Use of letrozole versus clomiphene citrate combined with gonadotropins in intrauterine insemination cycles:a pilot study[J].Fertil Steril,2006,85:1774-1777.
[20] Biljan MM,Hemmings R,Brassard N.The outcome of 150 babies following the treatment with letrozole or letrozole and gonadotropins[J].Fertil Steril,2005,84(suppl 1):s95.
[21] Mitwally MF,Casper RF.Single-dose administration of an aromatase inhibitor for ovarian stimulation[J].Fertil Steril,2005,81:229-231.
[22] 徐晓航,张少娣,张翠莲.来曲唑在促排卵中的有效性和安全性分析[J].生殖医学杂志,2014,07:594-598.
[23] Chaudhuri AR,Chatterjee S.Frozen embryo transfer:the present practice and beyond[J].J Basic Clin Physiol Pharmacol,2013,24:125-130.
[24] Fisher SA,Reid RL,Van Vugt DA,et al.A randomized double-blind comparison of the effects of clomiphene citrate and the aromatase inhibitor letrozole on ovulatory function in normal women[J].Fertil Steril,2002,78:280-285.
[25] 陈小莉,郑志群,叶琴.两种剂量来曲唑与克罗米芬对多囊卵巢综合征患者子宫卵巢血流动力学的影响[J].生殖与避孕,2011,31:838-842.

