溶胶-凝胶法制备TiO2-GO 光催化剂的研究
贺亚南,贾瑛,张永勇,秦章程
(第二炮兵工程大学603 教研室,陕西 西安 710025)
自石墨烯于2004 年被发现以来[1],其独特的碳二维平面结构使之具有极大的理论比表面积以及在常温下优良的导电性能,已成为光催化复合材料领域研究的热点之一[2-4]。
氧化石墨烯(GO)是石墨经过强氧化后深度液相分散得到的一种单层或较少层数石墨烯氧化物。因为大量的羟基、环氧基、羧基等亲水基团存在于GO 的二维结构表面或结构边缘[5-6],使其具备优良的亲水性及易化学修饰的特性。利用GO 中含氧活性基团化可以与多种有特定化学功能分子进行反应。如通过酰化或酯化反应可将化学基团修饰在石墨烯上;也可以通过π-π 堆叠作用[6]、离子键或氢键等非共价键方式,对石墨烯进行表面功能化修饰,或使其作为催化剂载体[7]。
本文以改进Hummer 法[8]制备氧化石墨烯,采用溶胶-凝胶法,以钛酸丁酯作为钛的前驱物,制备TiO2-GO 光催化复合材料,对航天推进剂偏二甲肼(UDMH)进行光催化降解,探讨了GO 对TiO2晶型、粒径及光催化活性的影响。
1 实验部分
1.1 试剂与仪器
钛酸四丁酯,化学纯;冰醋酸、无水乙醇、双氧水、磷酸二氢钠、柠檬酸均为分析纯;鳞片石墨;氨基亚铁氰化钠(TPF),自制[9]。
722 分光光度计;78-1 型磁力搅拌器;D/max-rB型X 射线衍射仪;JSM26700F 型扫描电镜。
1.2 材料制备
采用改进的Hummer 氧化法[8]制备氧化石墨。取一定量的氧化石墨,放入100 mL 蒸馏水中,超声振荡0.5 h,得到氧化石墨烯水溶液。
40 mL 无水乙醇加入2 mL 冰醋酸,搅拌下加入10 mL 钛酸丁酯,混合均匀,形成前驱物混合液。搅拌下将前驱物混合液以3 s/滴的滴速滴入氧化石墨烯中,滴加完毕后继续搅拌30 min,静置6 h 陈化,完成溶胶-凝胶转化,得到灰色溶胶。60 ℃干燥,得到松散灰白色块状干凝胶。研磨成粉末,于马弗炉中焙烧,取出后空气中冷却,再次研磨,得到呈灰白色的TiO2-GO 样品。将GO 添加量1%记为TiO2-GO-1;不同添加量x%记为TiO2-GO-X。
1.3 光催化活性实验
取初始质量浓度为20 mg/L 的UDMH 废水100 mL于烧杯中,投加催化剂量为1 g/L,置于暗处静置0.5 h 进行吸附。在室温下置于自制的紫外光反应器中进行降解实验。从开始降解计时,取10 mL降解液进行UDMH 浓度测定[9]。当加入TPF试剂的试液水浴后,1 000 r/min 离心45 min 后,用分光光度计于500 nm 处测量试液吸光度,计算UDMH 降解率。
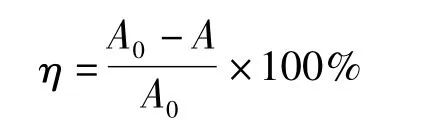
式中 η——UDMH 降解率,%;

2 结果与讨论
2.1 TiO2-GO-1
400,500,600,700 ℃焙烧4 h 的样品分别记为a、b、c、d;500 ℃下分别焙烧8,12 h 的样品记为e、f。2.1.1 XRD、SEM 分析 XRD 见图1,SEM 见图2。
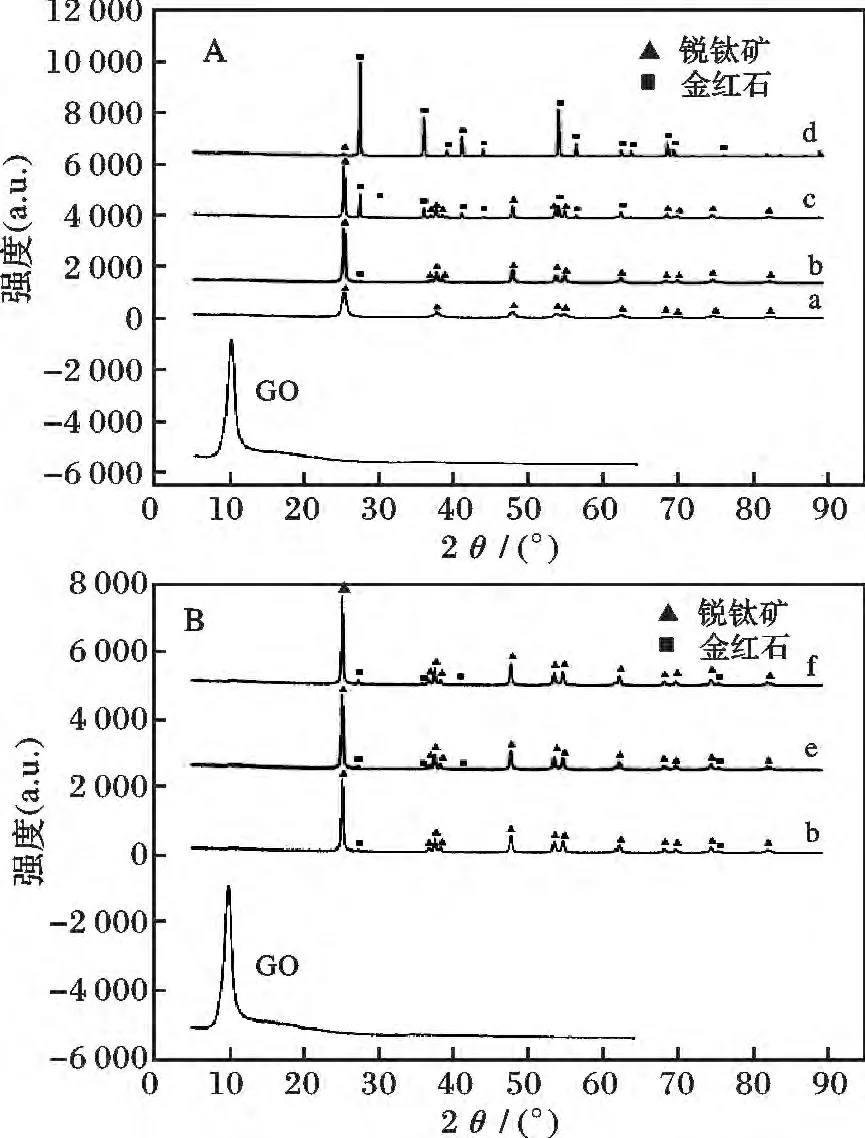
图1 TiO2-GO-1 样品的XRD 图Fig.1 XRD patterns of the TiO2-GO-1 samples

图2 TiO2-GO-1 样品的SEM 图Fig.2 SEM images of TiO2-GO-1 samples
由图1 可知,所有XRD 谱图均只出现了TiO2的衍射峰(锐钛矿相PDF65-5714,金红石相PDF65-0191),说明制得样品纯度高,无其它杂质。图1 中的A、B 下方在2θ =10°附近出现很强的衍射峰,为制备的氧化石墨(001)面的衍射峰,但在所有样品中均未出现,可能由于GO 被高度分散并被TiO2包覆或其浓度低于XRD 的检测限导致。
由图1A 可知,a 为纯锐钛矿,b、c 主要以锐钛矿相存在,d 主要以金红石相存在。由图2 可知,样品a、b 颗粒轮廓分明,结构松散,平均粒径相对较小;样品c、d 颗粒排列致密,出现明显的烧结现象,说明颗粒表面已经从锐钛矿转变为金红石,导致平均粒径剧增,与表1 计算结果相对应。在500 ℃焙烧TiO2-GO-1 均已出现金红石,并且在500 ℃以上焙烧,TiO2衍射峰强度明显变大,半峰宽变小,表明锐钛矿型TiO2结晶更加完善。与高伟等[10]在600 ℃焙烧2 h TiO2金红石含量=84. 8% 比较,600 ℃焙烧4 h 金红石含量=37.1%(XRD 的相变温度是当锐钛矿向金红石转变50%时的热处理温度),说明A-T 相变温度>600 ℃,与李佑稷等[11]的“TiO2/AC 复合体的相变温度为509 ℃比TiO2本体的相变温度465 ℃高”相比较,说明GO 的添加会使TiO2的锐钛矿向金红石的相变温度大大高。
500 ℃下焙烧不同时间的b、e、f 均为以锐钛矿为主的混晶结构,晶型比见表1。
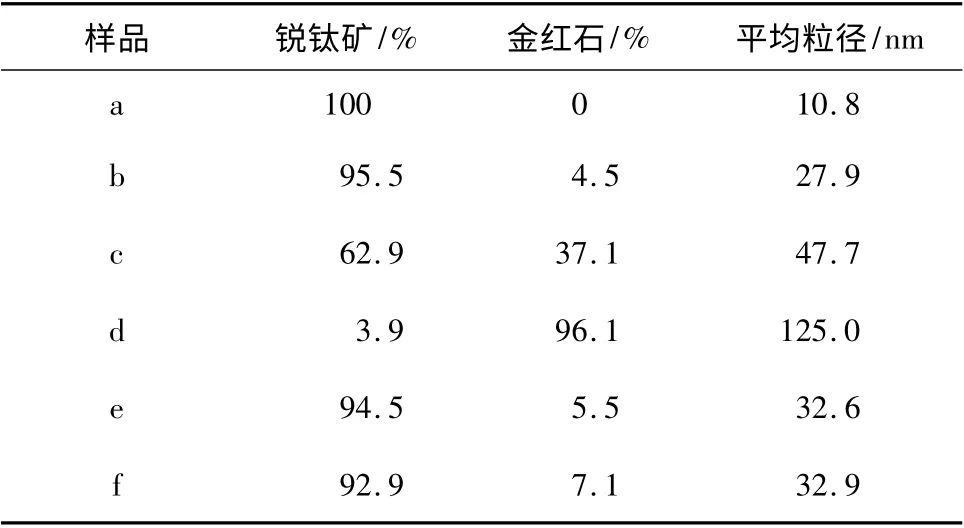
表1 TiO2-GO-1 样品的晶型含量与颗粒平均粒径Table 1 Crystal content and the average particle diameter of the samples of the TiO2-GO-1
随着焙烧时间延长,样品金红石含量增多,但增幅很小,同时粒径略微变大,与高伟等[10]实验相比,相变非常缓慢,说明同一温度下的相变是一个缓慢过程。图2 样品e 的SEM 图中,有大块絮状结构(图中黑框部分),为较大块的氧化石墨烯,而别的样品都未能发现絮状结构,有可能是氧化程度较强,单块氧化石墨烯较小而被TiO2包覆。
TiO2添加GO 后,锐钛矿向金红石的相变温度升高,相变过程缓慢,这可能是GO 极大的比表面积与强吸附力对TiO2晶型的转变阻遏作用,使相变过程所需要的活化能增大,从而导致相变过程减缓,这样更利于制备结晶度好的混晶结构。
2.1.2 光催化活性 TiO2-GO-1 对UDMH 废水的降解效果见图3。
由图3 可知,UDMH 的降解率随反应时间的延长而增加,同等条件下,样品a、b、c、e 和f 反应2 h对UDMH 降解率均>60%;而金红石相含量为96.1%的样品d,2 h 降解率仅为10.35%。a 为纯锐钛矿相,以锐钛矿相为主的混晶样品2 h 降解率均大于纯锐钛矿样品的2 h 降解率,其中降解率最高的为f,为80.32%,其锐钛矿含量∶金红石含量=92.1%∶7.9%,与高伟等光催化活性实验表明m(锐钛矿)/m(金红石)= 9/1 时样品的催化效果最佳[13]的结果相对应。
样品焙烧温度的升高,已生成的锐钛矿颗粒表面转变成金红石,从而形成了表面为金红石薄层的包覆结构,而金红石薄层不会阻挡锐钛矿激发价带电子所需的光线,因此并不影响锐钛矿型TiO2价带电子的激发。由于两种晶型TiO2费米能级不同,在两相界面间能产生Schottky 势垒,促进了电子及空穴的转移、分离并迁移到催化剂的表面。由于两相接触紧密,使得这种粒子内部的电子-空穴的分离效率较高,从而提高了光催化活性。同时随着焙烧时间增加,样品b、e、f 金红石含量不断增加,锐钛矿与金红石含量比例越来越接近m(锐钛矿)/m(金红石)= 9/1,混晶效应[14]进一步增强,光催化活性增高。
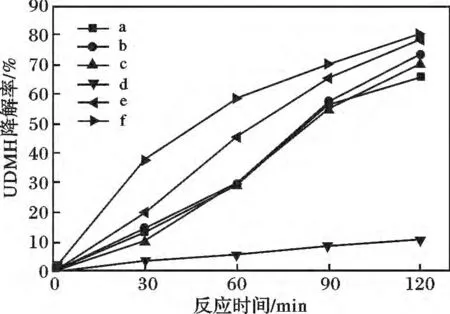
图3 TiO2-GO-1 在不同温度下焙烧4 h 样品对UDMH 的降解效果Fig.3 Image of UDMH degradation rate of TiO2-GO-1 calcined at different temperatures for 4 h
2.2 TiO2-GO-X 在500 ℃下焙烧12 h 的结果
X 为氧化石墨烯的质量分数(%),其余条件相同,在焙烧温度为500 ℃,为保证焙烧充分,焙烧时间为12 h 的条件下分别制备了纯TiO2、TiO2-GO-0.5、TiO2-GO-1、TiO2-GO-2. 5、TiO2-GO-5、TiO2-GO-10 样品。
2.2.1 XRD 见图4。
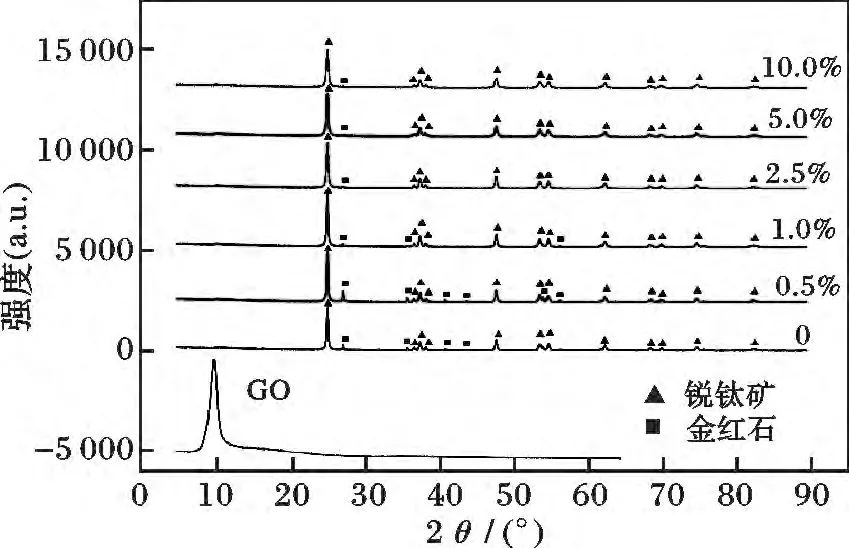
图4 TiO2-GO-X 在500 ℃下焙烧12 h 的XRD 图Fig.4 XRD patterns of TiO2-GO-X calcined at 500 ℃for 12 h
由图4 可知,所有样品均为混晶结构,随着GO添加量的增加,粒径不断变小,金红石含量减小。所有XRD 图谱中仍未出现氧化石墨的特征衍射峰。由表2 可知,纯TiO2颗粒平均粒径为39 nm,GO 添加量0.5%时,样品颗粒平均粒径比纯TiO2大,可能是因为GO 添加量少,单块GO 尺寸小以及其很强的吸附性,在形成凝胶时单块GO 吸附较多晶核,较多晶粒生长导致单个颗粒尺寸较大;GO 添加量>1%时,所有样品尺寸均小于纯TiO2,随着GO 添加量增多,平均粒径不断减小。这可能是因为随着GO 添加量增多,单块GO 吸附晶核量减少,晶粒生长过程中,构成单个颗粒的晶粒减少,从而使颗粒平均尺寸不断减小,团聚减少。
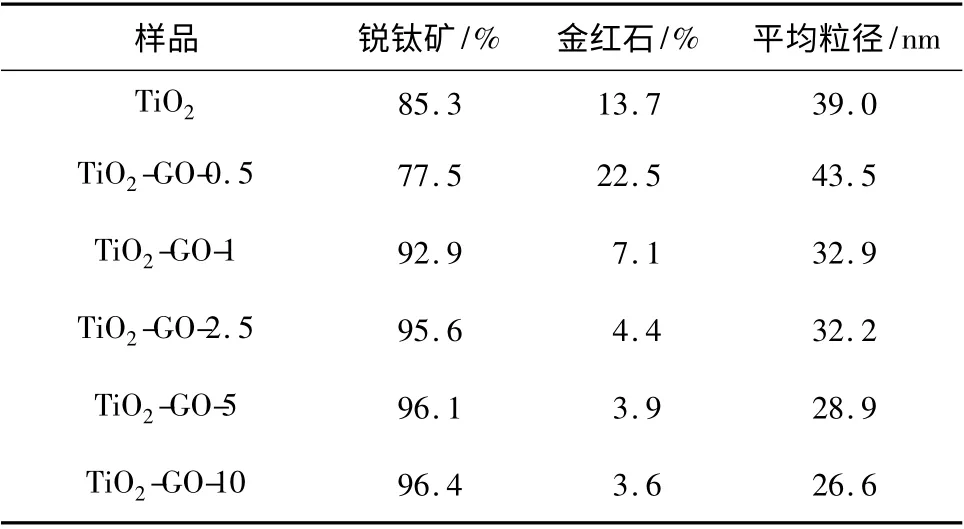
表2 TiO2-GO-X 在500 ℃下焙烧12 h 样品的晶型含量与颗粒平均粒径Table 2 Crystal content and the average particle diameter of samples of the TiO2-GO-X calcined at 500 ℃for 12 h
2.2.2 光催化活性 图5 是TiO2-GO-X 对20 mg/L的UDMH 2 h 降解率图。
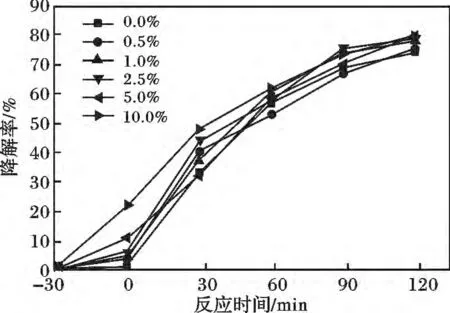
图5 TiO2-GO-X 对UDMH 的降解率Fig.5 Image of UDMH degradation rate of TiO2-GO-X
表3 为各样品30 min 对UDMH 的吸附率。由表3 可知,TiO2对UDMH 30 min 的吸附率最低,只有0.40%,而GO 添加最大的TiO2-GO-10 的30 min吸附率最高,为22.38%,随着GO 添加量的逐渐增多,TiO2-GO 的30 min 对UDMH 的吸附率逐渐增高。TiO2对UDMH 的2 h 降解率也是TiO2-GO-10最高,为80.36%,而纯TiO2的降解率最低,为74.92%,说明GO 的添加对TiO2的光催化活性有提升。TiO2-GO-10 因为GO 的添加量增多,对UDMH的吸附能力增强。TiO2-GO 的光催化活性均高于纯TiO2,可能是因为GO 的添加,可以起到半导体光敏剂的作用,使TiO2-GO 费米能级向正方向偏移,对可见光的吸收性能增强,GO 在TiO2中因其良好的导电性,减少电子与空穴的复合几率,同时TiO2的比表面积增大和加强了活性组分高的分散程度增加了有效反应活性位[15-18],相对于纯TiO2增强了光催化活性。
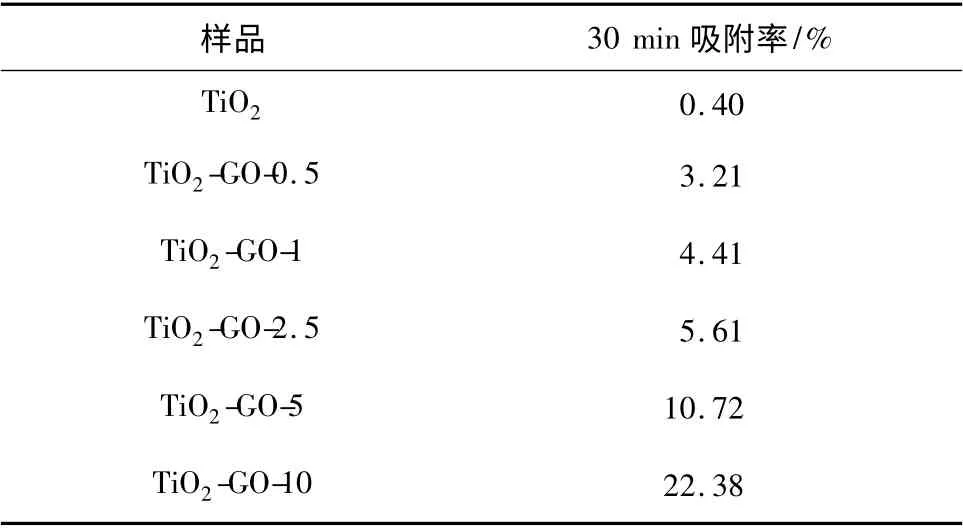
表3 TiO2-GO-X 对UDMH 的30 min 吸附率Table 3 The adsorption rate of UDMH for 30 min of TiO2-GO-X
3 结论
使用改进Hummer 法制备了氧化石墨烯,然后采用溶胶-凝胶法制备TiO2-GO 复合材料。考察了焙烧温度、焙烧时间和GO 用量对复合材料晶型、粒径的影响及光催化活性。结果表明,GO 的添加不会改变TiO2的晶型,但会提高TiO2锐钛矿向金红石的相变温度,减缓相变速度;随着GO 添加量的增加,TiO2粒径减小,减小团聚,复合材料吸附性增强,并使相同温度下由锐钛矿相向金红石相转变变难。氧化石墨烯的引入有利于增强TiO2的光催化活性,UDMH 的降解率提高,并且对UDMH 的吸附作用大大增强。
[1] Novoselov K S,Geim A K,Morozov S V,et al. Electric field effect in atomically thin carbon films[J]. Science,2004,306:666-669.
[2] Chae H K,Siberio Perez D Y,Kim J.A route to high surface area,porosity and inclusion of large molecules in crystals[J].Nature,2004,427:523-527.
[3] Schadler L S,Giannaris S C,Ajayan P M.Load transfer in carbon nanotube epoxy composites[J]. Appl Pys Lett,1998,73:3842-3844.
[4] Zhang Y,Tan J W,Kim P,et al.Experimental observation of quantum hall effect and Berry’s phase in graphene[J].Nature,2005,438:201-204.
[5] Jeong H K,Lee Y P,Lahaye R J W E,et al.Evidence of Graphitic AB stacking order of Graphite oxides[J]. Am Chem Soc,2008,130:1362-1366.
[6] Barinov A,Malcioglu O B,Fabris S,et al.Initial stages of oxidation on graphitic surfaces:Photoemission study and density functional theory calculatons[J]. Phys Chem C,2009,113:9009-9013.
[7] 柏嵩,沈小平.石墨烯基无机纳米复合材料[J].化学进展,2010,22(11):2107-2116.
[8] Hummers W S,Offeman R E.Preparation of Graphite oxide[J].Journal of the American Chemical Society,1958,80(6):1339.
[9] 国防科工委后勤部.火箭推进剂监测防护与污染治理[M].北京:国防科技大学出版社,1993:655-658.
[10] 高伟,吴凤清,罗臻,等. TiO2晶型与光催化活性关系的研究[J].高等学校化学学报,2001,22(4):660-662.
[11] 李佑稷,李效东,李君文,等.活性炭载体TiO2/活性炭中二氧化钛晶粒生长及相变的影响[J]. 无机材料学报,2005,20(2):291-298.
[12]晋勇,孙小松,薛屺. X 射线衍射分析技术[M]. 北京:国防工业出版社,2008:171-172.
[13]Spurr R A,Myers H.Quantitative analysis of anatase rutile mixture with an X-ray diffractometer[J]. Anal Chem,1957,29(5):760-762.
[14]唐爱东,任艳萍.二氧化钛催化剂晶型调控技术的研究进展[J].中国粉体技术,2010,16(3):69-73.
[15]Zhang X Y,Li H P,Cui X L.Preparation and photocatalytic activity for hydrogen evolution of TiO2/graphene sheets composite[J].Inorg Chem,2009,25(11):1903-1907.
[16] Stankovich S,Dikin D A,Dommett G H B,et al. Graphene-based composite materials[J]. Nature,2006,442:282-286.
[17]Novoselov K S,Geim A K,Morozov S V,et al.Two-dimensional gas of massless Dirac fermions in graphene [J].Nature,2005,438(7065):197-200.
[18]Zhang H,Lv X,Li Y,et al.P25-Graphene composite as a high performance photocatalyst[J]. ACS Nano,2009,4(1):380-386.
——以金红石为例

