卟啉衍生物与功能性蛋白作用的光谱学性质研究
宋熙熙,金鑫,宗乾收,董杰
(1.嘉兴学院 化学与纺织工程系,浙江 嘉兴 314000;2.嘉兴学院 生物与化学工程学院,浙江 嘉兴 314000)
卟啉及其衍生化合物广泛存在于生物体内,在光合作用、细胞携氧等过程中起到关键的作用,在能量转移方面也有着优异的表现,因此在电化学,靶向药物等很多领域有巨大的发展前景。血清白蛋白是动物血浆中含量最丰富的功能蛋白质,具有良好的结合能力,在运输内外源物质、维持生理功能等方面有重要的意义。考察卟啉与血清白蛋白相互作用的过程有利于认清功能蛋白质在肌体内部储运分子的过程,并通过主要作用力提高其导向的能力,为生物体转运、识别和结合分子奠定相应的基础。
1 实验部分
1.1 试剂与仪器
N,N-二甲基甲酰胺(DMF)、三羟甲基氨基甲烷、Tris-盐酸(HCl)均为分析纯;四苯基卟啉(H2TPP),实验室自制;牛血清白蛋白(BSA),上海励瑞生物科技有限公司;实验用水为二次蒸馏水。
Cary Eclipse 荧光分光光度计;UV2550 紫外-可见分光光度计。
1.2 实验方法
配制Tris-HCl 缓冲溶液0.1 mol/L,四苯基卟啉溶液1 ×10-4mol/L,BSA 溶液1 ×10-5mol/L。
四苯基卟啉DMF 溶液,DMF 为参比,扫描紫外光谱,记录吸光度变化。不同浓度H2TPP 与BSA 溶液混合,稀释定容,扫描荧光发射光谱,激发波长为280 nm,记录荧光强度。
2 结果与讨论
2.1 紫外光谱
四苯基卟啉在有机溶剂DMF 中的紫外吸收光谱见图1。

图1 四苯基卟啉的紫外光谱曲线Fig.1 The UV spectrum of H2TPP
由图1 可知,电子从高占据分子轨道跃迁到最低空轨道,在420 nm 附近产生较强吸收的Soret 带是由于a1u(π)-eg(π*)跃迁产生的,属于第二电子激发态;电子跃迁在500 ~670 nm 区间出现的4 个弱吸收Q 带[1],是由于a2u(π)-eg(π*)跃迁产生的,属于第一电子激发态。并随着波长的增加,吸收谱带的相对强度逐渐减弱。
2.2 荧光光谱
在298.15 K 时测得的四苯基卟啉与BSA 的荧光光谱图见图2。

图2 四苯基卟啉对BSA 的荧光猝灭曲线Fig.2 Effect of H2TPP on the fluorescent emission spectra of BSA
由图2 可知,在350 nm 附近有较强的荧光峰,随着四苯基卟啉的浓度的增加,BSA 的荧光强度逐渐下降,内源荧光有规律性的发生猝灭作用。同时,BSA 最大荧光发射峰位发生微弱的蓝移,可能是四苯基卟啉与BSA 在基态时形成了复合物,可能从一定程度影响功能蛋白质的二级结构,从而导致了荧光体系的荧光强度降低而发生一定的蓝移,从而可能影响蛋白质的生理活性。
2.2.1 猝灭作用 引起BSA 内源性荧光猝灭的原因可能是由于动态或静态猝灭引起的,动态猝灭是猝灭剂与荧光给体的激发态分子之间发生相互作用,这一过程遵从Stern-Volmer 方程(1)[2-3]:
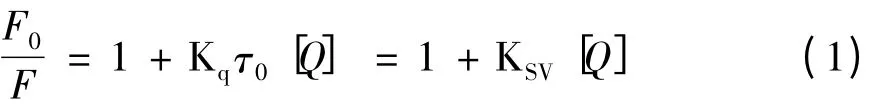
KSV表示动态猝灭常数,Kq表示双分子猝灭过程的速率常数,τ0为猝灭剂不存在时荧光物质的平均寿命,生物大分子的荧光平均寿命根据文献报道[1]大约为10-8s。
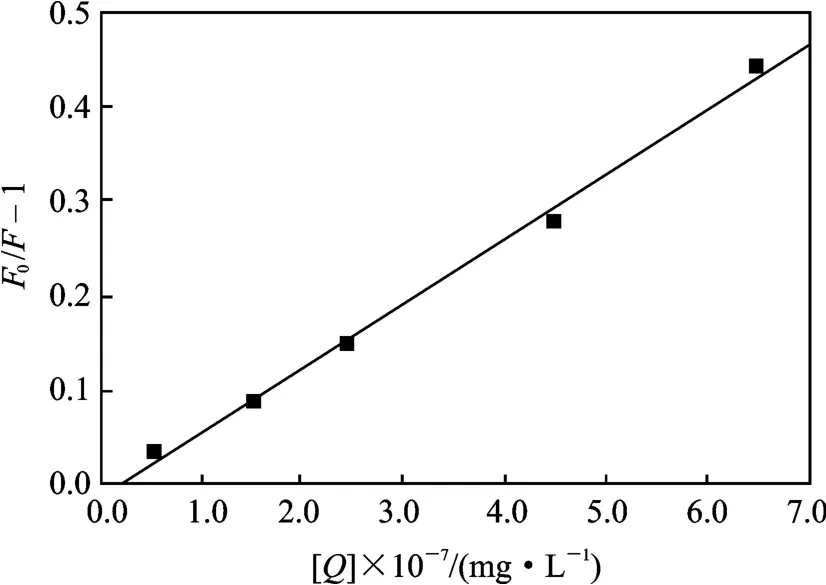
图3 荧光猝灭的Stern-Volmer 图Fig.3 Fluorescent intensity quenching of Stern-Volmer plot
由图3 可知,随着H2TPP 浓度的变化,F0/F-1呈良好的线性关系,可以计算得Kq和KSV见表1。在动态猝灭过程中,一般情况下各类猝灭剂对生物分子的最大扩散碰撞猝灭常数 Kq不大2 ×1010L/(mol·L),然而这两个温度下的Kq都>2×1010L/(mol·L),则该猝灭不是因为H2TPP 对BSA 动态碰撞引起的动态猝灭。

表1 不同温度下H2TPP 与BSA 的猝灭常数Table 1 Quenching parameters of BSA withH2TPP at different temperatures
在静态猝灭中,猝灭剂分子与蛋白质靶分子形成配合物,其结合常数越大,则药物分子的活性越高,得到了荧光强度F、猝灭剂浓度[Q]、结合平衡常数K0和结合数n 之间的关系[4-5](2):

以lg[Q]为横坐标,lgF/(F0-F)坐标作图,见图4。求得平衡常数K0,n,见表2。
说明BSA 分子与四苯基卟啉分子以1∶1 形式结合形成复合物,该复合物随温度的升高,结合常数增大,符合静态猝灭的规律,同时也反映了该结合作用活性较高。
2.2.2 结合作用 猝灭剂分子与生物分子之间的作用力通常包括氢键、静电引力、范德华力和疏水作用力等,或是几种作用力的综合表现。当温度变化不大时,结合反应的焓变可看成一个常数,根据以下热力学公式[6]:

计算得H2TPP 与BSA 相互作用的热力学常数,见表3。
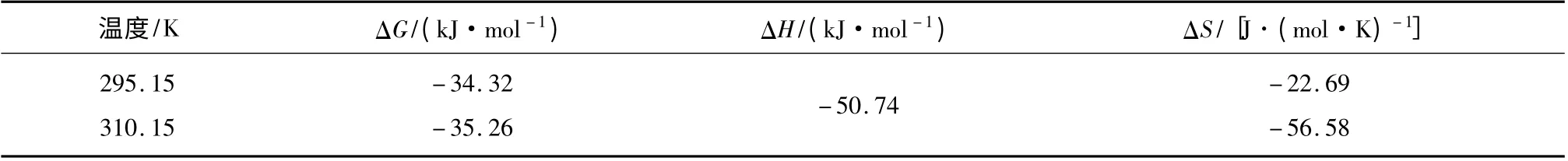
表3 BSA 与H2TPP 结合的热力学函数Table 3 Thermodynamics parameters of BSA with H2TPP
根据过程是吉布斯生成自由能ΔG <0,该反应是自发进行的,说明反应生成稳定的复合物而放出能量,热力学焓变ΔH 和熵变ΔS 都<0,H2TPP 与BSA 之间的作用力主要是范德华力和氢键,但其中的疏水作用也不能忽略。白蛋白的结构非常复杂,在它的研究过程中宏观的表现通常是几种作用力共同作用的结果,但容易受外界环境因素的影响。
2.2.3 同步荧光 利用同步荧光可以了解分子对蛋白质构象的影响[4]。通过选择合适的波长差可将普通荧光光谱上相互重叠的荧光峰分开。蛋白质的内源荧光主要是色氨酸和酪氨酸残基所引起的,研究发现,同步荧光光谱Δλ=15 nm,Δλ=60 nm 分别显示酪氨酸残基,色氨酸残基的光谱特性见图4。
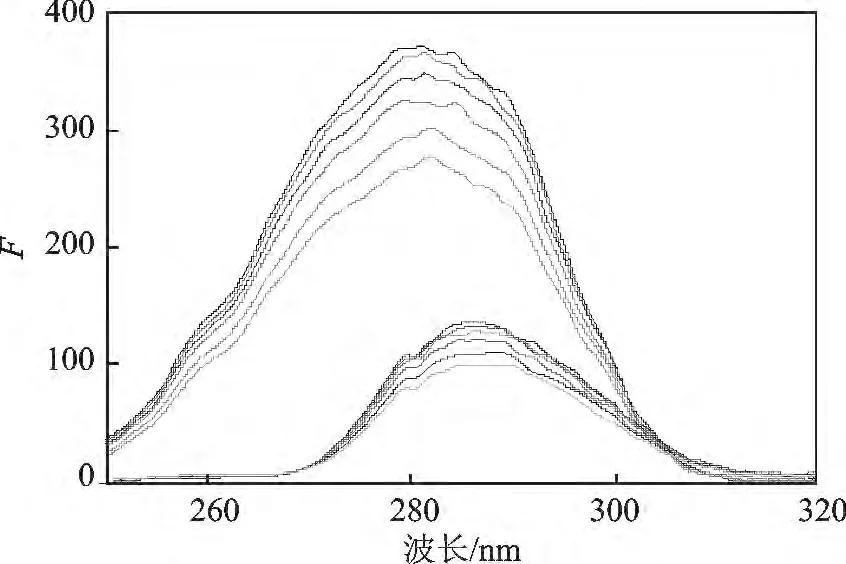
图4 四苯基卟啉对BSA 的同步荧光光谱Fig.4 Synchronous fluorescence spectra of BSA with H2TPP
由图4 可知,当△λ=60 nm 时荧光强度变化明显,所以该结合作用可能是由于四苯基卟啉与色氨酸的结构比较相似而结合,导致了荧光猝灭。
3 结论
主要通过紫外光谱研究了四苯基卟啉的紫外可见光谱性质,H2TPP 有一个较强的Soret 带和4 个Q带,分别是a1u(π)-eg(π*)和a2u(π)-eg(π*)跃迁引起的。并通过荧光光谱研究了H2TPP 与BSA 相互作用,H2TPP 对BSA 的内源荧光有猝灭作用,通过Stern-Volmer 方程等模型计算了该相互作用的猝灭常数、结合常数、结合位点,判定该过程为静态猝灭。并通过热力学常数的变化,说明该过程是自发进行,主要推动力为氢键和范德华力,通过同步荧光光谱,判断该结合位点主要在BSA 的色氨酸残基位置。
[1] 陈声芳. 卟啉低聚物的合成及光谱性质研究[D]. 重庆:重庆大学,2012.
[2] 吕艳阳,张秀兰. 荧光光谱法研究四(对甲氧基苯基)卟啉铅与牛血清白蛋白的相互作用[J].光谱实验室,2013,30(2):843-846.
[3] 王慢想,李强.卟啉及其衍生物的紫外-可见光谱[J].光谱实验室,2011,28(3):1165-1169.
[4] 颜梅,陈欣. 荧光光谱法研究二溴羟基卟啉与蛋白质的结合作用机理[J]. 光谱学与光谱分析,2008,28(6):1322-1326.
[5] 高玲,刘阁.荧光法研究meso-四羧基苯基卟啉与牛血清白蛋白的作用机理[J]. 化学研究与应用,2011,23(9):1164-1168.
[6] 郭灿城,李和平. meso-5,10,15,20-四[4-(N-吡咯烷基)苯基]卟啉的合成及对牛血清白蛋白的作用[J].高等学校化学学报,2003,24(2):282-287.

