壳聚糖对废水中Ni2+吸附的动力学研究
尚秀丽 夏德强 索陇宁 本连芳(兰州石化职业技术学院,甘肃 兰州 730060)
随着新材料和高新技术的不断发展,金属镍被广泛应用于电镀、催化、电池以及功能材料等领域[1-3]。镍的大量使用不仅加快了镍资源的消耗也对生态环境造成严重污染,长期饮用被镍污染的水和食物会引发鼻癌、肺癌、白血病、心肌梗塞、中风和尿毒症等疾病[4]。目前处理含镍废水的主要方法有生物法、离子交换法、化学沉淀法、吸附法、电解法及溶剂萃取法等[5],其中吸附法以其高效率、低成本、无二次污染等优点成为研究热点。
壳聚糖(chitosan,CTS)是天然高分子甲壳素在碱性条件下水解并脱去部分乙酰基后生成的衍生物,由于其分子中含有氨基(-NH2)和羟基(-OH),几乎可以与所有的过渡金属离子结合,因此其在重金属离子吸附方面的应用研究尤为广泛[6-8]。与传统的絮凝剂相比,壳聚糖具有吸附容量大、成本低、无毒、不造成二次污染等优点[9]。本实验以壳聚糖为吸附剂,对废水中的Ni2+进行吸附富集,研究了壳聚糖加入量、吸附温度、振荡时间对Ni2+吸附率的影响,探讨了壳聚糖吸附Ni2+的动力学特征。
1 实验部分
1.1 试剂与仪器
壳聚糖(脱乙酰度92%),镍标准溶液(瑞士Fluka公司),硫酸镍,醋酸,硝酸,丁二酮肟等试剂均为分析纯。
UV-1801紫外可见分光光度计,FA1604N型电子分析天平,PHS-3C型精密酸度计,SHA-C水浴恒温振荡器,TDL-40台式离心机,DZF-O真空干燥箱。
1.2 实验方法
取一定质量的壳聚糖置于250ml锥形瓶中,加入30mL含镍10mg/L的废水溶液,在一定条件下置于恒温摇床中振荡,控制摇床的转速为120r/min,吸附平衡后,将溶液离心分离取上清液,用紫外分光光度计分析样品中N2+的浓度,分别用式(1)、式(2)计算吸附率和吸附量。
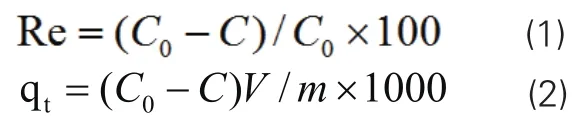
式中:Re为吸附率(%);tq为t时刻的吸附量(mg/g);C0和C分别为吸附前与吸附后溶液的质量浓度(g/L);V为溶液体积(L);m为壳聚糖的质量。
1.3 分析方法
采用丁二酮肟分光光度法测定溶液中Ni2+的质量浓度[10],即在氧化剂存在的碱性溶液中,镍与丁二酮肟作用生成酒红色的可溶络合物,于波长465nm处测定吸光度,绘制Ni2+的质量浓度x(mg/L)与吸光度A的标准曲线,根据标准曲线、测得样液的吸光度计算溶液中Ni2+的质量浓度。
2 结果与讨论
2.1 壳聚糖加入量对Ni2+吸附率的影响
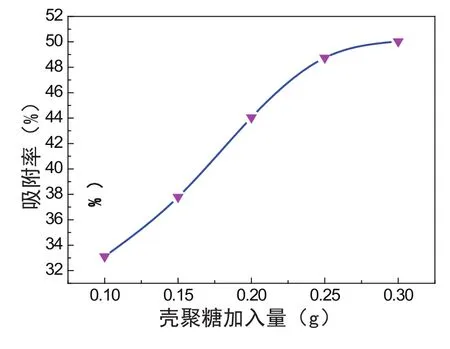
图1 壳聚糖用量对Ni2+吸附率的影响
分别称取0.1g,0.15g,0.2g,0.25g,0.3g的壳聚糖于250mL的锥形瓶中,加入质量浓度为10mg/L含Ni2+废水30mL,于25℃、120r/min振荡1h,将溶液离心分离,取上清液测量其吸光度计算吸附率,结果如图1所示。从图可以看出,壳聚糖添加量在0.1-0.25g时,其对废液中Ni2+的吸附率迅速上升,用量超过0.25g时,吸附率增加缓慢并逐渐趋于平衡。这是因为壳聚糖用量增加导致有效吸附集团增多,即增加了壳聚糖与金属离子的活性吸附位。
2.2 振荡时间对Ni2+吸附率的影响
准确称取0.25g壳聚糖置于250mL的锥形瓶中,加入30mL含镍离子10mg/L的废水,于40℃下恒温振荡,振摇速率为120r/min,振荡时间分别为:10、20、30、60、90、120min,测定其吸光度计算吸附率,结果如图2所示。从图2可以看出,在吸附前60min,壳聚糖对镍离子的吸附率迅速上升,从27.53%上升到54.32%;60min后随着时间的增加,对Ni2+的吸附趋于平衡,吸附率仅增加2.85%。这种现象可能是由于吸附开始时是一种表面吸附,吸附速率较大;当表面吸附达到平衡后,水中Ni2+逐渐向壳聚糖内部迁移、扩散,这种迁移是一个相对缓慢的过程。因此,壳聚糖对镍离子吸附的最佳时间为60min。
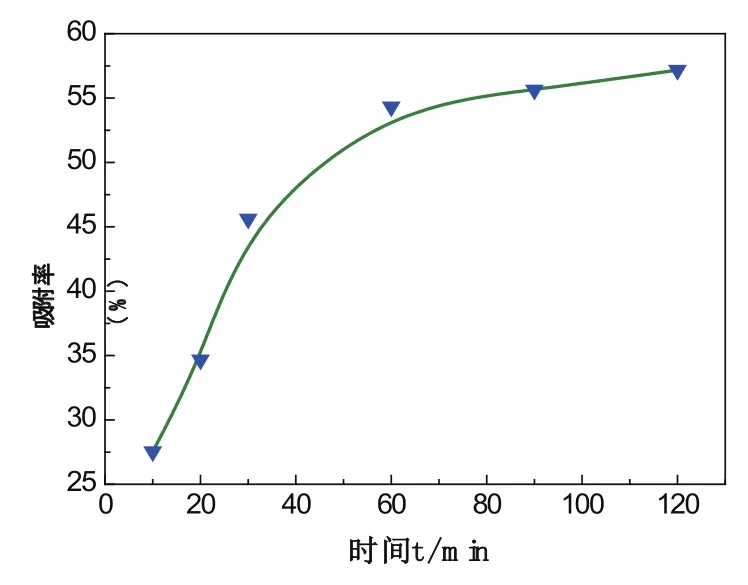
图2 振荡时间对Ni2+吸附率的影响
2.3 Ni2+的吸附动力学
称取0.25g壳聚糖于250mL锥形瓶中,加入质量浓度为10mg/L的Ni2+溶液30mL,在120r/min的转速下,分别于20、40、60℃吸附,该吸附过程可以用准一级(式3)或准二级(式4)动力学模型描述[11]。
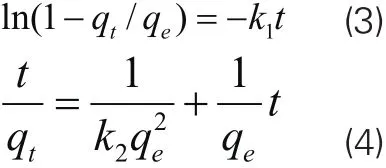
式中:tq、eq分别为t时刻Ni2+吸附量、Ni2+的平衡吸附量(mg/g);1k为准一级动力学速率常数(min-1),2k为准二级动力学常数。对实验所测得的动力学数据分别采用准一级动力学模型和准二级动力学模型拟合,结果如图3、图4所示。
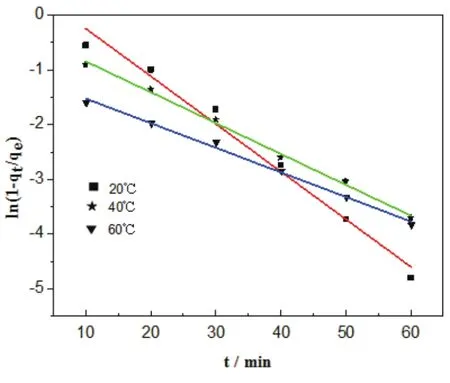
图3 Ni2+吸附的准一级动力学模型

图4 Ni2+吸附的准二级动力学模型
对比图3、图4,壳聚糖对Ni2+的吸附更加符合准二级动力学模型,其相关参数如表1所示。表1中三个方程的相关系数R2均大于0.9892,进一步说明壳聚糖对废水中Ni2+的吸附符合准二级动力学模型。吸附率和K2都随温度的升高而增大,表明该吸附过程为吸热过程,温度升高有利于Ni2+的吸附。
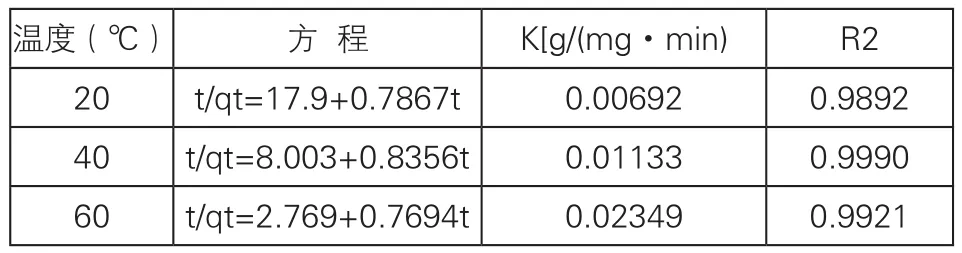
表1 吸附的动力学参数
3 结 语
1)壳聚糖是天然高分子材料,对镍离子具有很好的吸附能力,以壳聚糖做吸附剂处理含镍废水,不造成二次污染,具有良好社会效益。
2)静态吸附实验表明,最佳吸附剂用量为0.25g、吸附时间为60min,镍离子在壳聚糖表面的吸附率随温度升高而增大。吸附过程符合准二级动力学模型。
[1]宋艳阳,原思国,周从章. 弱酸离子交换纤维对含镍废水的吸附性能研究[J].功能材料,2012,43(15):2014-2017.
[2]雷静彬,黄富平,于青,等. 2-(N,N-二羧甲基氨甲基)氢醌金属配合物(钴、镍、锌)的合成、晶体结构及电化学性质研究[J]. 无机化学学报,2012,28(03):572-578.
[3]袁建超,梅铜简,王学虎,等. 含溴α-二亚胺镍( Ⅱ) 配合物的合成、表征及催化乙烯聚合反应[J].高等学校化学学报,2011,32(05):1200-1204.
[4]杨金杯,陈玉成,余美琼,等.001×14.5 离子交换树脂对镍(Ⅱ)的吸附[J].环境工程学报, 2013,7(08):3019-3024.
[5]余静,邱海浪,卢腾飞,等. 萃取净化电镀含镍废水研究[J].水处理技术,2014,40(04):43-51.
[6]胡惠媛, 朱虹. 壳聚糖及其衍生物对重金属离子的吸附[J].化学进展,2012,24(11):2212-2223.
[7]Krishnapriya K R,Kandaswamy M. Synthesis and characterization of a crosslinked chitosan derivative with a complexing agent and its adsorption studies toward metal(II)ions[J].Carbohydrate Research,2009,344(13):1632-1638.
[8]Paulino A T,Santos L B, Nozaki J. Removal of Pb2+, Cu2+, and Fe3+ from battery manufacture wasterwater by chitosan produced from sikworm chrysalides as a lowcost adsorbent[J]. Reactive and Functional Polymers,2008,68(2):634-642.
[9]Crini G.,Badot P.M. Application of chitosan,a natural aminopolysaccharide,for dye removal from aqueous solutions by adsorption processes using batch studies: A review of recent literature.Progress in Polymer Science,2008,33(4) : 399-447.
[10] 齐文启,曾胜年,汪志国,等. 水和废水监测分析方法[M]. 北京:中国环境出版社,2002.373-377.
[11]贾海红,王学松,韩宝平. 壳聚糖吸附酸性品红的平衡及动力学研究[J].环境工程学报, 2011, 5(08):1800-1804.

