包埋聚乙二醇的气相硅胶整体柱的制备及作用机理研究
吴倩倩,施介华,2
(1.浙江工业大学药学院,浙江杭州310012;2.浙江工业大学绿色化学合成技术国家重点实验室培育基地,浙江杭州310032)
包埋聚乙二醇的气相硅胶整体柱的制备及作用机理研究
吴倩倩1,施介华1,2
(1.浙江工业大学药学院,浙江杭州310012;2.浙江工业大学绿色化学合成技术国家重点实验室培育基地,浙江杭州310032)
以四乙氧基硅烷为单体,醋酸为催化剂,采用溶胶-凝胶法制备了包埋聚乙二醇的气相硅胶整体柱。通过探针分子的热力学参数和线性溶剂化能相关性模型对溶质分子与整体固定相之间的相互作用机理进行了深入研究。热力学参数的结果表明,在所研究的温度范围内,探针分子的lnk与1/T具有显著的线性相关性,这表明探针分子与整体固定相之间的相互作用力是恒定不变的;同时线性溶剂化能相关性的研究结果表明,探针分子与固定相之间的作用力主要包括偶极-偶极作用、氢键作用和色散作用,且顺序依次为偶极-偶极作用、氢键作用和色散作用。
硅胶整体柱;气相色谱;热力学参数;线性溶剂化能相关性
硅胶整体柱是在管内通过原位聚合而形成的具有双孔结构的新型色谱柱。硅胶整体柱大都采用烷氧基硅烷作为单体,采用溶胶-凝胶法制备而成,通过该方法制备的整体柱具有机械强度高和化学稳定性好等优点[1-3]。
在20世纪60年代末到70年代初,整体柱作为传统填充柱的替代品而出现并应用于气相色谱,那时的整体柱主要是由能够形成开放式孔结构的聚氨酯泡沫体制备而成,具有高热稳定性、低压降和较好的完整性等优点,但同时由于柱材料与管壁之间无键合作用,在加热过程中,柱材料易与管壁脱离[4]。21世纪初,Svec和他的同事们[5]将毛细管整体柱应用于现代气相色谱,他们所制备的毛细管整体柱是由聚二乙烯基苯在熔融的石英毛细管柱中制成,并使用3-(三甲基硅烷基)甲基甲烯酸丙酯对毛细管进行预处理,不仅增加了黏附性,而且使原料能与管壁形成化学键合,解决了第一代整体柱高温下易脱落的缺点。而后毛细管硅胶整体柱因其具有分离效能高、柱容量大、化学稳定性和热稳定性好等特点逐渐引起人们的注意。Korelev等人[6]的研究表明,在柱前压低于100 Bar时,其长度不能大于50 cm,在最优分离条件下,可在80 s内完成对5种轻烃类化合物的分离,提高柱前压,可将其分离时间缩短至20 s。Popova等人[7]的研究中,以HETPs为标准考察整体柱与开管柱的柱容量大小,结果表明,整体柱的柱容量每米超出开管柱30倍以上。
本研究采用四乙氧基硅烷为单体,醋酸为催化剂,制备了包埋聚乙二醇的气相硅胶整体柱,并通过对探针分子的热力学参数和线性溶剂化能相关性模型的研究,初步探讨了溶质分子与整体固定相之间的相互作用机理。
1 实验部分
1.1材料与仪器
四乙氧基硅烷(AR),购自上海五联化工厂有限公司;聚乙二醇(相对分子质量为1万,AR),购自国药集团化学试剂有限公司;冰醋酸(AR),购自杭州化学试剂有限公司;无水乙醇(AR),购自杭州龙山精细化工有限公司;实验用水,均为二次蒸馏水;其他有机试剂,均为分析纯。
85-1型磁力搅拌器,购自上海志威电器有限公司;Agilent气相色谱仪6820(FID检测器)及Agilent Cerity QA-QC色谱工作站,均购自美国安捷伦科技有限公司;石英毛细管(内径为0.53 mm i.d.),购自河北永丰锐沣色谱器件有限公司。
1.2毛细管硅胶整体柱的制备
1.2.1毛细管柱的预处理
将毛细管柱用1 mol/L的NaOH冲洗,并在70℃恒温箱中加热2 h,然后用水冲洗至中性,再用1 mol/L的HCl冲洗,接着再放入70℃恒温箱中加热2 h,然后再用水冲洗至中性,于150℃下通氮气干燥后备用。
1.2.2硅胶整体柱的制备
将0.6 g聚乙二醇和3 mL 0.3 mol/L的醋酸水溶液置于具塞圆底烧瓶中,搅拌均匀后,加入2.5 mL的无水乙醇,搅拌5 min后再加入4 mL的四乙氧基硅烷,在30℃水浴条件下搅拌1 h。接着,将此溶胶装填到毛细管柱中。柱两端严格排气密封后,放入70℃恒温箱陈化24 h。陈化好的湿柱用N2气吹扫10 h;然后,以0.5℃/min的升温速率从70℃升温至180℃,并恒温老化过夜,即可得到包埋聚乙二醇的气相硅胶整体柱。
1.2.3色谱条件
载气:N2(99.999%);流速:1.5 mL/min;分流比:50∶1;气化室温度:250℃;检测器温度:250℃。
2 结果与讨论
2.1热力学参数测定
吉布斯自由能(ΔG°)、焓变(ΔH°)和熵变(ΔS°)常用于表征色谱特征和溶质分子与固定相之间的相互作用。一般认为:ΔH°是溶质分子与固定相之间作用力大小的量度,由它们各种相互作用参数共同决定,ΔH°越大,溶质与固定相的作用越强;ΔS°反映了分配过程中溶质分子与固定相之间的有序度,对于同一种固定相来说,ΔS°主要取决于溶质分子的构型,分子排列的有序度越高,ΔS°的值就会越负。
在色谱中,热力学参数与溶质分子的保留值和柱温之间的关系可以用范特霍夫方程式来描述[8]:
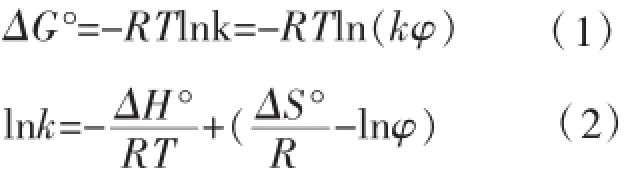
式中,R为气体常数,K为分配系数,指在一定温度下,处于平衡状态时,组分在固定相中的浓度和在流动相中的浓度之比,反映了溶质在两相中的迁移能力。k为容量因子,指在一定温度和压力条件下,组分在固定相和流动相分配平衡时,分配在固定相和流动相中的质量比。φ为相比,可定义为色谱柱中流动相体积与固定相体积之比。在本次试验中,相比约等于0.126。
本研究选取26种化合物作为探针分子,分别测定5个温度条件下的各自的容量因子k,并作lnk与1/T相关图,其结果如表1所示。结果表明,探针分子的lnk与1/T的线性相关性良好(R2>0.99),该探针分子在色谱的保留过程中,溶剂的ΔS°和ΔH°是不变的,即探针分子与固定相的作用力在所研究的温度范围内是恒定的。
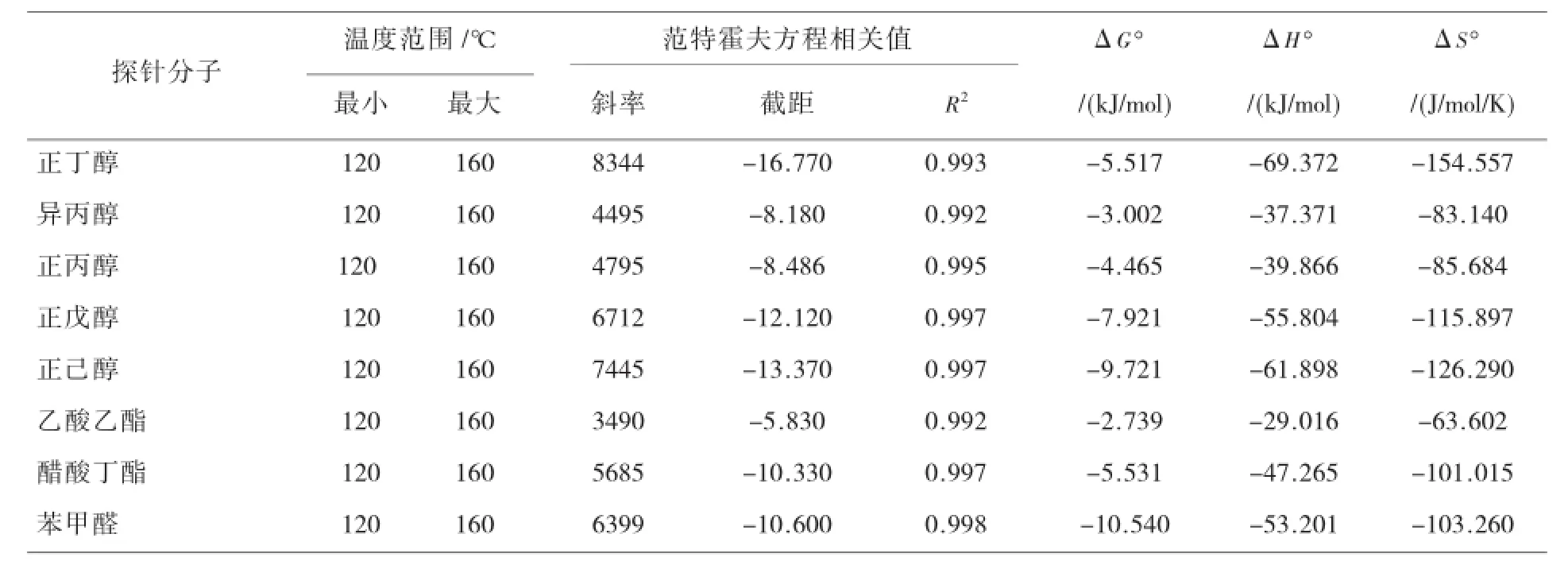
表1 探针分子的吸附热测定结果
ΔG°=ΔH°-TΔS°计算(413.15K)
从表1中可以看出,焓变是负值,表明探针分子与固定相之间的相互作用过程是放热过程,探针分子从气相转移到固定相的过程是比较稳定的;熵变是负值,表明探针分子与固定相之间的排列是有序的,不利于探针分子的保留。为确保探针分子在固定相上的保留行为,需要具有一个焓补偿的过程。而且焓变和熵变之间满足|ΔH°|>|TΔS°|,即ΔG°<0,表明探针分子的保留过程是焓驱动的过程[9]。
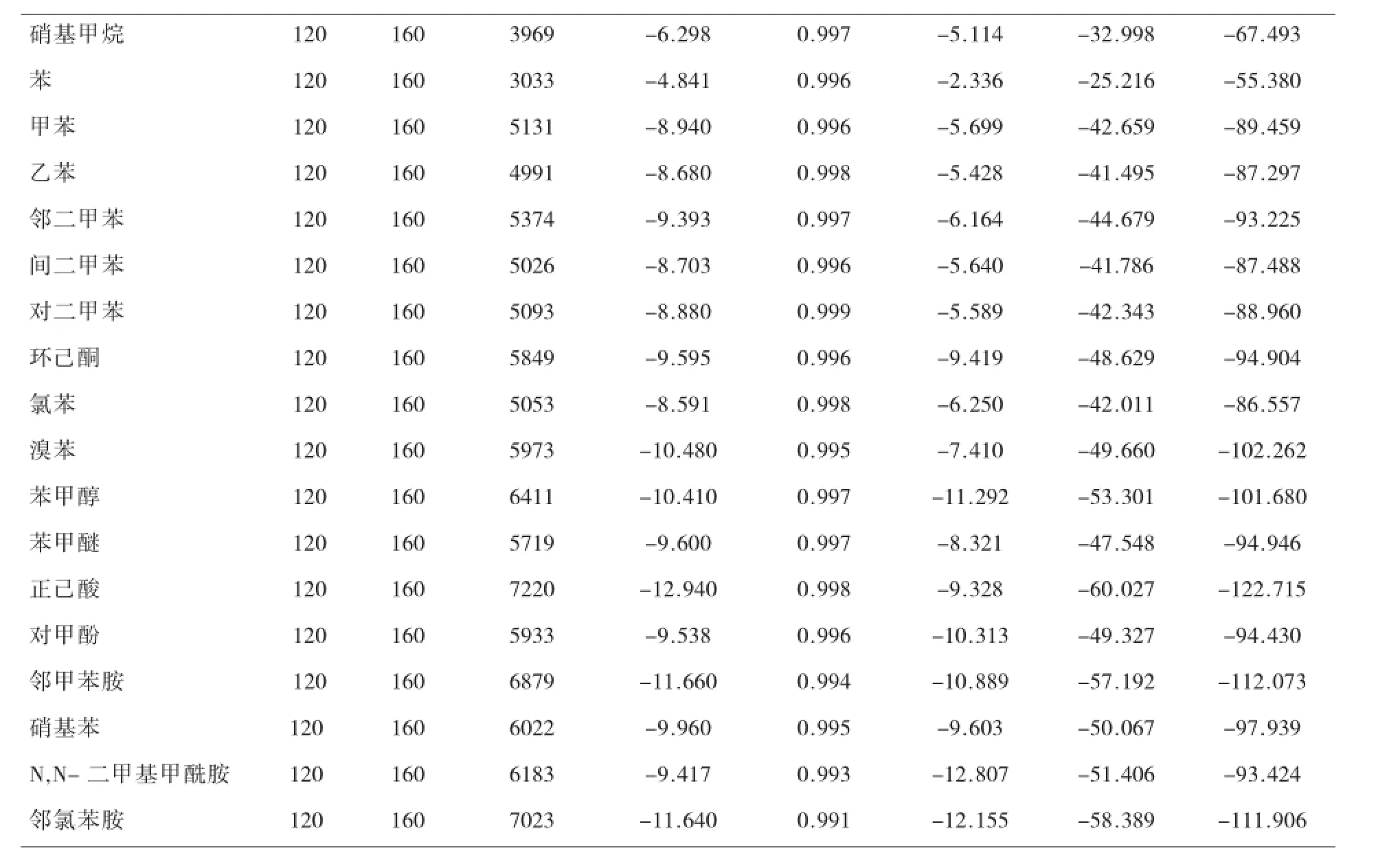
为了进一步研究探针分子在固定相上的保留机理,对探针分子的焓变和熵变的相关关系进行了分析。结果表明,26种探针分子的焓变(ΔH°)和熵变(ΔS°)之间存在良好的线性关系(图1),且统计补偿温度(slope)与平均试验温度(413.15K)存在着很大的差异,说明探针分子在该整体固定相上的保留过程中,存在着焓熵补偿行为,也就是说溶质与整体固定相之间的相互作用方式比较相似,作用机理也较为相似。
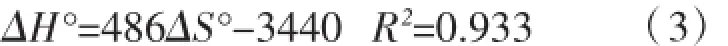
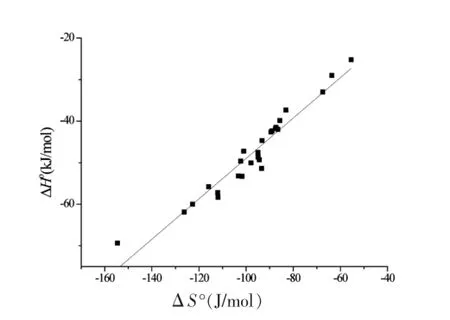
图1 不同探针分子的ΔH°与ΔS°的关系
2.2线性溶剂化能相关性
在色谱系统中,溶质与固定相之间有多种相互作用的方式,因此关于其保留机制的探讨也是一个非常复杂的过程。目前,常用的表征气相色谱固定相特征的方法主要有保留指数[10]、麦氏常数[11]及Abraham提出的线性溶剂化能相关性(LSER)模型[12]。本研究采用线性溶剂化能相关性模型对溶质与整体固定相之间的相互作用方式进行了初步探讨。
该模型可以用如下公式进行表示[13]:
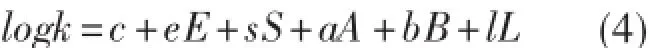
式中,E,S,A,B,L分别是溶质描述符,其中E代表溶质的孤对电子的能力;S代表溶质的偶极作用;A代表氢键酸性即给质子性;B代表氢键碱性即受质子性;L代表色散力。k为特定温度下溶质的容量因子;c是系统常数;e,s,a,b, l分别表征溶质的孤对电子的能力、偶极作用、氢键酸性、氢键碱性及色散力与固定相相互作用的能力。
本研究选用26种溶质作为探针分子,其探针分子的溶剂化描述参数[14-15]及在3个温度下的保留值,如表2所示。为了评价各个参数在LSER模型中的适用性,对探针分子的溶剂化描述符进行皮尔逊相关分析,结果见表3。从表3中可以看出,0.01的水平E和L的相关系数为0.658,表明E和L具有显著的相关性。因此,LSER模型中eE项可移除,从而使模型可以简化为:
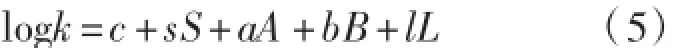
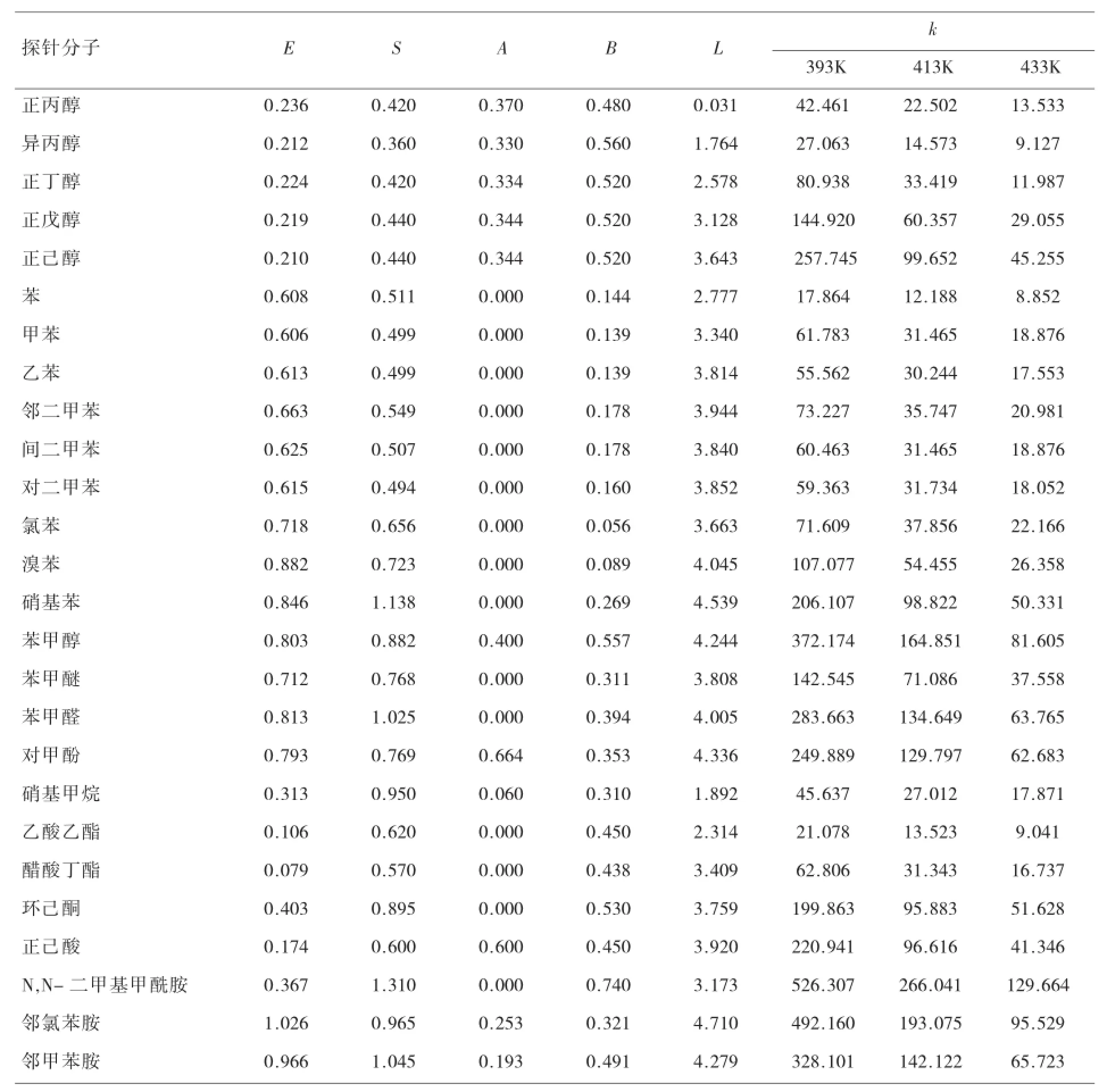
表2 探针分子的溶质描述符及保留值
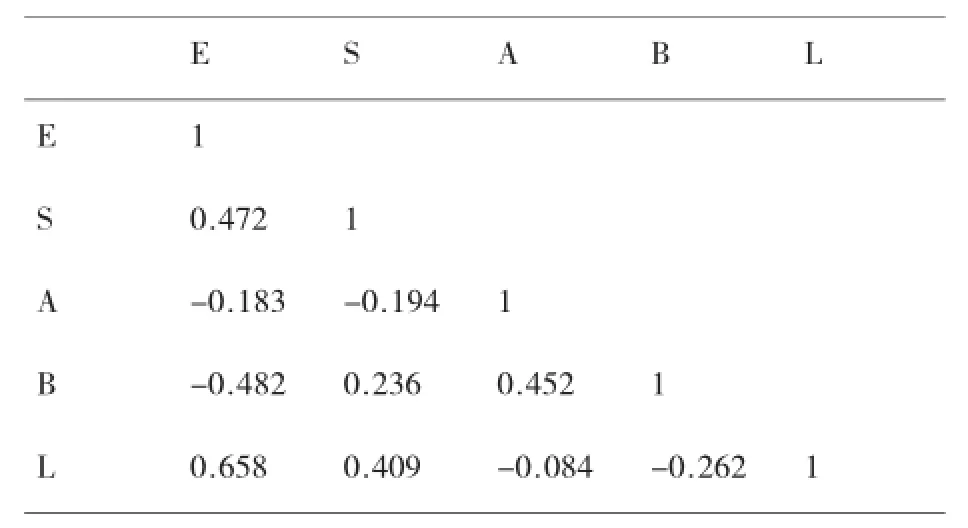
表3 溶质描述符的相关系数矩阵
然后,对logk和溶质描述符S,A,B,L进行逐步回归分析,发现logk与参数B并没有显著的线性关系。则LSER模型可进一步简化为式(6),并对logk和剩余溶质溶剂化参数进行逐步线性回归分析,结果见表4。
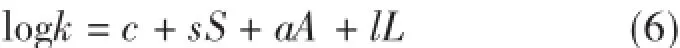
在统计学中,通常使用标准系数来解释自变量对因变量的影响程度,标准系数越大,则相应自变量对因变量的影响程度就越大。在本研究中,选用β来评估各种作用力的贡献。从表4可以看出,各参数的β值不同,表明色谱保留过程中溶质各种性质的作用力在与固定相的相互作用中贡献也不相同,主要表现为S>A>L,即溶质与固定相的相互作用力特征为偶极-偶极作用>氢键作用>色散作用。
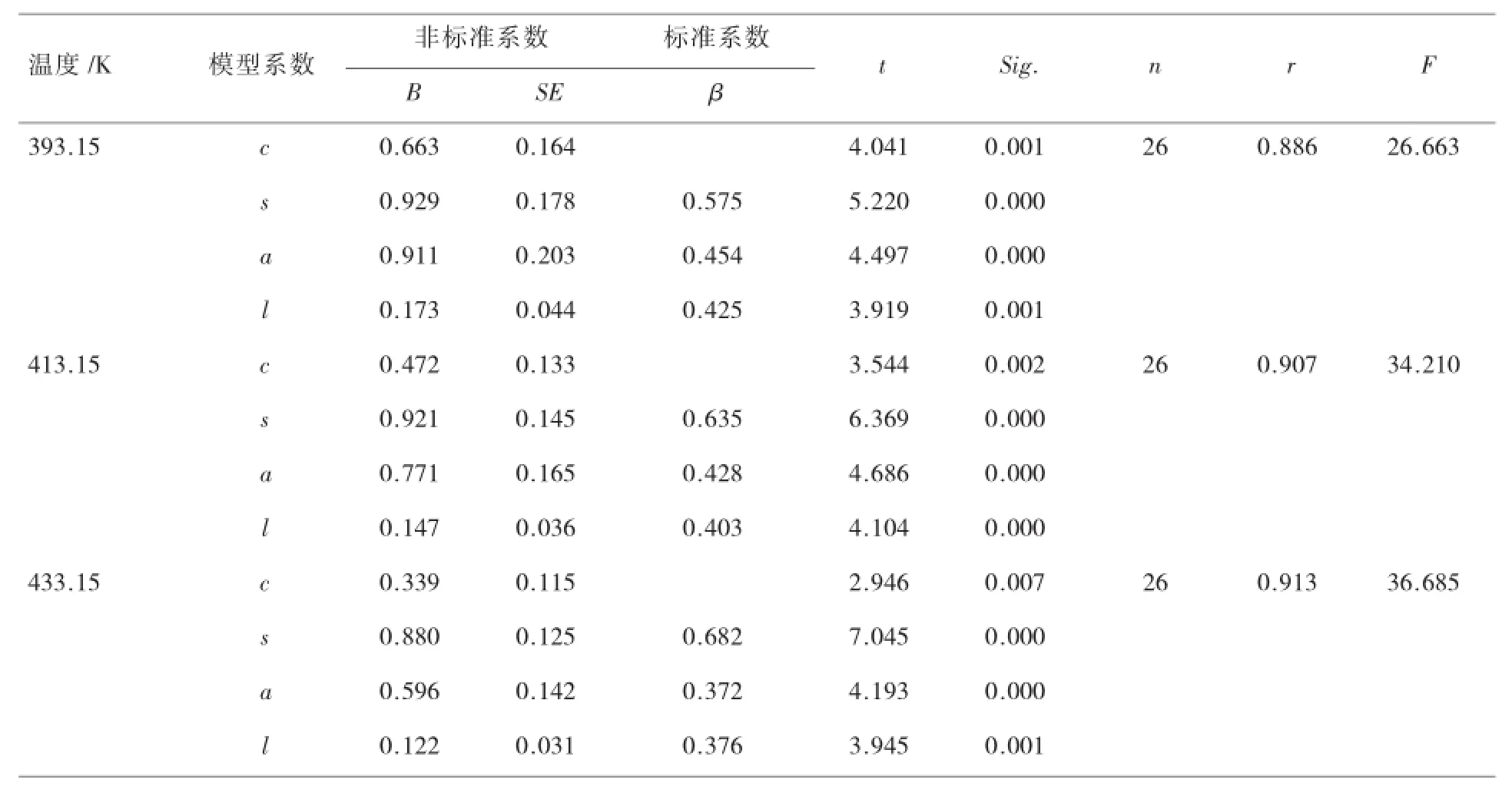
表4 固定相溶剂化参数逐一分析结果
为了评估简化后LSER模型的适用性,通过模型公式(6)计算得到的预测值logkpred和实验值logkex进行了相关分析,如图2所示。由图2可知,在所考察的温度范围内,预测值和实验值具有良好的线性关系,表明建立的LSER模型具有较好的准确性和预测能力。
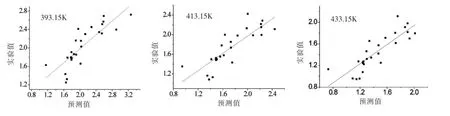
图2 理论值与实验值的关联图
3 总结
本研究采用四乙氧基硅烷作为单体,制备了包埋聚乙二醇的气相硅胶整体柱,并通过热力学参数及线性溶剂化参数的测定对探针分子与固定相之间的相互作用机理进行了阐述。通过热力学参数的测定,表明lnk与1/T之间具有显著的相关性,在研究的温度范围内,探针分子与固定相之间的相互作用力是恒定不变的,并且焓变和熵变的线性分析结果也表明了探针分子在固定相的保留是一个焓驱动的过程。线性溶剂化能相关性研究表明,该整体柱上探针分子与固定相之间的作用力主要包括偶极-偶极作用、氢键作用和色散作用,且顺序依次为偶极-偶极作用>氢键作用>色散作用。本研究为整体柱应用于气相色谱提供了理论基础,后续可以针对化合物在整体柱上的分离进行深入的应用研究。
[1]Minakuchi H,Nakanishi K,Soga N,et al.Octadecylsilylated Porous Silica Rods as Separation Media for Reversed-PhaseLiquidChromatography[J].1996(68):3498-3501.
[2]Lu J,Ye F,Zhang A,et al.Preparation and evaluation of ionic liquid-gold nanoparticles functionalized silica monolithic column for capillary electrochromatography [J].Analyst,2012,24(24):5860-5865.
[3]Rahim A A,Nofrizal S,Sssd B.Rapid tea catechins and caffeine determination by HPLC using microwave-assisted extraction and silica monolithic column[J].Food Chem,2014,147(4):262–268.
[4]Schnecko H,Bieber O.Foam filled column in gas chtomatography[J].Chromatographia,1971,4(3):109-112.
[5]D Sýkora,E C Peters,F Svec,et al.Molded porous polymer monoliths:A novel format for capillary gas chromatography stationary phases[J].Macromolecular Materials and Engineering,2000(1):42-47.
[6]A.Korolev A,P.Popova T,E.Shiryaeva V,et al.Permeability of monolithic capillary columns in gas chromatography[J].Russian journal of physical chemistry,2005(3): 457-460.
[7]A.KorolevA,P.PopovaT,E.ShiryaevaV,etal.Permeability, porosity,and structure of monolithic capillary columns in gas chromatography[J].Russian Journal of Physical Chemistry,2006,80(1):120-123.
[8]Jensen D S,Teutenberg T,Clark J,et al.Elevated Temperatures in Liquid Chromatography,Part III:A Closer Look at the van't Hoff Equation[J].LC-GC North America,2012,30(12):1052-1057.
[9]Bruno T J,Widegren J A.Enthalpy of adsorption for hydrocarbons on concrete by inverse gas chromatography [J].Journal of Chromatography A,2011,1218(28): 4474-4477.
[10]Mühlen C V,Marriott P J.Retention indices in comprehensive two-dimensional gas chromatography[J]. Analytical&Bioanalytical Chemistry,2011,401(8): 2351-2360.
[11]G.Zenkevich I,A.Makarov A.A New Application of McReynolds Constants to the Characterization of the Chromatographic Properties of Stationary Phases [J].Journal of Analytical Chemistry,2005,60(9): 845-850.
[12]PooleC F,AriyasenaTC,Lenca N.Estimation of the environmental properties of compounds from chromatographic measurements and the solvation parameter model[J].Journal of Chromatography A,2013,1317(19): 85–104.
[13]Vitha M,Carr P W.The chemical interpretation and practice of linear solvation energy relationships in chromatography[J].J Chromatogr A,2006,(1126): 143-194
[14]Abraham M H.Scales of solute hydrogen-bonding:their construction and application to physicochemical and biochemical processes[J].Chemical Society Reviews,1993(2):73-83.
[15]Poole C F,Atapattu S N,Poole S K,et al.Determination of solute descriptors by chromatographic methods [J].Anal Chim Acta,2009,652(1-2):32-53.
10.13752/j.issn.1007-2217.2015.04.006
2015-05-19

