腹腔镜切除术联合伊马替尼治疗胃肠道间质瘤的临床观察
Chaurasia Prasad Bidyanand,田夫,胡小苗 长江大学临床医学院
向进见,蒋雪峰,肖宝来,谢建平 荆州市第一人民医院普通外科,湖北 荆州434000
胃肠道间质瘤(Gastrointestinal Stromal Tumors,GIST)是一种起源于胃肠道壁Cajal细胞的间叶源性肿瘤,发病率较低,约为(14~20)/百万。中老年人是高发人群,50岁以下人群患病比较少见,无明显性别差异[1]。GIST多数发生于胃和小肠,约占80%以上,结直肠、食道较少,肠系膜、网膜及后腹膜罕见。组织学上GIST有上皮样细胞、偶或多形性细胞及梭形细胞组成,依据细胞的形态可将其分为3类:梭形细胞和上皮细胞混合型(约10%)、上皮细胞型(约20%)、梭形细胞型(约70%)。临床上一般将肿瘤大小、肿瘤部位、异常有丝分裂数和术中破裂情况作为比较可靠的预后指标[2]。现在的治疗方法有手术、辅助治疗及新辅助治疗的个体化治疗方案[3,4]。外科手术切除是临床治疗GIST的首选方式[5],但是单纯的手术不能给患者带来良好的预后。腹腔镜下间质瘤切除手术已较多用于临床,与传统开腹手术相比,前者能否达到后者手术安全性及根治度,甚至在其他方面超越后者,仍是目前研宄的重点与热点[6]。酪氨酸激酶抑制剂甲磺酸伊马替尼是一种新型的分子靶向制剂[7],它的应用改变了GIST的治疗现状。研究证实,伊马替尼能有效缓解GIST患者的病情,改善预后,在中危和高危的间质瘤术后患者中,也能显著改善生存预后,降低肿瘤复发率[8]。本研究选取2010年1月至2012年10月在我院治疗的胃肠道间质瘤患者70例,对照组患者(35例)只接受手术治疗,研究组患者(35例)在术后接受甲磺酸伊马替尼治疗,观察两组患者的临床疗效,探讨影响预后的因素,现报道如下。
1 对象与方法
1.1 对象
选取2008年1月至2012年10月入住我院的胃肠道间质瘤患者,所有患者均接受根治性腹腔镜切除术治疗。纳入标准:①经免疫组织化学和组织形态学确诊为胃肠道间质瘤,CD117阳性,肿瘤完全切除且切缘阴性者。②改良NIH危险度分级为中危或高危患者。③年龄大于18岁,无严重术后并发症者。④术前未接受任何化疗或放疗。⑤EcoGPs评分≤2分。排除标准:①术前接受舒尼替尼等靶向药物治疗者。②心、肝、肾等重要器官功能障碍者。共纳入研究70例,其中男性33例,女性37例。年龄33~76岁,平均年龄(58.5±10.5)岁。临床症状:消化道出血、腹部包块、腹痛、肠梗阻等。本研究经过我院道德理论委员会批准且所有患者知情并签署知情同意书。
1.2 分组
根据随机原则将所有患者统一编号,用计算机随机选数,研究组和对照组各35例。研究组术后给予伊马替尼辅助治疗,对照组患者仅接受手术治疗。
1.3 治疗方法
1)手术方法 常规消毒、铺巾,穿刺建立二氧化碳气腹,气腹压为10~14mmHg,根据手术需要及时调整患者体位。Trocar穿刺部位按常规并结合术中需要完成。为避免肿瘤种植,去气腹前应注意彻底冲洗腹盆腔,移出标本时均需用取物袋保护切口。对于胃底部肿瘤直径>5cm,且贴近胃贲门区的肿瘤,经直视定位后,采用腹腔镜辅助近端胃切除术。对于胃底部及胃大、小弯处直径<5cm的胃间质瘤,经直视定位后,应用超声刀游离目标区域及周围韧带,采用腹腔镜切割吻合器进行胃部分切除术,延长左上腹主操作孔穿刺套管切口后取出标本。术中充分游离胃段血管及切断胃左动、静脉,在贲门上1cm切断食管,延长左上腹穿刺套管切口长度和肿瘤直径相仿,将近端胃提出体外,距肿瘤2cm外采用直线切割器切断胃组织并移除标本,然后选择Orvil吻合系统进行食管胃吻合。
2)服药方法 研究组患者在术后1个月左右服用甲磺酸伊马替尼(瑞士诺华制药公司提供),用法为每日1次,每次剂量为400mg,连续服用,最短者服用12个月,最长者服用24月,平均18个月。服药开始时患者无肿瘤复发或转移的影像学证据,且无明显治疗禁忌证。
1.4 随访
采用门诊复诊和电话方式随访,术后随访2年,每6个月随访1次。随访时进行血液学、腹部CT扫描和肝脏B超等检查,分析患者肿瘤大小、异常有丝分裂数、危险程度分级等因素对于预后的影响。两组患者最长随访24个月,最短随访6个月,平均随访18个月。
1.5 统计学分析
采用SPSS14.0统计软件包进行分析,计量资料用(±s)表示,采用t检验,计数资料采用χ2检验,采用Kaplan-Meier法及log-rank检验分析患者生存情况,采用Cox比例风险模型进行多因素分析,同时计算95%置信区间。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者病理学特点及无复发生存率估计
两组患者一般资料与临床病理学特点比较差异无统计学意义(P>0.05),见表1。研究组和对照组患者1年无复发生存率分别为100%和82.9%(95%CI 71.4%~97.1%),2年无复发生存率分别为94.3%(95%CI 85.0%~100%)和62.9%(95%CI 42.9%~80.0%),术后使用伊马替尼辅助治疗能明显延长患者无复发生存时间(log-rank,P=0.003;HR=0.143,P=0.005)。见表1。
2.2 腹腔镜切除术联合伊马替尼对中危或高危患者复发转移率影响
两组患者最长随访24个月,最短随访6个月,中危患者中,研究组无1例肿瘤复发转移,对照组有5例(11.4%)出现肿瘤复发转移,两组无复发生存率无明显差异(log-rank,P=0.059;HR=0.021,95%,CI0.00~26.8,P=0.435)。高危患者中,研究组2例(5.7%)出现复发转移,对照组有13例(37.1%)出现肿瘤复发转移,两组无复发生存率差异显著(log-rank,P=0.029;HR=0.0225,95%,CI0.00~73.8,P=0.045)。
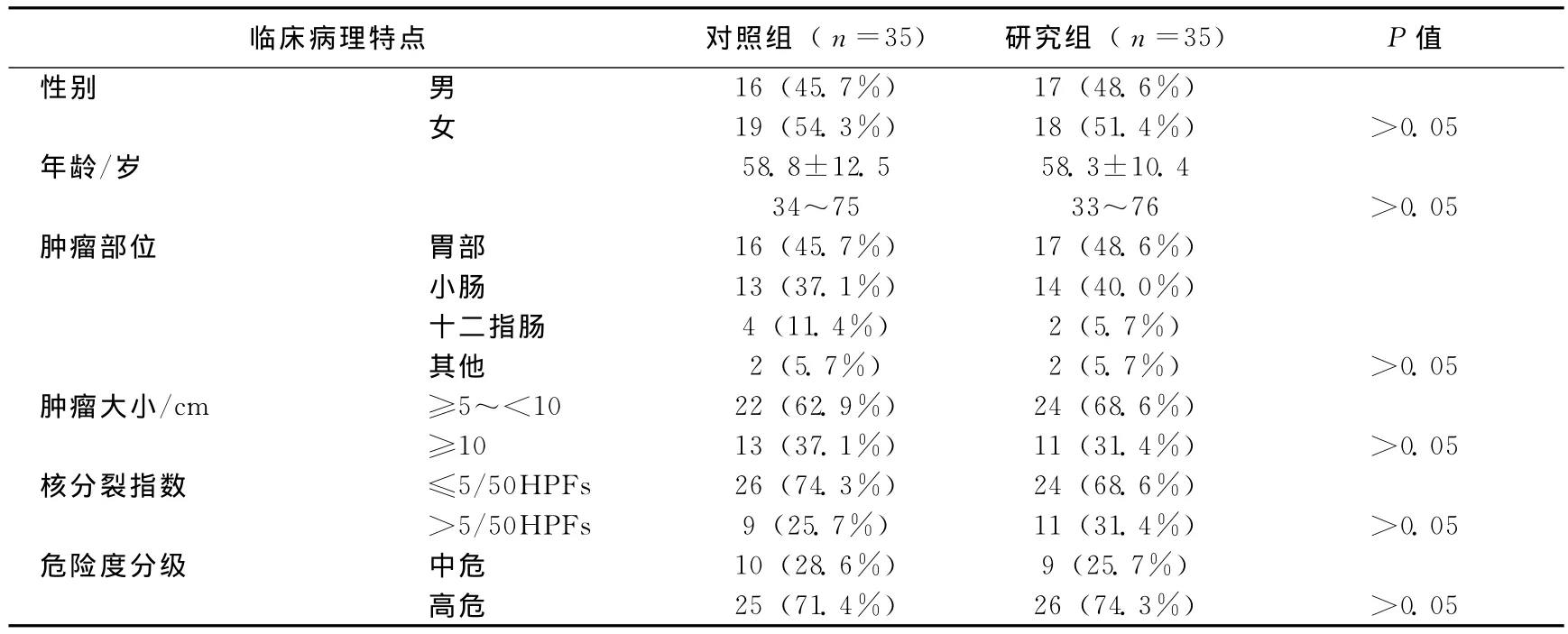
表1 两组患者临床病理学特点
2.3 胃肠道间质瘤患者临床特征单因素生存分析
采用COX风险比例模型对可能影响患者预后的因素进行单因素分析,结果显示,年龄、性别和肿瘤部位对存活率无影响(P>0.05),肿瘤大于10cm、有丝分裂数>5/50HPFs、高危、伊马替尼辅助治疗是影响患者预后的因素。见表2。
2.4 胃肠道间质瘤患者预后的多因素分析
将上述单因素分析中有统计学意义的各因素行COX回归分析,示危险度、肿瘤大小、有丝分裂数和伊马替尼辅助治疗是影响预后的独立性因素。见表3。
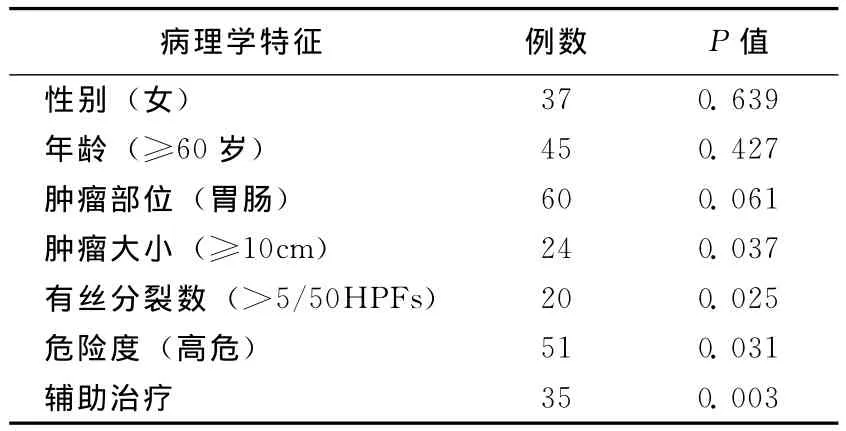
表2 胃肠道间质瘤患者临床特征单因素生存分析
3 讨论
一般认为,胃肠道间质瘤是一种恶性肿瘤,其恶性程度根据异常有丝分裂数目和肿瘤大小分为低、中、高。GIST可发生于胃肠道的任何部位,是最常见的消化道间叶肿瘤,占胃肠道恶性肿瘤的1%~3%。本研究中患者年龄多在50岁以上,平均年龄(58.5±10.5)岁,男女比例为1∶1.12,与文献报道一致[9]。临床上一般将肿瘤大小、肿瘤部位、异常有丝分裂数和术中破裂情况作为比较可靠的预后指标。
手术治疗是胃肠间质瘤首选的治疗方法,但手术一般仅用于一些原发的、低危、局限的的胃肠间质瘤,对于中危或高危患者术后复发率较高,复发时间多在术后第18~24个月[10]。接近90%的GIST患者存在KIT或PDGFR突变,酪氨酸激酶抑制剂伊马替尼恰恰可以抑制KIT,从而抑制肿瘤细胞的增殖,2001年,Joensuu率先使用甲磺酸伊马替尼成功治疗胃肠间质瘤[11],从此GIST的治疗便进入了分子靶向治疗时代。伊马替尼对转移性或不可切除间质瘤效果较好,能够稳定疾病的进展,延长患者的生存时间。GIST的标准治疗是肿瘤能被完全切除,但较高的术后复发率表明手术不可能完全治愈GIST。因此,手术联合伊马替尼来治疗GIST备受肿瘤学专家的重视。国外有超过50%患者使用伊马替尼治疗效果显著,有75%~85%患者达到稳定期,手术联合伊马替尼治疗约70%的转移性SIST患者效果明显,优于传统的放疗和化疗[12]。我国16家医院对GIST应用手术联合伊马替尼治疗的多中心临床研究中指出[13],对于有复发转移等高风险患者,术后给予伊马替尼能够降低肿瘤转移和复发率。本研究采用美国国立卫生研究院(NIH)制定的危险度分级法,NIH危险度分级是目前临床应用最广泛最合理的预测GIST患者术后复发的方法,得到临床大多数专家认可。其将GIST患者分为高危、中危、低危和极低危。本研究运用NIH分级,对纳入研究的中危和高危GIST患者回顾性分析,研究组患者长期服用甲磺酸伊马替尼,剂量是400mg/d,结果显示,研究组和对照组患者1年无复发生存率分别为100%和82.9%(95%CI 71.4%~97.1%),2年无复发生存率分别为94.3%(95%CI 85.0%~100%)和62.9%(95%CI 42.9%~80.0%),术后使用伊马替尼辅助治疗能明显延长患者无复发生存时间(log-rank,P=0.003;HR=0.143,P=0.005)。中危患者中,研究组无1例肿瘤复发转移,对照组有5例(11.4%)出现肿瘤复发转移,两组无复发生存率无明显差异(log-rank,P=0.059;HR=0.021,95%,CI0.00~26.8,P=0.435)。高危患者中,研究组2例(5.7%)出现复发转移,对照组有13例(37.1%)出现肿瘤复发转移,两组无复发生存率差异显著(log-rank,P=0.059;HR=0.021,95%,CI0.00~26.8,P=0.435),伊马替尼对高危患者辅助治疗的效果较明显。

表3 胃肠道间质瘤患者预后的多因素分析
De Matteo等[14]采用随机、双盲、安慰剂对照的研究方法,对644例原发GIST的患者采用手术联合伊马替尼的方法治疗。结果表明,术后使用伊马替尼辅助治疗1年的患者,1年的无复发生存率显著优于安慰剂组,且药物不良反应较小,耐受性较好。Gold等[15]通过对119例GIST复发转移的患者进行研究,并对患者存活率与影响因素分析后发现,肿瘤的大小和有丝分裂对GIST患者术后的存活率有明显的影响。临床上一般将肿瘤大小、肿瘤部位、异常有丝分裂数和术中破裂情况作为比较可靠的预后指标[2]。本研究采用COX风险比例模型对可能影响患者预后的因素进行单因素分析,结果显示,年龄、性别和肿瘤部位对存活率无影响(P>0.05),肿瘤大于10cm、有丝分裂数>5/50HPFs、高危、伊马替尼辅助治疗是影响患者预后的因素。胃肠道间质瘤患者预后的多因素分析,显示危险度、肿瘤大小、有丝分裂数和伊马替尼辅助治疗是影响患者预后的独立性因素。综上所述,笔者认为,腹腔镜切除术联合伊马替尼治疗GIST,大多数患者症状改善的同时,肿瘤也得以有效的控制,显著提高其无复发生存率,治疗效果在高危患者中最为明显。
[1]De Vogelaere K,Hoorens A,Haentjens P,et al.Laparoscopic versus open resection of gastrointestinal stromal tumors of the stomach [J].Surg Endosc,2013,27(5):1546~1554.
[2]Melstrom L Q,Phillips J D,Bentrem D J,et al.Laparoscopic versus open resection of gastric gastrointestinal stromal tumors[J].Am J Clin Oncol,2012,35(5):451~454.
[3]Blay J Y.New paradigms in gastrointestinal stmmal tumour management [J].Ann Oneol,2009,20(Suppl 1):18~24.
[4]张云,曹晖 .分子靶向治疗胃肠间质瘤的进展 [J].中华消化外科杂志,2009,8(6):478~480.
[5]Miettinen M,Lasota J.Histopathology of gastrointestinal stromal tumor [J].J Surg Oncol,201l,104(8):865~873.
[6]吴红华,董梅珍 .罗哌卡因局部浸润联合多瑞吉贴膜对腹腔镜胆囊切除术后的镇痛效果及安全性评价 [J].实用药物与临床,2014,17(3):302~304.
[7]燕玮,杨威 .达沙替尼应用于伊马替尼耐药的慢性粒细胞白血病的研究进展 [J].实用药物与临床,2012,15(2):108~110.
[8]箫岗,牟一平,陈灵华,等 .腹腔镜治疗胃间质瘤的体会 [J].中华普通外科杂志,2011,26(1):64~65.
[9]Heath E I,Infante J,Lewis L D,et al.A randomized,doubleblind,placebo-controlled study to evaluate the effect of repeated oral doses of pazopanib on cardiac conduction in patients with solid tumors[J].Cancer Chemother Pharmaeol,2013,71(3):565~573.
[10]寿春晖 .伊马替尼术后辅助治疗中危或高危胃肠道间质瘤研究 [D].杭州:浙江大学,2011.
[11]Joensuu H,Roberts P J,Sarlomo-Rikala M,et al.Effect of the tyrosine kinase inhabitor STI571in a patient with a matastatic gastrointestinal stromal tumor[J].N Eng J Med,2001,344(14):1052~1056.
[12]Popping D M,Elia N,Marret E,et al.Protective effects of epidural analgesia on pulmonary complications afterabdominal and thoracic surgery:a meta-analysis[J].Arch Surg,2008,143(10):990~1000.
[13]Heinrich M C,Corless C L,Demetri G D,et al.Kinase muta-tions and imatinib response in patients with metastatic gastrointestinal stromal tumor[J].Clin Oncol,2003,21(23):4342~4349.
[14]Dematteo R P,Owzar K,Antoneseu C R,et al.Efficacy of afjucant imatinib mesylate following complete resection of localized,primary gastrointestinal stromal tumor(GIST)at high risk of recurrence:the US Intergroup phaseⅡtrial ACOSOC Z9000[C].American Society of Clinical Oncology,2008.
[15]Gold J S,Van Der,Zwan S M,et al.Outcome of metastatic GIST in the era before tyrosine kinase inhibitors [J].Ann Surg Oncol,2007,14:134~142 .

