镁、铝合金的腐蚀与防护
马安博
(西安航空职业技术学院,陕西西安710089)
自然界绝大多数的物质都有变成氧化物或是形成稳定化合物的倾向,除了金、铂等贵金属外,自然界中甚少有纯金属存在。因此,从矿石或是氧化物中提炼完成所需的工程材料,例如:铁、铜、铝、镁时,它们就开始有了回归到稳定状态的趋势,在环境许可下,它们会再度变为金属化合物,这种现象可认为是发生腐蚀的基本原因。这些环境的基本因素有:水分、温度,或是酸、碱、盐等化学物质。
腐蚀危害遍及日常生活和几乎所有行业,包括冶金、化工、能源、矿山、交通、机械、航空航天、信息、农业、食品、医药、海洋开发、基础设施等。因此研究与解决金属腐蚀问题与防止污染、减轻公害、保证人类健康生存等密切相关。腐蚀给人们带来了巨大的经济损失,造成了灾难性的事故,消耗了宝贵的自然资源。
1 腐蚀的定义
有关腐蚀的定义有不同的说法。埃文斯认为:金属腐蚀是金属从元素态转变为化合态的化学变化及电化学变化。方坦纳认为:金属腐蚀是金属冶金的逆过程(图1 示)。尤力格认为:物质(或材料)的腐蚀是物质(或材料)受环境介质的化学、电化学的作用而被破坏的现象[1]。目前,一致认可的定义是:材料腐蚀是材料受其周围环境介质的化学、电化学和物理作用下引起失效破坏的现象。金属腐蚀是金属与周围环境(介质)之间发生化学或电化学作用而引起的破坏或变质,如铁在自然界的腐蚀。非金属腐蚀是非金属材料由于在环境介质的化学、机械和物理作用下,出现老化、龟裂、腐烂和破坏的现象(图2 示)。如涂料和橡胶由于阳光(老化)和化学物质作用引起开裂、鼓泡等现象。这是由于化学键在紫外线作用下断裂而导致失效。
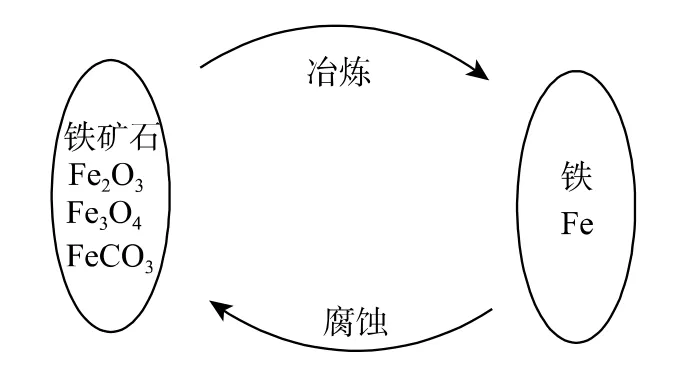
图1 金属腐蚀与金属冶金的关系Fig.1 Relationship of metal corrosion and metallurgy

图2 材料腐蚀与环境因素的关系Fig.2 Relationship of corrosion and environmental factors
人类很早都开始了对腐蚀及防护技术的研究。早在两千多年前,我们中华民族就创造了与现代铬酸盐(或重铬酸盐)钝化处理相似的防护技术。金属腐蚀现象的解释是首先从金属的高温氧化开始的。16 世纪50年代,俄国科学家罗蒙诺索夫指出,没有外界空气进入,烧灼过的金属重量仍保持不变,并证明金属的氧化是金属与空气中最活泼的氧气所致。1830年,德拉李夫在有关锌的硫酸溶液的研究中,第一次明确地提出了有关腐蚀的电化学特征的观点(微电池理论)。1881年,卡扬捷尔研究了酸金属溶解的电化学本质。20 世纪初确立了腐蚀历程的基本电化学规律。我国的腐蚀与防护科技工作是在新中国成立之后获得了很大的发展[2]。
2 腐蚀的基本原理
2.1 电化学腐蚀原理
金属材料与电解质溶液相互接触时,在固/液相界面上将发生有自由电子参加的氧化还原反应,导致接触面处的金属变为金属离子、络合离子而溶解或者生成氢氧化物和氧化物等稳定化合物,从而破坏了金属材料的性能,这个过程称为电化学腐蚀。腐蚀原电池的工作原理如图3 示[3]。

图3 腐蚀原电池示意图Fig.3 Schematic diagram of galvanic corrosion
产生电子的反应叫氧化反应;消耗电子的反应叫还原反应。由此可见,腐蚀原电池实质上是一个短路原电池,即电子回路短接,电流不对外做有用功,且只能导致金属材料的破坏。一个腐蚀电池必须包括阳极、阴极、电解质溶液和外电路四部分。
2.2 高温氧化和热腐蚀
金属的高温腐蚀是金属在高温下与环境中的氧、硫、氮、碳等发生反应导致金属的变质或破坏的过程。由于金属腐蚀是一个金属失去电子的氧化过程,因此金属的高温腐蚀也常常广义地被称为高温氧化。热腐蚀是指金属材料在高温工作时,基体金属与沉淀在表面的熔盐(主要为Na2SO4)及周围气体发生的综合作用而产生的腐蚀现象;金属发生热腐蚀的特征如图4 所示[4]。腐蚀产物的外层为疏松的氧化物和熔盐;次内层为氧化膜;氧化膜下为硫化物。

图4 金属热腐蚀示意图Fig.4 Schematic diagram of metal thermal corrosion
根据产生热腐蚀的温度不同,可将它分为高温热腐蚀和低温热腐蚀两类。高温热腐蚀是指温度超过盐膜的熔点的热腐蚀,此时沉积的盐膜处于熔融状态,通过氧化膜的裂纹和孔硫化基体金属,加速金属的氧化,其典型的纤维组织是由于形成硫化物而耗尽基体中参与反应的元素。低温热腐蚀是指发生在温度低于盐膜熔点的热腐蚀。这时虽然从温度上盐膜未达到熔点,但是由于金属的硫化物的熔点较低,容易生成熔点更低的金属-金属硫化物共晶体,同样使表面局部盐膜成为熔融状态,加速了腐蚀。
3 铝镁合金微弧氧化对耐蚀性能的影响
对镁铝合金的防腐保护包括表面改性和防护性膜层或涂层。表面改性主要是指离子注入和激光处理两种方法;防护性的膜层或涂层包括电沉积涂层、转化膜、阳极极化、氢化物涂层、有机涂层和气相沉积[5]。
下面以镁合金为例,在以镁合金为主耗材之一的轻量化制造已引起相关产业高度关注,但由于镁的电极电位很低,在潮湿气氛中与其它高电位金属接触时,极易产生接触腐蚀,而镁合金的电极电位更低,更易产生腐蚀[6];同时,由于金属表面不平整,存在由杂质构成的阴极相,因此在潮湿的气氛中极易发生电化学反应,形成点腐蚀,所以镁合金在生产实践中的应用受到很大限制。镁合金作为结构材料或壳体材料时,不可避免要与其它金属材料相接触,发生连接腐蚀,必须采取可靠的表面防护措施。
通常所说的接触腐蚀就是指连接腐蚀,即在腐蚀介质环境(可以为大气、电解液、潮湿环境等)下,材料由于接触致使材料失去原有的性能与表面形态所形成的腐蚀。接触腐蚀中基体材料与附着物或不同电位材料的直接接触或电连接,形成电偶对或形成狭窄缝隙是接触腐蚀的前提条件。按照腐蚀机理来分,接触腐蚀包含电偶腐蚀、缝隙腐蚀以及电偶腐蚀与缝隙腐蚀共同作用三种情况。
由于镁合金中通常含有较多电极电位较高的重金属等组元(特别是Fe、Cu、Ni),而且镁及其合金在实际应用中经常与其它高电位金属(如钢、铜等)接触,产生缝隙或电极电位差,易形成腐蚀电池,发生电偶腐蚀或缝隙腐蚀。实际应用中常常忽视镁合金组合件的电偶腐蚀而造成的灾难性破坏已成为镁合金结构应用的障碍。例如,在海洋环境中,电偶腐蚀除了可加速镁合金构件腐蚀外,还可诱发点蚀、缝隙腐蚀、应力腐蚀等工程中更严重的腐蚀破坏。通常镁基体中与阴极相邻的局部区域都会产生严重腐蚀,阴极可能是外部与镁合金相接触的其它金属,也可能是镁合金内的第二相或杂质。在盐水环境中,通过严格控制杂质含量如Fe、Ni、Cu及Fe-Mn 比可以减轻内部腐蚀,提高镁合金抗腐蚀性能。
为了避免镁合金发生严重的接触腐蚀,必须采取如下措施:(1)选择与镁电化学相容的异金属或在镁基体上镀一层与镁电化学相容的金属;(2)采用适当的表面处理对镁和异金属进行保护;(3)异金属加绝缘的垫圈或填充填料,避免出现封闭回路;(4)设计合理的结构,避免“大阴极小阳极”的结构;(5)在封闭化合物或底漆中加入铬酸盐,抑制微电池作用。
目前采取的防腐措施主要是通过微弧氧化工艺处理镁、铝合金制品,使其表面生成一层与基体以冶金方式结合的氧化镁或氧化铝为主的陶瓷层,陶瓷制的高硬度、高阻抗和高稳定性满足镁合金抗高温腐蚀、连接(电偶)腐蚀、擦伤腐蚀及铝合金防海水腐蚀、高温热蚀和改善耐磨等性能要求。
[1]肖纪美,曹楚南. 材料腐蚀学原理[M]. 北京:化学工业出版社,2002.
[2]何业东,齐慧滨. 材料腐蚀与防护概论[M].北京:机械工业出版社,2005.
[3]赵麦群. 金属的腐蚀原理与测试技术[M]. 机械工业出版社.
[4]王登峰. 高电位镁牺牲阳极的研究[D]. 太原理工大学硕士学位论文,2006.
[5]张荣发,单大勇,陈荣石,等. 微弧氧化在提高镁合金耐蚀性上的应用[J]. 材料工程,2007.
[6]张志富. 镁合金的腐蚀与防护的研究[D]. 西北工业大学硕士学位论文,2004.

