高选择性位阻胺脱硫剂的研制及性能测试
郭晓丹,诸林,焦文超,陈倬
高选择性位阻胺脱硫剂的研制及性能测试
郭晓丹,诸林,焦文超,陈倬
(西南石油大学化学化工学院,四川成都 610500)
以环氧氯丙烷和浓盐酸为原料通过开环反应制备中间产物1,3-二氯-2-丙醇,将该产物与叔丁胺通过亲核取代反应合成可用于气体脱硫的位阻胺1,3-二叔丁胺基-2-丙醇(DTBP),并用红外谱图(IR)及核磁共振氢谱(1H NMR)对其进行了结构表征。采用单因素变量法对反应条件进行优化,研究表明,以100%无水乙醇为反应介质,当1,3-二氯-2-丙醇与叔丁胺的摩尔比为1∶3,反应温度为140℃,反应时间为3h时,所制得的DTBP产率最高,为92.3%。脱硫性能测试结果表明:在相同的实验条件下,DTBP溶液的H2S脱除率及吸收选择性均优于-甲基二乙醇胺(MDEA)溶液。
位阻胺;选择性脱硫;合成;优化;评价
油气田采出的天然气及炼厂气都须经过脱硫处理后才能得到应用[1-2]。对于高CO2/H2S比的工业气体,如果能进一步提高脱硫剂的H2S吸收选择性,必将使溶剂循环量减小,设备投资及操作费用降低,因此开发选择性更高的脱硫剂具有重要的现实意义[3-4]。
我国天然气工业应用最广泛的选择性脱硫剂是-甲基二乙醇胺(MDEA),但对CO2/H2S较高的工业气体的选择性脱硫效果不太理想[5]。针对此情形20世纪末国内外展开了对空间位阻胺脱硫剂的研究,这类脱硫剂酸气负荷、净化度及选择性等关键指标均优于MDEA,但合成条件苛刻且成本较高的缺点限制了其工业推广[6]。近年来国内外对于高选择性脱硫剂的研究多见于以MDEA为基础的配方溶液,而对于基础脱硫剂的研制则较少[7]。
本工作以研制合成方法简单、原料易得、水溶性良好和选择性高的位阻胺脱硫剂为出发点进行研究,制备既可以单独使用也可以与其他脱硫剂复配使用的高效脱硫剂。
1 分子设计思路
空间位阻胺是氨基(—NH2)上的氢原子被体积较大的烷基或其它基团取代后形成的胺类化合物的统称[8-9]。研究表明,当—NH2引入基团的位阻系数大于1.74时,空间位阻胺的H2S吸收选择性会大大提高[10],且空间位阻系数越大,位阻胺的选择性越高[11-12]。基于以上认识,本工作力图设计一种在分子链两端各有一个空间位阻基团的醇胺,一方面提高位阻胺的选择性,同时保证其水溶性。
结合分子设计原理及参考文献[13-15],以环氧氯丙烷和浓盐酸为原料合成中间产物1,3-二氯-2-丙醇,通过在1,3-二氯-2-丙醇分子两端引入位阻系数较大的叔丁基,制备含有两个位阻基团的高选择性空间位阻胺1,3-二叔丁胺基-2-丙醇,其合成路线如式(1)、式(2)。
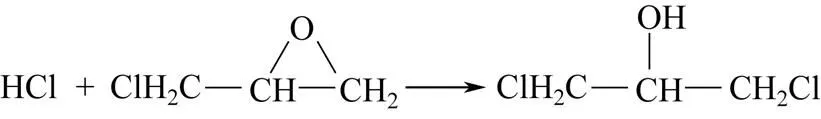
(2)
2 实验部分
2.1 试剂与仪器
叔丁胺、浓盐酸、环氧氯丙烷、NaOH、乙酸乙酯(EA)、无水乙醇,无水硫酸镁,均为分析纯,成都科龙化工试剂厂;MDEA(CP级),中国石油西南油气田分公司天然气研究院。
优普UPH超纯水器,西安优普仪器设备有限公司;高温高压反应釜CWYF-3,威海市正威机械设备有限公司;旋转蒸发仪R201D,巩义市予华仪器有限公司;红外光谱仪WQF-520型,北京瑞利分析仪器有限公司;核磁共振仪400MHZ,瑞士布鲁克斯公司;气体检测仪MOT500-H2S,深圳科尔诺电子科技有限公司;模拟脱硫装置,实验室自行搭建。
2.2 合成步骤
以分子设计思路为依据制备1,3-二叔丁胺基-2-丙醇(DTBP),实验装置流程及合成步骤如图1。
1—三口烧瓶反应装置;2—分液漏斗;3—高温高压反应釜;4—回流装置
(1)在装有磁子、温度计、滴液漏斗和回流管的250mL三口烧瓶1中加入50mL浓盐酸,将烧瓶置于恒温磁力水浴锅中,在30℃下缓慢滴加45mL环氧氯丙烷,控制滴加时间为0.5h;滴加完毕后升温至45℃,继续反应2h。将反应后溶液冷却至室温,并转移至分液漏斗2中;保留上层有机相,经干燥处理后得到无色透明状液体1,3-二氯-2-丙醇[16]。
(2)将上述制备的1,3-二氯-2-丙醇和叔丁胺以摩尔比为1∶3,投入装有反应介质(反应物总量的100%)的反应釜3内(控制反应釜的搅拌速度为200r/min),在140℃下自压反应3h;待反应结束后,将冷却至65℃的反应液倒入单口烧瓶4中,并加入一定量的NaOH溶液(NaOH与1,3-二氯-2-丙醇的摩尔比为2∶1),在70℃下回流反应0.5h;然后将反应后的溶液冷却至室温并用分液漏斗分出上层有机相,下层液用EA萃取2次;将萃取液与有机液混合,经无水硫酸镁干燥处理后,用旋转蒸发仪减压蒸馏,最后冷却结晶可得淡黄色针状固体。
2.3 表征与评价
对在最佳反应条件下合成的目标产物用WQF-520型红外光谱仪和核磁共振仪进行表征。
用室内脱硫装置进行脱硫剂性能测试[3],流程见图2。含一定比例N2、H2S和CO2混合气体6经钢瓶减压后,在采样阀7处分析气体组成,由压差计3计量其压力,由流量计2控制气体流量,混合气体进入一个装有一定量的待评吸收剂的吸收器1中鼓泡吸收。吸收一定时间后,在吸收器上出口采样阀4处做尾气分析;关闭气源,旋开吸收器下出口三通考克5,从9处采集富液样作液相分析。气相H2S含量用快速管法[17]测定,液相中的H2S含量使用经典的碘量法进行测定。
1—吸收器;2—流量计;3—压差计;4—尾气采样阀;5—三通考克; 6—进气;7—进气采样阀;8—尾气;9—富液
(1)当原料气H2S为2.35%(为体积分数),CO2为53.0%,N2为44.65%,吸收温度为35℃,以等量且质量分数均为30%DTBP和MDEA溶液为吸收剂,吸收时间为10min,分别考察DTBA和MDEA溶液的H2S脱除率(S)[18]。
(2)当原料气H2S为0.85%,CO2为12.8%,N2为86.35%,吸收温度为室温时,用等量的且质量分数均为24% DTBP和MDEA水溶液分别吸收混合气20min、30min、40min、50min、60min,考察其吸收选择性()[19-20](H2S与CO2在吸收后富液中的摩尔浓度比/H2S与CO2在尾气中的体 积比)。
3 结果与讨论
3.1 合成反应的条件优化分析
采用单因素变量法,分别考察反应物配比、反应温度、反应时间及反应介质(纯水/无水乙醇)对反应产率的影响,探究最佳的反应条件。
3.1.1 反应物配比对产率的影响
以无水乙醇为介质,投加量为叔丁胺和1,3-二氯-2-丙醇总量(以下简称反应物总量)的100%,反应物总量恒定,改变叔丁胺与1,3-二氯-2-丙醇的摩尔比,在140℃下自压反应3h。由图3中可知,当叔丁胺与1,3-二氯-2-丙醇以理论摩尔比(2∶1)反应时,产物的产率较低,随着叔丁胺的增加,1,3-二氯-2-丙醇的转化率增大,使反应产率增大,当叔丁胺与1,3-二氯-2-丙醇的摩尔比为3∶1时,产率达到最大。此时继续增大叔丁胺的用量,产率反而变小,这是因为过量的叔丁胺与生成的HCl发生中和反应,使体系的副产物增加,产率下降。
3.1.2 温度对反应产率的影响
以无水乙醇为介质(投加量为反应物总量的100%),叔丁胺与1,3-二氯-2-丙醇以摩尔比为3∶1自压反应3h,得到温度与反应产率的关系曲线如图4所示。随着温度的升高,活化分子数增多,反应产率增大,但温度超过140℃后,反应产率开始下降,这是由于温度过高使溶剂气化严重,溶剂充当反应介质的作用弱化造成的,因此最佳的反应温度为140℃。
3.1.3 反应时间对反应产率的影响
以无水乙醇为介质(投加量为反应物总量的100%),叔丁胺与1,3-二氯-2-丙醇以摩尔比为3∶1在140℃下进行自压反应,由图5可知,随反应的进行,反应产率不断增大,3h后反应产率基本不变,从节能考虑,最佳的反应时间为3h。
3.1.4 反应介质对反应产率的影响
在叔丁胺与1,3-二氯-2-丙醇以摩尔比为3∶1,反应温度为140℃,反应时间为3h的条件下,分别用纯水和无水乙醇作为反应介质,其用量与反应产率的关系如图6。由于目标产物结构对称,更易溶于极性更小的无水乙醇,促进反应正向移动,由勒夏特列原理可知,反应物转化率变大,故以无水乙醇作为反应介质的反应产率高于纯水,且当无水乙醇用量为反应物总量的100%时,反应产率最大。
3.2 IR分析
图7为合成反应产物的IR分析。图7中2966cm−1为C—H伸缩振动吸收峰,由于此值低于3000cm−1,证明目标产物为饱和化合物;3399cm−1宽的吸收峰为形成分子间氢键的O—H伸缩振动吸收峰;1218cm−1为C—O的伸缩振动吸收峰;1363cm−1为C—N的伸缩振动吸收峰,两端叔丁基的空间效应使其特征值偏高;1570cm−1处为N—H的变角振动吸收峰;实验产物的IR图与目标产物的官能团对应,初步判断合成的物质为目标产物。
3.31H NMR分析
图8为产物的1H NMR分析,谱图中氢原子个数与化合物中氢原子个数相同。分子中叔丁胺基中的甲基氢出现在1.074处,共18个;分子中 与—NH相连的亚甲基氢出现在2.526~2.692处,为耦合的八重峰,共4个;分子中的—NH活泼氢及—OH活泼氢出现在2.868处,共3个(图8中此处的积分值大于实际值,原因是进行核磁表征的溶剂为氘代丙酮,谱图中会有水峰,与此处活泼氢的峰重叠),其中2个—NH活泼氢;分子中与—OH相连的—CH上的活泼氢出现在低场区3.513~3.569处,为耦合的九重峰,共1个。图8中2.050处为丙酮的甲基氢的峰。实验所得产物的1H NMR图与目标产物的结构对应,与目标产物的标准图谱基本吻合。
3.4 脱硫性能测试
DTBP与MDEA溶液的脱硫性能比较见表1。从表1中可以看出,相同的实验条件下DTBA对H2S的脱除率s值比MDEA大,其对CO2的脱除率c值比MDEA小。研究表明:在选择性脱硫过程中,CO2的存在会抑制脱硫剂对H2S的吸收,因此脱硫剂的c越小,s越大,脱硫剂的性能越好。因此DTBP的脱硫性能优于MDEA。
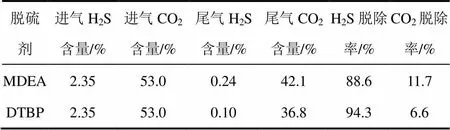
表1 DTBP与MDEA溶液的脱硫性能比较
室温下等量的质量分数均为24%的DTBP和MDEA溶液的吸收选择性()如图9所示。
吸收时间不同,脱硫剂的酸气负荷不同,由图9可知,DTBP在很宽的酸气负荷范围内具有优于MDEA的H2S吸收选择性。这是因为胺与H2S的反应是一个快速的质子交换反应,吸收过程为气膜控制,而CO2和胺之间的反应十分复杂[7]。MDEA因其N原子上没有活泼H,与CO2的反应速率很小,因而具有一定的H2S吸收选择性。与MDEA相比,DTBP中与N原子相连的是空间位阻系数为1.74的叔丁基,且对称分布,其空间位阻大大增加,研究表明,位阻胺分子中与N原子连接的基团的空间位阻越大,其与CO2反应的速率越小,选择性越高[8]。因此DTBP具有比MDEA更高的H2S吸收选择性。
4 结 论
(1)设计并制备了一种位阻胺类脱硫剂:以环氧氯丙烷和浓盐酸为原料合成了中间产物1,3-二氯-2-丙醇,通过在1,3-二氯-2-丙醇上引入叔丁基合成了一种淡黄色针状固体物质,经IR及1HNMR表征,确认其为目标产物DTBP。
(2)通过单因素变量法,得出最佳反应条件,即自压条件下,反应釜搅拌速度为200r/min,以100%无水乙醇作为反应介质,当叔丁胺与1,3-二氯-2-丙醇的摩尔比为3∶1,反应温度为140℃,反应时间为3h时,所制得的1,3-二叔丁胺基-2-丙醇的产率最高。
(3)实验室脱硫评价实验表明:在相同的实验条件下,1,3-二叔丁胺基-2-丙醇对H2S的吸收选择性及H2S脱除率均优于MDEA。
[1] 孙娇,孙兵,姬春彦,等. 天然气脱硫过程的胺液污染问题及胺液净化技术研究进展[J]. 化工进展,2014,33(10):2771-2777.
[2] Liu M,Wang J Q,Ke W,et al. Corrosion behavior of X52 anti-H2S pipeline steel exposed to high H2S concentration solutions at 90℃[J].,2014,30(5):504-510.
[3] 李晓,李少平,詹敏,等. 高选择性脱硫吸收剂的研制[J]. 华东理工大学学报,1999,25(3):265-268.
[4] 李奇,李伟,姬忠礼,等. 高含硫天然气装置㶲分析[J]. 化工进展,2014,33(12):3176-3182.
[5] Priyabrata P,Ahmad A K,Sameer A A,et al. Role of aqueous methyldiethanolamine (MDEA) as solvent in natural gas sweetening unit and process contaminants with probable reaction pathway[J].,2015,24:124-131.
[6] 常宏岗. TBGA位阻胺合成及选择性脱硫研究[J]. 石油与天然气化工,1990,19(3):21-25.
[7] 韩淑怡,王科,黄勇,等. 醇胺法脱硫脱碳技术研究进展[J]. 天然气与石油,2014,32(3):19-22.
[8] Lu J G,Zheng Y F,He D L,et al. Selective absorption of H2S from gas mixtures into aqueous solutions of blended amines of methyldiethanolamine and 2-tertiarybutylamino-2-ethoxyethanol in a packed column[J].,2006,52(2):209-217.
[9] Huang K,Chen Y L,Zhang X M,et al. Experimental study and thermodynamical modelling of the solubilities of SO2,H2S and CO2in-dodecylimidazole and 1,1-[oxybis(2,1-ethanediyloxy-2,1- ethanediyl)]bis(imidazole):An evaluation of their potential application in the separation of acidic gases[J].,2014,378:21-33.
[10] 韩淑怡,王科,黄勇,等. 醇胺法脱硫脱碳技术研究进展[J]. 天然气与石油,2014,32(3):19-22.
[11] 陈赓良. 空间位阻胺-新型选择性脱硫溶剂[J]. 天然气工业,1986,6(3):92-96.
[12] 王璐,杨敬一,徐心茹,等. 胺分子结构与CO2反应速度常数关系的研究[J]. 石油与天然气化工,2010,39(2):95-99.
[13] Sartori G. Process for the selective removal of hydrogen sulfide from gaseous mixtures with severely sterically hindered secondary aminoether alcohols:US,4405585[P]. 1983-09-20.
[14] Stogryn E L. Process for preparing secondary aminoether alcohols:US,4487967[P]. 1984-12-11.
[15] Avtandil T,Eldar M,Vaqif A. Synthesis of substituted-alkylamines in aqueous media[J].,2013,3:31-35.
[16] 罗勣深,余赐章,熊庭辉,等. 从环氧氯丙烷制备1,3-二氯-2-丙烷[J]. 中国医药杂志,1991,22(7):322.
[17] 杨翠定,顾侃英,吴文辉,等. 石油化工分析方法[M]. 北京:科学出版社,1990:178-182.
[18] 徐宏建,郑志胜,张成芳. 实验室模拟脱硫装置及脱硫剂的评价[J]. 华东理工大学学报,2002,28(3):314-317.
[19] 周学厚,陈赓良. 四川天然气净化工艺技术发展的回顾与展望[J]. 石油与天然气化工,1991,20(1):13.
[20] Mandal B P,Biswas A K,Bandyopadhyay S S,et al. Selective absorption of H2S from gas streams containing H2S and CO2into aqueous solutions of-methyldiethanolamine and 2-amino-2- methyl-1-propanol[J].,2004,35(3):191-202.
Development and performance test of a highly selective and sterically hindered amine desulfurizer
,,,
(College of Chemistry & Chemical Engineering,Southwest Petroleum University,Chengdu 610500,Sichuan,China)
With epoxy chloropropane and concentrated hydrochloric acid as raw material,the intermediate product 1,3-dichloro-2-propanol was prepared by ring opening action. A novel sterically hindered amine 1,3-dibutylamine-2-propanol (DTBP),which can be used for gas desulfurization,has been synthesized by nudeophilic substitution between 1,3-dichloro-2-propanol and-butylamine,and then the chemical structure of this desulfurizer was demonstrated by IR and1H NMR. The reaction conditions were optimized by the method of single factor variable,and the study showed that with the 100% anhydrous ethanol as reaction medium,when the molar ratio between 1,3-dichloro-2-propanol and-butylamine was 1∶3,the reaction temperature was 140℃,and the reacting time was 3 hours,the yield of DBTP was 92.3%,which was the maximum. The laboratory desulfurization performance test indicated that the capacity of H2S absorption and the absorption selectivity of DTBP solution were higher than those of MDEA under the same reaction conditions.
sterically hindered amine; selective desulfuration; synthesis; optimization; evaluation
TE 622;TE 624
A
1000–6613(2015)09–3291–06
10.16085/j.issn.1000-6613.2015.09.013
2015-01-12;修改稿日期:2015-03-31。
郭晓丹(1989—),女,硕士研究生。联系人:诸林,教授,博士生导师,主要研究方向为能源化工与环境保护。E-mailzhulinswpi65@gmail.com。

