紫贻贝壳对醚菌酯吸附性能的研究
王雅颖,郭 健,纪丽丽,韩丝银,应知伟,宋文东,*
(1.浙江海洋学院食品与医药学院,浙江舟山316022;2.浙江海洋学院石化与能源工程学院,浙江舟山316022;3.广东海洋大学食品科技学院,广东湛江524088;4.浙江海洋学院海洋科学与技术学院,浙江舟山316022)
紫贻贝壳对醚菌酯吸附性能的研究
王雅颖1,郭健1,纪丽丽2,韩丝银3,应知伟4,宋文东2,*
(1.浙江海洋学院食品与医药学院,浙江舟山316022;2.浙江海洋学院石化与能源工程学院,浙江舟山316022;3.广东海洋大学食品科技学院,广东湛江524088;4.浙江海洋学院海洋科学与技术学院,浙江舟山316022)
以舟山废弃的紫贻贝壳资源为研究对象,通过添加膨化剂高温煅烧制备多孔性紫贻贝壳粉吸附材料,利用热重分析(TG)、红外光谱分析(IR)、比表面积(BET)测定对紫贻贝壳粉的物化性能进行了表征;采用正交实验设计优化了紫贻贝壳粉吸附农药醚菌酯的工艺条件。结果表明:紫贻贝壳酸洗后粉碎,过100目筛,1000℃条件下煅烧60min,制得紫贻贝壳粉比表面积达到2.638×103m2/g;紫贻贝壳粉去除100mL 0.6g/L醚菌酯的最优条件为:pH10.0,温度30℃,时间40min,紫贻贝壳粉用量0.3g,在此条件下,醚菌酯去除率高达36.07%,可开发成一种新型脱农药果蔬清洗剂。
紫贻贝壳,醚菌酯,吸附
农业生产离不开农药,尤其是在治理农作物病虫害过程中遇到突发性灾害,而喷洒化学农药是最有效的防治方法[1],目前,我国由于存在违规使用禁用农药、施药技术落后等诸多方面问题,已导致全国受农药污染的农田约1.6×107hm2,主要农产品的农药残留超标率很高,有些地区甚至高达14.3%[2-4]。为此,市场上各类果蔬洗涤剂产品逐渐增多,大部分产品都注明能有效去除果蔬表面的农药残留[5-6],但由于大多数果蔬洗涤剂的成分为化学表面活性剂,使用后存在农药脱除效果不明显、化学残留等问题。贝壳粉是一种廉价的天然清洁材料,可应用于吸附各种气体、液体杂质和细菌[7-12],效果显著,目前日本有利用贝壳粉制成的果蔬清洗剂,而国内市场未见,贝壳粉作为一种新型吸附剂具有经济高效且操作简单等优点,因此,如何充分利用贝壳资源实现废弃物再利用的重要课题越来越引起人们的重视[13-15]。
舟山是全国贻贝的主产区,出口量占全国总量的60%以上。嵊泗岛贻贝年产量约8万吨,产生贝壳约6.4万吨,贻贝壳被废弃堆积成山,既给环境造成影响同时又浪费了资源。本文以舟山废弃的紫贻贝壳为原料,经过粉碎、煅烧制得紫贻贝壳粉吸附材料,以农药中的醚菌酯为例,考察了紫贻贝壳粉对其吸附性能的最优条件,旨在为资源丰富的紫贻贝壳的综合利用及开发相关绿色环保型洗涤产品提供理论依据。
1 材料与方法
1.1材料与仪器
紫贻贝壳舟山地区废弃;膨化剂自制;醚菌酯美邦80%水分散颗粒;草酸钠含量>99.8%;浓硫酸质量分数98%;其他试剂均为分析纯;实验用水蒸馏水。
JP-300A高速多功能粉碎机永康市久品工贸有限公司;YFX7/12Q-GC箱式电炉上海意丰电炉有限公司;BK122T-B BET比表面积测定仪北京精微高博科学技术有限公司;Nicolet Nexus 6700FTIR傅立叶红外光谱仪美国尼高力公司;202-A数显电热恒温干燥箱上海阳光实验仪器有限公司;AR124CN电子天平奥豪斯仪器有限公司;HC7-1维基差热天平北京恒久科学仪器厂;HJ-6多头磁力加热搅拌器荣华仪器制造有限公司。
1.2主要工艺流程
紫贻贝壳→化学酸洗→粉碎→热重分析→高温煅烧→红外光谱分析→紫贻贝壳粉吸附醚菌酯→测定醚菌酯去除率。
将洗净的紫贻贝壳在0.5%的盐酸水溶液中浸泡30min,除去紫贻贝壳表面各种杂质,将酸洗后的贝壳敲碎,放入高速多功能粉碎机粉碎1min,通过热重分析确定其煅烧温度,烘干后进行高温煅烧。
紫贻贝壳热重分析条件:紫贻贝壳粉0.0257g;空气气氛;20~900℃;程序升温速率10℃·min-1。
紫贻贝壳粉红外光谱分析:将样品粉末和磨细的溴化钾按1∶100的比例在玛瑙研钵中混合均匀,与手动压片机上制成透明薄片进行测试。红外光谱仪测定条件如下:分辨率4cm-1,扫描16次,扫描范围4000~400cm-1[16]。
1.3煅烧温度对紫贻贝壳粉比表面积的影响
将酸洗后的紫贻贝壳粉碎,过100目筛,称取5g的紫贻贝壳粉7份,添加一定量膨化剂,分别在500、600、700、800、900、1000、1100℃下高温煅烧60min,用BET比表面积分析仪测定所得紫贻贝壳粉的比表面积。
紫贻贝壳粉比表面积分析条件:吸附质为高纯氮气;体系温度77.350K;测试时间30min[14]。
1.4醚菌酯去除率的测定[17]
取水样1mL(含浓度为0.06g/mL醚菌酯),用蒸馏水稀释至100mL,置于250mL锥形瓶中,加入5mL硫酸溶液(质量分数98%的浓硫酸与蒸馏水体积比1∶3配得)摇匀后加入10mL 0.01mol/L KMnO4溶液并放入沸水浴中加热30min;取下锥形瓶加入10mL 0.01mol/L Na2C2O4标液,摇匀后立即用0.01mol/L KMnO4溶液滴定至显微红色(冷却前完成),记录KMnO4溶液消耗量V。
KMnO4溶液浓度的标定:将滴定后的溶液水浴加热至70℃后加入10mL Na2C2O4标准溶液(0.01mol/L),再用0.01mol/L KMnO4溶液滴定至显微红色。记录KMnO4溶液的消耗量,按照下式求得KMnO4溶液的校正系数(K):
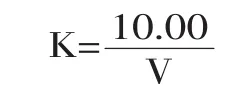
式中:V—KMnO4溶液消耗量(mL)。
本实验另取1mL纯水样进行空白对照。
高锰酸钾指数CODMn的计算方法如下:
CODMn(O2,mg/L)={[(10+V1)K-10]-[(10+V0)K-10]C}M×8×1000/V2
式中:V1—滴定水样时KMnO4的消耗量;V0—空白实验中KMnO4溶液消耗量(mL);V2—醚菌酯水样量(mL);K—校正系数;M—KMnO4溶液浓度(mol/L);8—氧(1/2 O)摩尔质量;C—稀释的水样中含水的比值(C=0.99)。
去除率计算公式为:

其中,CODMn0为吸附前的高锰酸钾指数,CODMn1为吸附后的高锰酸钾指数。
1.5紫贻贝壳粉对醚菌酯吸附性能的条件优化
1.5.1单因素实验
1.5.1.1吸附pH实验量取100mL 0.6g/L醚菌酯溶液5份于锥形瓶,各放入0.3g贝壳粉吸附剂,分别调节pH至6、7、8、9、10,在室温条件下振荡30min,静置沉淀后取上层清液1mL,稀释至100mL,用高锰酸钾滴定法测定CODMn,计算去除率。
1.5.1.2吸附温度实验量取100mL 0.6g/L醚菌酯溶液5份于锥形瓶,各放入0.3g贝壳粉吸附剂,调节pH至10,分别在温度为20、30、40、50、60℃的条件下振荡30min,静置沉淀后取上层清液1mL,稀释至100mL,用高锰酸钾滴定法测定其CODMn,计算去除率。
1.5.1.3吸附时间实验量取100mL 0.6g/L醚菌酯溶液5份于锥形瓶,各放入0.3g贝壳粉吸附剂,调节pH至10,在室温条件下分别振荡10、20、30、40、50min,静置沉淀后取上层清液1mL,稀释至100mL,用高锰酸钾滴定法测定其CODMn,计算去除率。
1.5.1.4紫贻贝壳粉用量实验量取100mL 0.6g/L醚菌酯溶液5份于锥形瓶,分别加入0.1、0.2、0.3、0.4、0.5g紫贻贝壳粉,调节pH至10,在室温条件下振荡30min,静置沉淀后取上层清液1mL,稀释至100mL,用高锰酸钾滴定法测定其CODMn,计算去除率。
1.5.2正交实验设计以醚菌酯去除率为考察指标,在单因素实验的基础上,采用L9(34)正交表对吸附条件进行进一步优化,其因素水平安排见表1。
2 结果与分析
2.1紫贻贝壳热重分析
图1结果显示,在300~500℃区间内,紫贻贝壳粉发生了一次缓慢失重现象,这是因为紫贻贝壳表面的少量有机物发生降解;在775~885℃区间内,贝壳粉发生第二次快速失重现象,推测是由于紫贻贝壳的主体材料CaCO3发生了分解,生成CaO,放出大量CO2;一般CaCO3分解生成CaO的临界温度为897℃左右,而由图1推测可知,紫贻贝壳粉中CaCO3在800℃之前便发生了分解,相比而言紫贻贝壳中生成CaO更加节能。图1整体反应了紫贻贝壳的热分解规律,由此可选择紫贻贝壳煅烧温度优化水平区间为500~1000℃。
2.2煅烧温度对紫贻贝壳粉比表面积的影响

表1 紫贻贝壳粉吸附醚菌酯因素水平表Table 1 Factors and their coded levels used in orthogonal array design

图1 紫贻贝壳热重分析曲线Fig.1 TGA of Mytilus edulis shells powder

图2 紫贻贝壳煅烧温度对比表面积的影响Fig.2 Effect of temperature of calcination on specific surface area
由图2可知,随着煅烧温度的升高,紫贻贝壳粉的比表面积逐渐增大,煅烧温度在500~800℃时比表面积增大缓慢,在800~900℃之间贝壳粉的比表面积迅速增大,当煅烧温度高于900℃比表面积增大缓慢。这是因为贝壳中含有的有机物,在一定高温中发生分解,产生一定的孔隙,当温度升高至800~900℃区间时,推测占贝壳大部分主体材料的CaCO3发生分解,同时产生大量的孔隙,900℃以后分解反应基本完成,1000℃分解相对彻底,紫贻贝壳比表面积达到2.638×103m2/g,而1100℃时紫贻贝壳比表面积也未有明显增大,故选取煅烧温度为1000℃。
2.3紫贻贝壳红外光谱分析

图3 紫贻贝壳红外光谱分析曲线Fig.3 Infrared spectrum analysis of Mytilus edulis shells
红外谱图中的1410cm-1附近的宽峰和875cm-1附近的尖锐吸收峰为碳酸钙所具有的红外吸收特征,而3642cm-1处尖锐吸收峰则属于氧化钙的红外吸收特征。由图3可知,紫贻贝壳粉经1000℃高温煅烧后的红外光谱中,3642cm-1处的吸收峰很强,而1410cm-1附近的宽峰和875cm-1附近的尖锐吸收峰较弱,说明紫贻贝壳粉在1000℃灼烧后,样品绝大部分已经分解为氧化钙,证实了上述推测,因此,放出CO2产生大量的孔隙。
2.4紫贻贝壳粉吸附醚菌酯的单因素实验
2.4.1吸附pH对醚菌酯去除率的影响由图4可知,在酸性条件下醚菌酯去除率相对较低,随着pH的增大,醚菌酯的去除率不断升高,在中性和弱碱性的条件下吸附效果较好,这是因为醚菌酯呈弱酸性,贝壳粉在碱性条件下可与醚菌酯发生中和反应,降低醚菌酯含量,即提高醚菌酯去除率。而通常果蔬清洗时碱性过大会对感官造成影响,GBT24691-2009规定果蔬清洗剂的pH范围为6.0~10.5,因此选取贝壳粉吸附醚菌酯最佳pH为10。
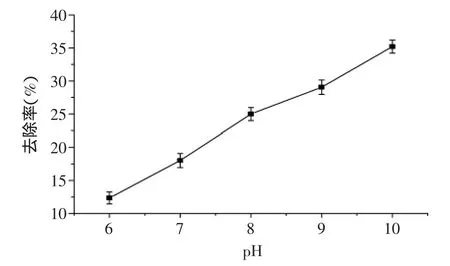
图4 pH对吸附效果的影响Fig.4 Effect of pH on adsorption
2.4.2吸附温度对醚菌酯去除率的影响由图5可知,在20~60℃之间,随着温度的升高,贝壳吸附剂对醚菌酯的吸附性能逐渐增强,但整体趋势不明显。这是因为,紫贻贝壳粉吸附醚菌酯是一个吸热过程,温度升高时,一方面,醚菌酯溶液中有机分子的动能增大;另一方面,紫贻贝壳粉吸附性能增强,从而提高了紫贻贝壳粉对醚菌酯的吸附量。由于温度对醚菌酯去除率影响不大,蔬果清洗常用温度一般为室温,故选取紫贻贝壳粉吸附醚菌酯最佳温度为20℃。

图5 温度对吸附效果的影响Fig.5 Effect of temperature on adsorption
2.4.3吸附时间对醚菌酯去除率的影响由图6可知,在吸附的10~30min期间,随着时间的延长,贝壳吸附剂对醚菌酯的去除率迅速提高,30min后,随着时间的延长,去除率升高幅度很小。这是由于贝壳内部存在大量微孔,可以吸附大量的醚菌酯分子,30min后吸附基本趋于饱和状态,变化不大。故选取贝壳粉吸附醚菌酯时间为30min。

图6 吸附时间对吸附效果的影响Fig.6 Effect of time on adsorption
2.4.4紫贻贝壳粉用量对醚菌酯去除率的影响由图7可知,随着紫贻贝壳粉用量的增加,醚菌酯去除率随之升高,当紫贻贝壳粉用量为0.3g时,醚菌酯的去除率达到30.36%,已经接近最大值,此时再增加紫贻贝壳粉用量,醚菌酯去除率增加不明显,这是因为当醚菌酯浓度一定时,紫贻贝壳粉用量超过一定范围,它的吸附能力也不会再提高,而是维持在一个平衡的状态,故选取贝壳粉吸附醚菌酯贝壳粉最佳用量为0.3g。
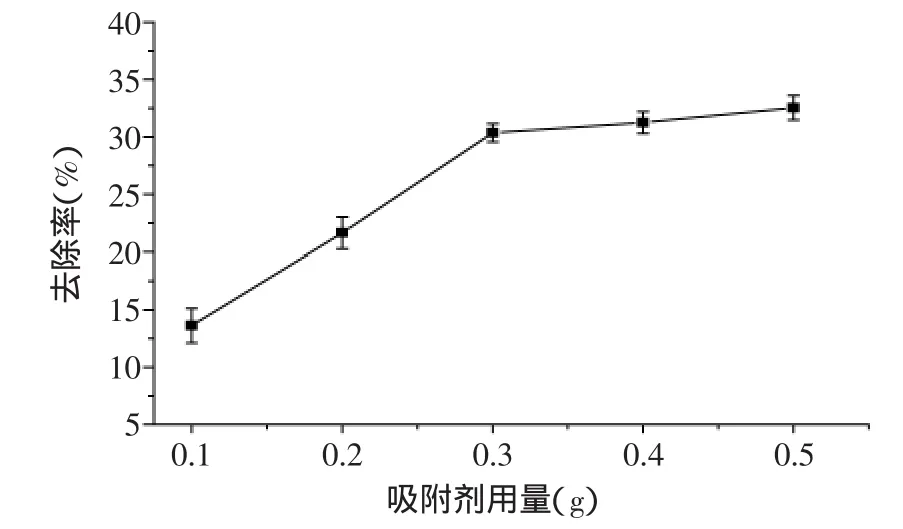
图7 紫贻贝壳粉用量对吸附效果的影响Fig.7 Effect of dosage of Mytilus edulis shells powder on adsorption
2.5紫贻贝壳粉吸附醚菌酯的正交实验
由表2分析可知,对醚菌酯去除率影响的大小次序为A(pH)>D(贝壳粉用量)>C(吸附时间)>B(吸附温度),即pH对醚菌酯去除率效果影响最大,贝壳粉用量对去除效果影响次之,吸附时间对去除率效果影响较小,吸附温度对醚菌酯去除率效果影响最小。根据k值,得出最优组为A3B3C3D2,即pH10.0,吸附温度30℃,吸附时间40min,贝壳粉用量0.3g,在此条件下,通过进一步实验验证得醚菌酯去除率为36.07%,高于正交实验的最优组A3B1C3D2去除率34.22%。通过表3各因素方差分析,结果与表2一致,且pH对醚菌酯去除率影响具有显著性,吸附温度、时间、贝壳粉用量对醚菌酯去除率影响不显著。因此,紫贻贝壳粉对醚菌酯去除率最优条件为A3B3C3D2,即pH10.0,吸附温度30℃,吸附时间40min,贝壳粉用量0.3g,在此条件下,醚菌酯去除率为36.07%。
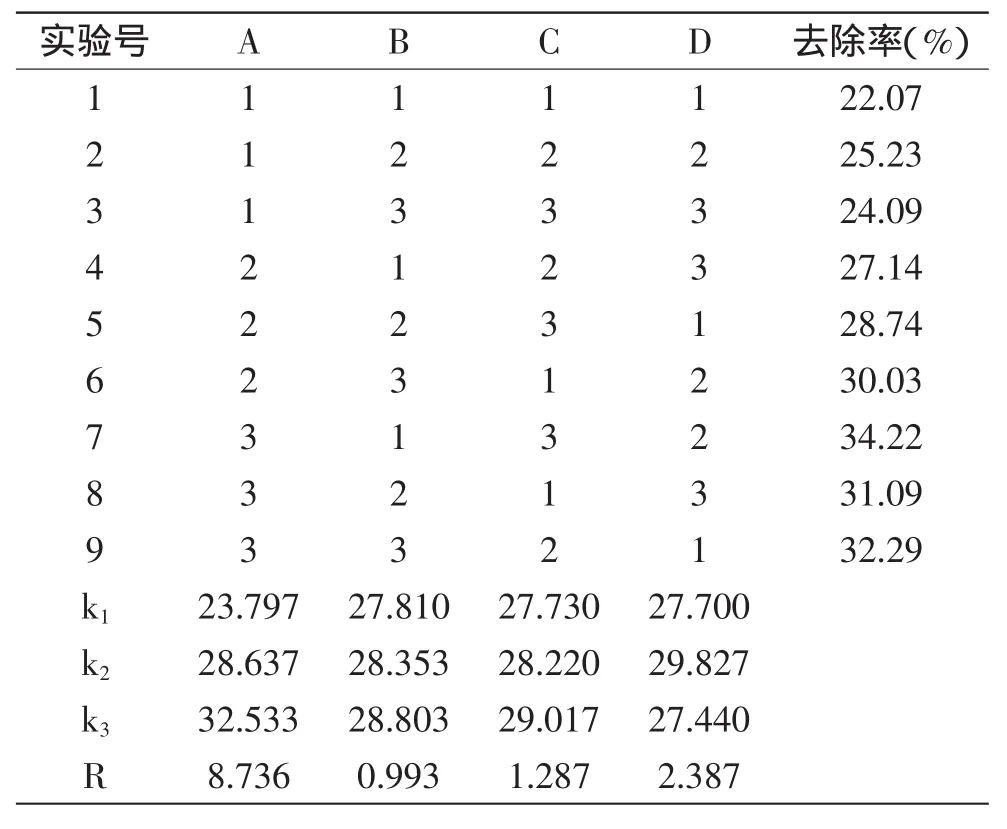
表2 紫贻贝壳粉吸附醚菌酯正交实验设计及结果Table 2 Orthogonal array design scheme and corresponding results

表3 方差分析表Table 3 Analysis of variance
3 结论与讨论
本文将紫贻贝壳酸洗后粉碎,经高温煅烧制得高比表面积紫贻贝壳粉;通过正交实验优化了其去除醚菌酯的工艺条件,结果表明,各因素对醚菌酯去除率影响大小次序是pH>贝壳粉用量>吸附时间>吸附温度,同时确定了紫贻贝壳粉去除100mL 0.6g/L醚菌酯最适工艺条件,即pH10.0,吸附温度30℃,吸附时间40min,贝壳粉用量0.3g,在此条件下,醚菌酯去除率为36.07%。因此,紫贻贝壳粉对醚菌酯有较好的吸附性能,可开发成一种新型脱农药残留果蔬清洗剂。
良好的清洗方式不仅能够除去果蔬残留的化学农药,杀死引起疾病的微生物,而且还能够延长蔬菜的货架期[18-21]。目前传统清洗果蔬的方式及化学或天然物质复配洗涤剂[22]清洗果蔬,对农药残留问题影响较弱,或对环境存在危害,一些物理、化学或生物降解方法[23-25]成本较高,不易普遍应用,而用废弃贝壳为原料生产果蔬清洗剂,成本低,效果佳,生产加工过程方便简易、周期短,易于产业化,不仅解决了贝壳堆积引起的环境危害,而且实现了贝壳的“变废为宝”,经济效益高,具有广阔的市场和应用前景。
[1]张一宾,张怿.农药[M].北京:中国物资出版社,1997:13-55.
[2]刘慧超.关于农药残留[J].北京农业,2004(8):36.
[3]质检总局.近半蔬菜农药残留超标[EB/OL].http://www.southcn. com/news/hotpersue/200110300002.htm.
[4]食品商务网.贵阳农残超标率最低[EB/OL].http://www.21food. cn/html/news/26/179171.htm.
[5]宗荣芬,刘文卫,梅建新.蔬果洗涤剂对农药残留去除率的研究[J].中国卫生检验杂志,2003(4):441-442.
[6]魏斌.家庭洗涤用品[M].北京:轻工业出版社,1985:85.
[7]Kwon HB,Lee CW,Jun BS,et al.Recyling waste oyster shells for eutrophication control[J].Resources Conservation and Recycling,2003,41:75-82.
[8]叶志隆,熊小京,芦敏.贝壳填料曝气生物滤池的硝化特性研究[J].中国给水排水,2006,22(3):1-8.
[9]Jun S,Hirokazu S.Hirom itsu Kojima Kinetic analysis of the bactericidal action of heated scallop-shell powder[J].International Journal of Food Microbiology,2001,71:211-218.
[10]魏巍,贺淹才.从扇贝壳制取活性氧化钙及其抑菌效果初探[J].生物技术,2005,15(5):77-78.
[11]曾名勇,林洪峰,刘树青,等.海洋生物保鲜剂OP-Ca抗菌特性的研究成果[J].中国海洋药物,2002(4):27-31.
[12]段杉,陈海梅,林秋峰,等.贝壳粉煅烧物的防腐作用研究[J].中国食品添加剂,2007(6):74-78.
[13]梁艳,赵杰,王来,等.贝壳的有机质及生化矿化机制分析[J].生物学杂志,2006,23(6):19-23.
[14]胡学寅,周丽丽,齐兴义.贝壳吸附材料的制备与表征[J].应用科技,2008,35(3):70-72.
[15]熊涛,乐易林.生物保鲜技术的研究进展[J].食品与发酵工业,2004,30(2):111-113.
[16]夏静芬,钱国英,陈亮,等.傅里叶变换红外光谱法对珍珠粉和贝壳粉的研究[J].光谱实验室,2010,27(2):524-528.
[17]GB11892-89中华人民共和国国家标准-水质高锰酸盐指数的测定[S].
[18]Toivonen PMA,Brummell DA.Biochemical bases of appearance and texture changes in fresh-cut fruit and vegatables[J].Postharvest Biology and Technology,2008,48(1):1-14.
[19]燕平梅,樊文菊,王青,等.不同清洗剂对鲜切豇豆品质的影响[J].食品工程,2010(1):40-44.
[20]王丹,李雪,马越,等.不同清洗剂对鲜切西兰花贮藏期间品质的影响[J].食品与机械,2013,29(5):190-193.
[21]刘嫦娥,胡波,吴敏,等.农产品农药残留的危害与预防[J].现代农业科技,2012(14):290.
[22]武丽丽.食品工业清洗剂的研究进展[J].工业与公共设施清洁,2014(7):40-43.
[23]季静,杨晓倩,郭冬梅,等.蔬菜表面残留磷酸酯类有机磷农药降解方法研究[J].山东大学学报,2009,47(7):122-124.
[24]Fuentes MS,Benimeli CS,Amoroso SA,et al.Isolation of pesticide-degrading actinomyeetes from a contaminated site:Bacterial growth,removal and dechlorination of organochlorine pesticides[J].International Biodeterioration&Biodegradation,2010(64):434-441.
[25]Basfar AA,Mohamed KA,Al-Saqer OA.De-contamination of pesticide residues in food by ionizing radiation[J].Radiation Physics and Chemistry,2012,81(4):473-478.
Study on adsorption property of Mytilus edulis shell powder for kresoxim-methyl
WANG Ya-ying1,GUO Jian1,JI Li-li2,HAN Si-yin3,YING Zhi-wei4,SONG Wen-dong2,*
(1.College of Food and Medical,Zhejiang Ocean University,Zhoushan 316022,China;2.College of Petrochemical and Energy Engineering,Zhejiang Ocean University,Zhoushan 316022,China;3.College of Science,Guangdong Ocean University,Zhanjiang 524088,China;4.College of Marine Science and Technology,Zhejiang Ocean University,Zhoushan 316022,China)
Abandoned Mytilus edulis shells in Zhoushan were made into sorptive material of porous Mytilus edulis shell powder by burning at high temperature with swelling agent.Physical and chemical properties of Mytilus edulis shell powder were characterized with the methods of TGA,IR,and BET,and absorbing kresoxim-methyl technology of Mytilus edulis shell powder was optimized by orthogonal array design methods. Specific surface area of Mytilus edulis shells powder was found to be 2.638×103m2/g after getting acid pickling,smashed,and calcined for 60min at 1000℃.The optimum conditions of Mytilus edulis shell powder to remove 100mL 0.6g/L kresoxim-methyl were found to be adsorption at 30℃and pH10.0 for 40min with 0.3g dosage of Mytilus edulis shell powder.Under the condition,removing rate of kresoxim-methyl reached up to 36.07%,and it could be developed as a new kind of fruit and vegetable cleaning agent which would remove pesticides.
Mytilus edulis shells;kresoxim-methyl;adsorption
TS254.9
B
1002-0306(2015)10-0210-05
10.13386/j.issn1002-0306.2015.10.035
2014-08-01
王雅颖(1990-),女,在读硕士研究生,研究方向:海洋资源高值化利用研究。
宋文东(1960-),男,博士,教授,研究方向:海洋资源高值化利用研究。
广东省自然科学基金(S2012020011054)。

