气相色谱法测定苦参素提取过程中有机溶剂残留量
杨建林,金西成,黄洁,单敏
(1.宁夏回族自治区西吉县人民医院,宁夏固原756299;2.陕西省西安市食品药品检验所,陕西西安710054)
气相色谱法测定苦参素提取过程中有机溶剂残留量
杨建林1,金西成1,黄洁2,单敏2
(1.宁夏回族自治区西吉县人民医院,宁夏固原756299;2.陕西省西安市食品药品检验所,陕西西安710054)
目的建立测定苦参素提取过程中有机溶剂残留量的气相色谱(GC)法。方法色谱柱为0.25~0.18mm的二乙烯苯-乙基乙烯苯型高分子多孔小球(401有机担体),2m×3.2mm玻璃柱,进样口及检测器温度为220℃,柱温为130℃,N230mL/min,H230mL/min,Air300mL/min,S 101×23,进样量为100μL。结果二氯甲烷及氯仿线性范围均为2~10μg/mL;二氯甲烷RSD为0.1%,最低检出限为0.201 9 ng,定量限为0.605 7 ng;氯仿RSD为0.3%,最低检出限为0.218 6 ng,定量限为0.655 8 ng。二氯甲烷的平均加样回收率为99.73%(n=9),氯仿的平均加样回收率为100.21%(n=9)。结论该法线性关系、精密度及回收率均较良好,结果准确可靠,可用于苦参素提取过程中残留二氯甲烷及氯仿的测定。
气相色谱法;苦参素;二氯甲烷;氯仿
苦参素是苦参碱的N-氧化物,是从豆科植物苦豆子中提取分离得到的生物碱,主要成分为氧化苦参碱[1],在一定条件下可转化为苦参碱[2],具有多方面的药理作用和功效,如抗炎、抗病毒、抗肝纤维化、保肝降酶、抗肿瘤、升高白细胞、抗心律失常等作用[3-4]。因其不良反应较少[5],故被广泛应用于临床。本试验中建立了检测苦参素提取过程中有机溶剂二氯甲烷及氯仿残留量的气相色谱法,现报道如下。
1 仪器与试药
GC-14C型气相色谱仪(日本岛津公司),包括FID检测器,N2010色谱工作站。苦参素(西安富捷生物技术有限公司试制,批号为20011123,20011127,20011202);二氯甲烷、氯仿(国药集团化学试剂有限公司,含量不小于99.5%);水为蒸馏水。
2 方法与结果
2.1 色谱条件
色谱柱:0.25~0.18mm的二乙烯苯-乙基乙烯苯型高分子多孔小球(401有机担体),2m×3.2mm玻璃柱,进样口及检测器温度:220℃;柱温:130℃;N2:30 mL/min,H2:30 mL/min,Air:300mL/min,S:101×23;进样量:100μL。理论板数按二氯甲烷峰及氯仿峰计算。
2.2 溶液制备
分别精密称取二氯甲烷及氯仿适量,加无有机物的水配制成4μg/mL的溶液作为对照品溶液。取本品0.3 g,精密称定,置10mL容量瓶中,加无有机物的水适量,溶解,并稀释至刻度,静置,取上清液,作为供试品溶液。
2.3 方法学考察
线性关系考察:分别取二氯甲烷及氯仿适量,精密称定,分别加水配制成10,8,6,4,2μg/mL的溶液,进样100μL,以峰面积积分值(Y)为纵坐标、进样质量浓度(X)为横坐标绘制标准曲线,得二氯甲烷回归方程Y=3 019.4X+663.3,r=0.997 9(n=5);氯仿回归方程Y=35 253X+5 509.3,r=0.996 6(n=5)。结果表明,二氯甲烷及氯仿质量浓度均在2~10μg/mL范围内与峰面积线性关系良好。
精密度试验:精密量取二氯甲烷对照品溶液(6μg/mL)及氯仿对照品溶液(6μg/mL)各100μL,连续进样5次,测定,计算峰面积。结果的RSD分别为0.1%,0.3%(n=5),表明仪器精密度良好。
检出限与定量限确定:取二氯甲烷及氯仿适量,分别加水配制成10,8,6,4,2μg/mL的溶液,进样100μL。结果于2μg/mL质量浓度检出二氯甲烷峰及氯仿峰,二氯甲烷和氯仿的检出限分别为0.201 9 ng和0.218 6 ng;定量限分别为0.605 7 ng和0.6558 ng。
重复性试验:依法制备供试品溶液,按拟订色谱条件进样5次测定。结果,二氯甲烷、氯仿含量的RSD分别为0.1%和0.2%(n=5),表明该方法重复性良好。
稳定性试验:取同一供试品溶液,按拟订色谱条件分别于0,2,4,8,12,24 h时进样测定。结果二氯甲烷、氯仿峰面积的RSD分别为0.5%和1.0%(n=6),表明供试品溶液在24 h内基本稳定。
加样回收试验:取本品0.15 g,精密称定9份,分别置10 mL容量瓶中,分别精密加入二氯甲烷、氯仿对照品溶液(10μg/mL)0.8,1.0,1.2mL,加无有机物的水稀释至刻度,依法制备供试品溶液,分别测定结果,见表1。
2.4 样品含量测定
按拟订方法制备供试品溶液,在拟订色谱条件下,进样测定3批样品中二氯甲烷、氯仿的含量,用外标法计算均符合规定。结果见表2。
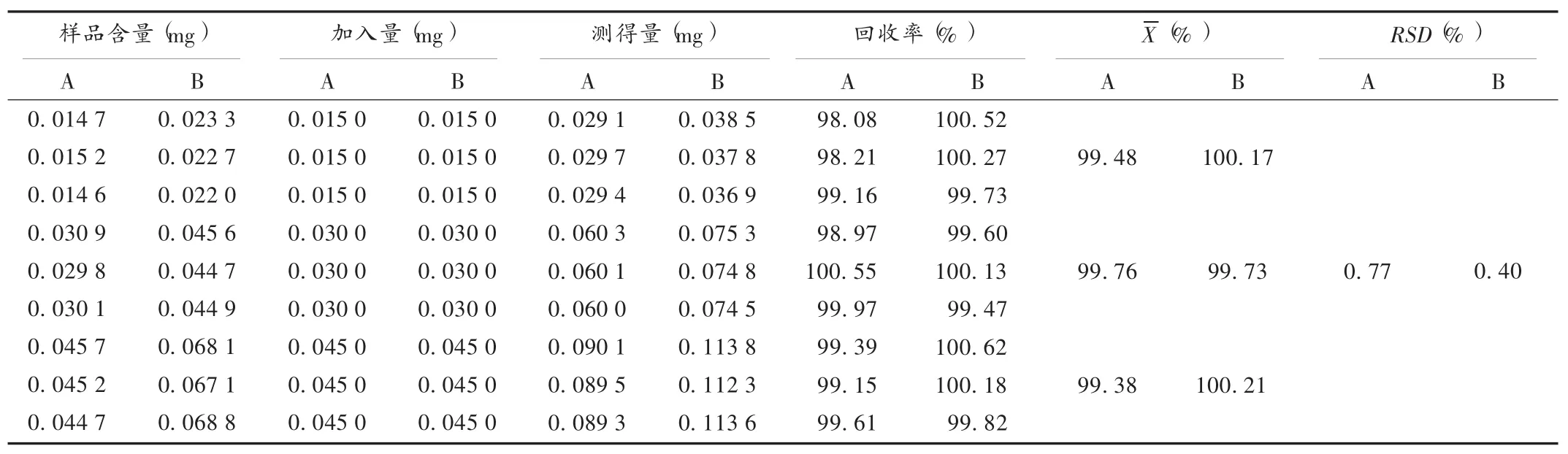
表1 二氯甲烷和氯仿加样回收试验结果(n=9)
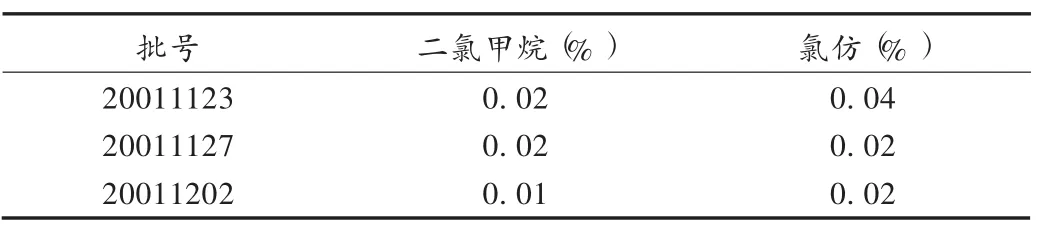
表2 样品中二氯甲烷及氯仿含量测定结果
3 讨论
苦参素的提取是利用苦参生物碱与酸结合成盐溶于水,与其他酸水不溶性杂质分离,再用氢氧化钠碱化,碱液用有机溶剂萃取,回收有机溶剂,得总生物碱,将总生物碱溶于乙醚。因苦参碱在乙醚中溶解而氧化苦参碱不溶,而将其二者分离,该方法操作简单,提取率高,无需特殊生产设备,通过重结晶后样品纯度可达98.0%以上。有机溶剂可回收。
苦参素具有喹诺里西啶类生物碱结构,溶于水、氯仿、乙醇,难溶于乙醚、石油醚[6]。苦参素在提取过程中,使用了氯仿、二氯甲烷、乙醚、乙醇等溶剂,而氯仿、二氯甲烷属二类残留溶剂[7],而其余则属毒性尚不足的4类溶剂,故根据药典要求对其氯仿、二氯甲烷残留量进行了测定。
[1]常萍,袁永荣,王本杰.苦参素片人体生物等效性研究[J].山东大学学报,2004,42(4):484-486.
[2]史丽娟,石磊,宋光耀.氧化苦参碱肝脏药理作用的研究进展[J].世界科学技术:中医药现代化,2014,16(2):448-450.
[3]吴晓丽,王柏.苦参素微孔渗透泵片的研制[J].中国药科大学学报,2010,41(1):45-49.
[4]刘月.苦参素注射剂系列品种及苦参药材质量控制研究[D].福州:福建中医药大学,2012.
[5]李正蓉.苦参素的药理与临床研究进展[J].华西药学杂志,2003,18(6):435.
[6]张冬青,程怡,钟翠丽.苦参素脂质体的体外释放度研究[J].广东轻工职业技术学院学报,2011,10(3):25-27.
[7]国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社,2010:附录ⅧP.
Determination of Residual Organic Solvents during Oxymatrin Extraction Process by Gas Chromatography
Yang Jianlin1,Jin Xicheng1,Huang Jie2,Shan Min2
(1.Xiji County People′s Hospital,Guyuan,Ningxia,China 756299;2.Xi′an Municipal Institute for Food and Drug Control,Xi′an,Shaanxi,China 710054)
Objective To establish a method for determination of residual organic solvents during the extraction process.Methods The chromagraphy column was 0.25-0.18 mm divinylbenzene-ethyl vinyl benzene type porous polymer beads(401 organic carrier body),2 m×3.2 mm glass column,inlet and detector temperature was 220℃,the column temperature was 130℃,N230 mL/min,H230 mL/min,Air 300 mL/min,S 101×23,and the injection volume was 100μL.Results Dichloromethane and chloroform linear was about in the range of 2-10μg/mL;dichloromethane RSD was 0.1%,the lowest detection limit was 0.201 9 ng,the limit of quantitation was 0.605 7 ng;chloroform RSD was 0.3%,the lowest detection limit was 0.218 6 ng,and the limit of quantitation was 0.655 8 ng.The average recovery of dichloromethane was 99.73%(n=9),and average of chloroform was 100.21%(n=9).Conclusion The method has good linearity,precision and recovery.The result is accurate and reliable for the determination of residual dichloromethane and chloroform.
gas chromatography;oxymatrin;dichloromethane;chloroform
R284.1;R282.71
A
1006-4931(2015)22-0128-02
2015-05-07;
2015-07-25)

