紫荆花精油体外抗氧化活性研究
马雪梅,胡鹏飞,方玲,唐伟,王利平,于烦烦,毕淑峰
(黄山学院生命与环境科学学院,安徽黄山245041)
紫荆花精油体外抗氧化活性研究
马雪梅,胡鹏飞,方玲,唐伟,王利平,于烦烦,毕淑峰*
(黄山学院生命与环境科学学院,安徽黄山245041)
研究紫荆花精油的体外抗氧化活性。采用水蒸气蒸馏法提取紫荆花的精油,以ABTS·、·O2-、亚硝酸钠清除作用和金属离子螯合作用为指标评价紫荆花精油的体外抗氧化活性。研究结果表明,紫荆花25%精油对ABTS·、·O2-、亚硝酸钠的清除作用和金属离子螯合作用的效果明显,其ED50值分别为24.11、64.46、101.55、54.65 μL。紫荆花精油具有较好的体外抗氧化活性,样品量与抗氧化活性存在剂量依赖关系。
紫荆花;精油;抗氧化活性
食品与空气中氧气的氧化反应造成食品变质和营养损失,生物体衰老与疾病也与生物体内自由基代谢失衡密切相关。因此,抗氧化剂在食品保藏和延缓衰老、疾病治疗过程中发挥重要作用。丁基羟基茴香醚(BHA)、二丁基羟基甲苯(BHT)等人工合成抗氧化剂有潜在的毒性、致癌等缺点,天然抗氧化剂因其安全、无毒、高效等优点,受到关注和欢迎,从植物中寻找天然抗氧化剂意义重大。
紫荆花是豆科紫荆属紫荆(Cercis chinensis Bge)的花,又名满条红,原产于中国,作为观赏植物,在我国广泛栽培。紫荆花含有黄酮、甾醇、色素、挥发油等生物活性物质[1-4],紫荆花黄酮、色素对羟自由基和超氧阴离子自由基有清除作用[5-6],但对紫荆花挥发油的抗氧化活性鲜有报道。本试验以ABTS·、·O2-、亚硝酸钠的清除作用和金属离子的螯合作用为指标综合评价紫荆花精油的抗氧化活性,为紫荆花的开发利用和天然抗氧化剂的研究提供科学参考。
1材料与方法
1.1 材料与仪器
紫荆花于2013年4月采自黄山学院校园。2,2-联氮基-双-(3-乙基苯并噻唑啉-6-磺酸)二氨盐(ABTS,Regal Biotechnology Company);菲洛嗪(Ferrozine,东京化成工业株式会社);无水乙醚、2,6-二叔丁基-4-甲基苯酚(BHT)、乙二胺四乙酸(EDTA)等均为国产分析纯。UV754N紫外可见分光光度计:上海精密科学仪器有限公司。
1.2 方法
1.2.1 紫荆花精油的提取
称取60 g样品置于挥发油提取器500 mL圆底烧瓶中,加350 mL蒸馏水,在连接管位置加10 mL无水乙醚。按水蒸气蒸馏法提取6 h,收集无水乙醚层,用无水硫酸钠干燥,常温挥发无水乙醚溶剂,得到具有浓郁香味的淡黄色透明油状物,共提取8次。用丙酮将精油稀释成体积分数25%,存放冰箱备用。
1.2.2 紫荆花精油对ABTS·清除作用的测定[7]
将等量的7 mmol/LABTS溶液与2.45 mmol/L过硫酸钾混合后置于暗处12 h。用甲醇将ABTS溶液稀释至在734 nm处吸光度为(0.70±0.02)。将不同体积(20 μL~100 μL)样品加入2 mL ABTS自由基溶液中,6 min后测其吸光度Ai。测定2 mLABTS自由基溶液与样品体积相同甲醇混合后的吸光度A0;测定2 mL甲醇溶液与不同体积样品液的吸光度Aj。
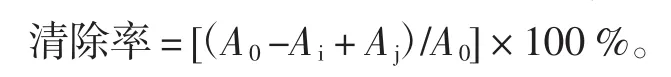
1.2.3 紫荆花精油对亚硝酸钠清除作用的测定[8]
将0.5 mol/L柠檬酸钠-盐酸缓冲液(pH3.0)5.0 mL置于10 mL容量瓶中,加入1 mL 0.1 g/L的NaNO2溶液和20 μL~100 μL 25%挥发油,用蒸馏水定容至刻度,37℃下反应1 h。取1 mL反应液,加入4 g/L对氨基苯磺酸溶液2 mL和2 g/LN-1-萘乙二胺盐酸盐1 mL,摇匀放置15 min,在540 nm处测吸光度值AX;同时做对照实验测其吸光度A0。
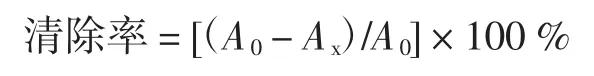
1.2.4 紫荆花精油对金属离子的螯合作用的测定[9]
取不同体积(20 μL~100 μL)25%挥发油,用丙酮将各样品体积补至100 μL。加入2.8mL蒸馏水、50 μL 2mmol/L的FeCl2·4H2O和50μL5mmol/L的Ferrozine1,10 min后在562 nm处测吸光度At,以100 μL丙酮代替挥发油样品作为空白对照,测其吸光度A0。
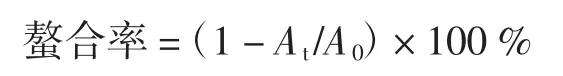
1.2.5 紫荆花精油对超氧阴离子自由基清除作用的测定[10]
分别向5支试管加入4.5 mL 50 mmol/LTris-HCl缓冲液(pH8.2)和20、40、60、80、100 μL挥发油,再分别加入80、60、40、20、0 μL丙酮,混匀后在25℃恒温水浴中保温20 min,取出后立即加入在25℃预热过的3 mmol/L邻苯三酚溶液0.3 mL(以10 mmol/LHCl溶液配制)启动反应。5 min后加4滴10 mol/L盐酸终止反应,在325 nm处测吸光度(An)。以加0.3 mL 10 mmol/L HCl代替邻苯三酚溶液为对照,测其吸光度(A0)。
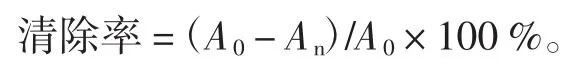
2结果与分析
2.1 紫荆花精油对ABTS·的清除作用
ABTS·清除法是一种测定总抗氧化能力的方法,具有操作简单、快速等优点[11]。紫荆花精油对ABTS·的清除作用见图1。
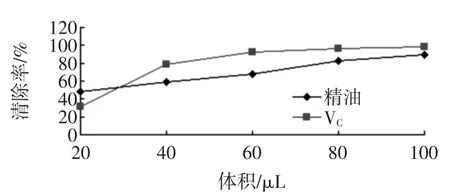
图1 精油对ABTS·的清除作用Fig.1Scavenging capacity against ABTS·of essential oil
由图1可知,25%紫荆花精油对ABTS·具有一定的清除能力,体积为100 μL时,清除率为89.29%。体积为20 μL时,25%精油对ABTS·的清除作用强于1 mg/mL的维生素C;体积为40 μL~100 μL时,25%精油对ABTS·的清除作用弱于1 mg/mL的维生素C。精油对对ABTS·的清除率随着样品体积的增加而增大,两者存在存在量效关系;精油体积(X)与清除率(Y)间的回归方程为Y=0.535 7X+37.085 1,R2=0.988 7。精油和维生素C的ED50(清除率为50%时的样品体积)分别为24.11、21.46 μL。
2.2 紫荆花精油对亚硝酸钠的清除作用
亚硝酸钠是一种防腐剂和腌制剂,广泛存在于多种食品中,亚硝酸盐是强致癌物亚硝胺的前体物质,清除亚硝酸盐具有防治癌症的功能[12]。紫荆花精油对亚硝酸钠的清除作用见图2。
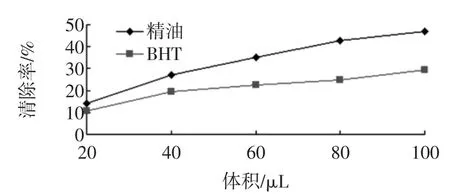
图2 精油对亚硝酸钠的清除作用Fig.2Scavenging capacity against sodium nitrite of essential oil
由图2可知,25%的精油对亚硝酸钠具有较好的清除能力,清除效果优于1 mg/mL的BHT。随着样品体积的增加,精油对亚硝酸钠的清除率逐渐增大,但增幅逐渐减少。精油体积(X)与清除率(Y)的回归方程为Y=0.404 3X+8.942 0,R2=0.963 9。精油和维生素C的ED50分别为101.55、195.61 μL,维生素C的体积为精油体积的1.93倍。
2.3 紫荆花精油对金属离子的螯合作用
金属离子在自由基氧化过程中起催化剂作用,螯合金属离子可以阻止自由基的链式反应。紫荆花精油对金属离子的螯合作用见图3。
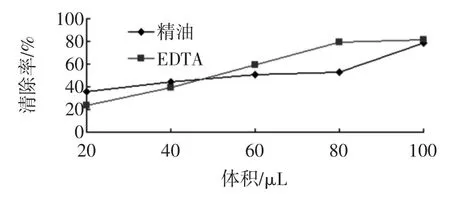
图3 精油对金属离子的螯合作用Fig.3Metal chelating ability of essential oil
由图3可知,25%紫荆花精油对金属离子具有一定的螯合作用,体积为100 μL时,螯合率为78.79%。体积为20 μL~40 μL时,25%紫荆花精油对金属离子的螯合效果优于0.5 mg/mL的EDTA;体积为60 μL~100 μL时,精油对金属离子的螯合效果弱于EDTA。在测定的体积范围内,精油体积与螯合率间呈正相关。精油体积(X)与螯合率(Y)的回归方程为Y=0.474 9X+ 24.045 1,R2=0.863 8。精油和EDTA的ED50分别为54.65、51.74 μL。
2.4 紫荆花精油对·O2-的清除作用
·O2-是人体内产生的第一个氧自由基,它不仅自身有毒性,而且经过一系列反应生成其他氧离子自由基,进一步损伤生物体。紫荆花精油对·O2-的清除作用见图4。
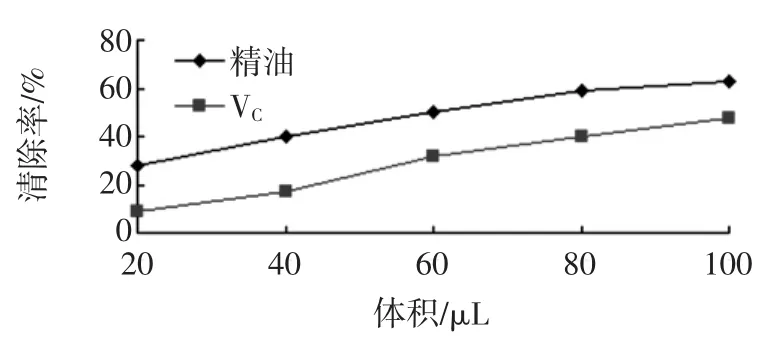
图4 精油对·O2-的清除作用Fig.4Scavenging capacity against·O2-of essential oil
由图4可知,25%紫荆花精油对·O2-有较好的清除能力,清除作用优于1 mg/mL的维生素C。在测定的体积范围内,清除率随着精油体积的增加而逐渐增大,两者呈剂量依赖关系。精油体积(X)与清除率(Y)的回归方程为Y=0.440 6X+21.601 1,R2=0.966 4。精油和维生素C的ED50分别为64.46、101.61 μL,维生素C的体积是精油体积的1.58倍。
3结论
本研究以ABTS·、·O2-、亚硝酸钠的清除作用和金属离子螯合作用为指标综合评价紫荆花精油的体外抗氧化活性。研究结果表明,紫荆花精油具有良好的体外抗氧化活性,且各指标与样品体积呈剂量依赖关系,其ED50分别为24.11、64.46、101.55、54.65 μL。紫荆花精油对ABTS·的清除效果最好,对金属离子螯合效果和·O2-清除效果次之,对亚硝酸钠的清除效果最差。因此,紫荆花精油在天然抗氧化剂的研发中具有应用前景。
[1]徐美奕,韩雅莉,东野广智,等.紫荆花总黄酮的分离纯化与光谱分析[J].中药材,2007,30(10):1252-1255
[2]朱庆英,何翠香.醇溶法提取紫荆花色素及其稳定性研究[J].食品工业科技,2009,30(2):268-270
[3]高虹,王俊卿,张思群,等.微波—表面活性剂协同提取紫荆花红色素的研究[J].食品工业科技,2004,25(6):108-110
[4]李勉,王金梅,康文艺.HS-SPME-GC-MS法分析紫荆花及其花蕾的挥发性成分[J].中成药,2009,31(7):1087-1090
[5]陈志红,徐美奕,龚先玲.紫荆花黄酮类化合物体外抗氧化活性研究[J].化学世界,2010,51(7):401-403
[6]王金亭,吴广庆,鞠秀萍.紫荆花色素提取液体外抗氧化活性的研究[J].化学与生物工程,2009,26(1):36-38
[7]杨少辉,宋英今,王洁华,等.雪莲果体外抗氧化和自由基清除能力[J].食品科学,2010,31(17):166-169
[8]陆占国,李伟,封丹.莳萝籽精油成分及清除亚硝酸钠研究[J].天然产物研究与开发,2010(22):479-482
[9]毕飞翔,张维维,孙强伟,等.紫花苜蓿叶挥发油的体外抗氧化活性研究[J].安徽农业科学,2013,41(9):4084-4085
[10]杨润亚,明永飞,王慧.无花果叶中总黄酮的提取及抗氧化活性研究[J].食品科学,2010,31(16):78-82
[11]张逸波,郑文杰,黄峙,等.硒杂环化合物SPO清除DPPH和ABTS自由基的光谱学研究[J].光谱学与光谱分析,2010,30(7):1866-1871
[12]李标,张鹏,蒋彬,等.毛白杜鹃挥发油化学成分及清除亚硝酸钠活性研究[J].中成药,2013,35(1):124-126
Study on Antioxidant Activity of Essential Oil from Cercis chinensis Flowers in Vitro
MA Xue-mei,HU Peng-fei,FANG Ling,TANG Wei,WANG Li-ping,YU Fan-fan,BI Shu-feng*
(College of Life and Environment Science,Huangshan University,Huangshan 245041,Anhui,China)
To study the antioxidant activity of essential oil from Cercis chinensis flowers in vitro.The essential oil from Cercis chinensis flowers was extracted by steam distillation and its antioxidant activity was evaluated by scavenging capacity againstABTS·,sodium nitrite,and metal chelating ability.The 25%essential oil exhibited significant scavenging capacity against ABTS·,·O2-,sodium nitrite,and metal chelating ability with ED50value of 24.11,64.46,101.55,54.65 μL,respectively.The essential oil from Cercis chinensis flowers exhibited significant antioxidant activity in vitro in a concentration-dependent fashion.
Cercis chinensis flowers;essential oil;antioxidant activity
10.3969/j.issn.1005-6521.2015.09.002
2013-12-23
安徽省大学生创新创业计划项目(201210375041);黄山学院自然科学基金项目(2015xkjq004)
马雪梅(1992—),女(汉),学士,研究方向:食品化学。
*通信作者:毕淑峰(1975—),男(汉),副教授,研究方向:天然产物化学。

