芳香族羧酸银(I)配合物的合成及其抑制脲酶的研究①
马承富,靖海瑞,刘慈,李玉广
(1.武汉纺织大学化学化工学院,湖北 武汉 430073;2.湖南师范大学化学化工学院,湖南 长沙 410006)
0 引言
脲酶又称尿素水解酶(编号为EC 3.5.1.5),它是一种含镍寡聚酶,具有绝对的专一性,它可以特异性地催化脲水解为氨和二氧化碳,其水解产物氨可为许多微生物体和植物的新陈代谢提供氮源,并对它们周围环境的pH值起着关键性调节作用[1];同时,这也引起自然界中许多负面效应[2-3].如脲酶可过度催化降解尿素生成挥发性的NH3和CO2,而引起氮肥肥效的丢失和导致土壤中氨离子浓度增加及pH值升高,影响植物的正常生长;脲酶也可作为一种病原体的毒素引发胃炎、胃溃疡及胃癌等疾病.如幽门螺杆菌利用自身产生的大量脲酶去催化水解脲,导致其周围的pH值升高,来抵抗胃酸的杀灭作用.因此,有必要寻找合适的脲酶抑制剂来科学调控脲酶的活性,消除其产生的负面效应.目前已报道的脲酶抑制剂主要有两类,它们分别为过渡金属离子类脲酶抑制剂和有机化合物类脲酶抑制剂[4-7].前者由于重金属离子具有较大的毒性,而受到了一定的应用限制;后者又因为有效抑制时间短、效率低及有毒副作用,应用上也有局限性[4-8].Rosi等[9]认为,有机小分子和重金属盐类形成配合物后,有机配体和金属离子均被固定在配合物骨架中,其毒性大大降低,发挥作用的时间也相对延长.配合物兼具无机和有机功能基团的性质和功能,其物理化学性能明显优于单功能基团.目前配合物类脲酶抑制剂仍没有被人们广泛报道[10].
另外,羧酸银(I)配合物在生物、光学、催化等方面具有潜在的应用.对羧酸银(I)化合物分子结构的研究在晶体工程学上也具有重要的意义.银离子可以形成新颖的一维、二维和三维配合物[11-14].我们分别以3-吡啶甲酸、3,5-二硝基苯甲酸、对苯二甲酸、联苯二甲酸及2-氨基吡啶、4-氨基吡啶、2-氨基嘧啶为原料,通过它们的自组装反应过程,制备了4种新的羧酸银(I)配合物,并测定了这些银(I)配合物的分子结构.研究芳香族羧酸银(I)化合物抑制脲酶的生物活性.
1 实验部分
1.1 化学试剂和仪器氧化银、3-吡啶甲酸、3,5-二硝基苯甲酸、对苯二甲酸、4,4’-联苯二甲酸、2-氨基吡啶、2-氨基嘧啶、4-氨基吡啶、1,6-己二胺购自Alfa Aesar,Jack豆脲酶购自Sigma-Aldrich公司,实验中所用药品均为分析纯,实验用水为超纯水.
配合物的C、H、N元素分析用Elementar Vario EL III元素分析仪(德国)测定,单晶结构用Bruker SMARTApex CCD II单晶衍射仪测定,配合物抑制脲酶的生物活性用synergyTM HT酶标仪(美国)测定.
1.2 羧酸银(I)配合物1 4的合成
1.2.1 [Ag2(L1)2(A1)2]2·H2O(1) 将25 mL的Ag2O(1 mmol,0.23 g)氨水溶液加入25 mL的3-吡啶甲酸(2mmol,0.25 g)氨水溶液,搅拌3min后,再加入2-氨基吡啶(1mmol,0.09 g),在室温下搅拌20min.过滤,将澄清溶液避光静置,室温挥发10 d,得到无色块状配合物1,取其母液进一步培养出其单晶固体.产率约55%.化学式为C44H42Ag4N12O9,元素分析实验值(计算值)%:C 40.15(40.21),H 3.37(3.22),N 12.83(12.79).
1.2.2 [Ag2(L2)2(A2)3]·H2O(2) 将25mL的Ag2O(1mmol,0.23 g)氨水溶液加入25mL的3,5-二硝基苯甲酸(2mmol,0.424 g)氨水溶液,搅拌3min后,再加入2-氨基嘧啶(1mmol,0.10 g),在室温下搅拌20min.过滤,将澄清溶液避光静置,室温挥发14 d,得到橙黄色块状配合物2,取其母液进一步培养出单晶固体.产率约31%.化学式为C26H25Ag2N13O12,元素分析实验值(计算值)%:C 33.41(33.48),H 2.75(2.70),N 19.53(19.52).
1.2.3 [Ag(A3)2]2(L3)·10H2O(3) 将25mL的Ag2O(1mmol,0.23 g)氨水溶液加入25mL的对苯二甲酸(1mmol,0.17 g)氨水溶液,搅拌3min后,再加入4-氨基吡啶(1mmol,0.09 g),在室温下搅拌20min.过滤,将澄清溶液避光静置,室温挥发14 d,得到无色块状配合物3,取其母液进一步培养出单晶固体.产率约60%.化学式为C28H48Ag2N8O14,元素分析实验值(计算值)%:C 35.88(35.91),H 5.91(5.17),N 11.90(11.97).
1.2.4 [Ag2(A4)2](L4)·4H2O(4) 将25mL的Ag2O(1mmol,0.23 g)氨水溶液加入25mL的4,4-联苯二甲酸(2mmol,0.24 g)氨水溶液,搅拌3min后,再加入1,6-己二胺(1mmol,0.09 g),在室温下搅拌20min.过滤,将澄清溶液避光静置,室温挥发14 d,得到无色块状配合物4,取其母液进一步培养出单晶固体.产率约36%.化学式为C26H48Ag2N4O8,元素分析实验值(计算值)%:C 39.99(41.07),H 6.49(6.36),N 7.36(7.37).
1.3 晶体结构测定选取合适大小的单晶体用于X线衍射测试[16-17],温度约为293(2)K,在Bruker SMARTApex CCD II衍射仪上收集强度数据,利用石墨单色器单色化了的Mo-Ka射线(λ=0.710 73 nm),采用ω-2θ扫描方式,收集2θ在2.0~55.0度范围内的衍射数据,得到一定数目的独立衍射点,同时可得到Ⅰ≥2σ(I)时衍射点的数目.羧酸银(I)化合物的衍射数据用SAINT程序进行还原处理,用SADABS程序进行数据校正,其中部分结构还进行了ψ吸收校正.在Pentium PC计算机上用SHELXS-97结构解析程序对晶体初始结构模型进行直接法解析.并利用SHELXL-97结构解析程序,采用全矩阵最小二乘法进行结构修正.化合物的氢原子坐标由差Fourier合成和理论加氢程序找出.所有氢原子的坐标和各向同性温度因子参加结构计算,但不参加修正.最后的残余峰均已不具有化学意义.羧酸银(I)化合物的晶体学数据及衍射强度的收集条件详情见表1.羧酸银(I)化合物的原子坐标、温度因子、主要键长、键角详情见表 2.CCDC 659659(1),CCDC 659658(2),CCDC 293904(3),CCDC 659657(4).
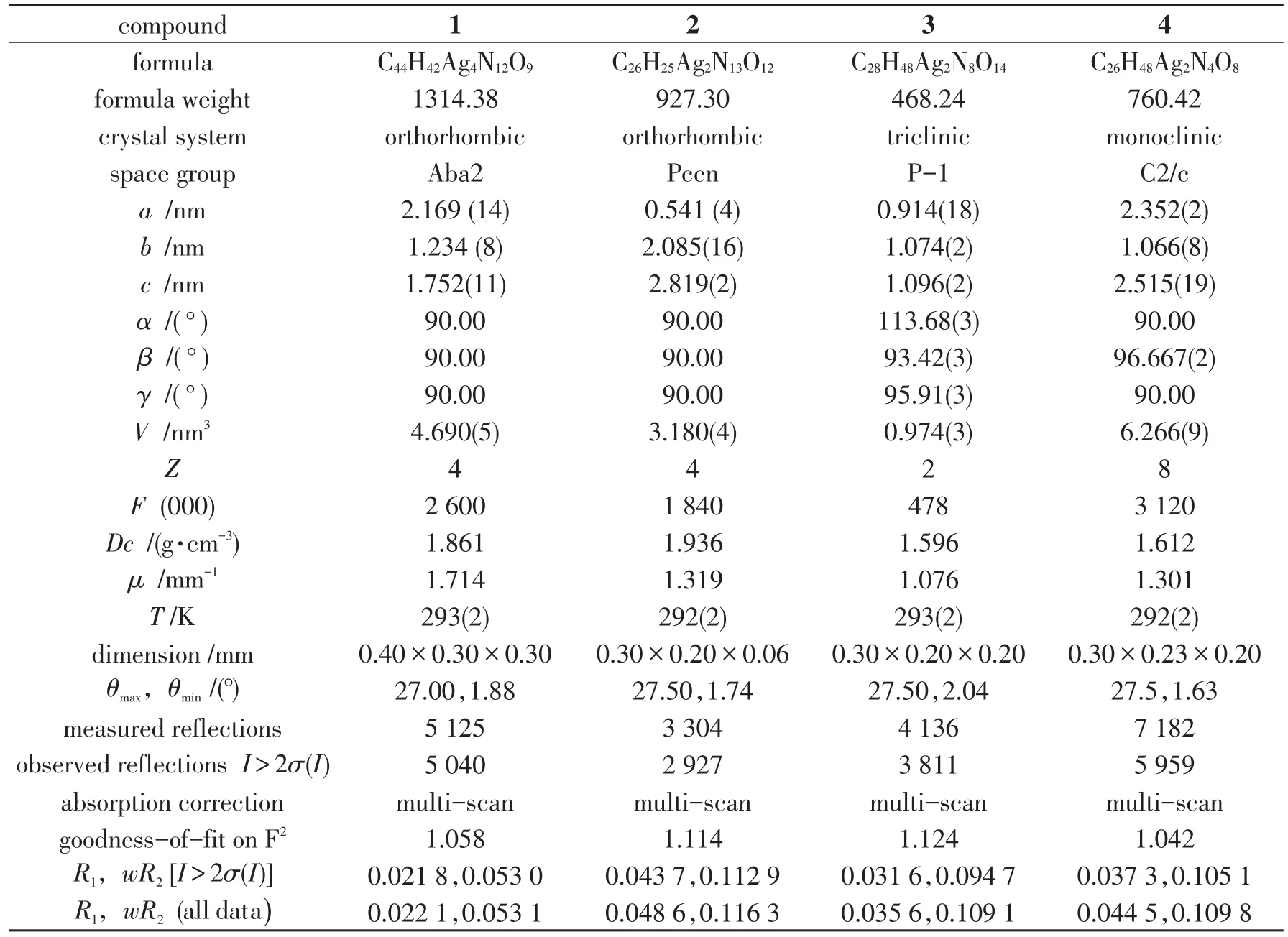
表1 配合物1 4的晶体学数据及衍射强度的收集条件
1.4 Ag(I)配合物的生物活性的测试用二甲亚砜和水(V/V,1∶1)的混合溶剂配制不同梯度浓度的待测配合物溶液.参照文献[17-18],将含有Jack豆脲酶(25 μL,10 kU·L-1)和各种浓度的待测配合物(25μL)的混合溶液放置在化验盘(96孔)中,37℃下预培养1 h.再加入含有脲酶(500 μmol·L-1)的Hepes缓冲溶液(0.2 mL,100 μmol·L-1;pH=6.8)和浓度为0.002%的酚红指示剂,并在37℃下进行培养.反应时间通过微盘读卡器(560 nm)来测量,测试缓冲溶液pH值从6.8提高到7.7时酚红指示剂的吸光度变化.
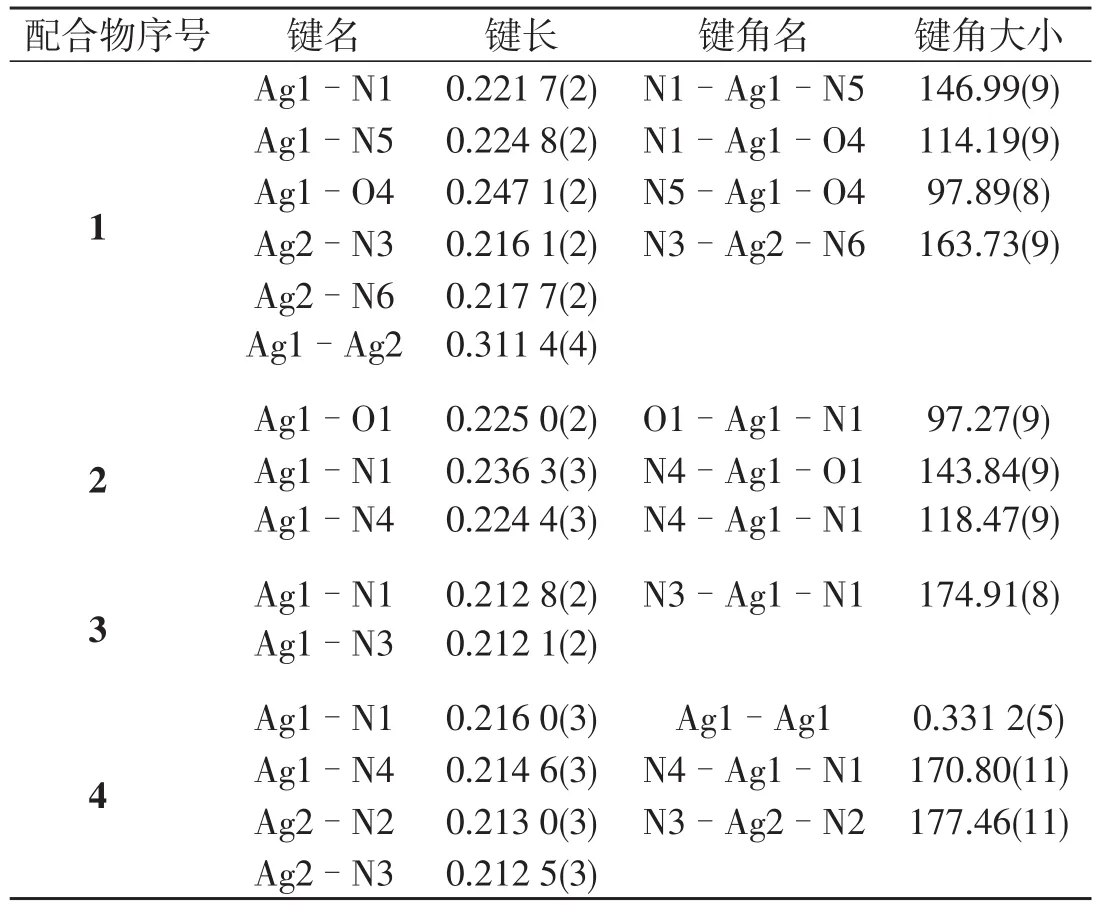
表2 配合物1 4的部分键长和键角 nm,(°)
2 实验结果与讨论
2.1 配合物[Ag2(L1)2(A1)2]2·H2O(1)的分子结构配合物1属于正交晶系,空间群为Aba2.如图1所示,在分子结构中存在着二配位和三配位的银金属中心[19-20].其中Ag1是由一个2-氨基吡啶的吡啶环上N原子和一个3-吡啶甲酸吡啶环上的N原子及一个羧基的桥连O原子形成三配位中心.Ag1-N1、Ag1-N5、Ag1-O4的键长分别为0.221 7(2)nm、0.224 8(2)nm、0.247 1(2)nm,N1-Ag1-O4、N5-Ag1-O4、N5-Ag1-N1的键角分别为114.(8)°、97.9(8)°、147.9(9)°;而Ag2是由一个2-氨基吡啶的吡啶环上N原子和一个吡啶环上的桥连N原子形成二配位中心[21-22].Ag2-N3、Ag2-N6的键长分别为0.216 1(2)nm、0.217 7(2)nm,N3-Ag2-N6的键角为163.73(9)°.Ag1与N1、N5、O4三个原子共平面较好,Ag1偏离其平面约为0.004 3 nm.3-吡啶甲酸以吡啶环上的N原子和一个羧酸O原子桥连两个Ag原子形成一个双核结构单元.该双核结构单元通过Ag…Ag弱相互作用进一步形成了一个二聚体.Ag…Ag的距离为0.311(4)nm,小于范德华半径的总和(0.340 nm)[21].此外,在配合物1中还存在分子间N4…O1和N4…O3的氢键弱相互作用(如表3所示).
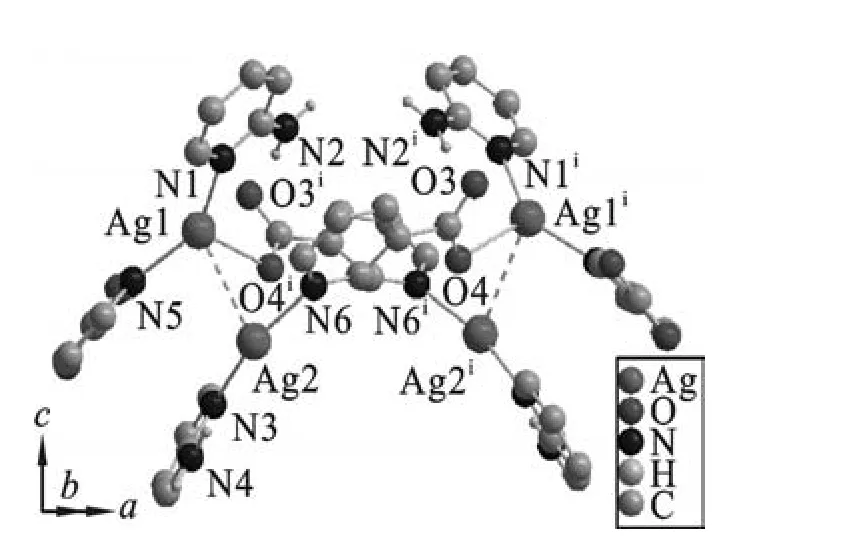
图1 配合物1的分子结构(对称代码:(i)1-x,2-y,z)
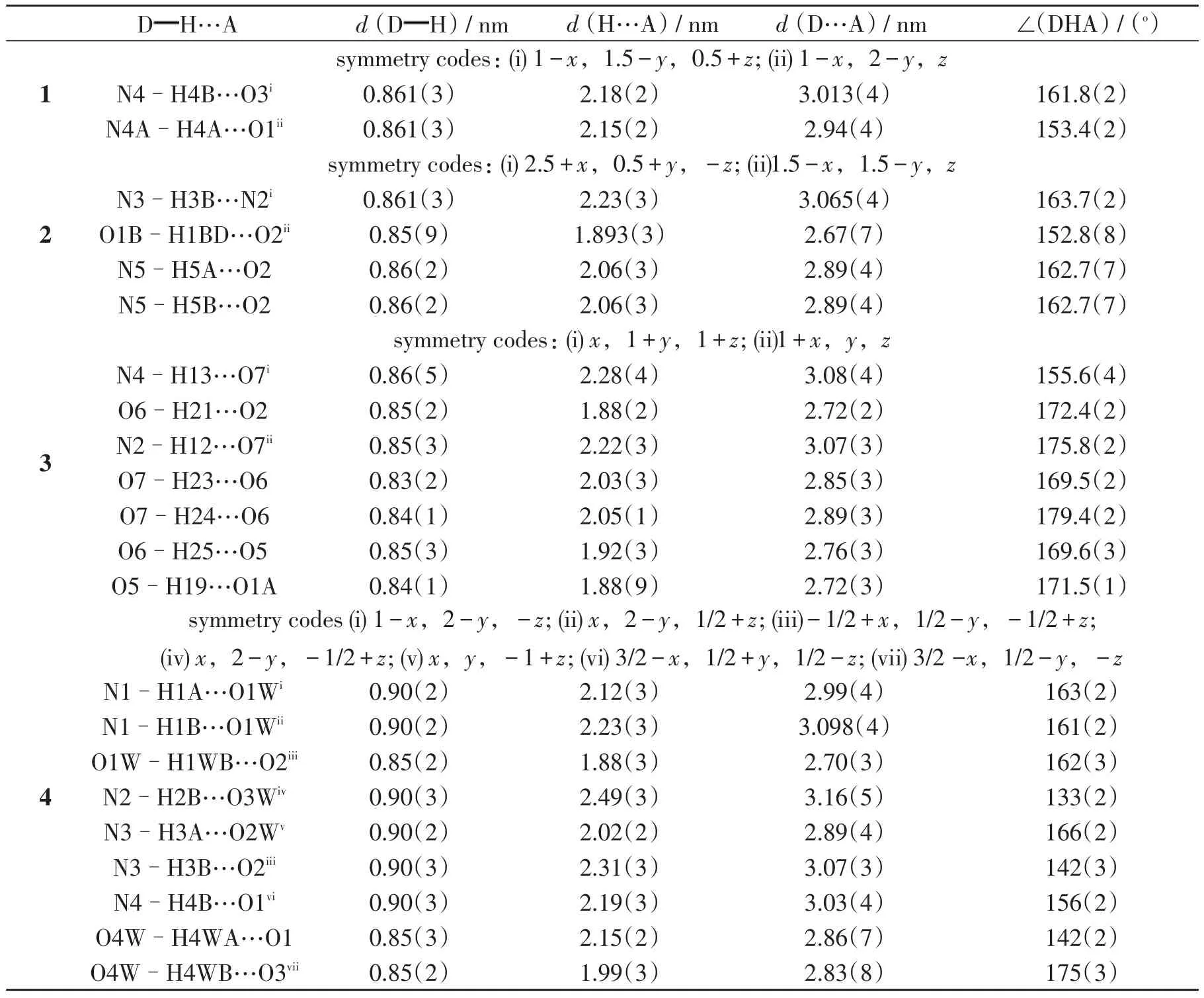
表3 配合物1 4的氢键数据
2.2 配合物[Ag2(L2)2(A2)3]·H2O(2)的分子结构配合物2属于正交晶系,空间群为Pccn.如图2所示,分子结构中银原子是由一个羧基O原子和两个嘧啶环上的N原子形成三配位金属中心.Ag1-O1、Ag1-N1、Ag1-N4 的键长分别为0.225 0(2)nm、0.236 3(3)nm、0.224 4(3)nm;N1-Ag1-N4、N1-Ag1-O1、N4-Ag1-O1的键角分别为118.5(8)°、97.3(8)°、143.8(8)°.在配合物2中,一个2-氨基嘧啶通过嘧啶环中两个N原子桥连两个银原子形成双核银的结构单元.Ag1与O1、N1、N4原子共平面性较好,Ag1偏离其平面约为0.002 9 nm.此外,在化合物2的对称轴上存在一个的晶格水分子,其通过分子间的氢键与上述双核银离子的结构单元进行作用(如表3所示).O1、O2、N5和O2构成了一个平面四边形.化合物2又通过N3…N2的分子间氢键弱作用,构成一维链状结构.

图2 配合物2的分子结构图(对称代码:(i)3/2-x,3/2-y,z)
2.3 配合物[Ag(A3)2]2(L3)·10H2O(3)的分子结构配合物3属于三斜晶系,空间群为P-1.如图3所示,分子结构中银原子是由两个吡啶环上的N原子形成二配位金属中心.Ag1-N1和Ag1-N3的键长分别为0.211 8(2)nm和0.2121(2)nm;N1-Ag1-N3的键角为174.91(8)°,略小于180°.两个吡啶的环平面的二面角约为4.1°,趋近于平行;而吡啶环平面和苯环平面的二面角平均为98.1°,趋近于垂直.在3的分子固体结构中存在着许多晶格水分子,这些水分子在形成3的固体结构过程中起着重要的作用.4-氨基吡啶的氨基与水分子及对苯二甲酸的羧基形成了一个复杂的氢键网络,构成配合物3的三维空间结构.此外,相邻4-氨基吡啶分子的吡啶环心的距离约为0.361 7 nm[24],存在π-π弱相互作用,形成偏移堆积,进一步加强配合物3的分子空间结构.

图3 配合物3的分子结构图(对称代码:(i)1-x,1-y,2-z)

图4 配合物4的分子结构图(对称代码:(i)x,1+y,z;(ii)3/2-x,3/2+y,1/2-z)
2.4 配合物[Ag2(A4)2](L4)·4H2O(4)的分子结构配合物4属于单斜晶系,空间群为C2/c.与配合物3相比,分子结构中银原子是由2个1,6-己二胺的末端N原子形成二配位金属中心,如图4所示.Ag1-N1和Ag1-N4A的键长分别为0.216 0(3)nm和0.214 6(3)nm,N1-Ag1-N4A的键角为170.80(11)°;而Ag2-N2和Ag2-N3的键长分别是0.213 0(3)nm和0.212 5(3)nm,N2-Ag2-N3的键角为177.46(11)°.1,6-己二胺通过2个末端N原子桥连2个Ag(I)原子,形成一维zigzag链状结构.相邻两个一维zigzag链的Ag…Ag之间的距离为0.331 2(5)nm,其略小于2个Ag原子的范德华半径之和(0.340 nm)[23],由此配合物4通过相邻一维zigzag链的Ag…Ag弱相互作用形成二维平面结构.在4的分子固体结构中也存在着许多晶格水分子,这些水分子在形成4的固体结构过程中起着重要的作用.
2.5 配合物1 4的生物活性分别测试了不同浓度时4种芳香族羧酸银(I)配合物抑制脲酶的生物活性.当羧酸银(I)配合物1、2、3和4的浓度为2.5μmol·L-1时,它们对脲酶催化水解尿素的生物活性的影响结果如图5所示.这4种银(I)配合物在测试抑酶实验中显示出不同程度上抑制脲酶的能力.相对于配合物4,在测试的16 h内配合物3明显地延长了脲酶催化水解尿素的反应时间,即配合物3的测试缓冲溶液pH值从6.8较缓慢地升高到7.7;配合物1和2在不同程度上也延长了脲酶催化水解尿素的反应时间.
如图6所示,这4种羧酸银(I)配合物具有不同的ⅠC50值(ⅠC50=0.12 ~ 21.35μmol·L-1).它们抑酶能力的强弱顺序为:3>2>1>4.在羧酸银(I)配合物3和4分子结构中,Ag(I)均为二配位,且都含有一些未配位的晶格水分子和羧酸根阴离子,但3抑制脲酶的能力显著强于4,这表明单核银结构的小分子比一维链状结构的大分子更有利于抑制脲酶;羧酸银(I)配合物1和2中,Ag(I)均为3配位,但2抑制脲酶的能力较强于1,这表明双核银离子结构的单体分子比双核银离子结构的二聚体分子更有利于抑制脲酶.
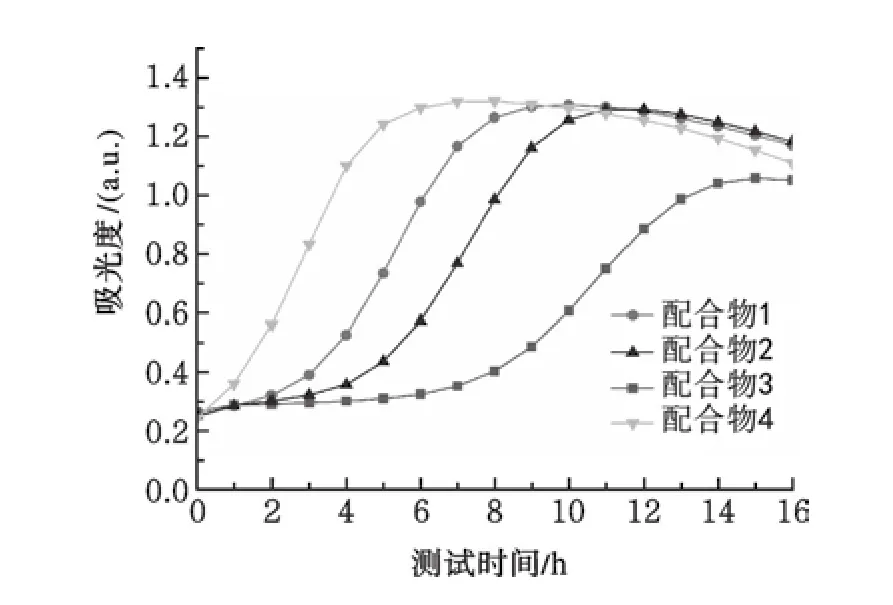
图5 含4种配合物(浓度为2.5μmol·L-1)的测试缓冲溶液

图6 4种羧酸银(I)配合物与脲酶作用的ⅠC50值
[1]Karplus PA,Pearson M A,Hausinger R P.70 Years of crystalline urease:what have we learned[J].Acc Chem Res,1997,30:330-337.
[2]Balasubramanian A,Ponnuraj K.Crystal structure of the first plant urease from jack bean:83 years of journey from its first crystal to molecular structure[J].JMol Biol,2010,400:274-283.
[3]CiurliS,BeniniS,Rypniewski WR,etal.Structural propertiesof the nickel ions in urease:novel insights into the catalytic and inhibition mechanisms[J].Coord Chem Rev,1999(190/192):331-355.
[4]Krajewska B,Ureases I.Functional,catalytic and kinetic properties:a review[J].J Mol Catal B Enzym,2009,59:9-21.
[5]于炎湖,詹志春,胡昌彬.脲酶抑制剂在反刍动物饲养中的应用[J].饲料工业,2003,24(7):4-5.
[6]王加启.脲酶抑制剂饲料添加剂产业化生产技术[J].中国畜牧兽医,2003,13:52-54.
[7]常巧玲.脲酶抑制剂在奶牛营养中的研究与应用[J].饲料与畜牧,2006(3):38-40.
[8]González R N,McKay C P,Mvondo D N.A possible nitrogen crisis for archaean life due to reduced nitrogen fixation by lightning[J].Nature,2001,412:61-64.
[9]Rosi N L,Kim J,Eddaoudi M,et al.Rod packings and metal-organic frameworks constructed from rod-shaped secondary building units[J].JAm Chem Soc,2005,127:1504-1518.
[10]柯爱飞,王趁义,牛习.脲酶抑制剂的研究现状与展望[J].安徽农业科学,2009,37(23):10883-10884.
[11]LiY G,Jiang Q B,Cheng K,etal.Syntheses and structural characterization of four new silver(I)complexeswith the N,N’(O)-bidentate bridging ligands[J].ZAnorg Allg Chem,2009(4):2572-2578.
[12]张奇龙,席晓岚,徐红.一维链状Ag(I)席夫碱配合物的合成和结构表征[J].分子科学学报,2008,28(10):154-156.
[13]方向倩,朱志彪,邓兆鹏,等.二维层状磺酸银髣配位聚合物的合成、晶体结构与性能研究[J].无机化学学报,2008,28(2):276-278.
[14]任艳平,孔祥建,龙腊生,等.异烟酸与Ag髣及硅钨酸配位聚合物的合成与晶体结构[J].无机化学学报,2012,27(6):1015-1020.
[15]Bruker AXSInc.Bruker,SMART(Version 5.628)and SAINT(Version 6.02)[CP/DK].Wisconsin:Bruker AXSInc,1998.
[16]Sheldrick GM.SADABS:Program for empiricalabsorption correction ofarea detector[CP/DK].University of Gettingen,1996.
[17]Tanaka T,Kawase M,Tani S.Urease inhibitory activity of simpleα,β-unsaturated ketones[J].Life Sci,2003,73:2985-2990.
[18]ZaborskaW,krajewska B,Olech Z.Heavymetal ions inhibition of jack bean urease:potential for rapid contaminant probing[J].J Enzyme Inhib Med Chem,2004,19:65-69.
[19]Cotton F A,Wilkinson G,Murillo C A,etal.Advanced inorganic chemistry[M].Chichester:John Wiley and Sons Ltd,1999:1085.
[20]Lancashire R J,Wilkinson G,Gillard RD,etal.In comprehensive coordination chemistry[M].Oxford:A Eds Pergamon Press,1987:775-850.
[21]Gimeno M C.Laguna A.In comprehensive coordination chemistry II[M].Mccleverty JA,Meyer T J,Eds.Boston:Elsevier Pergamon,2004(6):911-1145.
[22]Pyykko P.Strong closed-shell interactions in inorganic chemistry[J].Chem Rev,1997,97:597-636.
[23]BondiA J.Van der waalsvolumesand radii[J].Phys Chem,1964,68:441-451.
[24]Janiak C.A critical accounton π-π stacking inmetal complexes with aromatic nitrogen-containing ligands[J].Dalton Trans,2000,21:3885-3859.

