钕配位聚合物的合成、结构、电化学和荧光性质研究①
蔡李鹏,田瑶,徐娟,曾敏,范玉桥,王娟,朱文华
(1.有机化工新材料湖北省协同创新中心,湖北大学化学化工学院,湖北武汉430062;2.催化材料科学国家民委教育部重点实验室(中南民族大学),湖北武汉430074)
0 引言
稀土金属被称作“21世纪的材料”,它具有独特的物理化学性质,中国大量的稀土金属储备对经济和社会的发展具有深远影响[1-2].自二十世纪起,人们对稀土金属的研究,尤其是稀土金属的配位化学这一领域的研究愈来愈广泛.作为稀土金属中的一员,钕具有一些独特的化学发光性能.并且它与有机配体所形成的配合物,在发光材料[3],超导材料,分子结构塞,生物催化活性等领域已备受关注[4-7].
丁二酸是一种重要的羧酸化合物.羧酸化合物具有各式各样的配体,且大部分羧酸化合物与稀土金属所形成配合物都比较稳定,羧酸类配体是在组装配位聚合物时常用的配体,羧基不仅能以多种配位方式与金属离子键合,更可以与金属离子组合形成多核金属离子的次级结构单元,进而构造出各种各样的配位聚合物网状结构.同时,多羧基的取代位置可变,羧基的配位平面可旋转、取向灵活.可与金属离子组装成许多稳定的新型有趣的拓扑结构.羧酸类配位聚合物也在发光、催化、转化材料领域中被广泛研究.因此,它在配位化学中占有重要地位.国内外研究者对羧酸化合物和Nd(Ш)所形成配合物的报道屡见不鲜,例如,杨立荣合成了2,3-吡啶二羧酸和Nd(Ш)的配合物[8],RenataŁyszczek也合成了联苯-4,4-二羧酸和Nd(Ш)的配合物[9].在前人的基础上,为进一步探索羧酸类配位聚合物的结构和性质特点,本文中合成了一种丁二酸和Nd(Ш)的新型配合物,并研究了其热重、荧光和电化学性能.
1 实验部分
1.1 试剂与仪器所有药品都是未经处理的分析纯.配合物的红外光谱是由美国的NICOLET iS10光谱仪在400~4 000 cm-1范围内进行测量的(用KBr压片);紫外-可见吸收光谱由美国PE的Lambda 35在波长为200~800 nm范围内获得;荧光数据时在美国PE的LS-55荧光光谱仪上测量获得的;热重分析是在美国PERKIN ELMER公司TG/DTA热重分析仪上氮气氛围,升温速率为20℃/min条件下进行的.氧化还原峰是在室温下,用CH1660C电化学分析仪进行测试.
1.2 配合物的合成称取0.118 3 g丁二酸和0.220 1gNd(NO3)3·6H2O于烧杯中,再量取15mL蒸馏水混合均匀,搅拌0.5 h,用盐酸调节溶液pH值至3.8.再将溶液转移至25mL聚四氟乙烯内衬中,在170℃下加热5 d.反应完后冷却至室温,过滤,洗涤,保存滤液.两周后,滤液中有紫红色晶体析出.计算值(实验值):C,21.34(21.50);H,2.38(2.31).
1.3 X线单晶衍射结构测定将单晶配合物(0.09mm×0.10mm×0.12mm)置于Bruker SMARTAPEX CCD面探仪上在低温下,做单晶衍射,采用Mo-Kα射线(波长为0.071 073 nm),在296(2)K下收集衍射数据.数据的采集、索引以及原始晶胞的修正均采用SMART软件进行修饰.结构的整合和晶胞的修正用SAINT软件.每个数据集的吸收校正用SAINT软件.结构方案的细化和计算均还用SHELXTL[10-11]程序.晶体数据列于表1.

表1 单晶配合物的数据与结构
a)R1=∑||Fo|-|Fc||/∑|Fo|;b)
2 结果与讨论
2.1 红外光谱配合物的红外光谱在3 605 cm-1处的吸收是由于O H的伸缩振动造成的,表明配合物中含有水分子;在1 594 cm-1处的红外吸收是由配合物中的C O所引起的,因此可以证明羧基的存在;另外,在3 305 cm-1处有一个较宽的吸收谱带证明了配合物中氢键的存在.由此可以证明丁二酸和水分子与中心金属形成了配位聚合物.
2.2 晶体结构描述如图1所示,配合物单晶是三斜晶系,空间群为P-1.一个不对称单元中含有2个钕离子,3个丁二酸分子和2个水分子.钕与9个氧原子进行配位,形成一个九面体的配位化合物,其中9个氧原子有8个来源于丁二酸,一个来源于水分子,这些原子在Nd1-Nd2之间组成了3个变形的四边形,Nd1-Nd2之间的距离为0.412 7 nm,3个变形的四边形组成了一个靠椅式构型(如图2),在表2中给出了主要键长和键角的数据.

图1 晶体的不对称单元

图2 环状的椅式结构
如图3所示,钕与相邻的9个氧原子形成了一个多面体,相邻的Nd1和Nd2所形成的多面体成对出现.
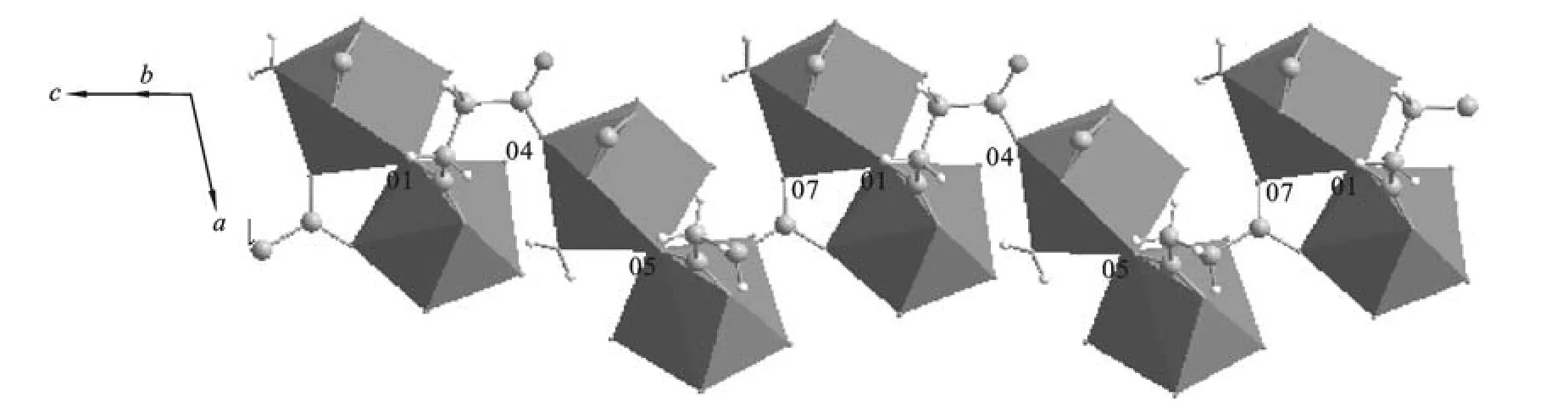
图3 配合物的一维多面体结构
相同的双核结构通过丁二酸中的O5和O7沿c轴形成了一个一维链状构型.Nd1-O5和Nd2-O7的键长分别为0.246 1(4)nm,0.241 2(5)nm.同样的,丁二酸中的O10和O11沿a轴形成了二维的网状结构,Nd2-O11和Nd1-O10的键长分别为0.250 5(5)nm,0.251 9(5)nm(如图4所示),表2列出了部分键长和键角的数据,键长范围从0.240 4(4)nm到0.261 2(4)nm,平均键长为0.250 0 nm,比报道过的九配合物[Nd2(pzdc)3(H2O)]n·nH2O[12]的Nd O键的平均键长为0.010 2 nm,配合物结构之间的氢键使得配合物之间更加稳定,表3给出了结构中的氢键键长和键角.在单元结构中,每2个不对称单元组成一个六角形,4个六角形通过丁二酸相互连接,形成一个沙漏状构型,如图5所示,构型中左上方有一个空隙,其尺寸大小为0.525 8 nm×0.445 8 nm,一些小分子,例如:H2、H2O分子等等都可以通过这个空隙.

表2 配合物中的部分键长和键角 nm,(°)
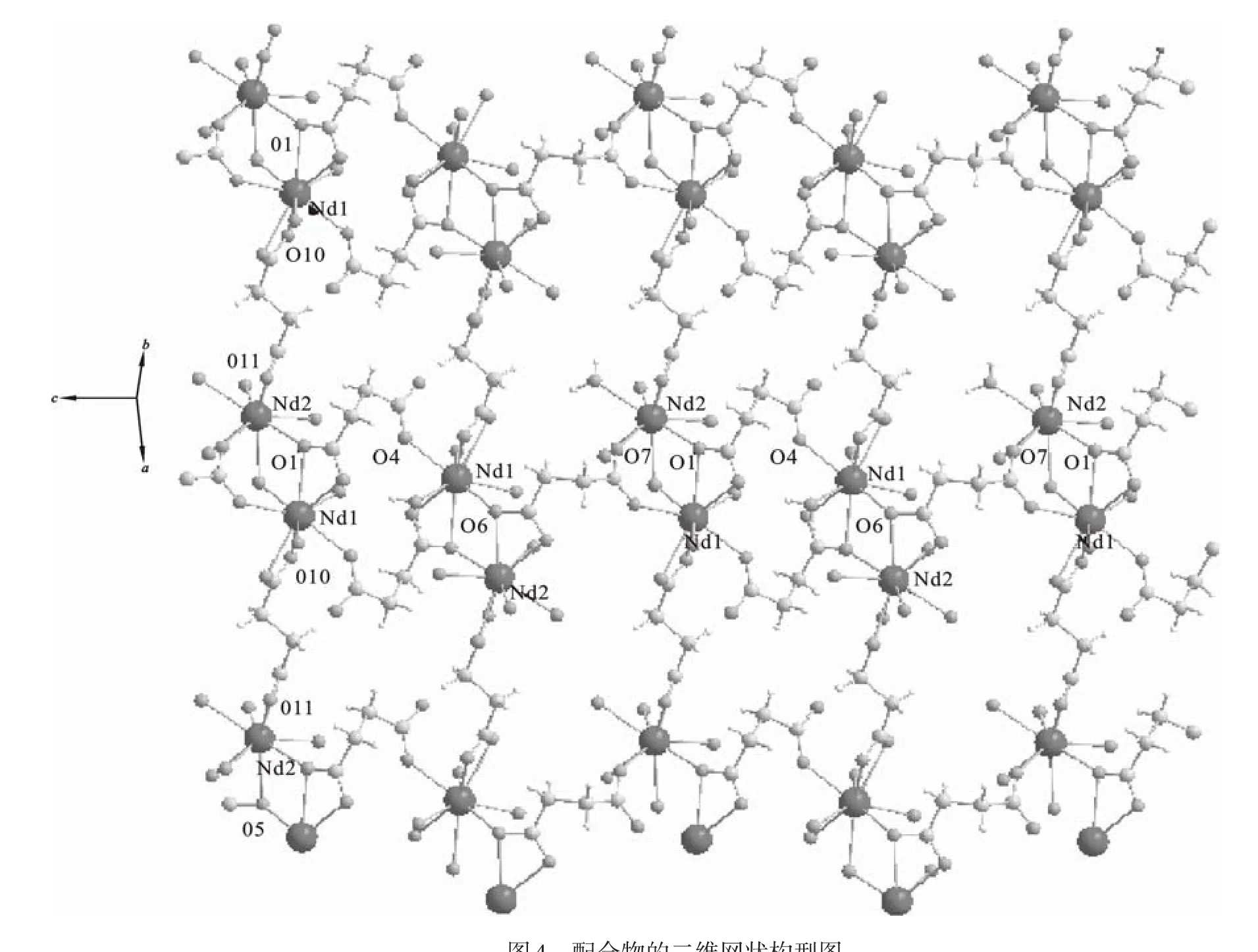
图4 配合物的二维网状构型图

表3 配合物中氢键键长和键角

图5 配合物的沙漏构型
2.3 紫外和荧光光谱配合物的紫外光谱是在水溶液中进行的.该配合物在204 nm处有一个吸收峰,而羧基中的C O的紫外吸收峰是在203 nm处.造成配体的紫外吸收向长波长方向移动的原因是形成配合物后的配体电子云密度降低,导致电子发生n→π*[13]跃迁.
配合物在H2SO4水溶液中的荧光光谱如图6所示,在激发波长为326 nm下,配合物的发射波长为367 nm,这主要是由配体的π*→n跃迁引起的.根据文献报道[14-16],钕和2,3-吡啶二羧酸所形成的配合物,在激发波长为350 nm时,发射波长为382 nm和402 nm,其中382 nm处的发射是配体中的羧基导致的,而402 nm处的发射时由吡啶环引起的.因此,配体中羧基的发射峰可归因于配体到中心电荷的迁移.
2.4 热重分析配合物Nd2(C4H4O4)3·2H2O在氮气氛围下,从室温到800℃的失重如图7所示,分3步失重:第1步失重0.9%,从室温到100℃,失去游离的水分子;第2步失重5.35%,从344.8℃到385.5℃,失去两个分子配位水分子;第3步失重31.54%,从385.5℃到752.1℃,失去2个分子的丁二酸.从752.1℃之后,剩余的1个丁二酸分子继续分解,最后剩下的残留物是Nd2O3.
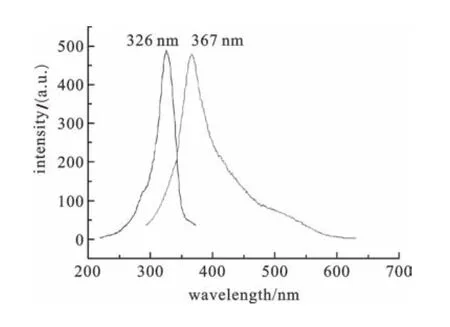
图5 配合物的荧光光谱
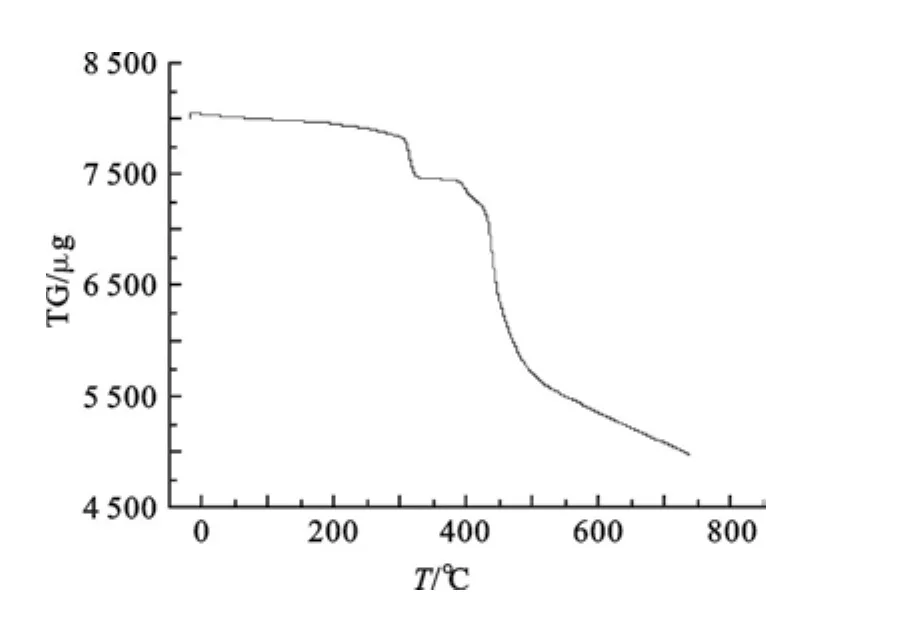
图6 配合物的TG曲线
2.5 电化学性质以碳电极为工作电极和参比电极组成二电极系统,以H2SO4作为支持电解质,在-0.4~0.3 V电势范围内用循环伏安法研究了配合物的电化学性质.如图8所示,配合物的循环伏安图中出现了一对氧化还原峰,其氧化还原峰电位分别为:Epa=0.024 V,Epc=-0.07 V,ΔEp=94mV,配合物对应的半峰电位分别为:Epa/2=0.107 V,Epc/2=-0.027 V,ΔEp/2=0.134 V.由文献可知[17-18],ΔEp>59mV时,配合物的氧化还原峰为不可逆的,而对于不可逆的氧化还原峰有|Ep-Ep/2|=47.7/αn(α=0.5),通过计算可得n=2,即不可逆的氧化还原中转移的电子数为2.
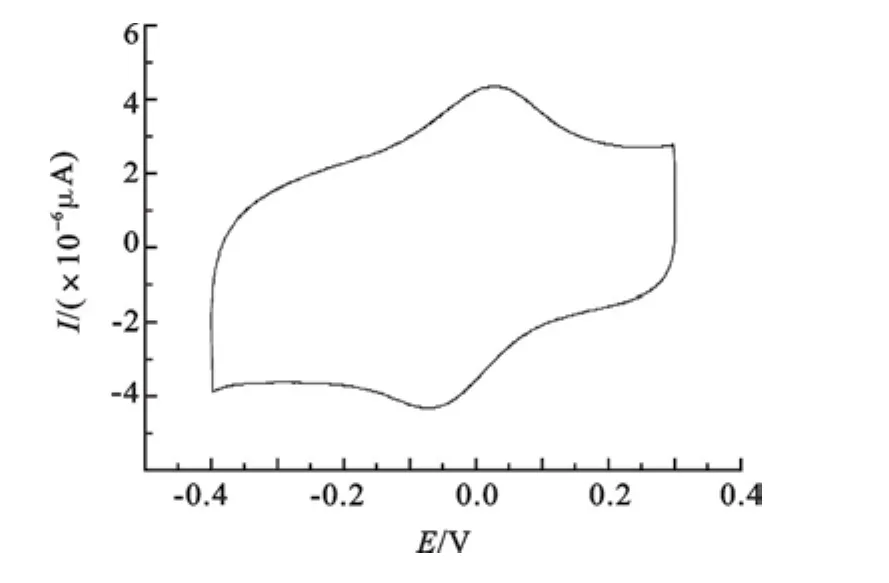
图8 配合物的循环伏安图(扫面速率5mv/s)
3 结论
本文中以丁二酸为配体,钕作为中心金属,用水热法合成了一种新的钕的配位聚合物[Nd2(C4O4H4)3·2H2O]n.该配位聚合物通过Nd O和C O键链接成为一维结构,再以相同的方式形成二维的网状结构.同时,由于配体的π*→n跃迁,配位聚合物在367 nm处有一个较强的荧光发射峰(λex=326 nm);另外,配位聚合物分3步失重,最后剩余Nd2O3;在-0.4~0.3 V电势范围内,配位聚合物在0.024 V和-0.07V处有一对不可逆的氧化还原峰,通过峰电位和半峰电位的计算公式|Ep-Ep/2|=47.7/αn(α=0.5),可以计算出转移电子数为2,由此可见,Nd(III)和Nd(V)之间的转换导致该配位聚合物具有电化学活性.
[1]She J,Gao C,Cui K,et al.Synthesis,crystal structure,and optical properties of a novel rare-earth complex Nd(C2F5COO)3·Phen[J].Structural Chemistry,2008,19(6):905-910.
[2]LiX,Wu X S,Sun H L,etal.Novel1-D double chain lanthanide complexes:synthesis,structure and luminescence[J].Inorg Chim Acta,2009,362(8):2837-2841.
[3]Wong K L,KwokW M,WongW T,etal.Green and red three-photon upconversion from polymeric lanthanide(III)Complexes[J].Angew Chemie Inter Edit,2004,43(35):4659-4662.
[4]Matrosov E I,Goryunova IB,Lysenko K A,et al.N-(1,5-dimethyl-3-oxo-2-phenyl-1,2-dihydropyrazol-4-yl)-P,P-diphenylamidophosphinate and its complexes with neodymium(III),erbium(III),thorium(IV),and uranyl nitrates:Synthesis and crystal and molecular structure[J].Russian Journal of Inorganic Chemistry,2011,56(4):539-544.
[5]Ye Q,Wang X S,Zhao H,et al.Spontaneous resolution of a novel chiral coordination polymer through supramolecular interactions and solventsymmetry breaking[J].Tetrahedron:Asymmetry,2005,16(9):1595-1602.
[6]Anna Mondry,Przemyslaw Starynowicz.Optical spectroscopy of neodymium(III)complexes with diethylenetriaminepentaacetic acid in solution and in[C(NH2)3]2[Nd(dtpa)(H2O)]·7H2O single crystal[J].Polyhedron,2000,19(1):771-777.
[7]Zhang L L,Yao Y M,Luo Y J,et al.Syntheses and crystal structures of four-coordinate aryloxo neodymium complexes[J].Polyhedron,2000,19(20):2243-2247.
[8]She J,LiD,Hou C,etal.Crystal structure and photophysical properties of a neodymium trifluoroacetate complex with 2,2’-bipyridine[J].Journal of Rare Earths,2011,29(3):193-197.
[9] Łyszczek R,Mazur L.Crystal structure,spectroscopic and thermal investigations of neodymium(III)biphenyl-4,4’-dicarboxylate framework[J].Central Europ J Chem,2012,10(4):1165-1174.
[10]Sheldrick GM.SHELXS-97:Program for the solution of crystalstructure[CP/DK].Gottingen:University of Gottingen,2008.
[11]Sheldrick GM.SHELXS-97:program for the refinement of crystalstructure[CP/DK].Gottingen:University of Gottingen,2008.
[12]MRs PALLAVI V.Synthesis and characterisation of Lanthanide thiourea simple and mixed complexes using urea,N-phenylurea and N,N-diphenyl-ureaas seondary ligand[J].Aslan Journal of Chemistry,1991,3(1):13-20.
[13]Chang JH,Dong QG.Principleof spectral analysis[M],Beijing,:Science Press,2012:10-49.
[14]Yang L R,Song S,ZhangW,et al.Synthesis,structure and luminescent properties of neodymium(III)coordination polymers with 2,3-pyrazinedicarboxylic acid[J].Synthetic Metals,2011,161(9):647-654.
[15]Wang Z J,Yang B H.UV and fluorescence spectral changes induced by neodymium binding of N,N′-ethylenebis[2-(ohydroxyphenolic)glycine]and N,N′-di(2-hydroxybenzyl)ethylenediamine-N,N′diacetic acid[J].Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy,2006,65(3):946-949.
[16]Mahata P,Ramy K V,Natarajan S.Synthesis,structure and optical properties of rare-earth benzene carboxylates[J].Dalton Trans,2007,36:4017-4026.
[17]Qiao Y,Da N,Chen D,etal.Spectroscopic properties of neodymium doped high silica glass and aluminum codoping effects on the enhancement of fluorescence emission[J].Applied Physics B,2007,87(4):717-722.
[18]Wang J,He F,Wang X,et al.Synthesis,structure and electrochemical behavior of an organic-inorganic hybrid compound based on Dawson-type polyoxo metalates[J].JCoord Chem,2011,64(13):2312-2320.

