HPLC法测定藏药五味甘露药浴颗粒中槲皮素、山柰素和盐酸麻黄碱
冯 欣, 周 刚, 王 茜, 登巴达吉*
(1.中国藏学研究中心藏医药研究所,北京 100101;2.内蒙古自治区食品药品检验所,内蒙古 呼和浩特 010020)
HPLC法测定藏药五味甘露药浴颗粒中槲皮素、山柰素和盐酸麻黄碱
冯 欣1,周 刚2,王 茜1,登巴达吉1*
(1.中国藏学研究中心藏医药研究所,北京100101;2.内蒙古自治区食品药品检验所,内蒙古呼和浩特010020)
目的 采用RP-HPLC法测定藏药五味甘露药浴颗粒(麻黄、刺柏、大籽蒿、水柏枝、烈香杜鹃)中槲皮素、山柰素和盐酸麻黄碱的量。方法 槲皮素、山柰素的测定,采用Zorbax SB-C18色谱柱(150 mm×4.6 mm,5μm);流动相为乙腈-0.2%磷酸溶液(20∶80);检测波长360 nm;体积流量1.0mL/min;柱温30℃。盐酸麻黄碱的测定,流动相为乙腈-0.092%磷酸溶液(含0.04%三乙胺和0.02%二正丁胺)(1.5∶98.5);检测波长为210 nm;体积流量1.0 mL/min。结果 槲皮素、山柰素分别在0.019 8~0.990 0μg(r=0.999 8)、0.014 4~0.721 2μg(r=0.999 9)范围内线性关系良好,平均回收率分别为97.5%、99.3%,RSD分别为1.4%、1.6%(n=6)。盐酸麻黄碱在0.016 592~0.248 9μg(r=0.999 9)范围内线性良好。平均回收率为101.4%,RSD为1.4%(n=6)。结论 本方法操作简单、结果准确,重复性好,可用于该药的质量控制。
槲皮素;山柰素;盐酸麻黄碱;五味甘露药浴颗粒;藏药
“五味甘露药浴”最早记载于著名藏医经典著作《四部医典》[1]中,是由麻黄、刺柏、大籽蒿、水柏枝、烈香杜鹃五味药组成的复方制剂,临床中主要用于治疗四肢僵直、关节肿痛、肌肉萎缩等“黄水”疾病,但此药禁忌对高血压、心脏病、高烧等患者进行治疗。该药的化学成分主要有挥发油类、黄酮类、萜、生物碱类。该药品目前的质量标准仅收载定性鉴别和薄层扫描法测定盐酸麻黄碱的量,操作繁琐,且准确性差,因此本实验采用HPLC法测定了大籽蒿、烈香杜鹃中黄酮类成分槲皮素、山柰素的量,修订了麻黄中盐酸麻黄碱的定量测定方法,从而为完善该藏药的质量标准提供基础和依据。
1 仪器与试药
U1tiMate 3000高效液相色谱仪系统(Chrome-1eon c1ient色谱工作站);Chrome1eon 6.80变色龙软件;U1tiMate 3000 Variab1e Wave1ength Detector二极管阵列检测器;U1tiMate 3000 Pump泵;U1tiMate 3000 Autosamp1er自动进样器;U1tiMate 3000 RS Co1umn Compartment柱温箱;槲皮素对照品(批号100081-200406)、山柰素对照品(批号086-200002)、盐酸麻黄碱(批号171241-200506)均购于中国食品药品检定研究院;五味甘露药浴颗粒(西藏奇正藏药股份有限公司生产,批号分别为Z20110915、Z20120121、Z20120709);甲醇(色谱纯,J.T.Baker公司,批号112700471);高纯水(自制);磷酸(天津市盛奥化学试剂有限公司,批号20110104);乙腈(色谱纯,CALEPURE公司,批号70145);三乙胺、二正丁胺为AR级。
2 方法与结果
2.1槲皮素、山柰素的测定
2.1.1供试品溶液的制备[2-7]取本品粉末(过三号筛)约1.0 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,密塞,称定质量,加热回流60 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,用微孔滤膜(0.45μm)滤过,取续滤液,即得。
2.1.2对照品溶液的制备 精密称取120℃干燥4 h的槲皮素、山柰素对照品0.024 75 g、0.009 02 g,置同一50 mL量瓶中,加流动相溶解并稀释至刻度,摇匀,精密吸取1.0 mL置25 mL量瓶中,加流动相稀释至刻度,摇匀,制成每1 mL分别含槲皮素19.8μg、山柰素7.2μg的溶液,作为对照品溶液。
2.1.3阴性对照溶液的制备 按五味甘露药浴颗粒处方比例称取适量除烈香杜鹃、大籽蒿的其余药味,按五味甘露药浴颗粒的前处理和制剂生产工艺制成缺烈香杜鹃、大籽蒿的五味甘露药浴的阴性样品,再按“2.1.1”项制备阴性供试品溶液并测定,结果空白溶液在与槲皮素、山柰素对照品相同保留时间处均未显色谱峰,故认为无干扰。见图1。

图1 槲皮素山柰素HPLC色谱图Fig.1 HPLC chromatograms of quercetin and kaempferoI
2.1.4标准曲线的制备 分别精密吸取槲皮素、山柰素对照品溶液0.2、1、2、3、4、5、10 mL置50 mL量瓶中加甲醇至刻度,摇匀。在上述条件下分析,以对照品进样量(μg)为横座标,峰面积为纵座标,绘制标准曲线。槲皮素回归方程Y= 2.395×106Ⅹ-1.410×103,r=0.999 8;山柰素回归方程Y=2.332×106Ⅹ+5.570×103,r= 0.999 9。结果表明,槲皮素在0.019 8~0.990 0 μg范围内线性良好,山柰素在0.014 4~0.721 2 μg范围内线性关系良好。
2.1.5精密度试验 精密吸取同一对照品溶液,重复进样5次,求得槲皮素RSD为0.2%,山柰素RSD为0.2%。
2.1.6稳定性试验 在室温下,将同一供试品溶液(批号Z20110915)分别于配制后0、2、4、6、12、24 h,进行测定,结果槲皮素RSD为0.9%,山柰素RSD为0.4%。
2.1.7重复性试验 取同一供试品(批号Z20110915)5份,分别处理测定5次,求得槲皮素RSD为1.8%,山柰素RSD为1.4%。
2.1.8加样回收试验 精密称取已知含有量(槲皮素1.073 8 mg/g,山柰素0.201 6 mg/g)的同一批号供试品(批号Z20110915)0.5 g,精密加入含槲皮素20.06μg/mL、山柰素4.02μg/mL的混合对照品甲醇溶液25 mL,按供试品溶液的方法制备,进样10μL,计算回收率,结果槲皮素平均回收率为97.5%,RSD为1.4%,山柰素平均回收率为99.3%,RSD为1.6%。具体见表1、表2。

表1 槲皮素回收率试验(n=6)Tab.1 Resu Its of recovery tests for quercetin(n=6)

表2 山柰素回收率试验(n=6)Tab.2 Resu Its of recovery tests for kaem pferoI(n=6)
2.2盐酸麻黄碱的测定
2.2.1供试品溶液的制备 取本品粉末(过三号筛)约0.5 g,精密称定,置具塞锥形瓶中,精密加入1.44%磷酸溶液50 mL,称定质量,超声处理(功率600W,频率50 kHz)30 min,放冷,再称定质量,用1.44%磷酸溶液补足减失的质量,摇匀,滤过,取续滤液,即得。
2.2.2对照品溶液的制备 精密称取盐酸麻黄碱对照品0.010 37 g,置50 mL量瓶中,加1.44%磷酸溶液使溶解并稀释至刻度,摇匀,精密吸取5.0 mL置25 mL量瓶中,加1.44%磷酸溶液稀释至刻度,摇匀,制成每1 mL含盐酸麻黄碱41.48μg的溶液,作为对照品溶液。
2.2.3阴性对照溶液的制备 按五味甘露药浴颗粒处方比例称取适量除麻黄的其余药味,按五味甘露药浴颗粒的前处理和制剂生产工艺制成缺麻黄的五味甘露药浴的阴性样品,再按“2.2.1”项制备阴性样品溶液并测定,结果阴性样品溶液在与盐酸麻黄碱对照品相同保留时间处均未显色谱峰,故认为无干扰。见图2。

图2 盐酸麻黄碱HPLC色谱图Fig.2 HPLC chromatogram s of ephedrine hydroch Ioride
2.2.4标准曲线的制备 分别精密吸取盐酸麻黄碱对照品溶液1、2、4、5、10、15 mL置25 mL量瓶中加1.44%磷酸溶液至刻度,摇匀。在上述条件下分析,以对照品进样量(μg)为横座标,峰面积为纵座标,绘制标准曲线。盐酸麻黄碱回归方程Y=9.467×106Ⅹ-8.879×102,r=0.999 9。结果表明,盐酸麻黄碱在0.016 592~0.248 9μg范围内线性良好。
2.2.5精密度试验 精密吸取同一对照品溶液,重复进样5次,求得盐酸麻黄碱RSD为1.0%。
2.2.6稳定性试验 在室温下,将一供试品溶液分别于配制后0、2、4、6、12、24 h,进行测定,结果盐酸麻黄碱RSD为1.5%。
2.2.7重复性试验 取同一供试品(批号Z20110915)5份,分别处理测定5次,求得盐酸麻黄碱RSD为1.1%。
2.2.8加样回收试验 精密称取已知含有量(盐酸麻黄碱0.201 6 mg/g)的同一批号供试品(批号Z20110915),精密加入盐酸麻黄碱(1.037 μg/mL)对照品1.44%磷酸溶液50 mL,按供试品溶液的制备方法制备,进样10μL,计算回收率,结果盐酸麻黄碱平均回收率为101.4%,RSD为1.4%。结果见表3。
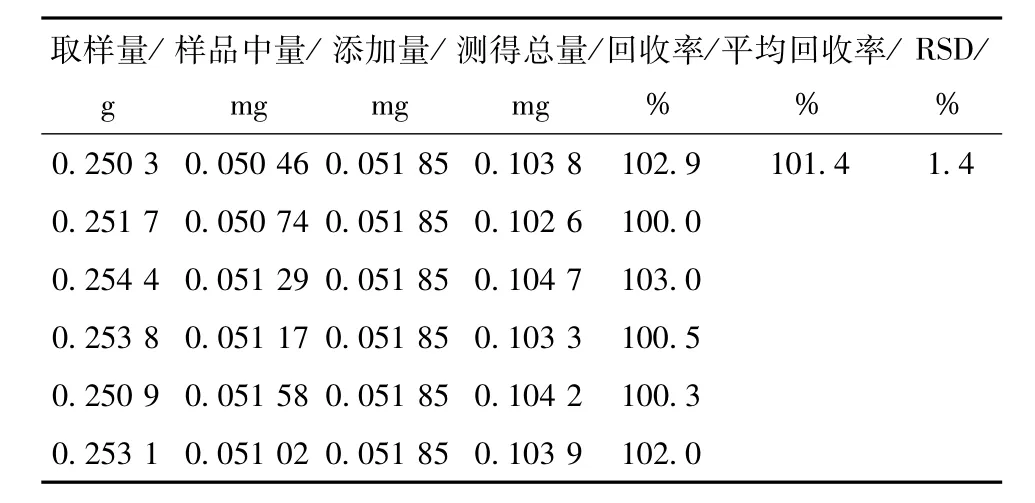
表3 盐酸麻黄碱回收率试验(n=6)Tab.3 ResuItsofrecoverytestsforephedrinehydrochIoride(n=6)
2.3样品测定 3批样品,各按“2.1”项及“2.2”项进行操作,制备成供试品溶液,测定,结果见表4。
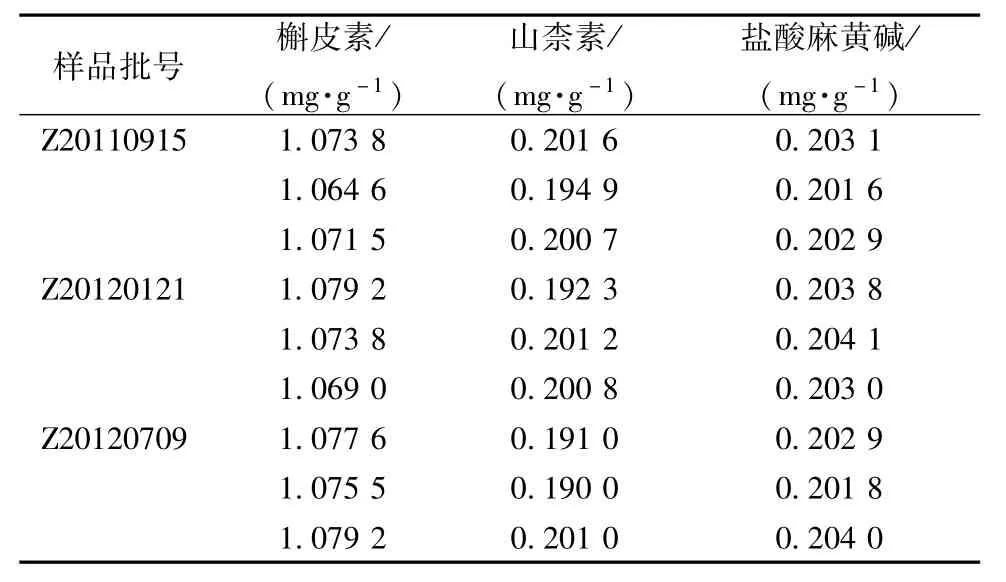
表4 样品测定结果(n=3)Tab.4 ResuItsofsampIedetermination(n=3)
3 讨论
3.1藏药制剂中处方药物组成多、成分复杂,选择合适的提取方法是质量分析的关键。本实验选择甲醇、80%甲醇、50%甲醇、乙醇,分别采用超声不同时间(15、30、60min)、加热回流60min进行提取,结果采用甲醇回流60min样品中槲皮素、山柰素的峰型较好,杂峰干扰较小,提取完全。
3.2本实验前期先测定烈香杜鹃中槲皮素和山柰素的量,在阴性对照中出现槲皮素峰,通过试验,发现烈香杜鹃和大籽蒿中均含有槲皮素,因此最后测定成药的总槲皮素、山柰素量[8-13]。
3.3盐酸麻黄碱测定参考《中国药典》2010年版,考察了回流提取30min,超声处理20min、30、60min进行提取,结果采用1.44%磷酸溶液超声处理30min即可以达到提取完全[2]。
3.4采用HPLC法测定盐酸麻黄碱的量,方法准确度更高,且盐酸麻黄碱作为一个特殊管理的化学物质,应该在生产中严格管控。
[1]纳顺达来,赛西娅.试述五味甘露药浴[J].中国民族医药杂志,2006,12(6):47.
[2]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:296.
[3]徐 飞,陆兔林,谢 辉.HPLC测定复方银杏颗粒中槲皮素、山柰素、异鼠李素及总黄酮醇苷含量[J].中成药,2007,29(11):1617.
[4]杨立昌,乙 引,林俊清,等.RP-HPLC测定苗药黑白保肝清颗粒中槲皮素的含量[J].中国实验方剂学杂志,2010,16(11):64.
[5]梁 洁,柳贤福,孙正伊,等.HPLC测定鱼腥草配方颗粒中槲皮素含量[J].中国实验方剂学杂志,2012,18(11):140.
[6]尹 玲,冯 芸,吴 姗,等.HPLC法测定菝葜提取物中槲皮素的含量[J].中国药房,2010,21(35):3312.
[7]许乾丽,鲍家科,茅向军,等.HPLC测定杠板归中槲皮素的含量[J].中国中药杂志,2009,34(16):2105.
[8]宋 勤,杨理明.HPLC法测定消渴降糖胶囊中槲皮素的含量[J].中国民族医药杂志,2011,(1):50.
[9]杜小伟,王京辉,肖斯婷,等.HPLC测定不同产地罗布麻叶中槲皮素、山柰素的含量[J].中国中医药信息杂志,2013,1(20):51.
[10]黄兴富,黎其万,刘宏程,等.高效液相色谱法同时测定苦荞中芦丁、槲皮素和山柰酚的含量[J].中成药,2011,33(2):158-160.
[11]黄兹英,王继良,黄敏洁,等.HPLC法同时测定夏枯草中芦丁、金丝桃苷、槲皮素和山柰酚[J].中成药,2012,34(3):137-140.
[12]黄俊忠,曾小平.HPLC法同时测定田七痛经胶囊中异鼠李素、槲皮素、山柰素[J].中成药,2012,34(10):76-79.
[13]周逸芝,刘训红,陈 菲,等.高效液相色谱法同时测定龙柴方中槲皮素、山柰素、异鼠李素[J].中成药,2013,35(10):103-106.
Determ ination of quercetin,kaem p feroIand ephedrine hydroch Ioride in W uwei Gan Iu Yaoyu Granu Ies by HPLC
FENG Xin1, ZHOU Gang2, WANG Qian1, DENG-ba-da-ji*
(1.Tibetan Medicine Institute,China Tibetology Research Center,Beijing 100101,China;2.HohhotCity in Inner Mongolia AutonomousRegion Institute for Food and Drug Control,Hohhot010020,China)
quercetin;kaempfero1;ephedrine hydroch1oride;Wuwei Gan1u Yaoyu Granu1es;Tibetmedicine
R927.2
A
1001-1528(2015)01-0120-04
10.3969/j.issn.1001-1528.2015.01.024
2014-03-23
冯 欣(1982—),男,助理研究员,从事藏药研究。Te1:(010)64972883,E-mai1:fengxin0303@163.com
登巴达吉(1959—),男(藏),研究员,从事藏医药研究。E-mai1:dbdj2009@1ive.cn