半胱氨酸亚金铵的合成、理化性质及电镀金应用
黄世玉,李德良,JA Finch,盛国军,李乐
半胱氨酸亚金铵的合成、理化性质及电镀金应用
黄世玉1,李德良1,JA Finch2,盛国军1,李乐3
(1. 中南林业科技大学环境科学与工程学院,湖南长沙,410004;2. McGill University, 3610University St., Montreal, QC , H3A 2B2, Canada;3. 长沙铂鲨环保设备有限公司,湖南长沙,410007)
以半胱氨酸为配体合成一种新型亚金配合物NH4Au(Cys)2,对该配合物进行元素分析、红外光谱、紫外光谱、热失重分析和导电性测量等理化性质研究;以该亚金配合物为金源开展相关的电镀金工艺探索,并通过四因素三水平的正交试验获得其最佳条件参数;采用扫描电子显微镜(SEM)和X线衍射(XRD)对镀金层的表面质量进行探讨。研究结果表明:该目标产物的分子式为NH4Au(Cys)2∙2H2O,该配合物中以半胱氨酸的巯基和金配位为成健特征,在170 ℃以下热稳定性较好,该亚金配合物是一个典型的离子化合物。在电流密度为200~300 A/m2,pH为10.5~12.0,温度为35~45 ℃,金质量浓度为15~25 g/L的电镀工艺条件下,得到粒度为0.5~1.0 μm的单质金,且主要沿着(111)面进行生长。
半胱氨酸亚金铵;合成;性质;电镀金;形貌
金配合物广泛应用于电镀行业,但是至今为止镀金业用得多的金盐均有剧毒性氰或腈,它们在生产、运输、使用过程中均带来安全危机和管理困惑;后续的含氰、腈废水由于其浓度较低,极易扩散,也给环境带来很大的破坏。多年来含氰镀金盐的替代品研究一直局限于如亚硫酸金[Au(SO3)2]3−、卤代金、硫代硫酸金[Au(S2O3)2]3−等[1−3],而这些替代品的稳定常数(亚硫酸金、卤代金和硫代硫酸金的稳定常数分别为1026,109和1028)远远低于亚金氰化物的稳定常数(1038)[4−5],且它们自身在溶液中往往伴随着分子内的氧化还原反应、歧化反应等问题,结果是漂金频繁,无法真正应用于当今的镀金领域[6−9]。近年来,市场上出现了一种名为“柠檬酸金钾”(也称丙二腈柠檬酸金钾)的所谓无毒金化合物[10],但它在实质上却既含有游离的氰化物[11]、也含数量极其可观的丙二腈,后者在存放、使用和使用后的废物(液、渣)处理过程中也会进一步通过氧化、还原、分解、降解等途径而向周边环境释放出液离的氰(包括负一价的氰离子和具有一定挥发性的分子型HCN),故这种所谓的“无毒镀金盐”并未改变其剧毒性的本质[12]。从“柠檬酸金钾”或“丙二腈柠檬酸金钾”采用硫氰酸盐作为还原剂在酸(柠檬酸)性条件下对氯化金进行还原以得到相关的亚金中间体,而在这样的酸(柠檬酸)性条件和相当高的制备温度(80~85℃)下[13−14],硫氰酸盐(如硫氰酸铵)是很容易分解而游离出氰根和氰化氢(HCN)的,因为氰化氢是弱酸且有一定的挥发性,这种游离的氰根或氰化氢既可与溶液中的(三价或一价)金配位而进入产品,也可作为杂质而混入产品中,这其实是社会上流传的“柠檬酸金钾或丙二腈柠檬酸金钾产品含游离氰”的实质原因。为了避免氰、腈的剧毒性安全隐患,通过多年的新型金化合物探索[15−17],本文作者制备一种新型的以氨基酸为配体、性能稳定、安全无毒的新型亚金配合物NH4Au(Cys)2∙2H2O,对其进行结构表征、性能和电镀金应用研究,并用SEM和XRD对相关镀金层产品的微观结构进行检测。
1 实验
1.1 原料
半胱氨酸(HCys):分析级,国药集团化学试剂有限公司生产;氯金酸(HAuCl4):分析级,阿拉丁试剂(上海)有限公司生产;亚硫酸钠(Na2SO3):分析级,天津市申泰化学试剂有限公司生产;氢氧化钠(NaOH):分析级,天津市申泰化学试剂有限公司生产;三乙醇胺(TEA):分析级,;5,5′-二甲基海因(DMH):分析级,阿拉丁试剂(上海)有限公司生产;柠檬酸(CA):分析级,长沙分路口塑料化工厂生产;碳酸钠(Na2CO3):分析级,长沙分路口塑料化工厂生产;缓冲溶液:分析级,优耐德引发剂(上海)有限公司生产; Ru/ Ir/Ti阳极板:分析级,宝鸡宝冶钛镍制造有限公司生产;镀镍铜板:长沙铂鲨环保设备有限公司生产;复合型电镀光亮剂:SDS型,长沙铂鲨环保设备有限公司 生产。
1.2 半胱氨酸亚金铵的合成
在磁力搅拌器上将2 g HAuCl4溶液,按(HAuCl4):(Na2SO3)=4:5缓慢滴加到Na2SO3溶液中,得到透明的溶液;然后将制备好的透明液用高浓的NH4Cys母液调节pH至碱性;再将上述溶液用旋转蒸发仪在40 ℃下浓缩结晶,得到3.1 g固体产物。
1.3 半胱氨酸亚金铵的电镀应用
配制0.1 mol/L的NH4Au(Cys)2,0.2 mol/L的TEA溶液,0.2 mol/L的DMH溶液和0.4 mol/L的(NH4)3PO4作为镀金母液,采用CA和Na2CO3作为pH调节剂;电源采用直流电源;通过霍尔槽试验,阳极板采用镀钌钛的惰性极板,阴极板则选取经预处理后长×宽×厚为15 mm×15 mm×0.2 mm的镀镍铜板作为镀金基材,在镍板上镀金。
1.4 半胱氨酸亚金铵的表征
配合物的相对分子质量其分布采用元素分析仪(EA,德国Elementar公司)/红外光谱仪(IR,美国热电2501公司)/紫外可见分光光度仪(UV,日本岛津公司)测定;采用日本岛津公司DTG−60H的热失重分析仪(岛津−DTG60−H)对配合物进行热失重分析,测试温度为20~800 ℃,升温速率为10 ℃/min,N2气氛,气体流量为50 mL/min。采用上海雷磁公司的DDS−11A电导率仪对配合物的导电性能进行分析;采用扫描电子显微镜(SEM,中科科仪公司)和X线衍射仪(XRD,日本岛津公司)对镀金层的颗粒和晶体特征进行检测。
2 结果与讨论
2.1 元素分析
半胱氨酸亚金产品采用2种方法进行元素分析。采用火焰原子吸收分析仪测定金属元素Au含量,用元素分析仪对非金属元素进行测定的结果(质量分数)为:Au 47.03%,C 8.11%,H 2.31%,N 15.51%和S 23.35%;NH4Au(Cys)2∙2H2O的元素含量理论计算值为:Au 46.35%,C 8.47%,H 2.35%,N 16.47%和S 22.58%。由此可知该配合物的分子式为NH4Au(Cys)2∙2H2O。
2.2 红外光谱及分析
NH4Au(Cys)2的红外光谱图如图1所示。
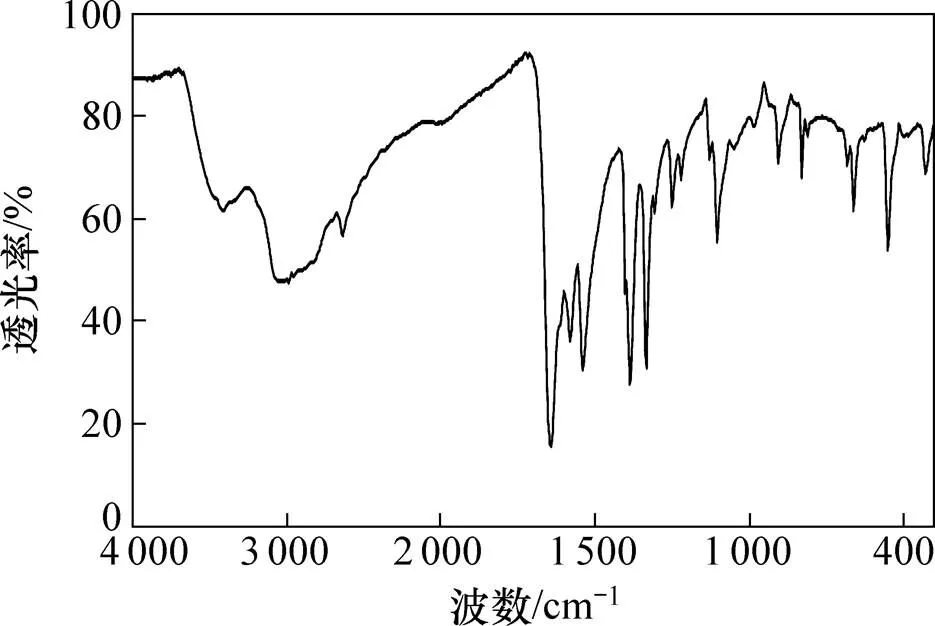
图1 NH4Au(Cys)2产品的IR光谱
从图1可见:在2 600~2 500 cm−1波数范围的属于巯基特征吸收峰消失了,表明来自配体的巯基已与中心金属金产生配位,配位基团的IR出现了典型的红移现象。图1中的双重峰表明产物NH4Au(Cys)2∙2H2O的形成,3 500~3 200 cm−1和1 600~1 560 cm−1分别对应于自由氨基和自由羰基的吸收峰,它们在配位前后无明显变化。
2.3 紫外光谱分析
NH4Au(Cys)2,HCys和HAuCl4的紫外吸收图谱比较如图2所示。
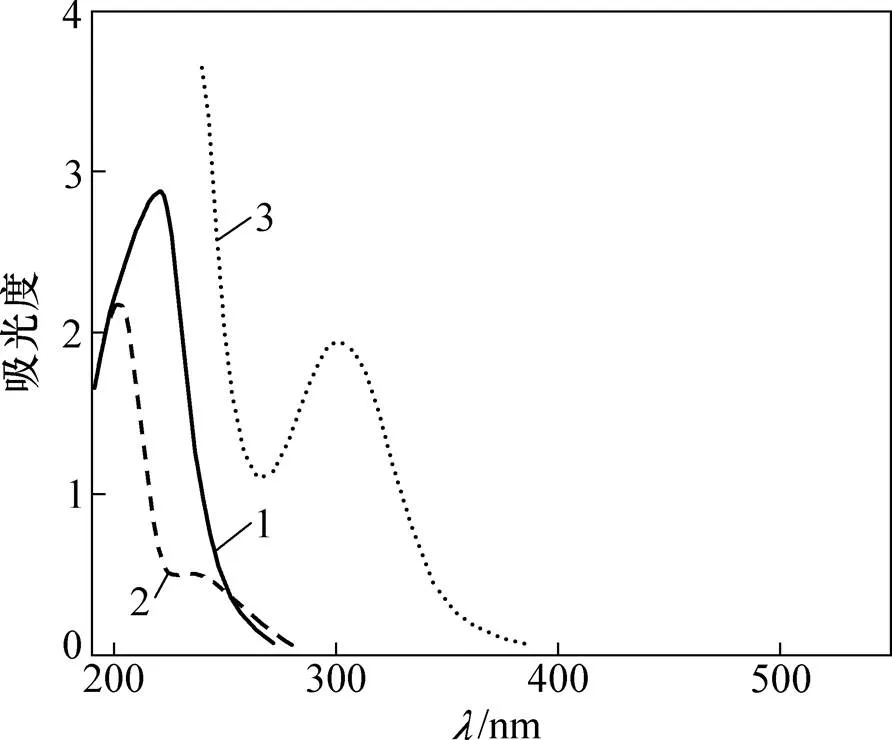
1—HCys;2—NH4Au(Cys)2;3—HAuCl4
从图2可见:HCys的紫外吸收光谱在235 nm处有1个明显的吸收峰,是由于助色团—SH和—NH2的作用下使生色团—COOH吸收峰产生红移效应而产生的;300 nm处的吸收峰则是三价金HAuCl4,它落在可见光区域,与d-d电子跃迁紧密相关;配合物NH4Au(Cys)2的紫外特征吸收峰是在205~210 nm,它明显比三价金的特征吸收波长更短,符合一价金的紫外吸收规律。由此可以知道,中心金属的价态对配合物结构、颜色以及稳定性起着主导作用。
2.4 热稳定性研究
NH4Au(Cys)2的热重分析曲线如图3所示。
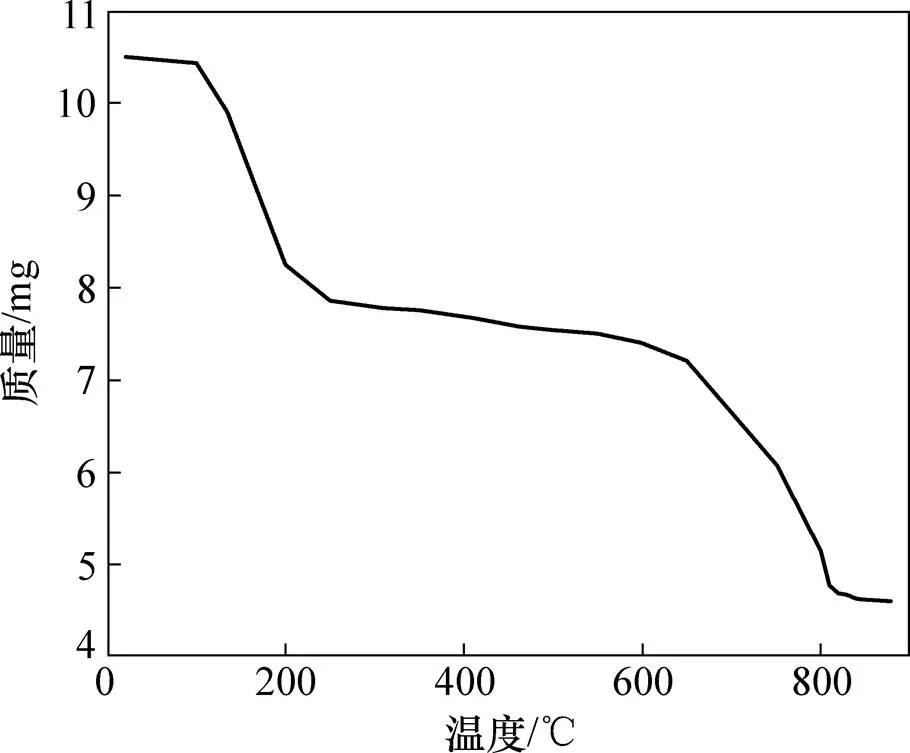
图3 NH4Au(Cys)2的TGA曲线
从图3可见:目标化合物在90 ℃左右失去其结晶水(对应的理论质量损失为0.73 mg),并且在90~175 ℃之间被分解为Au(Cys)(对应的理论质量损失为6.45 mg);若温度高于300 ℃,Au(Cys)将完全转变为金属状态的金。因此,该目标产物在陶瓷饰金、电镀金以及化学沉金等方面将有良好的应用前景。
2.5 电导率测量
将配合物在水中溶解,配制成0.01 mol/L的溶液,在室温条件下,测定了NH4Au(Cys)2的摩尔电导率为0.43 S·m2/mol,表明它是一种典型的电解质,可望应用于电镀、化学还原沉金、置换镀金(ENIG)和其他表面处理领域。
2.6 电镀工艺条件选择
以镀金层的色泽和结合力作为考核指标,采用四因素、三水平的正交试验法L9(34),对影响电镀金产品质量的主要因素即温度(℃)、金质量浓度(g/L)、电流密度(A/m2)和pH进行了筛选,结果如表1所示(其中镀金层的结合强度按国家标准GB/T 13913—92进行测定)。
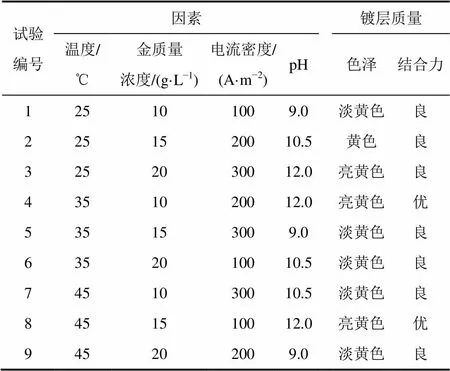
表1 镀金工艺条件的四因素、三水平正交试验法L9(34)方案及结果
从表1可见:该配合物电镀过程中的影响因素由大到小排序为:pH,温度,金浓度,电流密度。适宜的电镀金工艺条件参数为:pH 10.5~12.0,温度35~45 ℃,金质量浓度15~25 g/L,电流密度200~300 A/m2。
2.7 电镀金产品的表面形貌分析
对于在工况条件pH为12.0,温度为45 ℃,金质量浓度为20 g/L和电流密度为250 A/m2下所得到的电镀金样板,采用SEM和XRD被用来对电镀金层的微观形貌进行分析,分别如图4和图5所示。

图4 镀金产品的扫描电镜照片
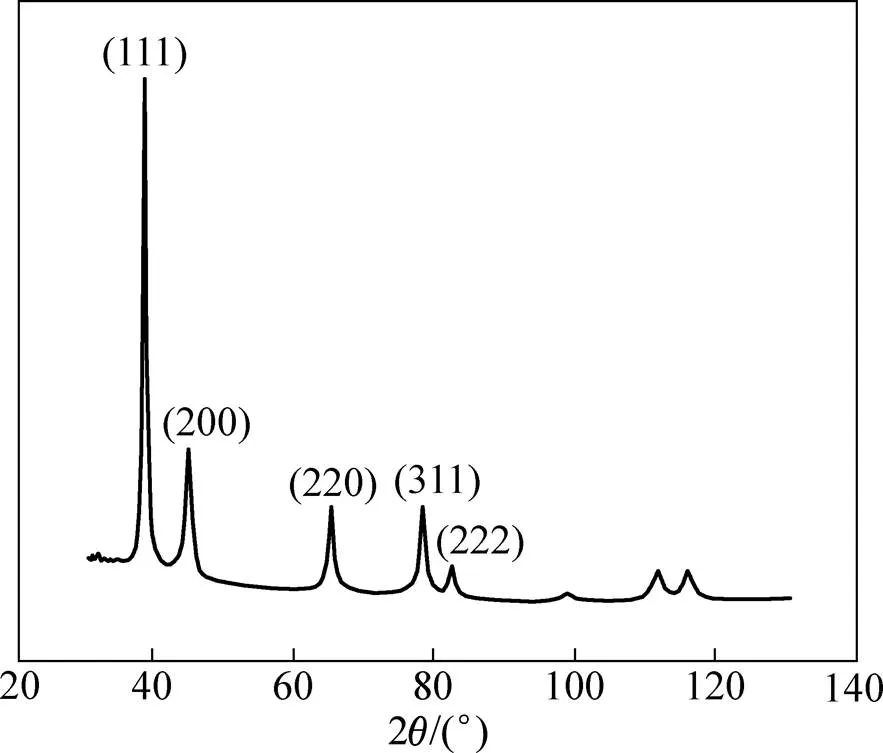
图5 镀金产品表面XRD谱
从图4可见:镀金层的表面光滑、粒度均匀,金颗粒粒径为0.5~1.0 μm。
从图5可见:沉积的金颗粒沿着(111),(200),(220),(311)和(222)方向生长,表明它具有面心立方结构的特征;在整个施镀过程中主要沿着(111)晶面 生长。
3 结论
1) 合成了一种新的亚金配合物即半胱氨酸亚金铵,对该配合物表征得出其分子式为NH4Au(Cys)2∙2H2O。
2) 通过对配合物电导率测定表明它是一种典型的离子化合物;热重分析说明它在170 ℃之前稳定,相关红外光谱研究表明Au(I)和半胱氨酸的巯基之间形成了强有力的配位键;紫外光谱显示其特征紫外吸收为205~210 nm。
3) 采用L9(34)正交试验得到电镀金的最佳工艺条件为:pH=10.5~12.0,温度35~45 ℃,金质量浓度15~25 g/L,电流密度200~300 A/m2。在该试验条件下所制得的电镀层色泽、结合力均好。
4) 采用SEM和XRD对相关的镀金层颗粒及形态进行分析,结果显示沉积的金粒度为0.5~1.0 μm,且它们主要沿着(111)晶面生长。
[1] Traut J, Wright J, Williams J. Gold plating optimization for tape automated bonding[J]. Plating and Surface Finishing, 1990(3): 30−33.
[2] 黎松强, 吴馥萍. 提高化学镀金沉积速率相关因素研究[J]. 黄金, 2007, 28(1): 5−8. LI Songqiang, WU Fuping. Study on the correlative factors to enhance the sedimentation rate in chemi gold plating[J]. Gold, 2007, 28(1): 5−8.
[3] 谭谦, 李宁, 刘海萍. 亚硫酸盐-硫代硫酸盐置换镀金液对Ni2+耐受能力的研究[J]. 电镀与环保, 2007(5): 16−19. TAN Qian, LI Ning, LIU Haiping. Study of tolerance capability of Ni2+in sulfite-thiosulfate immersion gold plating bath[J]. Electroplating and Pollution Control, 2007(5): 16−19.
[4] 黎鼎鑫, 王永录. 贵金属提取与精炼[M]. 长沙: 中南大学出版社, 2004: 62−64. LI Dingxin, WANG Yonglu. Precious metal recovery and refining[M]. Changsha: C entral South University Press, 2003: 62−64.
[5] Gamini S. Gold leaching in non-cyanide lixiviant systems: Critical issues on fundamentals and applications[J]. Minerals Engineering, 2004, 17: 785−801.
[6] 刘海萍, 李宁, 毕四富, 等. 无氰置换镀金工艺的研究[J]. 电镀与环保, 2007(4): 26−28. LIU Haiping, LI Ning, BI Sifu, et al. Study of non-cyanide immersion gold plating[J]. Electroplating and Pollution Control, 2007(4): 26−28.
[7] Amutha K, Shakkthivel P, Vasudevan T. 在以EDTA和柠檬酸为配位剂的酸性硫代硫酸盐–亚硫酸盐镀液中电沉积金[J]. 电镀与涂饰, 2007(8): 1−6. Amutha K, Shakkthivel P, Vasudevan T. Electrodeposition of gold from acidic thiosulfate-sulfite bath containing EDTA and citric acid as complexing agents[J]. Electroplating and Finishing, 2007(8): 1−6.
[8] 李贤成. 无氰亚硫酸钠镀金工艺[J]. 电镀与涂饰, 2005(9): 31−32. LI Xiancheng. Technics of non-cyanide gold plating with sodium sulfite[J]. Electroplating and Finishing, 2005(9): 31−32.
[9] 乐玮, 唐道润, 尹强, 等. 二甲基亚砜有机溶剂体系电镀金工艺[J]. 材料保护, 2013(3): 22−24. LE Wei, TANG Daorun, YI Qiang, et al. Imethyl sulfoxide organic solvent system electric plating process[J]. Material Protection, 2013(3): 22−24.
[10] 苏新虹, 邓银, 张胜涛, 等. 柠檬酸金钾无氰沉金厚度控制研究[J]. 印制电路信息, 2011(S1): 166−169. SU Xinhong, DENG Yin, ZHANG Shengtao, et al. Study on gold thickness control in Cyanide-free immersion gold process[J]. Printed Circuit Information, 2011(S1): 166−169.
[11] 邓银. 柠檬酸金钾无氰镀金技术研究[D]. 重庆: 重庆大学化学工程与技术学院, 2011: 33−36. DENG Yin. Study on cyanide-free immersion gold technology with gold potassium citrate[D]. Chongqing: Chongqing University. College of Chemistry and Chemical Engineering, 2011: 33−36.
[12] 张荣光, 周大龙. 以丙尔金为主盐的高纯度可焊性镀金工艺[J]. 电镀与涂饰, 2012(3): 1−3. ZHANG Rongguang, ZHOU Dalong. Process for electroplating of highly pure and weldable gold coating using KAu[CH2(CN)2] ·2(C6H5O7)·H2O as main salt[J]. Electroplating and Finishing, 2012(3): 1−3.
[13] 张群刚. 镀金用柠檬酸金盐及其制备方法: 中国, 200710193014. X[P]. 2008−08−27. ZHANG Qungang. Gold plated with gold citrate and its preparation method: China, 200710193014.X[P]. 2008−08−27.
[14] 王龙基. 从“丙尔金”的联想[J]. 印制电路信息, 2013(9): 3−4. WANG Longji. No arbitrary environmental law enforcement[J]. Printed Circuit Information, 2013(9): 3−4.
[15] 董明琪, 李德良, 徐天野, 等. 一种新的PCB无氰化学沉金工艺[J]. 表面技术, 2011(1): 104−106. DONG Mingqi, LI Deliang, XU Tianye, et al. A cyanide-free gold immersion process and its application in PCB[J]. Surface Technology, 2011(1): 104−106.
[16] 吴赣红, 李德良, 董坤, 等. 一种无氰化学镀金工艺的研究[J]. 表面技术, 2008(3): 52−54. WU Ganhong, LI Deliang, DONG Kun, et al. Technology research about non-cyanide gold plating[J]. Surface Technology, 2008(3): 52−54.
[17] JIN Wentao, LI Le, LI Deliang. “Au(Ⅲ)-cysteine” complex and its application in electro-less deposition[J]. Advanced Materials Research, 2012, 550/551/552/553: 1991−1994.
(编辑 杨幼平)
Synthesis, properties of NH4Au(Cys)2and its application in electroplating gold
HUANG Shiyu1, LI Deliang1, JA Finch2, SHENG Guojun1, LI Le3
(1. College of Environmental Sciences and Engineering, Central South University of Forestry and Technology, Changsha 410004, China; 2. McGill University, 3610University St., Montreal, QC, H3A 2B2, Canada; 3. Changsha Pt-Shark Environmental Co. Ltd., Changsha 410007, China)
Aurous-cysteine complex was synthesized, and related characterization including elemental analysis (EA), infrared spectroscopy (IR), ultraviolet (UV), thermogravimetric analysis (TGA) and conductivity were studied. The optimal electro-plating indexes were obtained by the Orthogonal test method. The micro-morphology of gold particles were investigated by SEM and XRD. The results show that the target product is NH4Au(Cys)2∙2H2O, UV and IR spectra reveals a strong coordinating bond form between Au(I) and the mercapta group of the cysteine. TGA curve explains that the product is thermally stable below 170 ℃. Conductivity data shows that it is a typical ionic compound. The electroplated gold particles are obtained by operating temperature 35−45 ℃, current density 200−300 A/m2, pH=10.5−12.0, gold mass concentration 15−25 g/L, respectively. They are pure Au0and in an even size of 0.5−1.0 μm, and grow along (111) plane predominantly.
NH4Au(Cys)2; synthesis; property; electroplating gold; morphology
10.11817/j.issn.1672-7207.2015.04.004
TQ153.1
A
1672−7207(2015)04−1197−05
2014−05−13;
2014−09−20
国家自然科学基金资助项目(20976201);湖南省自然科学基金资助项目(07JJ6156)(Project (20976201) supported by the National Natural Science Foundation of China; Project (07JJ6156) supported by the Natural Science Foundation of Hunan Province of China)
李德良,博士,教授,从事新型金配合物及应用研究;E-mail:globalize100@vip.163.com

