尿酸在聚呋喃丙烯酸电化学传感器上的电化学行为研究及测定
匡云飞,邹建陵,李 薇,杨颖群,许金生,冯泳兰,李玉明
(衡阳师范学院化学与材料科学学院,湖南衡阳 421008)
尿酸在聚呋喃丙烯酸电化学传感器上的电化学行为研究及测定
匡云飞,邹建陵,李薇,杨颖群,许金生,冯泳兰,李玉明
(衡阳师范学院化学与材料科学学院,湖南衡阳 421008)
用电聚合法制备了聚呋喃丙烯酸电化学传感器 (PFA/GCE),研究了尿酸 (UA)在该电化学传感器上的电化学行为,探讨了线性扫描溶出伏安法测定尿酸含量的最佳实验条件。结果表明:在含一定量UA的BR (pH=5.0)缓冲溶液中,以0.1 V/s在0.1~0.7 V电位范围内进行扫描,发现在约0.4 V左右处UA产生灵敏的氧化峰,其峰电流与其浓度在3.0×10-7~9.0×10-4mol/L范围内呈良好的线性关系,检出限(S/N=3)为8.5×10-8mol/L。该方法灵敏度高,抗干扰性强,电极制备简单,重现性好,可用于人体尿液中尿酸的测定。
尿酸;呋喃丙烯酸;线性扫描溶出伏安法;玻碳电极
尿酸(UA)是人体内蛋白质和核酸等生命物质的代谢产物,每人每天平均产生600 mg,其中2/3经尿液排出,正常人尿液中UA浓度为1.49~4.46 mmol/L,若含量过高(称高尿酸症或Lesch-Nyhan综合症),是许多疾病的征兆,如心血管疾病、痛风、肥胖、糖尿病、高胆固醇、高血压、肾病、心脏病等。因此,对人体尿液中UA的定量分析在药物控制及临床诊断等方面具有重要意义。目前测定UA的方法主要有色谱法[1-3]、电泳法[4]、光度法[5]。但光度法测定灵敏度低,且易受样品中存在的其它发色团的影响;色谱法样品处理过程过于繁琐,仪器价格昂贵,限制了它的使用范围。近年来,化学修饰电极法测定[6-13]UA引起人们极大兴趣,但有些电极制备较复杂,有些重现性和稳定性较差,等等。
本文用具有开发价值的新型有机合成原料呋喃丙烯酸(FA)作为修饰剂,利用循环伏安法研制了一种新型的电化学传感器聚呋喃丙烯酸修饰玻碳电极(PFA/GCE)。探讨了UA在该电化学传感器上的伏安性质。讨论了测定最佳条件,采用线性扫描溶出伏安法进行定量分析。将该电化学传感器用于人体尿液中UA的测定,能够显著提高分析的灵敏度、选择性和重现性。
1 实验部分
1.1主要仪器
EC550电化学工作站(武汉高仕睿联科技有限公司),SB超声波清洗机(宁波新芝生物科技股份有限公司),AE200型电子分析天平(梅特勒-托利多仪器有限公司),78-1磁力加热搅拌器(山东甄城华鲁电热仪器有限公司),H2601酸度计(上海大普仪器有限公司)
1.2主要试剂
10.0mmol/L UA标准储备液,0.01 mol/L呋喃丙烯酸溶液,0.2 mol/L磷酸盐缓冲溶液,0.2mol/LNa2HPO4溶液,1.0 mol/L HAc-Na Ac缓冲溶液,1.0 mol/L NH3-NH4Cl缓冲溶液等,所用试剂均为分析纯,未进一步处理,实验用水为高纯去离子水。

图1 尿酸的循环伏安a、PFA/GCE b、GCE+尿酸c、PFA/GCE+尿酸底液:BR缓冲溶液(p H=5.0)
1.3聚呋喃丙烯酸电化学传感器的制备
1.3.1玻碳电极的预处理及活化
将玻碳电极(GCE)用0.05μm Al2O3粉末抛光成镜面,依次用HNO3、无水乙醇和水超声清洗5 min,取出后用高纯去离子水冲净。再将电极置于0.5 mol/L H2SO4溶液中,于1.0~-1.0 V电位范围内以0.1 m V/s扫描速度采用循环伏安法进行活化处理,置于p H7.3 Na H2PO4-Na2HPO4缓冲溶液中保存备用。
1.3.2聚呋喃丙烯酸电化学传感器的研制
将已活化处理的GCE置于1.0 mmol/L FA的Na H2PO4-Na2HPO4缓冲溶液(p H=7.3)中,然后以活化处理后的GCE为工作电极,甘汞电极(SCE)为参比电极,铂柱(Pt)为对电极,采用循环伏安法在-1.5~1.5 V电位条件下电聚合5圈,取出后用水反复冲洗,即得聚呋喃丙烯酸电化学传感器(PFA/ GCE)。然后将传感器保存于p H7.3 Na H2PO4-Na2HPO4缓冲溶液待用。
1.4实验方法
移取一定量的UA标准工作液于含有10.0 m L BR缓冲溶液(p H=5.0)的电解杯中,然后以PFA/ GCE为工作电极,SCE为参比电极,Pt为对电极,在-0.2 V处富集25s,于0.1~0.7 V范围内,利用线性扫描溶出伏安法以0.1 V/s扫描速度进行测定,记录在0.4 V处的氧化峰峰电流,再以峰电流为纵坐标,UA浓度为横坐标,绘制工作曲线。
2 结果讨论与分析
2.1尿酸在修饰电极上的电化学行为分析
2.1.1尿酸在修饰电极上的循环伏安行为分析
以PFA/GCE为工作电极,SCE为参比电极,铂丝电极为对电极,分别在含1.0×10-4mol/L UA 的BR缓冲溶液(p H=5.0)和空白BR缓冲溶液(p H=5.0)中,于0.1~0.7 V的电位范围内,以0.1 V/s的扫描速度进行循环扫描,所得结果见图1所示。
GCE在空白缓冲液中无明显氧化峰,图中未标出;由图1可以看出:PFA/GCE在空白缓冲液中无明显氧化峰(曲线a);由曲线b知:UA在GCE上出现了一对不可逆的氧化还原峰,其中Epa=0.481 V,Epc=0.455,说明玻碳电极活化时,使玻碳电极表面结构发生变化,暴露出新鲜的电极表面,新鲜的碳原子作为活性中心催化了UA和电极之间的电子交换反应,提高了电极反应的灵敏度和可逆性[14]。由曲线c知:Epa=0.468 V,Epc=0.453。比较可得,UA在PFA/GCE上的氧化峰较GCE相对负移13 m V,且峰电流增大了约3.7倍。由此可知GCE经PFA修饰后,PFA共轭大П结构和引入的羧基,可以增加结合UA的活性中心,促使电子转移速度明显增强,所得结果与文献[15]相符。同时还发现UA在PFA/GCE上出现的还原峰较GCE的大,进一步说明PFA/GCE可以提高UA在电极上发生电极反应的可逆性和电催化活性。
2.1.2尿酸在修饰电极上的线性扫描溶出伏安行为分析
以PFA/GCE为工作电极,SCE为参比电极,铂柱电极为对电极,分别在空白BR(p H=5.0)缓冲溶液和含1.0×10-4mol/L尿酸的BR(p H=5.0)缓冲溶液中,在-0.2 V富集25s,于0.1 V~0.7 V的电位范围内,以0.1 V/s进行线性扫描溶出伏安法测定(图2)。GCE在空白缓冲液中无氧化峰,图中未标明。从图2中看出:在空白缓冲液中,于PFA/GCE上未发现氧化峰;在含一定量UA的BR缓冲液中,于GCE和PFA/GCE上均有一氧化峰,其峰电位分别为0.480 V和0.468 V。且后者的峰电流为前者的5倍,峰电位负移。由此可知于GCE上修饰PFA后能够提高UA的电子交换反应速度,增强对UA的电化学氧化的电催化作用。
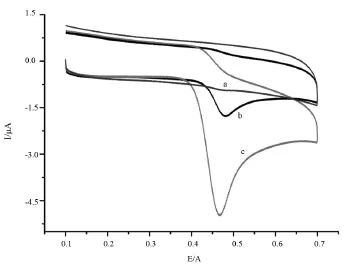
图2 尿酸的线性扫描溶出伏安a、PFA/GCE+缓冲液 b、GCE+尿酸+缓冲液c、PFA/GCE+尿酸+缓冲液
2.2电化学聚合条件的选择
在1mmol/L FA的Na H2PO4-Na2HPO4缓冲溶液中,经过反复试验,考察了不同的聚合电位范围、聚合圈数、聚合底液p H所制得的修饰电极对测定UA峰电流的影响。结果发现:聚合电位为-1.5~1.5V,聚合圈数为5圈,聚合底液Na H2PO4-Na2HPO4缓冲溶液的p H为7.2时,所得的电化学传感器对UA的响应最大,使用寿命最长,稳定性最好。
2.3线性扫描溶出伏安法测定尿酸实验条件的优化
2.3.1底液种类及p H
以PFA/GCE为工作电极,SCE为参比电极,铂柱电极为对电极,于0.1~0.7 V的电位范围内,以100m V/s在-0.2V处富集25s的条件下,考察不同底液(p H 5.0 NaA c-HAc、p H 4.6柠檬酸-柠檬酸钠、p H 5.0磷酸氢二钠-柠檬酸、p H 4.8邻苯二甲酸氢钾-氢氧化钠、p H 5.0 BR缓冲液等)对UA峰电流的影响。结果发现用p H 5.0 BR缓冲液效果最好、峰电流最大、峰形最佳,故本实验以此液为测定的最佳底液。
在上述实验条件下,同时还考察了不同p H (2.09~7.00)BR缓冲液对UA峰电流的影响,结果发现:当p H<5.0时,UA氧化峰电流随着p H的增大而增大;当p H>5.0时,峰电流随p H的增大而减少,且峰形变差。对于有质子参与的电化学反应,p H值的降低有利于还原反应的进行,但p H值过低可能会发生析氢等副反应,影响对尿酸的扩散作用,使电化学信号降低[16]。当p H=5.0时,峰电流最大,峰形最好,电极较稳定。同时发现峰电位随p H增大而负移,且呈线性关系:Epa(V)=-0.690p H+0.0084,相关系数R=0.997。表明UA是等电子等质子参加反应的[17]。
2.3.2扫描速度的影响
在上述实验条件下,采用线性扫描溶出伏安法测定1.0×10-4mol/L的尿酸溶液,改变扫描速度(图3)。结果发现:随着扫描速度的增加,峰电流也随之增大(图3a),且在0.025~0.7 V/s内,ip与v1/2呈线性相关,线性方程为ip(μA)=25.32v1/2(V/s)-3.07,R2为0.997,由此说明该电极过程受扩散控制。同时还发现其Ep与ln v呈线性相关,线性方程为Ep(V)=0.0164ln v(V/s)+0.5121,相关系数R为0.997。

图3 扫描速度的影响
2.3.3富集电位和富集时间的影响
以班会课为例,众所周知,学校的主题班会向来都是投入巨大,场面隆重,但由于班会的主题、活动常常与升学没有直接联系,所以很多学生并不重视,导致班集体的道德教育、学生的人格引导等学校德育功能收效甚微。而在微课程引领下的微班会则不同,用“微”打开了学生的心理市场,得到了他们的普遍认同。
在上述固定未变和已得出的最佳实验条件下,分别以0.1、0.0、-0.1、-0.2、-0.3、-0.4V为富集电位,考察了不同的富集电位对峰电流的影响,实验发现,于-0.2V处富集时峰电流最大,峰型最好;正移或负移,峰电流均较小,且有些峰形很差,背景电流也较大。故本实验的最佳富集电位为-0.2V。同时在-0.2V处富集不同的时间(5~120s),25s前随富集时间的延长,峰电流增大,超过25s后,峰电流减少。因此选择最佳富集时间为25s。
2.4 方法应用及电化学传感器性能评价
2.4.1工作曲线及检出限
在最佳实验条件下,于一定浓度范围内,采用线性扫描溶出伏安法测UA(图4)。实验结果发现:UA在3.0×10-7~9.0×10-4mol/L内时,ip与c有良好的线性关系,线性方程分别为ip(μA)= 2.186×104c(mol/L)+0.967,相关系数R为0.9992,检出限(S/N=3)为1.0×10-7mol/L。

图4 工作曲线
2.4.2选择性
在最佳的实验条件下,于1.0×10-4mol/L尿酸的BR缓冲液中,考察了该电化学传感的选择性,即研究了体内一些常见物质对UA测定的影响。结果表明,在±5%的误差范围内,大量的L-谷氨酸、L-赖氨酸、KCl、NaCl,葡萄糖,蔗糖;50倍的草酸和尿素;10倍的CC对UA测定没有干扰。
2.4.3重现性和稳定性的测定
在最佳实验条件下用同一电化学传感器对1.0 ×10-4mol/L UA连续11平行测定,实验结果RSD =2.8%,说明该法有较好的精密度。按传感器制备方法研制一批(6根)PFA/GCE,用测定方法测定,结果的RAD=3.3%,说明此方法的重现性较好。同时还考察了保存于p H7.3 Na H2PO4-Na2HPO4缓冲液中的传感器不同时间后再用以测定UA,实验结果发现:3周后电流仅下降6.7%,说明该电化学传感器比较稳定,可以循环利用。
2.4.4样品的测定和回收率实验
取正常人体尿液2.5m L,加到100m L容量瓶中用BR(p H=5.0)的溶液稀释后进行定容,配制成样品溶液。在最佳实验条件下用线性扫描循环伏安法测定样品。然后加入已知量的尿酸标准品进行回收率测定(表1)。由表1可知,所测得样品液中UA浓度的平均值为50.38μmol/L,即人体尿液中UA含量为2.015 mmol/L。加标回收率为98.76%~102.34%。

表1 样品的测定和回收率实验结果
[1]马晓丽,冉新建,孟磊,等.反相高效液相色谱法同时测定血清、尿液中尿酸、肌酐的含量[J].分析试验室,2014,33(6):638-641.
[2]周桂芳,傅旭春,王建平.高效液相色谱法测定血清中尿酸的含量[J].海峡药学,2012,24(2):249-250.
[3]施政,刘健,申屠建中,等.高效液相色谱法定量尿酸、黄嘌呤和次黄嘌呤在人体血清中的浓度[J].中国临床药理学与治理学,2013,18(5):532-536.
[4]张贝贝,宋智瑞,陈赞光.毛细管电泳和微流控芯片技术在临床尿检中的应用[J].分析科学学报,2013,29(3):425-430.
[5]吴永明,郑延军,陶武,等.分光光度法测定血清中尿酸的不确定度评定[J].分析试验室,2014,33(10):1143-1146.
[6]王长芹,徐海红,韩晓刚,等.活化玻碳电极直接测定全血中的尿酸[J].分析实验室,2007,26(1):27-31.
[7]张小林,彭艳芬,胡成国,等.十六烷基三甲基溴化铵修饰碳糊电极线性扫描伏安法测定尿液中尿酸[J].分析科学学报,2008,24(6):641-644.
[8]王晓明,孙登明.溴化十六烷基吡啶对尿酸电化学行为的影响及测定[J].化学传感器,2013,33(2):49-53.
[9]付海莹,王建秀,邓留.基于石墨烯和室温离子液体复合物溶胶修饰的玻碳电极制备尿酸电化学传感器[J].分析化学,2014,42(3):441-445.
[10]Rashmi D.Chaudhari,Abhijeet B.Joshi,Rohit Srivastava.Uric acid biosensor based on chemiluminescence detection using a nano-micro hybrid matrix[J].Sensors &Actuators:B.Chemical,2012,173:882-889
[11]Zhen-Huan Sheng,Xiao-Qing Zheng,Jian-Yun Xu,etal.Electrochemical sensor based on nitrogen doped graphene:Simultaneous determination of ascorbic acid,dopamine and uric acid[J].Biosensors and Bioelectronics,2012,34(1):125-131.
[12]Xianqing Tian,Changming Cheng,Hongyan Yuan,etal.Simultaneous determination of L-ascorbic acid,dopamine and uric acid with gold nanoparticles-β-cyclodextrin-grapheme-modified electrode by square wave voltammetry[J].Talanta,2012,93(15):79-85.
[13]孙娜,王宗花,夏建飞,等.聚对氨基苯磺酸/石墨烯复合修饰电极对尿酸的选择性灵敏测定[J].分析测试学报,2012,31(7):853-857.
[14]王德玉,张娜,张克营,等.聚茜素黄T膜修饰电极对尿酸电催化及对人尿中尿酸的检测[J].分析实验室,2012,31(3):113-115.
[15]霍瑞伟,贾丽萍,姚飞,等.Nafion-离子液体-碳纳米管复合膜修饰电极的制备及用于抗坏血酸、多巴胺及尿酸的同时测定[J].中国科学:化学,2013,43:1572-1583.
[16]孙娜,王宗花,夏建飞,等,聚对氨基苯磺酸/石墨烯复合修饰电极对尿酸的选择性灵敏测定.[J].分析测试学报.2012,31(7):853-857.
[17]匡云飞,邹建陵,邓培红,等.羧基化短碳纳米管修饰碳糊电极方波溶出伏安法测定尿酸[J].化学试剂,2011,33(1):47-50.
Electrochemical Behavior and Determination of Uric Acid at Poly Furanacrylic Acid Electrochemical Sensor
KUANG Yun-fei,ZOU Jian-ling,LI Wei,YANG Ying-qun,XU Jin-sheng,FENG Yong-lan,Li Yu-ming
(College of Chemistry and Materials Science,Hengyang Normal University,Hengyang Hunan 421008,China)
In this paper,the electrochemical sensor(PFA/GCE)was prepared by electro polymerization,and the electrochemical behavior of uric acid(UA)was studied.The optimal experimental conditions for the determination of uric acid by linear sweep stripping voltammetry were investigated.The results show that in the BR(p H=5.0)buffer solution with a certain amount of 0.1V/s,UA can be scanned in the range of 0.1~0.7 V potential,and the peak current and its concentration are linear.The peak current and its concentration are 3.0×10-7~9×10-4mol/L.The detection limit(S/N=3)is 8.5×10-7mol/L.The method is simple,reproducible and can be used for the determination of uric acid in human urine.
uric acid;furanacrylic acid;linear sweep stripping voltammetry;glassy carbon electrode
O657.1
A
1673-0313(2015)06-0010-05
2015-10-08
湖南省科技计划重点项目(2012FJ2002)
匡云飞(1963-):男,湖南祁东人,教授,主要从事配合物合成和电化学分析的研究。

