五味子粉末饮片颗粒度适宜性研究*
★ 陆晓晖** 唐芳瑞 马志林 邵 峰 黄慧莲 刘荣华*** (.佛山市顺德区第一人民医院 广东佛山5800;.江西中医药大学 南昌0004;.江西汇仁集团有限公司 南昌005)
北五味子为木兰科植物五味子Schisandrachinensis(Turcz.)Baill.的干燥成熟果实,具有补肾养心、收敛固涩、补益生津、强壮等功效,临床上用于治疗久泻不止、遗尿尿频、梦遗滑精、心悸失眠、自汗盗汗等症状[1-3],现代药理研究表明,以五味子醇甲、五味子甲素为代表的木质素类成分具有显著的保护肝细胞、改善肝功能[4],抑制宫颈癌细胞生长[5],抗脑缺血性损伤[6]、抗心肌细胞缺氧/复氧(H/R)损伤[7]、抗癫痫[8]、抗氧自由基和中枢神经抑制作用等活性[2]。虽有文献报道[9],不同粒度五味子饮片中五味子醇甲等6种木脂素成分含量存在明显差异,但仅局限与6种木脂素成分的含量变化上,对于不同粉碎度五味子粉末饮片的适宜性研究未见报道。本文将醋制五味子分级处理为不同粉碎度的粉末饮片,采用HPLC法同时测定其五味子醇甲和五味子甲素的提取率和进行HPLC指纹图谱的对比分析研究,采用干燥减重法测定比较总浸出物的含量变化,探讨五味子饮片进行粉末化处理分级后其质量的差异性,从而为五味子饮片的高效临床应用提供实验依据。
1 仪器与试药
1.1 仪器 高速中药粉碎机(YF-103,浙江省瑞安市永历制药机械有限公司,功率0.8kw,转速25000r/min);十万分之一电子天平(德国Sartorius公司);中国药典专用筛(1-9号筛,浙江省上虞市华康化验仪器厂);Waters-2695高效液相色谱仪(美国Waters公司),2996型二极管阵列检测器和Empower工作站;Aglient1200高效液相色谱仪,Agilent ChemStation工作站以及 VWD检测器(美国Aglient公司)。
1.2 试药 五味子醇甲对照品(含量测定用,批号110857-200102)、五味子甲素对照品(含量测定用,批号110764-200107)均购于中国药品生物制品检定所;甲醇(色谱纯,Dikmapure,DIMA TECHNOLOGY Inc.);甲醇(分析纯,上海振兴化工一厂);实验用水为双蒸水,自制。
1.3 药材收集与前处理 传统炮制醋制五味子饮片(购自江中中药饮片有限公司),经江西中医药大学刘荣华教授鉴定为正品,凭证标本存于江西中医药大学标本馆。
按照《中国药典》2010年版(一部)ⅡA“药材取样法”分别取五味子药材干燥品若干克,经粉碎机粉碎后,分别通过药典筛1-9号,制备成10个同一批次药材的不同颗粒度粉末饮片样品,编号依次为0-9号,备用,见表1。
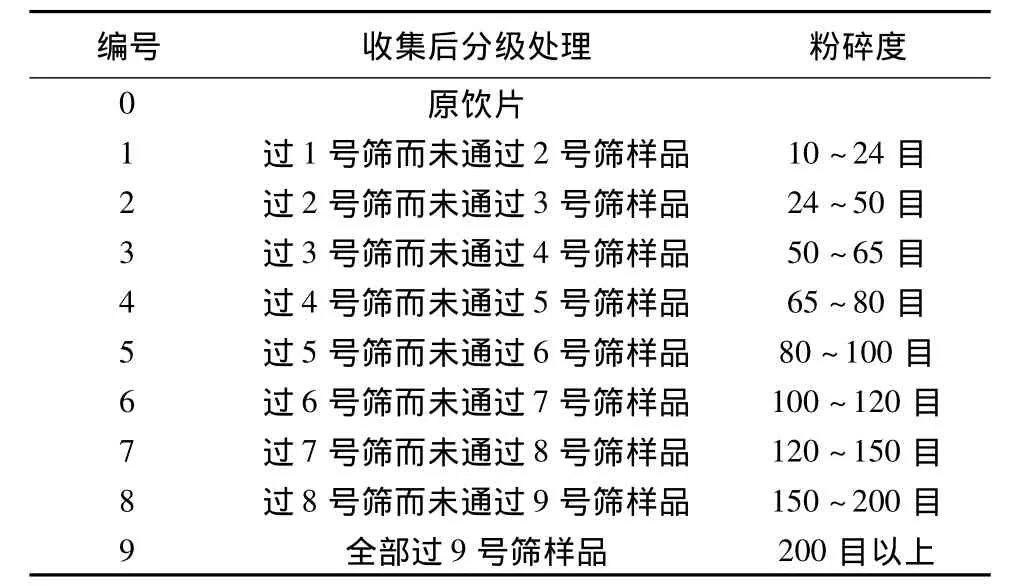
表1 样品分级处理过程
2 五味子醇甲、五味子甲素的提取率测定
2.1 HPLC色谱条件 Aglient1200 HPLC色谱仪,四元泵,真空脱气机,色谱柱:Aglient ZORBAX E-clipse XDB -C18Analytical 4.6mm ×250mm,5μm;流动相:乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱(0~12min,45% ~100%A;12~20min,100%A;20~25min,100% ~45%A);柱温:25℃;检测波长:225nm;进样量:10μL,流速:1.0mL/min。
2.2 供试品及对照品溶液的制备 根据常规饮片服用方式进行模拟,分别取各样品2.0g,以饮片质量:蒸馏水体积=1∶15,置于50mL圆底烧瓶中,加入30mL蒸馏水,称重,以沸水浴进行回流提取,提取时间30min,趁热过滤,放冷,加水补足重量,静置,取滤液1mL,以1∶1甲醇稀释定容至2mL,充分摇匀,吸取甲醇稀释液若干,通过0.45μm有机系滤头,得样品制备液,备用。
精密称取五味子醇甲对照品5.15mg、五味子甲素对照品4.37mg,同时置于10mL容量瓶中,加甲醇溶解并定容至刻度,摇匀,配成含五味子醇甲浓度为0.515 mg/mL,五味子甲素为 0.437mg/mL 的储备液。
2.3 系统适应性实验 分别精密吸取空白对照溶液、混合对照品溶液、供试品溶液各10μL,按“2.1项”下色谱条件依次注入高效液相色谱仪中,采用外标法测定含量,在上述条件下,得到色谱峰理论塔板数不低于6000,分离度均大于1.5。图中1号为五味子醇甲,2号为五味子甲素,结果见图1。
2.4 方法学考察
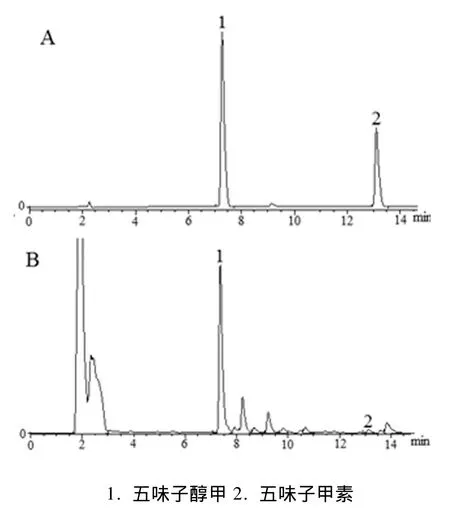
图1 混合对照品溶液(A)、五味子粉末饮片样品溶液(B)的HPLC色谱图
2.4.1 线性关系考察 精密量取对照品储备液分别稀释成含五味子醇甲和五味子甲素一系列浓度:五味子醇甲浓度分别为0.025 76,0.032 20,0.064 40,0.128 800,0.257 60 mg/mL;五味子甲素浓度分别为 0.005 47,0.002 735,0.001 368,0.000 5295,0.000 2735mg/mL。分别取上述溶液10μL进样,记录峰面积,以峰面积为纵坐标(Y),对照品溶液质量浓度(mg/mL)为横坐标(X),作线性回归方程。得五味子醇甲的回归方程为 Y=4.1588×104X-62.294,线性范围为:0.258μg ~ 2.580 μg(r=0.9993);五味子甲素的回归方程为 Y=4.1982×104X+8.8187,线性范围为 0.002 74μg~0.0547μg(r=0.9995)。
2.4.2 精密度试验 精密吸取同一混合对照品溶液,按“2.1”项下色谱条件连续进样5次,记录色谱峰面积,五味子醇甲和五味子甲素的峰面积RSD值分别为0.46%,0.34%。表明该仪器精密度良好。
2.4.3 重复性试验 精密称取7号样品5份,各2.0g,按“2.2”项下供试品处理方法制备,按“2.1”项下色谱条件进行分析,计算得五味子醇甲和五味子甲素的峰面积RSD值分别为0.62%、0.37%,表明该方法重现性良好。
2.4.4 稳定性试验 精密称取1号样品,按“2.2”项下方法制备得供试品溶液,在室温下放置,分别在0,3,6,9,12,24h 进行测定,记录色谱峰面积,并计算得到五味子醇甲和五味子甲素的峰面积RSD值分别为1.09%,1.28%。表明样品在24h内稳定性较好。
2.4.5 加样回收试验 精密称取已知含量的1号五味子粉末饮片5份,各1.0g,分别精密加入一定量的对照品,按“2.2”项下供试品溶液处理方法制备,按“2.1”项色谱条件进行色谱分析,由测得量与加入量计算回收率,结果见表2。由以下结果表明,五味子醇甲与五味子甲素的回收率符合实验要求,表明本实验方法的准确定良好。
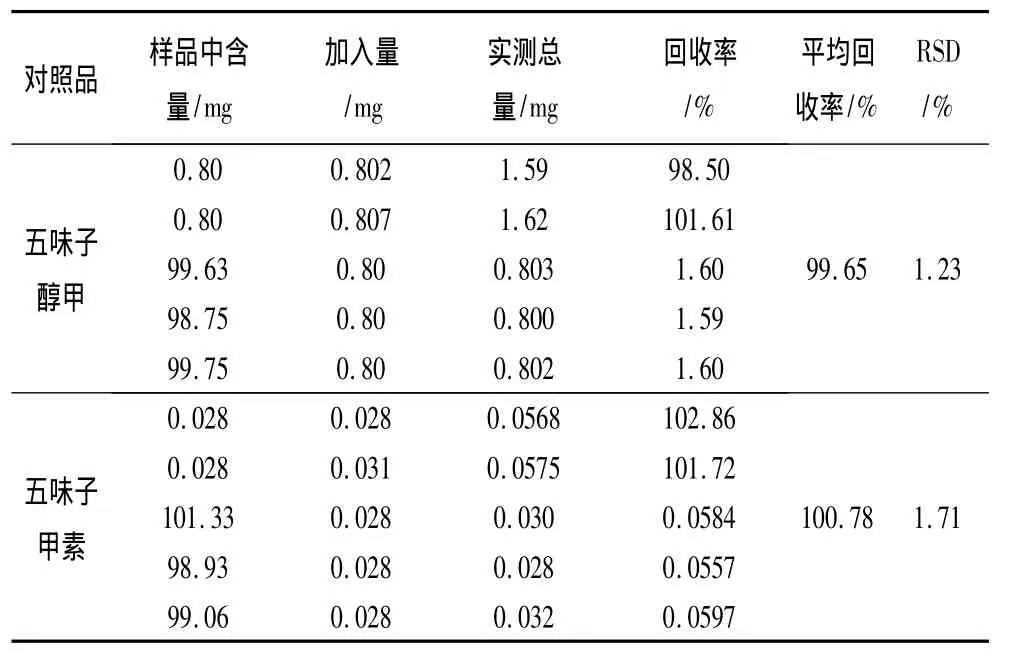
表2 五味子醇甲和五味子甲素加样回收率(n=5)
2.5 实验结果 根据上述方法测定了10种五味子粉末饮片五味子醇甲与五味子甲素的提取率,结果见表3。
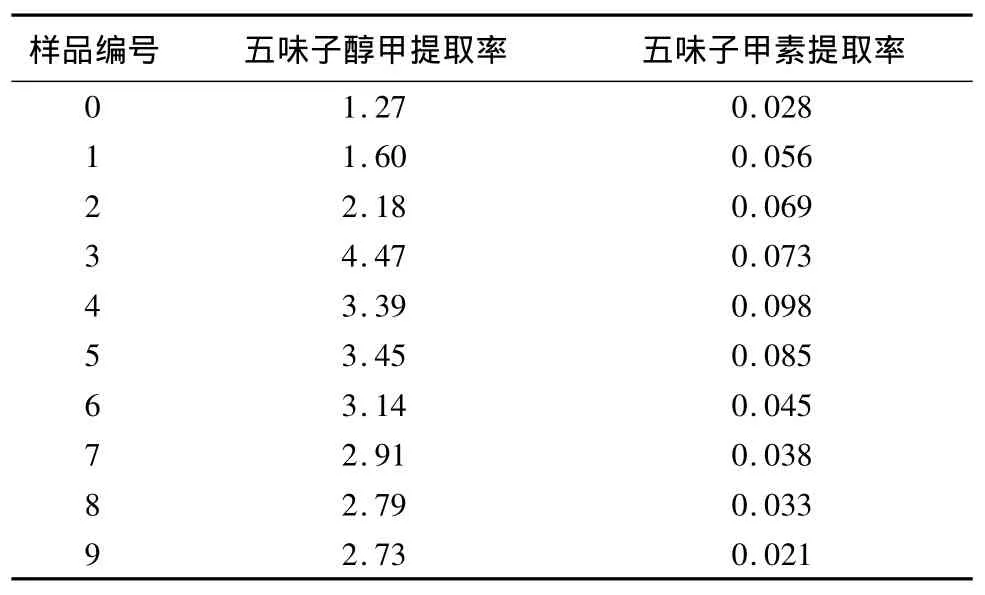
表3 五味子醇甲与五味子甲素的提取率结果(n=10)mg/g
3 五味子粉末饮片浸出物的测定
3.1 实验方法 分 别精密称定各五味子粉末饮片10.0g,平行测定10次,以饮片质量:蒸馏水体积=1:15,置于500mL圆底烧瓶中,加入150mL蒸馏水,以沸水浴回流提取30min,趁热过滤,放冷,水浴蒸发,减压干燥至恒重,采用减重法进行称定。
3.2 实验结果 见 表4。
4 HPLC指纹图谱的测定与分析
4.1 样品前处理 分 别精密称取五味子各组饮片各 1 .0g,以饮片质量:蒸馏水体积 = 1∶15,按照“2.2”项下制备供试品溶液的方法处理,得样品制备液,备用。
4.2 HPLC色谱条件 W aters-2695高效液相色谱仪(美国Waters公司),2996型二极管阵列检测器和Empower工作站;色谱柱:Aglient ZORBAX E-clipse XDB -C18Analytical 4.6mm ×250mm,5μm;流动相:乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱(0~20min,5% ~25%A;20 ~50min,25% ~80%A;50~60min,80%A),柱温:25℃,检测波长:252nm,进样量:10μL,流速:1.0 mL/min。
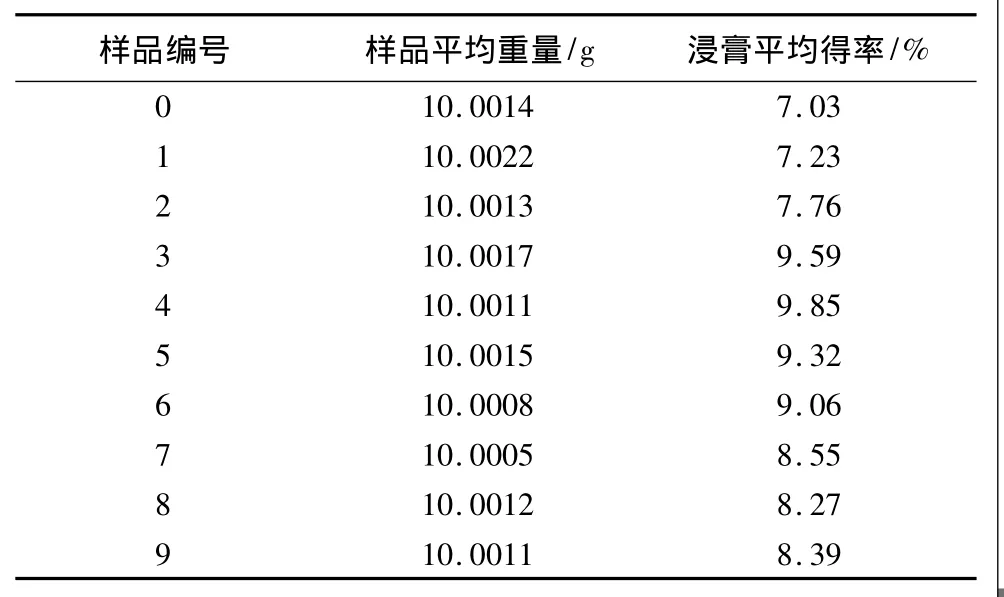
表4 五味子粉末饮片水提取浸膏得率(n=10)
4.3 结果
4.3.1 指纹图谱 按实验分析方法测定10种五味子粉末饮片的HPLC色谱指纹图谱叠加图如图2:
4.3.2 共有指纹峰的标定 利用“中药色谱指纹图谱相似度评价系统2004 A版”软件,以醋制五味子原饮片(0号)为参照峰生成五味子粉末饮片共有模式的对照指纹图谱。以5号峰为参照峰(S),其保留时间为1,各共有峰的相对保留时间如表5所示,结果表明RSD值小于3%,符合指纹图谱的要求。见图3。
4.3.3 共有指纹峰相对峰面积 根据五味子粉末饮片供试品HPLC指纹图谱测定结果,以5号峰为参照峰(S),以其峰面积为1,计算其他各共有指纹峰的相对峰面积,结果见表6。
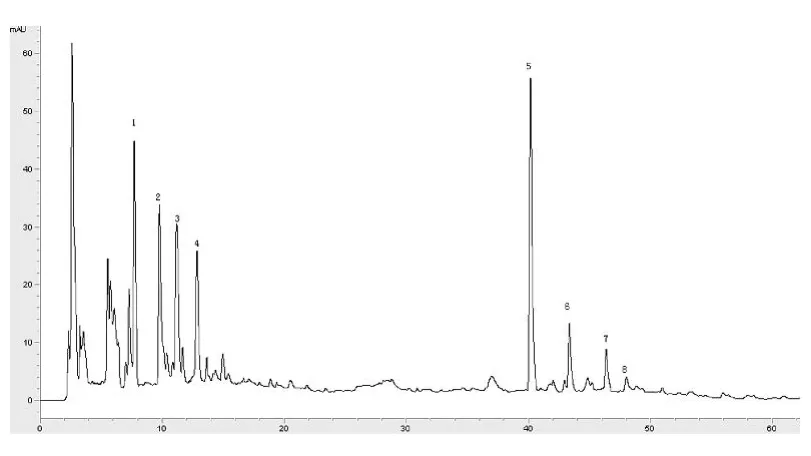
图3 五味子颗粒化饮对照指纹图谱共有峰的标定
4.3.4 非共有峰面积 通过对五味子样品的HPLC指纹图谱结果测定,统计各组饮片非共有峰面积占总峰面积比值,其共有峰面积百分比在43.44% ~53.19%,结果见表7。
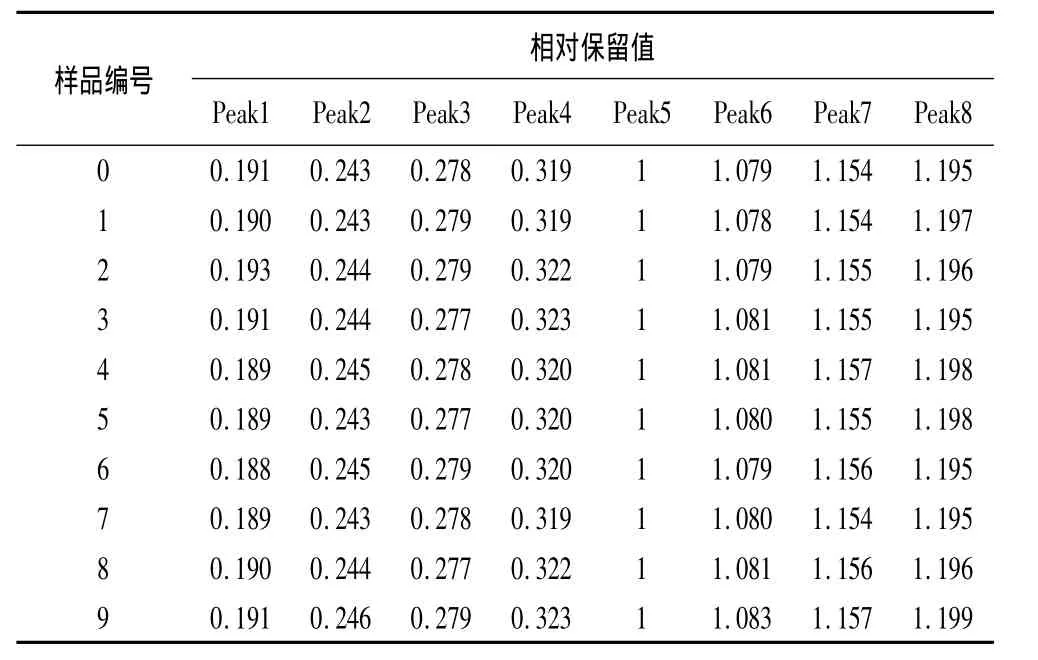
表5 五味子粉末饮片HPLC指纹谱图的共有峰相对保留时间
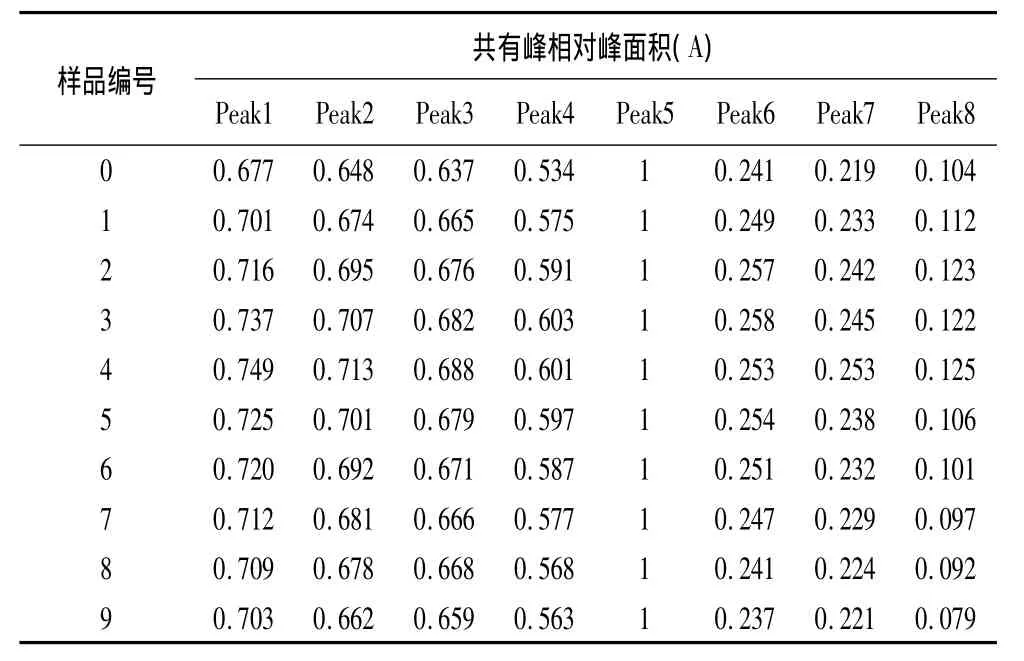
表6 五味子粉末饮片指纹图谱共有峰的相对峰面积
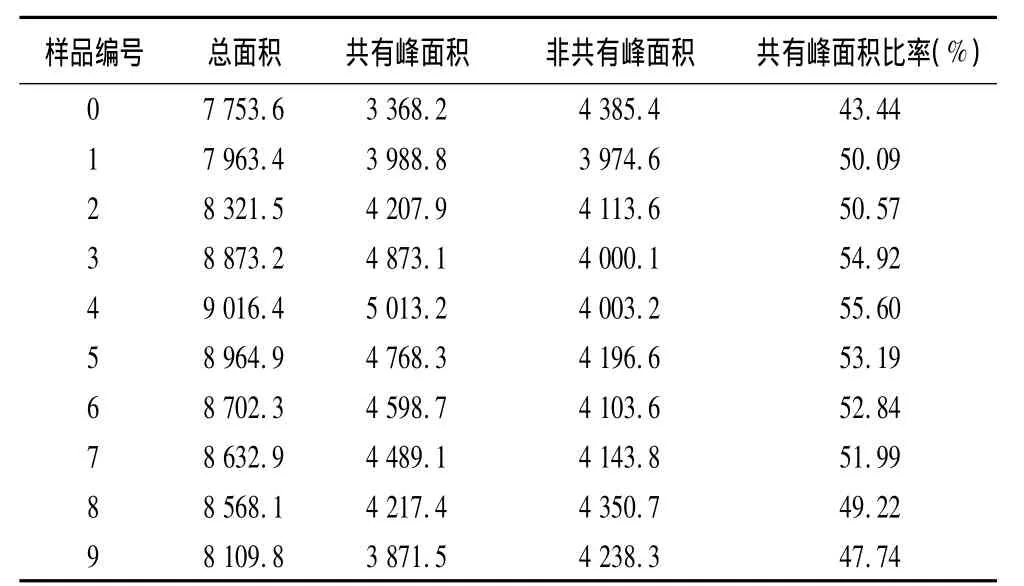
表7 五味子粉末饮片指纹图谱总峰面积、共有峰面积、非共有峰面积
5 讨论
五味子粉末粗细对五味子醇甲与五味子甲素的溶出呈现一定规律性变化,随着粉碎度由粗到细,两者的提取率均呈现先升高后降低的趋势,五味子粉末饮片在50~65目范围内五味子醇甲的溶出达最大值(4.47mg/g),是原饮片的3.5倍多,是200目以上细粉样品的1.64倍;而五味子甲素的溶出在65~80目范围内出现最大值(0.098mg/g),是原饮片的3.5倍,是200目以上细粉样品的4.67倍,充分表明五味子粉碎处理的确对有效成分的溶出具有相当大的影响。粉碎度在50~80目之间时,有利于两种主要有效成分溶出。
五味子粉末饮片浸出物利率最高是在65~80目粉碎度范围内,浸出率达到9.85%,是原饮片浸出率的 1.4倍,其次是 50~65目,浸出率达到9.59%。65~80目以上时,随着颗粒细度的增加,浸出率出现相对小幅度下降的趋势,说明并不是颗粒度越细得膏率越高。粉碎度在50~100目范围内有利于提高五味子饮片的浸出物得率。
指纹图谱研究表明,粉碎度在65~80目范围内样品指纹图谱指纹峰总面积最大(9016.4),其次是80~100目(总面积8964.9)和50~65目(总面积8873.2)。
结合五味子浸出物得率、以及有效成分五味子醇甲与五味子甲素的提取率测定结果和HPLC指纹图谱研究结果,我们初步认为50~80目范围的五味子粉末饮片的溶出效果最佳。
[1]国家药典委员会.中华人民共和国药典.一部[S].北京:化学工业出版社,2010:61-62.
[2]国家药典委员会.中华人民共和国药典.一部[S].北京:化学工业出版社,2010:X A,附录62.
[3]中药饮片炮制工艺与质量标准及GMP实施实用手册[M].北京:中国中医药出版社,2006,1 033-1 038.
[4]姚莹,寿迪文,崔勤敏.南北五味子中木脂素对急性肝损伤小鼠保护作用的比较[J].中华中医药学刊,2014,32(6):1 465-1 467.
[5]郑若洋,何冬梅,李江滨,等.五味子对体外培养宫颈癌细胞生长的抑制作用[J].亚太传统医药,2013,9(1):44-45.
[6]姜恩平,王帅群,王卓,等.北五味子总木脂素对脑缺血模型大鼠神经细胞凋亡及 p-AKT表达的影响[J].中国中药杂志,2014,39(9):1 680-1 684.
[7]刘威,张成义,沈楠,等.五味子乙素对乳鼠缺氧/复氧损伤心肌细胞的保护作用及其机制[J].吉林大学学报 (医学版),2014,5(14):977-980.
[8]张国辉,王赞,邢军,等.五味子木脂素的抗癫痫作用及神经保护研究[J].中国现代药物应用,2014,8(4):247.
[9]苏桃,陆兔林,毛春芹,等.不同粒度五味子有效利用率评价[J].中国实验方剂学杂志,2012,18(3):96-99.

