Meta 分析:导管消融治疗心房颤动合并心力衰竭的系统评价
周鑫斌 缪静 武丽 徐晓明
心房颤动(房颤)和心力衰竭(心衰)是心血管疾 病领域两大难题,两者常相互并存,有着相似的危险因素,并能相互影响而陷入恶性循环,使得患者死亡风险显著增加,给治疗带来巨大挑战。理论上来说,房颤转复为窦性心律能减少其对心功能的不利影响,从而改善心衰预后。但研究显示,通过抗心律失常药物,如胺碘酮等转复心律并未显著改善房颤[1]或房颤合并心衰患者[2]的预后,可能是由于药物不足以维持窦性心律或者其本身的不良反应所致。与此同时,研究显示,导管消融在转复房颤心律方面的有效性显著优于药物控制,但这些研究中房颤患者心功能大多正常,导管消融能否有效改善房颤合并心衰患者的心功能仍未确定。因此,本研究采用Meta 分析方法对导管消融治疗房颤合并心衰患者的临床试验进行系统评价,以期为临床提供参考。
1 对象与方法
1.1 研究资料
采用计算机系统检索 Embase、PubMed、Cochrane 图书馆、ClinicalTrials. gov、中国生物医学文献数据库(CBM)、中国期刊全文数据库(CNKI)、中国科技期刊数据库(VIP)以及万方数据库,检索年限从建库至2014 年10 月。分别采用英文检索词(“atrial fibrillation”)AND(“heart failure”OR“left ventricular systolic dysfunction”OR “reduced left ventricular systolic function”)AND (ablation OR“catheter ablation”OR“pulmonary vein isolation”)及相应中文检索词检索,无语种及研究类型限制。手工检索相关参考文献、综述或之前发表的系统评价,避免遗漏。
1.2 纳入及排除标准
纳入标准:(1)采用导管消融治疗房颤合并心衰患者,房颤类型无限制。心衰定义为左心室收缩功能不全[左心室射血分数(left ventricular ejection fraction,LVEF)<50%]或出现NYHA 心功能分级Ⅱ级以上症状。(2)研究至少纳入并随访10 例患者。(3)随访时间至少6 个月。(4)有研究指标的原始数据。排除标准:(1)重复发表的研究结果或无对照的研究。(2)采用手术消融如迷宫手术(Cox Maze)等研究。(3)数据不完整。
1.3 资料提取与质量评价
由两位研究者独立进行,并交叉核对,意见不同协商解决。提取资料包括:研究类型、样本例数、患者基线特征情况(包括患者年龄、性别比例、房颤平均病程、冠心病比例)、房颤类型(阵发性、持续性或永久性)、随访时间、随访期间维持窦性心律患者比例、结局指标(LVEF 变化、并发症发生率)等。采用Cochrane 协作网工具评价随机对照试验质量[3],而观察性研究(病例对照研究和队列研究)则采用Newcastle-Ottawa 量表评分系统(分值范围0 ~9分)[4]。
1.4 结局指标
主要结局指标为导管消融术后LVEF 变化,次要指标为手术相关严重并发症的发生率。
1.5 统计学分析
采用STATA 12.0(Stata Corp,College Station,TX)软件统计分析消融术后LVEF 变化,其资料采用加权均数差(WMD)及95% 置信区间(confidence interval,CI)表示。各纳入研究的异质性采用Q 检验,当I2<50%认为无显著异质性而采用固定效应模型合并效应量,否则采用随机效应模型,并分析异质性来源。纳入研究的发表偏移采用漏斗图直观分析,并用Egger's 和Begg's 检验定量检测,当P <0.05 认为有显著发表偏移。在排除低质量或高权重研究后行敏感性分析,考察结果稳健性。以纳入研究中不同的人群特征因素为变量,采用Meta 回归方法分析其对导管消融术后LVEF 变化的影响大小。
2 结果
2.1 纳入研究的特点
共检索到相关文献2268 篇,其中英文文献1613 篇,中文文献655 篇(图1)。严格按照文献的纳入与排除标准进行逐层筛选后,最终纳入15 项研究,包括4 项随机对照试验(RCT)[5-8]、11 项观察性研究(5 项队列研究[9-13],6 项病例对照研究[14-19]),共2026 例患者,其中686 例接受导管消融治疗,基线资料特征见表1。15 项房颤导管消融的研究中,5项[5,6,8,14,18]对照组采用药物治疗,9 项[9-13,15-17,19]对照组为LVEF 正常或接近正常患者,1 项[7]为对比房室结消融加双心室起搏治疗。在本次系统评价中,主要关注的是房颤合并心衰患者导管消融术后心功能改善情况及不良事件发生率,而对于对照组患者的组成类型未强制要求。
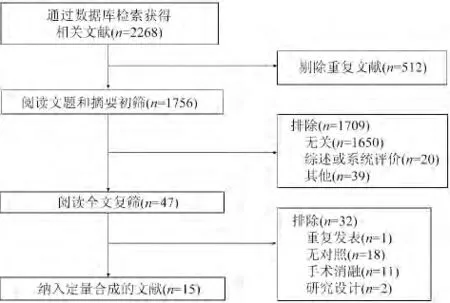
图1 文献筛选流程图
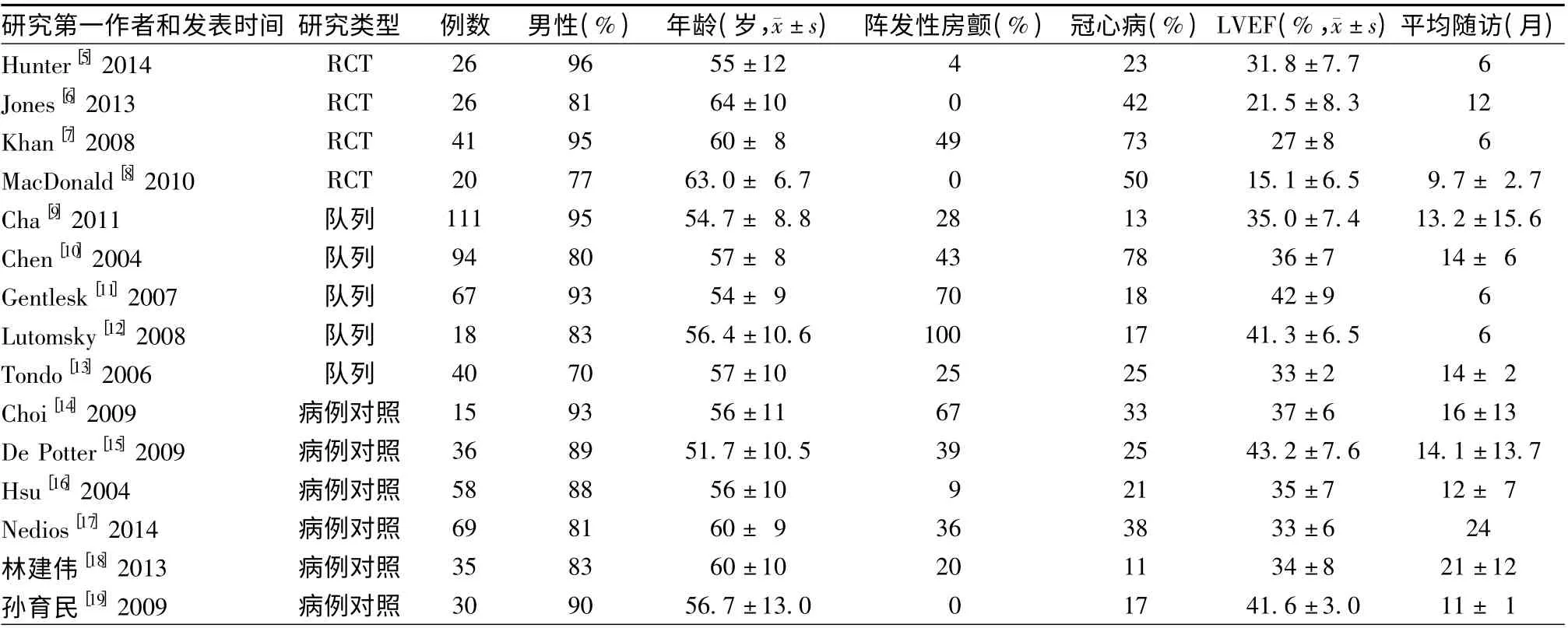
表1 纳入研究中患者基本特征比较
2.2 质量评价
纳入的RCT 研究质量均在中等以上,潜在偏倚风险低;观察性研究Newcastle-Ottawa 评分为4 ~8分,平均(5.3 ±1.3)分。
2.3 结局指标
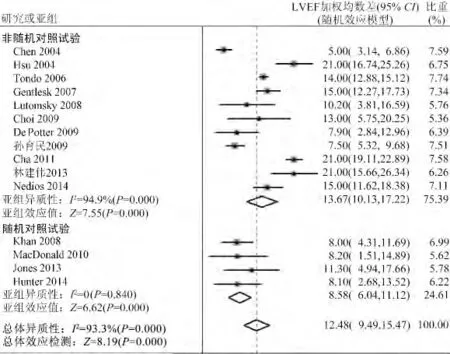
图2 导管消融术前后LVEF 均数差比较的Meta 分析结果
Meta 分析显示,导管消融术后LVEF 显著升高(WMD 12.48%,95% CI 9.49% ~15.47%,P <0.001)。但研究间存在显著异质性(I2=93.3%,P<0.001,图2)。为探索异质性来源,根据不同研究类型进行亚组分析,结果显示,4 项RCT 术后LVEF增幅为8.58% (95% CI 6.04% ~11.12%,P <0.001),研究间未存在异质性(I2= 0%,P =0.840);11 项观察性研究LVEF 增幅为13.67%(95% CI 10.13% ~17.22%,P <0.001),但研究间异质性显著(I2=94.9%,P <0.001,图2)。进一步Meta 回归分析显示,各项研究中纳入人群的冠心病患者比例及研究类型对异质性有较显著影响,校正后强度分别为34.5%和8.4%。
通过漏斗图定性及Egger's(P = 0.783)和Begg's(P=1.000)定量检验证实,纳入文献未存在显著发表偏移(图3)。敏感性分析中,去除质量最低研究、最大权重研究或变换分析的效应模型,并未改变结论。
2.4 Meta 回归分析
Meta 单因素回归分析显示,各项研究中纳入人群的冠心病患者比例与导管消融术后LVEF 升高存在负相关性,β =-0.86(95% CI-0.76 ~-0.97,P = 0.02,图4)。意味着冠心病患者比例每下降1%就会使得导管消融术后LVEF 平均升高0.86%。该结果提示,合并冠心病的患者,其获益可能会少于其他类型患者。其余变量,如不同平均年龄(P =0.82)、基础LVEF 值(P =0.78)、男性患者比例(P =0.83)、非阵发性房颤(即持续性或永久性房颤)患者比例(P=0.86)、术前房颤平均病程(P =0.31)、随访期间维持窦性心律患者比例(P = 0.89)及随访时间(P =0.18)与LVEF 升高无显著相关性。
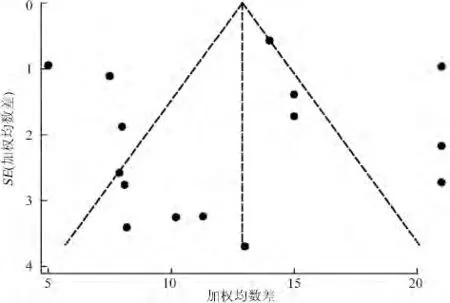
图3 纳入研究的漏斗图
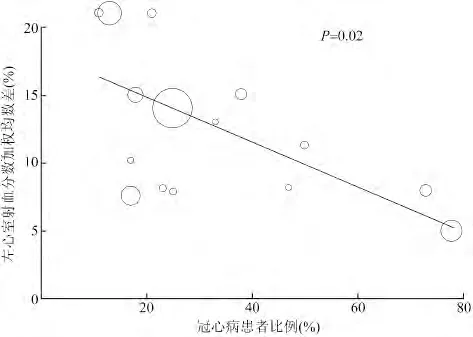
图4 冠心病患者比例与左心室射血分数变化的Meta 回归分析结果
2.5 安全性分析
15 项研究中,共14 项研究描述了导管消融手术相关严重并发症,包括手术相关死亡、围术期脑卒中、心脏压塞及消融相关肺水肿等。并发症发生率为0 ~13.6%,平均(4.8 ±3.6)%。
3 讨论
本研究通过系统评价方法显示,导管消融能显著增加房颤合并心衰患者LVEF 值,从而改善该类患者心脏收缩功能及预后。然而,所有纳入的研究之间存在显著异质性,该异质性可能来源于不同研究类型或各项研究中不同的冠心病患者比例、房颤类型等。
亚组分析显示,4 项RCT 研究之间未存在显著异质性(I2=0%),其合并结果显示,导管消融术后LVEF 平均增加8.58%。虽然总体异质性较显著,考虑到4 项RCT 研究偏倚风险均较低,导管消融显著改善房颤合并心衰患者LVEF 的结果仍值得肯定,但合并冠心病患者的获益似乎要少于合并其它疾病患者,提示术后LVEF 升高与心衰的病因存在一定相关性。
房颤是心动过速性心肌病(tachycardia-induced cardiomyopathy,TIC)常见病因之一,可因房室失同步收缩而出现LVEF 下降和心衰。持续性房颤、平均心室率及房颤病程或为TIC 的独立危险因素[20]。房颤导管消融术很大程度上改变了不规则心脏舒缩周期等对心衰的不良影响,可显著改善左心室收缩功能,增加LVEF,从而改善患者的运动耐力、生活质量及预后。并且,心衰症状的改善也可减少术后房颤的复发,阻断这一恶性循环。研究中非心衰的房颤患者术后LVEF 增加幅度为1.56%,显著少于合并心衰的患者。但纳入的研究大多采用心脏超声来评价LVEF,相比于心脏磁共振成像等手段,这一评价措施对合并房颤患者可能存在一定偏差。大多数研究并未说明LVEF 的评估是在房颤还是窦性节律下进行的,这也增加了其术后LVEF 显著上升的不确切性。
前期有大规模研究显示,导管消融在房颤患者中并发症总体发生率为5.9%,严重并发症发生率为2.2%[21]。本研究所纳入试验中的严重并发症发生率与之相当或略高,可能源于纳入心衰等合并疾病患者,或者源于样本量不充足。此外,并发症发生率与不同手术方式及术者有直接相关性,随着导管消融技术日渐成熟,并发症发生率可能会进一步降低。
通常来说,随访期内房颤复发率以及房颤的类型会对术后患者LVEF 值变化产生影响。由于纳入的各研究对术后房颤复发患者、维持窦性心律患者以及不同类型房颤患者的LVEF 值并未分别进行评价,且纳入研究的随访时间相对较短,尚不足以观察到所有房颤复发情况,很难判断这些混杂因素对LVEF 的变化结果是否有潜在的显著影响。
因此,笔者将上述因素分别进行Meta 回归分析,结果显示,对于消融术后LVEF 的增长,只有纳入患者冠心病的比例与其有较强的负相关性,其他因素,包括房颤类型及房颤复发患者比例,对结果均未见显著影响。
但值得指出的是,纳入的研究中大部分为选定类型患者,其年龄相对较轻(平均56.9 岁)、男性比例也偏高(平均86.3%)。在这样的人群中,伴有结构性心脏疾病的患者,如冠心病患者,对效应量的影响可能会被放大。通常意义上来说,持续性或永久性房颤,以及随访期间未发生房颤复发的患者,术后LVEF 变化应更加显著。但回归分析显示,这两项因素与LVEF 升高之间未存在显著相关性。考虑到上述纳入人群的选定性及其他可能的混杂因素,这一结果能否代表总体房颤合并心衰患者情况仍待进一步验证。
本研究尚存不少局限性,如纳入不同类型研究及房颤患者,纳入研究的随访时间相对较短,各研究间存在显著的异质性,对照组纳入的患者类型或干预措施不同等。这些因素一定程度上限制了导管消融有效性的阐释,但导管消融对于该类患者的获益是值得肯定的,笔者期待更多纳入患者类型更全面、随访时间更久的试验来证实本研究结果。虽然房颤合并心衰患者的导管消融治疗目前仍存在不少争议,也未获得全面推广,但随着其有效性与安全性被越来越多试验证实和肯定,导管消融或可成为该类患者更好的治疗选择。
[1] Caldeira D,David C,Sampaio C. Rate vs rhythm control in patients with atrial fibrillation and heart failure:a systematic review and meta-analysis of randomised controlled trials. Eur J Intern Med,2011,22:448-455.
[2] Chatterjee S,Sardar P,Lichstein E,et al. Pharmacologic rate versus rhythm-control strategies in atrial fibrillation:an updated comprehensive review and meta-analysis. Pacing Clin Electrophysiol,2013,36:122-133.
[3] Higgins J,Green S,Cochrane Collaboration. Cochrane Handbook for Systematic Reviews of Interventions. Hoboken, NJ:JohnWiley& Sons,2008.
[4] Wells G,Shea B,O'Connell D,et al. The Newcastle-Ottawa Scale (NOS)for assessing the quality of nonrandomised studies in meta-analyses,2012. URL:http://www. ohri. ca/programs/clinical_epidemiology/oxford.asp.
[5] Hunter RJ,Berriman TJ,Diab I,et al. A randomized controlled trial of catheter ablation versus medical treatment of atrial fibrillation in heart failure (the CAMTAF trial). Circ Arrhythm Electrophysiol,2014,7:31-38.
[6] Jones DG,Haldar SK,Hussain W,et al. A randomized trial to assess catheter ablation versus rate control in the management of persistent atrial fibrillation in heart failure. J Am Coll Cardiol,2013,61:1894-1903.
[7] Khan MN,Jais P,Cummings J,et al. Pulmonary-vein isolation for atrial fibrillation in patients with heart failure. N Engl J Med,2008,359:1778-1785.
[8] MacDonald MR, Connelly DT, Hawkins NM, et al.Radiofrequency ablation for persistent atrial fibrillation in patients with advanced heart failure and severe left ventricular systolic dysfunction:a randomised controlled trial. Heart,2011,97:740-747.
[9] Cha YM,Wokhlu A,Asirvatham SJ,et al. Success of ablation for atrial fibrillation in isolated left ventricular diastolic dysfunction:a comparison to systolic dysfunction and normal ventricular function.Circ Arrhythm Electrophysiol,2011,4:724-732.
[10] Chen MS,Marrouche NF,Khaykin Y,et al. Pulmonary vein isolation for the treatment of atrial fibrillation in patients with impaired systolic function. J Am Coll Cardiol,2004,43:1004-1009.
[11] Gentlesk PJ,Sauer WH,Gerstenfeld EP,et al. Reversal of left ventricular dysfunction following ablation of atrial fibrillation. J Cardiovasc Electrophysiol,2007,18:9-14.
[12] Lutomsky BA,Rostock T,Koops A,et al. Catheter ablation of paroxysmal atrial fibrillation improves cardiac function: a prospective study on the impact of atrial fibrillation ablation on left ventricular function assessed by magnetic resonance imaging.Europace,2008,10:593-599.
[13] Tondo C,Mantica M,Russo G,et al. Pulmonary vein vestibule ablation for the control of atrial fibrillation in patients with impaired left ventricular function. Pacing Clin Electrophysiol,2006,29:962-970.
[14] Choi AD,Hematpour K,Kukin M,et al. Ablation vs medical therapy in the setting of symptomatic atrial fibrillation and left ventricular dysfunction. Congest Heart Fail,2010,16:10-14.
[15] De Potter T,Berruezo A,Mont L,et al. Left ventricular systolic dysfunction by itself does not influence outcome of atrial fibrillation ablation. Europace,2010,12:24-29.
[16] Hsu LF,Jais P,Sanders P,et al. Catheter ablation for atrial fibrillation in congestive heart failure.N Engl J Med,2004,351:2373-2383.
[17] Nedios S,Sommer P,Dagres N,et al. Long-term follow-up after atrial fibrillation ablation in patients with impaired left ventricular systolic function:the importance of rhythm and rate control.Heart Rhythm,2014,11:344-351.
[18] 林建伟,蒋汝红,刘强,等. 射频导管消融与药物室率控制治疗心房颤动合并心力衰竭患者的疗效比较. 心电与循环,2013,32:382-384,392.
[19] 孙育民,刘旭,王骏,等. 导管消融治疗持续性心房颤动伴左室功能不全的临床评价. 中国介入心脏病学杂志,2009,17:213-217.
[20] 沈才杰,陈晓敏,何斌,等. 心房颤动致心动过速性心肌病及导管射频消融术后左心室射血分数恢复的影响因素分析. 中国介入心脏病学杂志,2013,21:34-40.
[21] Cappato R,Calkins H,Chen SA,et al. Worldwide survey on the methods,efficacy,and safety of catheter ablation for human atrial fibrillation. Circulation,2005,111:1100-1105.

