高病毒载量E抗原阳性慢性乙型肝炎的优化治疗
涂德幸 胡小雄 詹建明 范惠珍 邓云梅
高病毒载量E抗原阳性慢性乙型肝炎的优化治疗
涂德幸 胡小雄 詹建明 范惠珍 邓云梅
目的 探讨高病毒载量E抗原(HBeAg)阳性慢性乙型肝炎的优化治疗策略。方法 将171例高病毒载量的HBeAg阳性慢性乙型肝炎患者随机分为3组,A组(n=46)单用干扰素α-2b治疗,B组(n=42)应用干扰素α-2b与阿德福韦酯初始联合治疗,C组(n=83)应用干扰素α-2b治疗26周后进行评估,应答较佳者(C1组,n=36)继续单用干扰素治疗,应答不佳者(C2组,n=47)加用阿德福韦酯治疗。各组患者的干扰素均于52周后停药,继续随访至104周,阿德福韦酯持续口服至104周。观察各组的生化学、病毒学、免疫学和联合应答率。结果 治疗后26、52、104周,联合用药组的病毒学应答率均高于干扰素单药组(均P<0.001)。治疗后104周,观察组(B组、C1组和C2组)的生化学应答率、HBeAg血清转换率均高于对照组(P=0.014,P=0.024),其中B组的联合应答率亦显著高于A组(P=0.027)。各组患者治疗期间未出现严重不良反应。结论 相对于单用干扰素,联合阿德福韦酯治疗高病毒载量HBeAg阳性慢性乙型肝炎能够获得更高的应答率。
病毒性肝炎;乙型;干扰素;阿德福韦酯;疗效
目前的乙型肝炎抗病毒治疗方案对于高病毒载量的乙型肝炎病毒E抗原(HBeAg)阳性慢性乙型肝炎患者存在一定的局限性。中外指南均明确指出,治疗前乙型肝炎病毒(HBV)DNA低水平(中国指南<4×107IU/mL,欧洲指南<2×108IU/mL)是干扰素治疗应答的阳性预测因素[1-2]。然而,对于高病毒载量患者的治疗,各大指南尚无明确的指导性意见。这类患者通常年轻,绝大部分为母婴传播,刚刚突破免疫耐受,病毒载量较高(>1×107IU/mL),转氨酶水平持续或间断轻中度升高,免疫活跃状态尚不稳定,单独使用干扰素治疗效果欠佳。因为年轻,且面临升学、就业、结婚、生育等问题,这类患者通常不愿意接受长疗程的核苷(酸)类似物治疗。那么,探索一种新的、行之有效的治疗策略,优化治疗效果,对于这类患者显得尤为重要。本研究拟探讨干扰素联合阿德福韦酯治疗高病毒载量的HBeAg阳性慢性乙型肝炎的疗效。
1 资料与方法
1.1 一般资料 本研究以年轻、高病毒载量、HBeAg阳性的慢性乙型肝炎患者为观察对象,并排除其他合并症或免疫干扰因素。入选病例来自本院2012年7月~2013年6月肝病科住院患者,均签署知情同意书。
1.1.1 病例入选标准 (1)年龄16~35岁,男女不限;(2)HBsAg阳性>6个月;(3)HBeAg阳性;(4)HBV DNA>1×107IU/mL;(5)丙氨酸氨基转氨酶(ALT)或门冬氨酸氨基转移酶(AST)水平2~10倍正常值上限(ULN);或:转氨酶持续或间断升高1~2ULN超过6个月;或:尽管转氨酶水平<2ULN,但肝穿刺病理显示炎症活跃(≥G2);(6)既往未接受过抗HBV药物治疗;(7)无肾脏器质性疾病或功能障碍,血肌酐水平正常。
1.1.2 病例排除标准 (1)妊娠或近2年内有生育要求者;(2)合并其他肝炎病毒(甲型、丙型、丁型、戊型肝炎病毒)或人类免疫缺陷病毒感染;(3)合并其他肝病,如药物性肝损害、酒精性肝病、非酒精性脂肪性肝病、自身免疫性肝病等;(4)失代偿期肝硬化;(5)合并甲状腺功能亢进、系统性红斑狼疮、银屑病等自身免疫性疾病;(6)合并心、肺、肾、血液系统等重要脏器功能障碍或器质性病变;(7)恶性肿瘤;(8)既往有癫痫病史或精神障碍者(如抑郁症);(9)半年内使用过糖皮质激素、免疫抑制剂或肿瘤化疗药物者;(10)治疗前中性粒细胞<1.0×109/L,和(或)血小板<50×109/L,和(或)转氨酶>10ULN,和(或)总胆红素>51μmol/L。
1.2 分组与治疗方法 按照1∶1∶2原则,将200例符合上述标准的病例随机分为A、B、C 3组,治疗26周后根据应答状况将C组再进一步分为C1和C2两个亚组。治疗及随访过程中,A组有4例、B组有8例、C组有17例患者因为各种原因中途退出研究。各组治疗方法如下。
1.2.1 A组 即对照组(n=46),普通干扰素组α-2b注射液(北京凯因生物技术有限公司,国药准字S20030032)5MU IM QOD,疗程52周。停药后随访至104周。
1.2.2 B组 初始联合组(n=42),即接受上述干扰素治疗方案的同时,服用阿德福韦酯片(齐鲁制药有限公司,国药准字H20080032)10mg PO QD。52周停用干扰素,继续口服阿德福韦酯治疗至104周。
1.2.3 C组 优化治疗组(n=83),即接受上述干扰素治疗方案26周后,进行初始评估,出现HBeAg血清转换或HBV DNA较基础值下降≥2log10IU/mL(设为C1组,n=36),则继续干扰素单药治疗至52周,然后停药随访至104周;若未出现HBeAg血清转换且HBV DNA较基础值下降<2log10IU/ mL(设为C2组,n=47),则加用阿德福韦酯联合治疗,52周后停用干扰素,继续口服阿德福韦酯至104周。
1.3 临床检测 各项检测均由本院检验科进行,采用全自动五分类血液分析仪(日本Sysmex XT-2000i)进行血细胞分析;全自动生化分析仪(日本Olympus AU2700)检测ALT等生化指标;酶联免疫吸附试验(ELISA)法检测HBV血清标志物(上海科华生物工程股份有限公司);实时荧光定量聚合酶链式反应(PCR)法检测HBV DNA载量(中山大学达安基因股份有限公司),检测下限100 IU/mL。
1.4 应答判定标准 抗病毒治疗应答的判定标准主要有病毒学应答、免疫学应答、生化学应答和联合应答。生化学应答指血清ALT和AST恢复正常,即ALT<50U/L、AST<40U/L;病毒学应答指血清HBV DNA检测不到(PCR法)或低于检测下限,早期(治疗后26周)病毒学应答指HBV DNA较基线下降≥2log10IU/mL;免疫学应答指血清HBeAg转阴或HBeAg血清学转换;联合应答指治疗后ALT恢复正常,且HBV DNA检测不出(PCR法)和HBeAg血清学转换[3]。
1.5 统计学方法 应用SPSS13.0统计软件进行统计分析。HBV DNA数据经常用对数转换后进行比较分析。计量资料以“x±s”表示,采用单向方差分析进行比较。计数资料比较采用
Pearson χ2检验,若单元格理论频数小于5,则采用Fisher’s精确概率法。P<0.05为差异有统计学意义。
2 结果
2.1 人群基线资料 研究纳入高病毒载量的HBeAg阳性慢性乙型肝炎患者171例,其中男118例,女53例,平均年龄(26.3±5.5)岁,平均转氨酶水平(221.4±109.0)U/L,平均HBV DNA水平(7.8±0.5)log10IU/mL。3组人群治疗前各项资料比较差异无统计学意义,具有可比性。见表1。
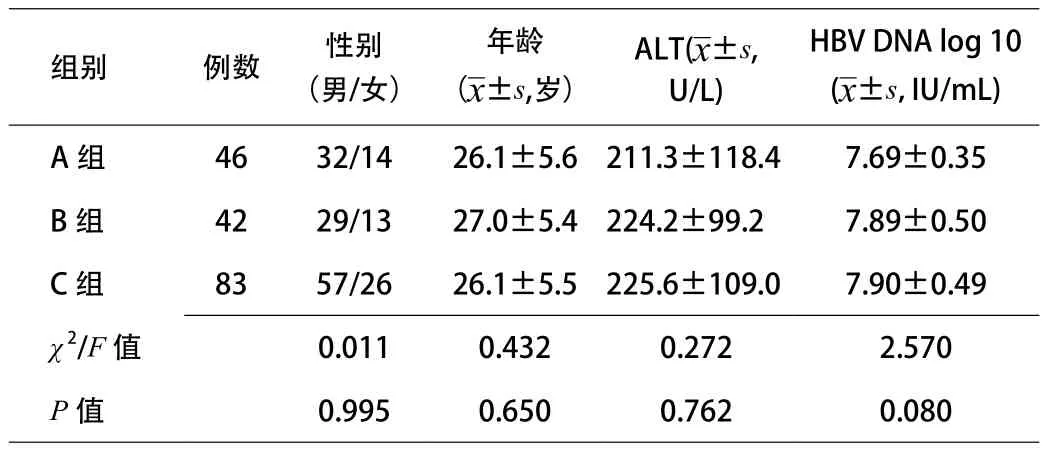
表1 研究人群的基线临床资料特征
2.2 治疗后26周应答状况 治疗26周,3组患者的生化学应答率、HBeAg血清转换率和联合应答率差异均无统计学意义,而B组的病毒学应答率显著高于另外2组(均P<0.001)。见表2。其中C组有36例HBV DNA值较基线水平下降>2log10IU/mL,下一阶段进入C1组,继续单用干扰素治疗至52周;剩余47例患者病毒学应答不佳,下一阶段进入C2组,加用阿德福韦酯联合治疗。
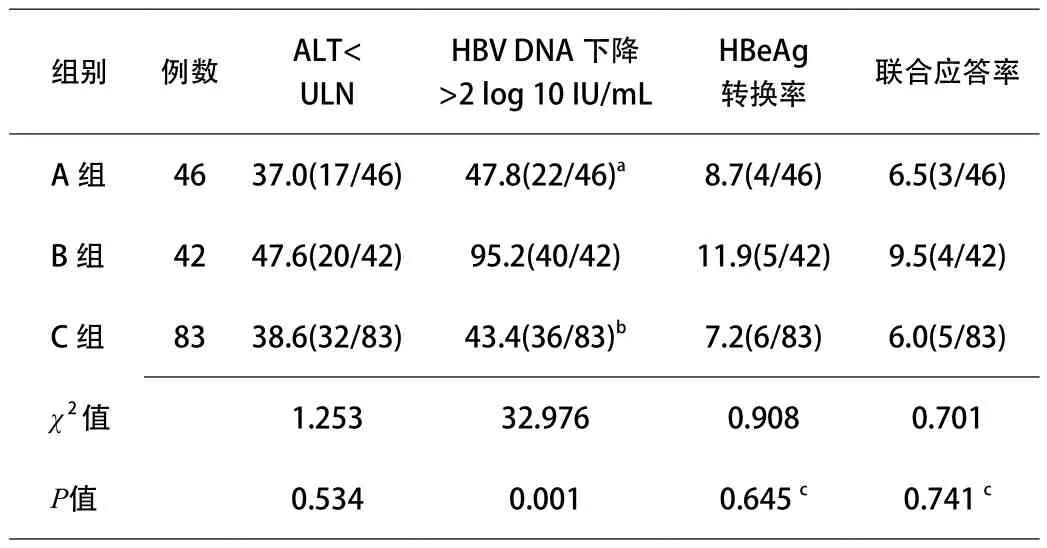
表2 治疗后26周各组患者治疗应答状况比较(%)
2.3 治疗后52周应答状况 治疗后52周病毒学应答率(HBV-DNA<100IU/mL患者的比例)B组显著高于A组(95.2% vs 37.0%,P<0.001)、C1组(95.2% vs 44.4%,P<0.001)和C2组(95.2% vs 78.7%,P=0.023),而C2组亦显著高于A组(78.7% vs 37.0%,P<0.001)和C1组(78.7% vs 44.4%,P=0.001),即联合用药组的病毒学应答率均高于干扰素单药组(4组整体比较P<0.001)。联合应答率B组、C1组和C2组略高于对照组(A组),但差异无统计学意义(P=0.321)。见表3。
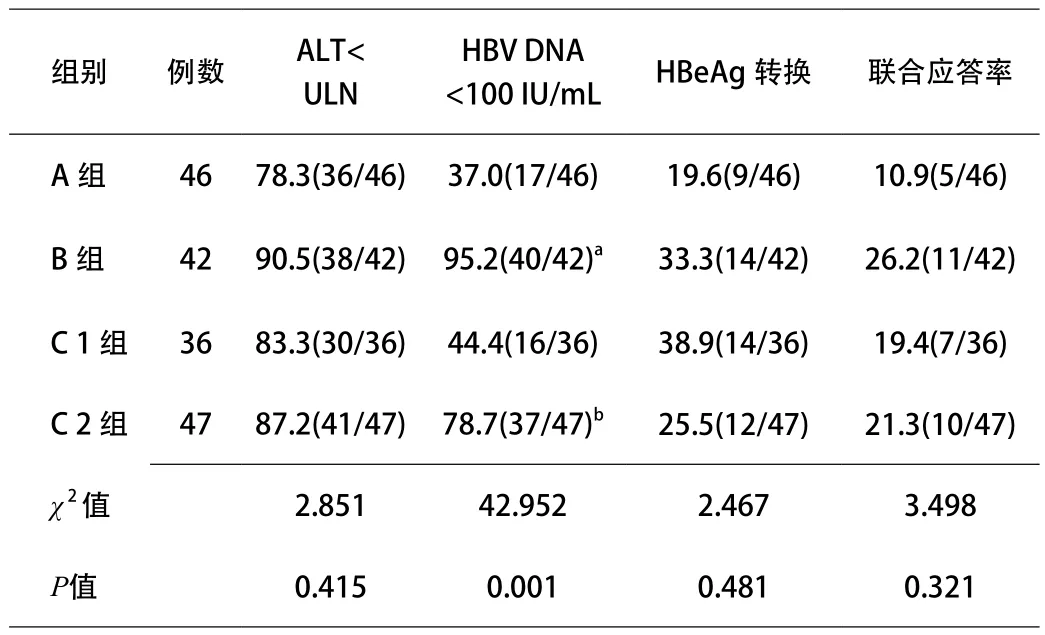
表3 治疗52周各组患者治疗应答状况比较[%(n)]
2.4 治疗后104周应答状况 治疗后104周,3个观察组的生化学应答率、病毒学应答率和HBeAg血清转换率均显著高于对照组(P值分别为0.014,0.001和0.024)。病毒学应答率,B组显著高于A组(95.2% vs 28.3%,P<0.001)和C1组(95.2% vs 38.9%,P<0.001),C2组亦显著高于A组(97.9% vs28.3%,P<0.001)和C1组(97.9% vs 38.9%,P<0.001)。生化学应答率:B组(97.6% vs 80.4.4%,P=0.011)和C2组(95.7% vs 80.4.4%,P=0.022)均显著高于A组。HBeAg血清转换率:B组(40.5% vs 17.4%,P=0.016)、C1组(47.2% vs 17.4%, P=0.004)和C2组(38.3% vs 17.4%,P=0.025)均显著高于A组。联合应答率:4组整体比较差异无统计学意义(P=0.160),但分层进行两两比较时B组显著高于A组(P=0.027),而C1组与A组比较(P=0.267)、C2组与A组比较(P=0.093),差异均无统计学意义。见表4。
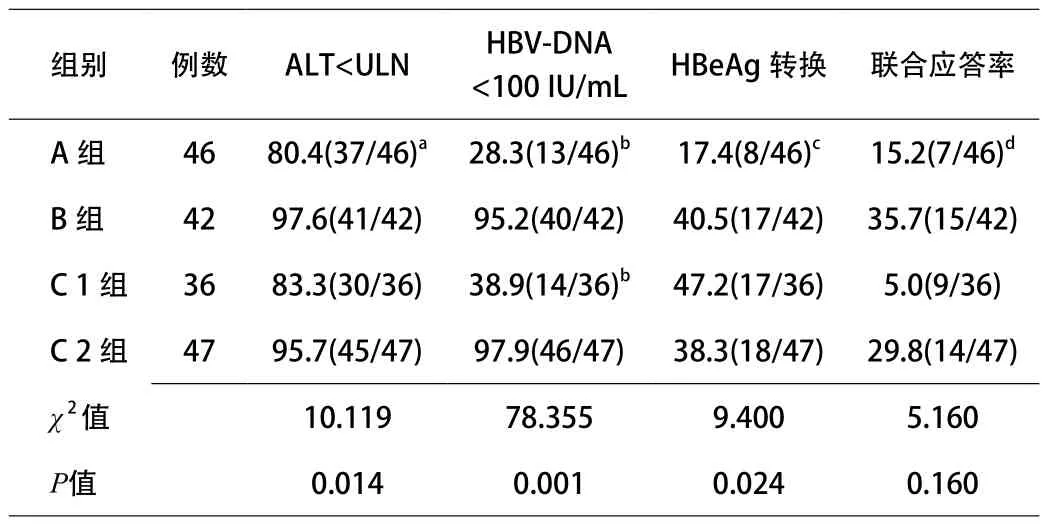
表4 治疗104周各组患者治疗应答状况比较[%(n)]
2.5 不良反应与不良事件 干扰素治疗初期,96%患者(164例)均出现不同程度发热、头痛、肌肉和关节酸痛等流感样症状;79%患者(135例)出现一过性骨髓抑制,主要表现为中性粒细胞减少;8例患者出现皮疹;1例患者出现轻度甲状腺功能减退。上述不良反应经对症处理后,均能继续耐受治疗。其中A组有3例患者、C1组有1例患者干扰素治疗期间出现转氨酶显著升高(>10ULN),经短暂停用干扰素及护肝治疗后好转。
所有口服阿德福韦酯的患者均未出现肾功能损害、继发性范可尼综合征等不良反应。其中B组有2例患者、C2组有1例患者治疗至78周时出现病毒学突破,经检测证实存在阿德福韦酯耐药,给予加用恩替卡韦治疗后至104周检测病毒低于检测下限,未出现生化学突破。
A组有5例,C1组有2例患者在52~104周随访期间出现病毒学突破、转氨酶升高(P=0.303)(A组与C1组出现病毒学突破及转氨酶升高患者的比例的比较),考虑肝炎复发后改为口服恩替卡韦治疗。其余无其他严重不良事件。
3 讨论
我国现有的慢性HBV感染者约9300万人,其中慢性乙型肝炎患者约2000万例[1]。抗HBV治疗的策略有两种:即注射干扰素和口服核苷(酸)类似物(NA)。前者具有免疫调节和抑制病毒复制的双重功效,但须符合较严格的治疗指征,且副作用相对较多;后者抑制病毒复制的效果明显,但面临疗程较长、治疗终点不确定、长期治疗过程中出现耐药及停药后复发等问题。
然而,对那些病毒载量高的HBeAg阳性慢性乙型肝炎,干扰素治疗效果通常应答不佳[3],或疗效不持久,停药后容易复发。而这部分患者通常年轻,面临升学等一系列问题,不愿意接受长疗程的核苷(酸)类似物治疗。因此,我们探索了干扰素联合阿德福韦酯的策略,以期提高有效率,缩短疗程。结果显示,无论是初始联合,还是经干扰素治疗优化选择后叠加阿德福韦酯,其病毒学应答率均显著优于干扰素单药治疗。随访至104周,观察组的生化学应答率、免疫学应答率均优于对照组(P<0.05),其中B组的联合应答率亦高于对照组(P=0.027),提示联合治疗有效,与既往研究报道结果相符[4-5]。而且,随访至104周,C1组的HBeAg血清转换率明显高于A组(P=0.004),提示通过26周单用干扰素的筛选评估,可以遴选出部分潜在对干扰素应答较好的病例,这部分病例继续干扰素足疗程治疗,可以获得更佳的应答率。而对于那部分干扰素应答不佳的病例(C2组),加用阿德福韦酯口服后,亦可获得相对较高的HBeAg血清转换率(38.3%)和联合应答率(29.8%)。
当然,也有学者尝试过干扰素联合或序贯其他NA治疗,如拉米夫定[6]、替比夫定[7]、恩替卡韦[8],结论不一,究竟联合哪种药物更有效,尚无头对头研究结果可对比。
总之,干扰素联合阿德福韦酯治疗高病毒载量的HBeAg阳性慢性乙型肝炎,取得了较好的治疗效果,为部分难治性乙型肝炎提供了一种新的方案选择。
[1] 中华医学会肝病学分会,中华医学会感染病学分会.慢性乙型肝炎防治指南(2010年版)[J].中华内科杂志,2011,52(2):168-179.
[2] European Association for the Study of the Liver.EASL Clinical Practice Guidelines:Management of chronichepatitis B virus infection[J].J Hepatol,2012,57(1):167-185.
[3] 涂徳幸,胡小雄,邓云梅,等.干扰素α-2b治疗132例慢性乙型肝炎患者临床观察[J].天津药学,2015,27(3):48-51.
[4] Wursthorn K,Lutgehetmann M,Dandri M,et al.Peginterferon alpha-2b plus adefovir induce strong cccDNA decline and HBsAg reduction in patients with chronic hepatitis B[J].Hepatology,2006,44(3):675-684.
[5] Wang YD,Zhao CY,Wang W,et al.Improved efficacy by individualized combination therapy with Peg IFN-a 2a and ADV in HBeAg positive chronic hepatitis B patients[J].Hepatogastroenterology,2012,59(115):680-686.
[6] Lau GKK,Piratvisuth T,Luo KX,et al.Peginterferon Alfa-2a,Lamivudine,and the Combination for HBeAg-Positive Chronic Hepatitis B[J].N Engl J Med,2005,352:2682-2695.
[7] 张玮,Sandeep Kumar Karn,张琼方,等.HBV患者替比夫定治疗后序贯干扰素疗效观察[J].中华肝脏病杂志,2013,21(8):570-574.
[8] 李晶.α-干扰素联合恩替卡韦治疗慢性乙型肝炎早期疗效[J].肝脏,2012,17(10):714-716.
Objective To investigate the optimization of treatment strategies with high viral load E antigen (HBeAg) positive chronic. Methods HBeAg-positive chronic hepatitis B patients with high viral load 171 cases were randomly divided into three groups, A group (n=46) alone interferon α-2b treatment, group B (n=42) with interferon α- 2b and adefovir initial combination therapy, after the group C (n=83) treatment with interferon α-2b 26 weeks to assess response preferred by (C1 group, n=36) to continue treatment with interferon alone, in poor response (C2 group, n=47) plus adefovir. Patients in each group were in the 52 weeks of interferon after stopping, continued follow-up to 104 weeks of adefovir dipivoxil orally to 104 weeks duration. Observed biochemical each group, virology, immunology and joint response rate. Results 26,52,104 weeks, virologic response rate of the combination group after treatment is higher than the interferon monotherapy group (P<0.001). 104 weeks after treatment, the observation group (group B, C1 group and C2 group) biochemical response rate, HBeAg seroconversion rate was higher (P= 0.014, P=0.024), in which the combined response rate of group B also A group was significantly higher (P=0.027). No serious adverse reactions occur during treatment of patients in each group. Conclusion With respect to interferon alone, the United adefovir high viral load HBeAg positive chronic hepatitis B can get a higher response rate.
Vird hepatitis; Hepatitis B; Interferons; Adefovir; Efficacy
10.3969/j.issn.1009-4393.2015.35.001
江西省科技支撑计划(20122BBG70109) 宜春市科技支撑计划(JXYC2014KSB015)
江西 336000 江西省宜春市人民医院感染科 (涂德幸 胡小雄詹建明 范惠珍 邓云梅)
胡小雄 E-mail:huxiaoxiong99@126.com

