参一胶囊联合多西紫杉醇+顺铂治疗晚期乳腺癌患者的临床疗效观察及对患者生活质量的影响
张绪良,王旭东Δ,唐东昕
(1.黄石市中心医院 普爱院区 肿瘤外科,湖北 黄石 435001;2.贵阳中医学院第一附属医院 肿瘤科,贵州 贵阳 550001)
参一胶囊联合多西紫杉醇+顺铂治疗晚期乳腺癌患者的临床疗效观察及对患者生活质量的影响
张绪良1,王旭东1Δ,唐东昕2
(1.黄石市中心医院 普爱院区 肿瘤外科,湖北 黄石 435001;2.贵阳中医学院第一附属医院 肿瘤科,贵州 贵阳 550001)
目的 探讨参一胶囊联合多西紫杉醇+顺铂治疗晚期乳腺癌患者的临床疗效及对患者生活质量的影响。方法 选择黄石市中心医院普爱院区肿瘤外科2013年7月~2014年12月收治的135例患者,随机将其分为治疗组(n=69)和对照组(n=66)。2组均进行常规基础治疗,对照组采用多西紫杉醇(75 mg/m2,2次/天)+顺铂(25 mg/m2,1次/天)治疗,治疗组在对照组的基础上联合参一胶囊(20 mg,2次/天)治疗,4周为1个疗程,连续治疗12周。观察比较2组临床疗效及生活质量情况。结果 治疗组的缓解率为63.77%,明显高于对照组的40.91%,2组比较差异有统计学意义(χ2=7.070,P=0.008)。治疗后,治疗组SF-36评分显著升高(63.87±12.08 vs 54.69±8.78)(P<0.05),且明显高于对照组(57.95±11.95)分(P<0.05)。治疗后,治疗组患者不良反应发生情况显著低于对照组,2组比较差异存在统计学意义(Z=2.858,P=0.004)。结论 参一胶囊联合多西紫杉醇+顺铂治疗晚期乳腺癌的临床效果显著,可以明显改善患者临床疗效及生活质量情况。
参一胶囊;多西紫杉醇;晚期乳腺癌;疗效;生活质量
乳腺癌是女性常见的发生在乳腺腺上皮组织的恶性肿瘤之一,约占所有恶性肿瘤的7%~10%左右,目前发病率占女性恶性肿瘤的第一位,且呈逐年上升趋势,好发于45~60岁,主要特点为易转移、易复发及预后较差[1]。临床中,乳腺癌患者主要表现为乳腺肿块、乳头溢液、皮肤改变、乳头乳晕异常及腋窝淋巴结肿等[2]。乳腺癌患者的主要死亡原因为远期转移,晚期复发转移性乳腺癌的治疗较为困难,全身化疗是治疗的主要方案被广泛应用,可以有效延长患者的生存期[3]。目前,紫杉类药物、顺铂均是最常用的化疗药物,不良反应较少,临床效果好;且随着医学的发展与进步,可以将多种化疗药物联合使用治疗晚期乳腺癌患者[4-5]。
乳腺癌的生长与转移,具有一定的新生血管依赖性[6]。我国学者将人参皂苷Rg3开发研制成为一类抗癌新药参一胶囊,用于晚期肺癌、乳腺癌等的辅助治疗。人参皂苷Rg3能显著抑制患者组织中血管内皮细胞生长因子(vascular endothelial growth factor, VEGF)的表达,抑制肿瘤新生血管生成,肿瘤细胞的营养供给被阻断,最终达到抑制肿瘤增殖、浸润与转移的目的[7]。VEGF是作用极强的促血管生成因子之一,而实体瘤的生长与血管生成密切相关;许多肿瘤细胞可以分泌大量的VEGF,肿瘤血管诱导生成,肿瘤细胞进入脉管系统,对肿瘤的侵袭与转移发挥促进作用。本院于2013年7月~2014年12月共收治晚期乳腺癌患者135例,采用参一胶囊联合多西紫杉醇+顺铂进行治疗,临床疗效确切,现报道如下。
1 资料与方法
1.1 一般资料 选自2013年7月~2014年12月来黄石市中心医院肿瘤科就诊的晚期乳腺癌患者135例,采用随机数字法随机分为治疗组和对照组。治疗组69例,年龄33~70岁,平均(46.26±15.52)岁,病程1~7年,平均(4.81±0.72)年,其中浸润性导管癌52例, 浸润性小叶癌12例,黏液液腺癌5例。对照组66例,年龄30~68岁,平均(46.13±14.30)岁,病程1.3~8年,平均(4.69±1.15)年,其中浸润性导管癌48例,浸润性小叶癌10例,黏液液腺癌8例。2组患者性别、年龄、病程和临床分型比较,差异均无统计学意义。
纳入标准:①所有患者符合《乳腺癌诊疗规范(2011年版)》中关于晚期乳腺癌的诊断标准[8],中医诊断符合《中药新药治疗初期乳痈(急性乳腺炎)的临床研究指导原则》[9];②临床表现为乳腺肿块,乳头溢液,皮肤改变,腋窝淋巴结肿大等;③乳腺MRI及组织病理学活检诊断符合晚期乳腺癌的标准。排除标准:①早期、中期乳腺癌患者;②乳腺结核等良性疾病,乳房恶性淋巴瘤,以及其他部位原发肿瘤转移到乳腺的继发性乳腺恶性肿瘤;③合并心、肝、肾等重要脏器功能异常。研究经本院医学伦理委员会批准,患者知情并签署知情同意书。
1.2 方法
1.2.1 治疗方法:对照组给予多西紫杉醇(多西他赛注射液,上海创诺制药有限公司,国药准字H20113165)75 mg/m2,静脉滴注前1天口服地塞米松7.5 mg,2次/天;给药前30 min肌肉注射50 mg苯海拉明,静脉滴注0.4 g西咪替丁预防过敏反应。顺铂(济南益民制药有限公司,国药准字H20050269)25 mg/m2静脉滴注,1次/天。治疗组:在对照组的基础上联合参一胶囊(吉林亚泰制药股份有限公司,国药准字Z20030044)20 mg,2次/天。2组均治疗4周为1个疗程,连续治疗12周。
1.2.2 疗效评定标准:化疗近期疗效评价根据WHO制定的实体瘤临床近期疗效标准:①完全缓解:所见的肿瘤病变完全消失,维持4周以上;②部分缓解:肿瘤病灶的最大直径及最大垂直横径之积缩小50%以上,其他病灶无增大,未出现新病灶,维持4周以上;③稳定:肿瘤病灶的最大直径及最大垂直横径之积缩小不足50%或增大不超过25%,未出现新病灶;④进展:肿瘤病灶的最大直径及最大垂直横径之积增大25%以上,或有新病灶出现。缓解率=(完全缓解+部分缓解)/总数×100%。生活质量采用健康调查简表(the MOS item short from health survey, SF-36)进行评定,包括生理机能、生理职能、躯体疼痛、一般健康状况、精力、社会功能、情感职能7个方面。不良反应采用《抗癌药物常见毒副反应分级标准(WHO)》进行评定,分为0-Ⅳ度,分级越高越严重。治疗后第2天进行疗效评估。

2 结果
2.1 临床疗效比较 治疗组缓解率63.77%,明显高于对照组的40.91%,2组疗效比较差异有统计学意义(χ2=7.070,P=0.008)。见表1。

表1 2组疗效比较[ n(%)]
*P<0.01,与对照组比较,compared with control group
2.2 2组SF-36评分比较 治疗组治疗后,SF-36评分显著高于治疗前(P<0.01),而且明显高于对照组(P<0.05)。其中一般健康状况,生理机能,生理职能,躯体疼痛,精力均明显提高(P<0.05或P<0.01);而社会功能,情感职能,精神健康则无明显统计学意义。见表2。
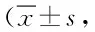
表2 2组SF-36评分比较分)Tab.2 Comparison of SF-36 score between two groups(±s,scores)
*P<0.01,与同组治疗前比较,compared with the same group pre-treatment;#P<0.01,与对照组比较,compared with control group
2.3 2组不良反应比较 治疗后,治疗组患者不良反应发生情况明显少于对照组,2组比较差异存在统计学意义(Z=2.858,P=0.004)。见表3。

表3 2组不良反应发生情况比较[n(%)]Tab.3 Comparison of adverse evens between two groups[n(%)]
3 讨论
在肿瘤的发生、发展过程中,血管的新生发挥着重要的临床意义。新生血管可以将生长状态的肿瘤与循环分流连接起来,有效运输并交换肿瘤生长所需物质;同时,肿瘤凭借新生血管为桥梁,通过血液循环将原发癌脱落下来的细胞转移至靶器官。因此,肿瘤的不断生长在很大程度上依赖于新生血管的生成,抑制破坏血管生成、阻断血供可以作为抑制肿瘤的有效治疗手段。其主要作用机制为阻止肿瘤细胞分泌TAFs、通过抑制金属蛋白酶等的表达而抗内皮细胞增殖与迁徙、通过抗TAFs受体的抗体来中和或阻断其TAFs生物学效应、干扰内皮细胞与细胞外基质的互助作用以阻断血管生成。
参一胶囊的主要成分为人参皂苷Rg3,是从人参中提取的一种有效单体,为四环三萜类人参二醇型皂苷。人参皂苷Rg3可阻断肿瘤细胞与纤维黏连蛋白相结合,破坏肿瘤细胞在血管壁基底膜的侵袭着床,抑制肿瘤内皮细胞增殖及对周围组织的浸润性生长,诱导肿瘤细胞凋亡,减少VEGF蛋白的表达,控制阻止新生血管的生成,最终发挥抑制肿瘤转移的作用[10]。另一方面,人参皂苷Rg3可以使HLA-DR、HLA-ABC、CD56等分子的表达增强,促进淋巴细胞增殖,CD4 /CD8 及Th1 /Th2等漂移至免疫增强的方向,外周淋巴细胞免疫功能有效增强,减弱由于化疗所导致的白细胞下降等不良反应,提高患者生存质量[11]。人参皂苷Rg3在发挥抗肿瘤、提高免疫功能的同时,还具有抗多药耐药性、抗疲劳及保护正常组织器官等作用[12];人参皂苷Rg3可明显减少甚至抑制由于环磷酰胺诱导所产生的骨髓细胞、外周淋巴细胞DNA的损伤,骨髓细胞凋亡及肝肾毒性减轻[13];通过增加肝糖原贮存,减少乳酸、尿素氮等代谢产物的积聚,达到抗疲劳的目的[14]。临床治疗中,人参皂苷Rg3与其他化疗药物联合使用,可以有效提高传统化疗的疗效,抑制肿瘤的生长转移[15]。多西紫杉醇是从红豆杉属植物中提取的天然抗肿瘤药物,属于细胞周期的特异性药物,其特点是抗癌谱广,细胞毒性强[16-18]。通过促进游离的微管蛋白聚合并抑制解聚,保持微管稳定,抑制纺锤体形成及细胞有丝分裂,细胞阻滞停留于G2与M期,抑制杀伤肿瘤细胞[19-20]。顺铂是细胞周期非特异性药物,主要作用于DNA链上的碱基,可有效抑制癌细胞的DNA复制过程及蛋白质的合成,广谱抗癌作用强,是晚期乳腺癌患者常用的一线治疗方案之一[21]。2者在临床中联合使用,无交叉耐药反应,不良反应未见重叠,安全性较好,可发挥协同作用[22-23]。本研究结果显示,治疗组缓解率(63.77%)明显高于对照组(40.91%);治疗后,治疗组SF-36评分由治疗前(54.69±8.78)分显著提高至(63.87±12.08)分,且明显高于对照组评分(57.95±11.95)分(P<0.05);患者不良反应发生分级显著低于对照组(P<0.05)。
综上所述,参一胶囊联合多西紫杉醇+顺铂治疗晚期乳腺癌临床疗效显著,毒副反应轻,可以有效改善患者生活质量。
[1] Alamgeer M, Ganju V, Kumar B, et al. Changes in aldehyde dehydrogenase-1 expression during neoadjuvant chemotherapy predict outcome in locally advanced breast cancer [J]. Breast Cancer Res, 2014,16(2):44-51.
[2] 中华人民共和国卫生部医政司. 乳腺癌诊疗规范(2011年版)[J]. 中国实用外科杂志, 2011, 10(10):902-907.
[3] 于理想, 余之刚. 多西他赛联合长春瑞滨在乳腺癌治疗中的应用[J]. 国际外科学杂志,2011,38(3):199-202.
[4] Fackler MJ, Lopez Bujanda Z, Umbricht C, et al. Novel methylated biomarkers and a robust assay to detect circulating tumor DNA in metastatic breast cancer[J].Cancer Res, 2014,74(8):2160-2170.
[5] Rudat V, El-Sweilmeen H, Brune-Erber I, et al. Identification of breast cancer patients with a high risk of developing brain metastases: a single-institutional retrospective analysis[J].BMC Cancer, 2014,14(1):289-294.
[6] 李晓辉,李军民,冯秋霞,等. 参一胶囊联合化疗对乳腺癌术后患者血清VEGF的影响[J]. 癌症进展,2012,10(4):374-376.
[7] 许鸿雁,庄庆媛. 人参皂甙Rg3 与化疗联合治疗晚期乳腺癌的临床观察[J]. 中国热带医学,2012,12(3):357-359.
[8] 中华人民共和国卫生部医政司. 乳腺癌诊疗规范(2011年版)[J]. 中国实用外科杂志, 2011,31(10):902-907.
[9] 郑筱英. 中药新药临床研究指导原则[M]. 北京中国医药科技出版社,2002:278-281.
[10] 林青凤,茅卫东,刘少平,等. 紫杉醇+顺铂联合参一胶囊治疗晚期三阴性乳腺癌临床观察[J]. 现代中西医结合杂志,2011,20(30):3830-3831.
[11] 张仲苗,江波,郑筱祥. 人参皂苷Rg3对肿瘤放疗患者外周血淋巴细胞的体外免疫增强作用[J]. 中国药学杂志, 2004, 39(4):261-264.
[12] Kim SW, Kwon HY, Chi DW, et al. Reversal of P-glycoprotein-mediated multidrug resistance by ginsenoside Rg3[J]. Biochem Pharmacol, 2003, 65(1):75-82.
[13] Zhang QH, Wu CF, Duan L, et al. Protective effects of ginsenoside Rg(3) against cyclophosphamide-induced DNA damage and cell apoptosis in mice[J]. Arch Toxicol,2008, 82(2):117-123.
[14] 寇小格,梁东良,李小瑞.参一胶囊联合卡培他滨治疗晚期乳腺癌临床观察[J].肿瘤防治研究,2011,38(3):319-321.
[15] 付静,赵翌.人参皂苷Rg3诱导细胞凋亡作用的研究[J].实用肿瘤杂志,2006,21(2): 125-127.
[16] 戴武松,杨蓉,陈焕伟.多西紫杉醇联合卡培他滨治疗晚期蒽环类耐药三阴乳腺癌的临床观察[J].中国医药指南,2015,13(1):121-122.
[17] 张振华.吉西他滨联合多西紫杉醇治疗复发转移性乳腺癌疗效分析[J].肿瘤基础与临床,2013,26(6):488-489.
[18] 燕平,艾淑颖,李志玖,等.希罗达联合多西紫杉醇治疗晚期乳腺癌40 例临床观察[J].实用癌症杂志,2014,29(3):327-329.
[19] 瞿广桥,刘景丽,邱越,等.周剂量多西紫杉醇联合毗喃阿霉素治疗初治晚期乳腺癌的近期疗效[J].广东医学,2012,33(4):3805-3806.
[20] 杨秋敏.多西紫杉醇联合表阿霉素新辅助化疗治疗三阴性乳腺癌与非三阴性乳腺癌的疗效比较[J].肿瘤基础与临床,2014,27(4):297-299.
[21] 纪春连,李秀丽,周少光,等.紫杉醇联合顺铂对阿霉素耐药晚期乳腺癌患者的疗效及护理方法[J].实用临床医药杂志,2015,19(2):101-103.
[22] Terazawa T,Kondo S,Hosoi H,et al. Transarterial infusion chemotherapy with cisplatin plus S-1 for hepatocellular carcinoma treatment: a phase I trial [J].BMC Cancer, 2014,30(14):301-309.
[23] 项庆增,王磊.紫杉醇联合顺铂治疗晚期复发转移乳腺癌的临床研究[J].中国实用医药,2015,10(8):163-164.
(编校:王冬梅)
Clinical effect and life quality study of Shenyi capsule combined with docetaxel and cisplatin in treatment of advanced breast cancer
ZHANG Xu-liang1, WANG Xu-dong1Δ, TANG Dong-xin2
(1. Department of Surgical Oncology, Huangshi Central Hospital, Huangshi 435001, China; 2. Department of Oncology, The First Affiliated Hospital of Guiyang College of Traditional Chinese Medicine, Guiyang 550001, China)
ObjectiveTo explore clinical effect and life quality study of Shenyi capsule combined with docetaxel and cisplatin in treatment of advanced breast cancer.Methods135 cases of advanced breast cancer of Huangshi Central Hospital were collected and diagnosed from July 2013 to December 2014 in accordance with the random number table,were divided into treatment group(n=69) and control group(n=66).Both groups were given regular basis treatment, control group was treated by docetaxel(75 mg/m2,twice a day)and cisplatin(25 mg/m2,once a day), and treatment group combined with Shenyi capsule(20 mg,twice a day)on the basis of control group treatment. 4 weeks were 1 course, and all the cases were taken 12 weeks of continuous treatment. Observed and compared the clinical efficiency and life quality of two groups.ResultsThe remission rate of 63.77% in treatment group was higher than control group of 40.91%, difference was statistically significant(χ2=7.070,P=0.008). After treatment, the SF-36 scale in treatment group significantly increased from(54.69±8.78) to(63.87±12.08), and higher than that of control group(57.95±11.95), differences were statistically significant(P<0.05).The adverse reactions in treatment group was lower than control group, difference was statistically significant(Z=2.858,P=0.000).ConclusionThe clinical effect in treatment of advanced breast canceris obvious by Shenyi capsule combined docetaxel and cisplatin. It can significantly improve clinical effect and life quality.
Shenyi capsule; docetaxel; advanced breast cancer; clinical effect; life quality
贵州省教育厅研究生工作站计划(黔教研合JYSZ字[2014]018)
张绪良,男,本科,主治医师,研究方向:乳腺肿瘤的治疗,E-mail: gym197811@163.com;王旭东,通信作者,男,本科,副主任医师,研究方向:妇科肿瘤的临床治疗;E-mail:hc1972046@163.com。
R737.9
A
1005-1678(2015)11-0097-03

