微波辅助活性炭负载氧化亚铜可见光催化剂制备及应用
李石擎,高晓燕,曹青喜,訾言勤,王广健
(1.上海师范大学 生命与环境科学学院,上海 200234;2.淮北师范大学 化学与材料科学学院,安徽 淮北 235000)
随着世界各国工业化的迅速发展,环境污染日趋严重,导致全球性的资源短缺、环境污染、生态破坏三大危机.治理环境污染问题越来越成为世界各个国家共同关注的问题之一.半导体光催化氧化是一种新兴多相高级氧化处理环境污染物技术.由于宽禁带半导体纳米TiO2光催化剂需要紫外光活化,不能利用可见光,近年来人们围绕TiO2的掺杂改性、敏化修饰及其纳米复合材料催化剂的制备和光催化性能开展.研究开发可见光响应的p 型纳米窄禁带半导体光催化剂,对纳米半导体光催化剂的应用具有重要的意义.陈金毅等[1]总结纳米Cu2O的制备、固定化及其在污染治理中的应用研究进展.洪建明等[2]利用超声辐照技术,成功地合成具有八面体形状的Cu2O 微晶,降解吡咯红B 有机染料,120 min 后降解效率接近90%.周波等[3]以硝酸铜为前驱体,通过水热法合成花状Cu2O/Cu复合纳米材料,在光催化下对有机染料普施安(Procion,即二氯均三嗪染料)有很好的降解作用,120 min 后对浓度为50 mg/L的二氯均三嗪染料降解率达65%.隆金桥等[4]使用NaBH4还原Cu2+合成Cu2O,并利用鼓空气来对浓度为100 mg/L 苯酚进行光催化降解,120 min 后降解效率达33%.黄智[5]等采用NaBH4还原Cu2+合成Cu2O颗粒,用生物效应灯模拟自然光源,对30 mg/L氯硝基苯光催化降解率在120 min后可达80%,300 min后降解率接近90%.张丽等[6]研究Cu2O 粒子对可溶性染料罗丹明B(5 mg/L)的光催化降解情况,在有氧化剂 H2O2(30%)的存在下,25 min光催化降解后,其降解率接近完全.因此,Cu2O可望作为新型p型半导体光催化剂,并在有机污染物治理中发挥重要作用.
以活性炭作为催化剂的载体,把光催化剂负载到活性炭上,由于其具有较高的比表面积、丰富的孔结构及特有的表面化学性质,不仅可使催化剂中的活性组分得到分散,且碳材料与活性组分的相互作用能够影响催化剂的活性.以活性炭为载体,利用CuSO4为铜源,以低成本的Na2SO3和少量葡萄糖为共还原剂,在HAc-NaAc缓冲溶液中,首次采用微波辐射法快速制备活性炭负载花状形貌的氧化亚铜光催化剂,研究利用可见光,在不加任何氧化剂的情况下对罗丹明B降解效果,并初步探讨其降解作用机理.结果表明,该可见光催化剂具有催化效率高,制备成本低,节能环保,可重复使用等特点,可望在工业化应用方面得到推广.
1 实验部分
1.1 仪器和试剂
试剂:实验所用试剂均为分析纯,所用溶液均用去离子水配制;无水硫酸铜,无水亚硫酸钠(上海化学试剂有限公司);葡萄糖(上海山浦化工有限公司);冰乙酸、硫酸(上海振兴化工厂);氢氧化钠(合肥工业大学化学试剂厂);罗丹明B(上海试剂三厂);圆柱状活性炭(AC,淮北恒信环保材料股份有限公司).
仪器:Bruker D8 型X 射线衍射仪,工作条件为:Cu 靶Kα线,起始角度:20°,终止角度:80°,管电压:40 kV,管电流:70 mA,扫描速度:8°/min;X-射线光电子能谱仪(英国VG 科学仪器公司,ESCALAB MK II).激发源为MgKa射线(能量为1 253.6 eV,自然线宽(0.7 eV),荷电校正采用污染C(1s)外标法,污染C(1s)的结合能为284.6 eV.扫描电镜(KY2800B);微波合成仪(Milestone,意大利);FA2004电子天平(上海横平仪器仪表厂);SHZ-D(Ⅲ)循环水式真空泵(上海予华仪器有限公司);紫外可见近红外分光光度计(日本,岛津公司);80-1 型电动离心机(江苏金坛市金城国胜实验仪器厂);DEF-6020 型真空干燥箱(上海博讯实业有限公司医疗制备厂),光化学反应仪(开封市宏兴科教仪器厂,氙灯光源)等.
1.2 Cu2O/AC催化剂的制备
活性炭的预处理:将活性炭放置于烧杯中,用蒸馏水煮沸20 min后倒出滤液,再向其中加入3 mol/L的硫酸溶液,使之浸没,然后搅拌几分钟,使其混合均匀,在室温下静置2 h.将活性炭滤出,用蒸馏水冲洗,直至冲洗后的溶液的pH 值不再改变,加入少量NaOH调至溶液呈中性.放于干燥箱中烘干,备用.
Cu2O/AC 的制备:在 100 mL、0.2 mol/L CuSO4与 50 mL 0.5 mol/L Na2SO3放置于 500 mL 的烧杯中反应,向其中加入300 mL pH 5 HAc-NaAc 的缓冲溶液及少量葡萄糖(0.8 g 左右即可,其中加入葡萄糖的主要作用是防止铜单质过多的析出,并起到一定的分散作用).分别加入0.50、1.0、2.0、3.0和4.0 g 处理过的活性炭,在80 ℃条件下在微波合成仪中反应20 min,得到暗紫红色不同负载量的催化剂Cu2O/AC(约1%~5%,分别标记为xCu2O/AC,其中x=0.1,0.2,0.3,0.4,0.5).通过筛分得到负载型催化剂,进一步真空抽滤得未负载的Cu2O粉体.
1.3 光催化降解方法
罗丹明B溶液的配制:称取适量罗丹明B固体配置成5 mg/L的罗丹明B溶液,置于棕色瓶中备用.实验分析采用分光光度法:在10 mL罗丹明B 溶液中,加入一定量的Cu2O/AC 催化剂,无光下静置,达到吸附平衡后,在光化学反应仪上进行光降解实验;光照结束后,用紫外可见近红外分光光度计测定不同催化剂在罗丹明B最大吸收波长(553 nm)处降解效果.试样的光催化降解率η以下式计算:
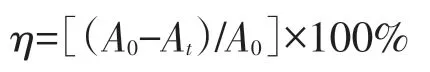
式中:A0:初始试样的吸光度值;At:反应时间为t时试样的吸光度值.
2 结果与讨论
2.1 催化剂Cu2O/AC的X-射线衍射(XRD)物相分析
不同温度下制备Cu2O和不同负载量下Cu2O/AC 催化剂的XRD 的谱图,如图1和图2所示.由图1可知,温度较低(图1(a),40 ℃)或时间较短(图1(b,c),皆为55 ℃)得到的是一种中间体,并没有真正的氧化亚铜生成,即反应不完全(a,b,c 反应时间分别为50 min、50 min和60 min).当温度较高(图1(d),80 ℃,反应时间20 min)出现氧化亚铜的标准衍射谱线[4-5,7],且没有其他的杂质峰出现,故选定此谱线(d)反应时制备Cu2O的最佳反应条件.
从图2可以看出,0.1Cu2O/AC的XRD花样和未经处理的活性炭的XRD花样相比变化不大,0.2Cu2O/AC 样品的花样中也仅能发现微弱的 Cu2O 的特征峰,0.3Cu2O/AC和0.4Cu2O/AC 的XRD 花样中 Cu2O 的特征峰则较为明显.这与氧化亚铜在活性炭表面的分散程度有关.由于活性炭载体具有较大的比表面积,当活性组分的负载量较低时,活性组分以非结晶的无定型态或微晶超微颗粒分散于其表面而表现出较高的催化活性;而当负载量较高时,部分活性组分则以大的微米颗粒结晶态形式析出而使得催化活性降低.因此确定浸渍液硫酸铜的最佳浓度为0.2 mol/L.

图1 不同温度下制备Cu2O 的XR D 花样
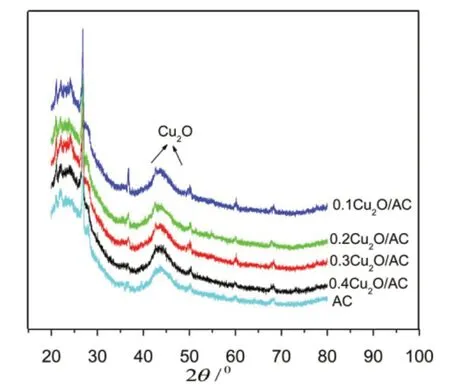
图2 不同负载量下Cu2O/A C 的XR D 花样
2.2 催化剂Cu2O/AC的表面形貌的扫描电子显微镜-能量色散谱(SEM-EDS)分析

图3 预处理后的A C 表面S EM 形貌

图4 Cu2O/A C 表面S EM 形貌
图3和图4分别是预处理的AC、Cu2O/AC的表面形貌图.从图3(右上角插图为部分区域的局部放大)预处理后的AC表面可以看出,处理后的AC表面更加清洁,表面粗糙,结构上由于微晶碳是不规则排列,在交叉连接之间有细孔,会产生碳组织缺陷,有利于有效组分Cu2O的牢固负载.
从图4可以看出,Cu2O/AC催化剂中的有效组分Cu2O呈花型放射状形貌,分布均匀,结晶较好,分散性好.
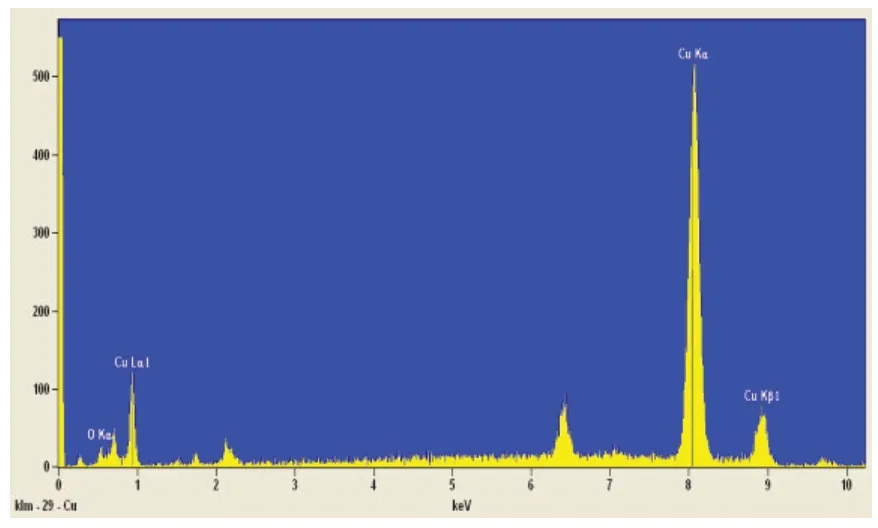
图5 Cu2O/A C 催化剂能量色散谱
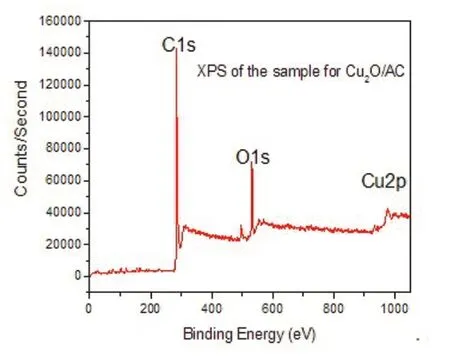
图6 Cu2O/A C 样品的全谱
图5的Cu2O/AC催化剂能量色散谱测试表明,元素重量比为O:Cu = 11.18:88.82,这一结果很好地符合Cu2O元素重量分析,因此可以说明制备的催化剂负载有效组分是纯相Cu2O,未检测到其他杂质,这一结果与XRD的分析是一致的.
2.3 催化剂Cu2O/AC的X-射线光电子能谱分析
XPS可以用于进一步探索催化剂表面有效组分Cu2O的价态分析,图6Cu2O/AC样品的全谱显示样品中含有O、Cu和C 3种元素,其中C来自活性炭和污染的碳,也就是说,样品中除含有活性炭外,还含有有效组分Cu和O元素,不含其它杂质成分.
图7为催化剂组分中O 1s壳层的高分辨光电子能谱.利用Gaussian 多峰拟合去卷积将不对称的O1s光电子能谱分为2个峰区,暗示催化剂表面有效组分中的氧有两种不同的化学环境,531.35 eV和532.85 eV分别归属于表面Cu2O的晶格氧(OL)和表面羟基氧(OOH)[8].
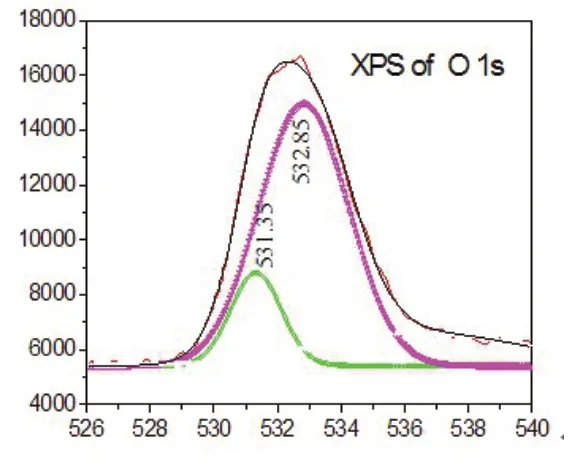
图7 O 1s的高分辨XPS 谱
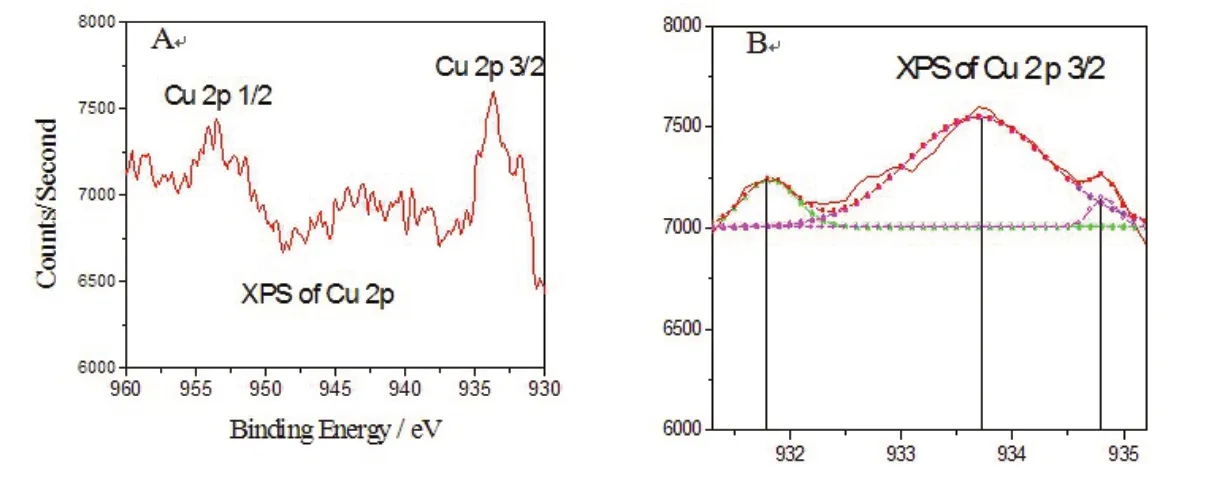
图8 Cu·2p壳层的高分辨XPS 谱(A)和Cu·2p3/2次能级的去卷积分峰拟合谱(B)
从图8A中可以看出Cu的2p 能级分裂为2p 3/2和2p 1/2两个次能级,分别对应于953 eV和932 eV.Cu 2p 3/2壳谱相对较宽,呈不对称结构,对其进行去卷积分峰拟合如图8B 所示.由图8B 可以看出,有效组分铜的化学环境呈现3种不同形式,其结合能为931.7,933.6和934.7 eV,分别归属于铜的不同价态,即分别是 Cu0、Cu+、Cu2+[8-9].从峰面积可以看出,大量的是以Cu+的形式存在的,即是Cu2O,其中有很少量的Cu0和Cu2+存在.Cu0单质的存在是由于在反应中深度还原的结果,更少量的Cu2+是由于生成CuO所致.正是由于极少量的Cu0存在,与Cu+之间的偶合效应,导致催化剂具有更高的催化活性[3].
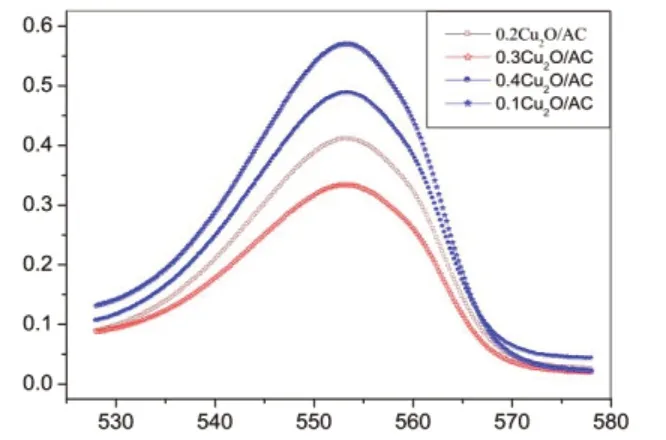
图9 不同Cu2O 负载量催化剂降解的影响
2.4 AC负载不同量Cu2O光催化剂对降解反应的影响
分别取 0.5 g 的 0.1Cu2O/AC、0.2Cu2O/AC、0.3Cu2O/AC和0.4Cu2O/AC 反应体系中,不同负载量Cu2O/AC催化剂对罗丹明B的降解效果如图9所示.
由图9可以看出,使用0.1Cu2O/AC 型负载量(即1%负载量的Cu2O)时,催化剂的光降解效率较低,随着负载Cu2O 量的增大,降解效率逐渐增大.当使用0.3Cu2O/AC型负载量(即3%负载量的Cu2O)时,降解效率达到最大.继续增加负载量超过0.4Cu2O/AC型负载量(即4%负载量的Cu2O)时,降解效率反而降低了.这可能是由于Cu2O的负载量过大时,堵塞活性炭的部分孔道,降低其比表面积,从而降低对水中有机物的吸附能力,导致催化剂活性下降.故选择0.3Cu2O/AC型负载量的催化剂为降解用催化剂.
2.5 反应时间对光降解反应的影响
在反应体系中,加入0.5 g的0.3 Cu2O/AC催化剂,每隔一定时间,取一次样,离心后,测定吸光度,计算降解率,结果如图10所示.

图10 反应时间对光降解反应的影响
由图10A可以看出,随反应时间的延长,光降解率逐渐提高.在2.5 h时,达到62.5%,之后,随着光照时间的加长,罗丹明B 的降解率增加地比较缓慢.考虑到增加降解时间,动力消耗及废水停留时间均增加,反应时间选择为2.5 h为宜.从图10B可以看出,如在反应体系中加入少量(0.5 g,30%)H2O2,其降解速率和降解效率迅速增加,30 min基本降解完成.与文献[6]中用Cu2O颗粒降解效率相比几乎无差异,却很好地解决催化剂从反应体系中的分离问题.
2.6 负载氧化亚铜的活性炭与活性炭的反应性能比较
将0.5 g AC及0.5 g 0.3Cu2O/AC进行催化性能对比,结果如图11所示.
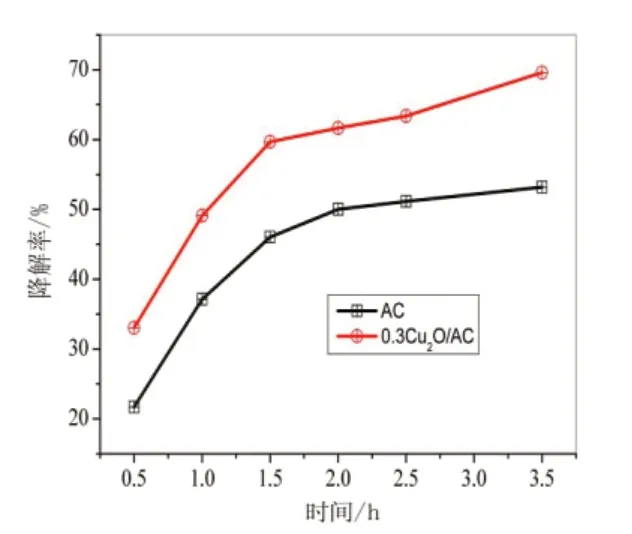
图11 活性炭与负载氧化亚铜活性炭降解率的比较
由图11可知,活性炭对于罗丹明B 的催化氧化也具有一定的催化能力,0.3 Cu2O /AC 对罗丹明B 的降解率随时间逐渐增加,在2.5 h时达到62.5%.活性炭本身对废水中的有机成分具有较强的吸附性能,初期吸光度的降低主要由活性炭的吸附及其表面的氧化引起;而在反应后期,活性炭的吸附逐渐达到饱和,罗丹明B吸光度的降低主要归结于其表面的氧化反应,因而降解率随时间增加趋缓.而负载氧化亚铜的活性炭催化剂在反应初期降解率仅比活性炭的高10%左右,后期随时间的加长增幅较大,在2.5 h时,降解率达62.5%,证明活性炭经负载氧化亚铜处理后显著提高了催化氧化活性及降解效率.
2.7 Cu2O/AC催化剂的用量对降解率的影响
为考察催化剂用量对催化氧化体系效率的影响,分别用不同量的催化剂对罗丹明B催化氧化反应进行研究,结果见图12.
从图12可以看出,催化剂用量低于0.5 g时,降解率随催化剂用量的增加明显升高;催化剂用量高于0.5 g时,降解率的增加不明显.综合考虑催化剂成本和降解率,选择催化剂加入量0.05 g/mL为宜.
2.8 Cu2O/AC催化剂循环利用率
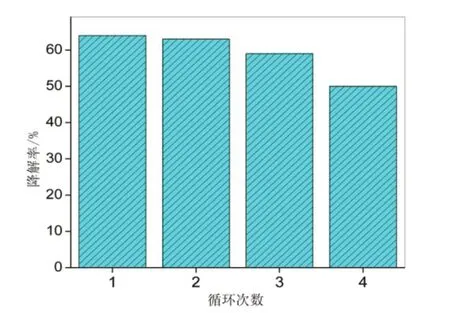
图13 Cu2O/A C 催化循环活性影响
为探讨催化剂在使用过程中的重复利用率,将催化剂Cu2O/AC经过光催化反应后,分离,清洗然后烘干,再进行光催化反应.图13给出Cu2O/AC 4次回收循环的催化活性.从图13中可以看出,催化剂在第1次和第2次使用时,降解率基本不变,第3次使用后略有降低,第4次使用时,催化效率明显下降.究其原因,可能是催化剂在多次长时间的光反应中受到光腐蚀,表层氧化为CuO,而CuO 对其吸附性能要比Cu2O差,导致催化剂表面的有机污染物脱附,从而引起溶液浓度的增加所致.从循环使用4次后,催化剂对其降解率仍然可以达到50%,说明催化剂具有良好的稳定性和循环利用率.
2.9 Cu2O/AC催化反应机理初步探讨
根据光催化理论,Cu2O 光催化降解的机理主要是光诱导半导体激发产生光生电子(e-)和空穴(h+),空穴具有氧化性,能与有机物结合,发生降解反应.同时光生电子和光生空穴在水溶液中会发生一系列反应[7].光生电子可被水中溶解O2捕获生成氧化性很强的·O2-和H2O2,两者可进一步反应生成O2和羟基自由基(·OH),·OH具有强氧化性,可以氧化大部分的有机污染物;光生空穴可被OH-捕获生成·OH.可以用如下步骤(1~9反应式)表示这一复杂的过程:
(1)Cu2O+hγ→e-+h+
(2)O2+e-→·O2-
(3)·O2-+H+→·HO2
(4)h++OH-→·OH
(5)h++H2O→·OH
(6)H2O2+·O2-→·OH+OH-+O2
(7)O2-+h+→O2
(8)2·OH →H2O2
(9)H2O2+h+→O2-+2H+
这些活泼的自由基主要是羟基自由基,可将有机污染物进行深度氧化,最终矿化为CO2和H2O,其可能的机理如图14所示.
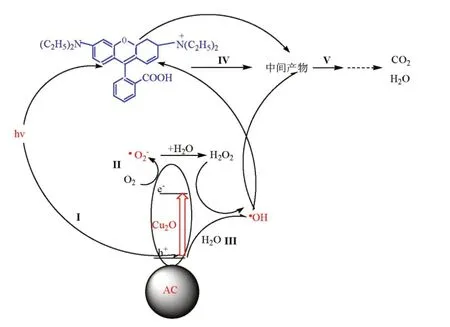
图14 Cu2O/A C 光催化降解机理
3 结论
以CuSO4为铜源,Na2SO3和少量葡萄糖为共还原剂,活性炭为载体,在微波辐射下快速、一步法制备Cu2O /AC可见光响应的光催化剂.AC表面的有效组分为纯相Cu2O,呈放射花状形貌.该催化剂能有效对有机污染物罗丹明B在不外加氧化剂下,只利用溶液中的溶解氧进行可见光的光催化降解,并初步探讨反应机理.催化循环实验表明该催化剂可方便从体系中分离,并可多次重复使用.
[1]陈金毅,张静,张文蓉,等.纳米Cu2O 可见光催化降解有机污染物的研究进展[J].五邑大学学报:自然科学版,2009,23(3):63–67.
[2]洪建明,邓昱,盛东.八面体形Cu2O 微晶的超声制备与表征[J].电子显微学报,2009,28(3):224–228.
[3]周波,刘志国,王红霞,等.花状Cu2O/Cu 的水热合成及其光催化性能[J].物理化学学报,2009,25(9):1841–1846.
[4]隆金桥,李远成.Cu2O光催化降解苯酚[J].化工设计,2004,14(6):42–44.
[5]黄智,张爱茜,韩朔睽,等.光催化氧化降解对氯硝基苯[J].环境化学,2003,22(3):150–153.
[6]张丽,杨迎春.氧化亚铜可见光催化降解罗丹明B的初步研究[J].成都信息工程学院学报,2006,21(5):711–714.
[7]翟纪伟,高荣杰,张雅栋.Cu2O光催化降解海水中苯酚的研究[J].海洋环境科学,2011,30(2):227–229.
[8]XIN Baifu,WANG Peng,DING Dandan,et al.Effect of surface species on Cu-TiO2photocatalytic activity[J].Applied Sur⁃face Science,2008,254:2569–2574.
[9]DU Yongling,ZHANG Nuo,WANG Chunming.Photo-catalytic degradation of trifluralin by SnO2-doped Cu2O crystals[J].Catalysis Communications,2010,11:670–674.

