78例住院低钾血症患者病因及临床特点分析
邢万佳,顾欣,曲卫,王静,李美晔,姜兆顺
(济南军区总医院,济南250021)
78例住院低钾血症患者病因及临床特点分析
邢万佳,顾欣,曲卫,王静,李美晔,姜兆顺
(济南军区总医院,济南250021)
目的 总结低钾血症发生的常见原因及临床特点。方法 回顾性分析78例以低钾血症入院患者的临床资料。结果 78例患者中糖尿病30例,甲状腺疾病16例,肾上腺疾病及肾脏病变各8例,原发性高血压7例,低钾性周期性麻痹5例,其他原因4例。低钾程度为轻度26例、中度27例、重度25例,其中肾脏病变患者低钾程度最重。结论 低钾血症以内分泌疾病及肾脏疾病所致者常见,肾脏疾病导致的低血钾多较为严重。对低钾血症应针对病因制定治疗方案。
低钾血症;内分泌代谢性疾病;病因学
低钾血症是临床常见的电解质紊乱之一,多种内分泌代谢性疾病、肾脏病变、胃肠道疾病乃至感染等均可通过减少钾摄入,促进钾由胞外向胞内转移或增加胃肠道、肾脏失钾导致低钾血症发生[1]。患者对轻度低钾血症可良好耐受,但中重度低钾血症仍危及生命[2]。由于目前临床对低钾血症的病因认识不全面,存在低钾血症病因筛查不明而致漏诊、误诊的现象。2000年1月~2014年8月,我们共收治78例低钾血症患者,现分析其临床资料,探讨其常见病因和临床特点。
1 资料分析
1.1 基本资料 本组78例低血钾症住院患者,男48例、女30例,年龄18~64岁。入院时血清钾1.5~2.5(2.1±0.3) mmol/L,均<3.5 mmol/L。轻度低血钾(血清钾3.0~3.5 mmol/L)26例(33.3%)、中度低血钾(血清钾2.5~3.0 mmol/L)27例(34.6%)、重度低血钾(<2.5mmo/L)25例(32.1%)。35例患者有肌无力,33例患者心律失常,20例患者尿少。
1.2 病因构成及其低钾情况
1.2.1 病因构成 78例低血钾症患者中原发病为糖尿病30例(38.5%),其中1型糖尿病1例,妊娠期糖尿病2例, 2型糖尿病27例;甲状腺疾病16例(20.5%),其中甲状腺机能亢进13例,甲状腺机能减低2例,甲状腺癌术后左甲状腺素钠片替代治疗1例;肾上腺疾病8例(10.3%),其中原发性醛固酮增多症7例,肾上腺皮质机能减低1例;肾脏病变8例(10.3%),其中失钾性肾病4例,肾小管酸中毒3例,Barter综合征1例;原发性高血压7例(9.0%),原发性低钾性周期性麻痹5例(6.4%),慢性胃炎、多发性骨髓瘤、病毒性心肌炎、癔症各1例(5.1%)。78例患者中因内分泌代谢性疾病(糖尿病、甲状腺病变、肾上腺病变)导致低钾血症者54例(69.2%),其中41例(75.9%)为轻、中度低钾血症,13例(24.1%)为严重低钾血症。27例2型糖尿病患者中21例(77.8%)应用胰岛素注射治疗,15例(55.6%)伴高血压者采用钙拮抗剂或噻嗪类利尿剂降压治疗。2例甲状腺机能减低患者因纳差、食欲减低摄入不足导致血钾降低。另14例均因高甲状腺激素水平导致钾向细胞内转移所致。肾上腺皮质机能减低1例,因纳差导致摄钾减少、糖皮质激素缺乏促进肾脏排钾增加导致血钾降低;原发性醛固酮增多症7例中伴高血压3例(42.9%),血清学检查均存在高醛固酮、低肾素血症及血浆醛固酮/肾素比值(ARR)增高,肾上腺影像学检查5例提示存在肾上腺瘤,均为单侧,另2例为肾上腺皮质增生。
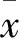

表1 78例不同病因低血钾患者血钾水平及低钾程度
注:与肾脏病变患者相比,*P<0.05。
1.3 治疗及转归 轻度低钾血症患者均口服补钾治疗,给予10%枸橼酸钾口服液10~20 mL,每日3~4次;中度低钾血症在口服补钾基础上酌情静脉补钾,重度低钾血症患者以静脉补钾为主,每日静脉补钾3~6 g,同时辅以口服补钾及心电监护。同时对原发病进行积极治疗,改善糖代谢,纠正甲状腺功能异常,调整降压药物配伍。对3例因肾上腺瘤导致的原发性醛固酮增多症患者行手术治疗,2例肾上腺增生者给口服醛固酮拮抗剂。1例肾小管酸中毒患者口服予枸橼酸钠钾合剂。2例原发性低钾性周期性麻痹患者在补钾同时应用β受体阻滞剂。4例Barter综合征给予保钾利尿剂联合补钾。所有患者出院时复查血钾均恢复正常。
2 讨论
低钾血症是临床常见的电解质紊乱,在随机住院患者中的发生率约为3%[4],约1/4为中重度低钾血症[5]。本组54例患者为内分泌代谢性疾病所致低钾血症。其中30例糖尿病患者应用胰岛素治疗。胰岛素可促进钾转移至胞内导致胞外钾降低[6];部分糖尿病患者伴有高血压,所用降压药物钙拮抗剂或利尿剂可促进胞外钾向胞内转移[7]。因此,对于采用胰岛素治疗的糖尿病患者,尤其联合降压药物时,应合理采用保钾及排钾降压药,必要时通过饮食或药物给予补钾治疗,并注意血钾监测。甲状腺机能亢进是导致轻中度低钾血症的主要内分泌疾病之一,可能的机制为增高的甲状腺激素刺激机体Na+-K+-ATP酶活性增强,增加儿茶酚胺分泌,同时甲亢患者易饥、多食促进胰岛素分泌,促进骨骼肌细胞对钾的摄取、促进钾向胞内转移[8]。剧烈运动、暴饮暴食后更易发生低钾血症。在治疗上除积极抗甲状腺治疗外,注意适当补钾,避免饱餐与剧烈运动,限制高糖食物摄入,均可有效避免低钾血症的发生。原发性醛固酮增多症亦是内分泌代谢性低钾血症的常见原因,增高的醛固酮通过肾远曲小管的钠钾交换促进钾排泄,常规补钾治疗难以纠正[9]。既往研究认为该病仅占高血压患者的1%,但近期研究显示约10%高血压患者合并醛固酮增多症[10]。本组原发性醛固酮增多症患者中仅42.9%为低血钾伴高血压,其余患者仅表现为低钾血症。因此,在低钾血症病因筛查中,对于青中年发病且可排除甲状腺及肾脏病变者,应当考虑原发性醛固酮增多症可能,及时进行血清醛固酮、肾素及血浆醛固酮/血浆肾素活性比值测定。
非内分泌代谢性低钾血症病因以原发性高血压常见。原因是原发性高血压患者常需多种降压药联合治疗。本组7例患者均采用两种以上降压药联合治疗,导致血钾降低。因此降压治疗中应注意应用保钾药物,提高日常膳食中钾的摄入量。肾脏疾病导致钾排出增多亦是非内分泌代谢性低钾血症的重要原因,无论远端或近端肾小管酸中毒均易导致低钾血症[3]。本组8例肾脏疾病患者反复乏力均在半年以上,其中6例为重度、2例为中度低血钾。因此,临床对中重度低钾血症患者,在排除内分泌代谢性疾病及药物因素后,需考虑肾脏长期过量排钾可能。原发性低钾性周期性麻痹是一种与离子通道异常有关的常染色体显性遗传疾病,好发于青壮年,男性外显率较高[11],本组5例均为男性,3例为重度低钾血症,均表现为阵发性双下肢或四肢软瘫。由于低血钾常出现于麻痹之前且纠正低钾血症可阻止肢体软瘫发作[12],因此及时识别并给予补钾十分重要。
多数患者对轻中度低钾血症可耐受,但严重低钾血症可导致横纹肌溶解、心律失常甚至呼吸心跳骤停[13],需临床高度重视。对低钾血症患者应进行详细的病史及用药史采集,同时相关检査宜全面细致,尤其需注意内分泌代谢性病因的筛查。治疗除适当口服或静脉补钾外,原发病的治疗更为重要。
[1] Assadi F. Diagnosis of hypokalemia: a problem-solving approach to clinical cases[J]. Iran J Kidney Dis, 2008,2(3):115-122.
[2] Ben SC, Hmouda H, Bouraoui K. Drug-induced hypokalaemia[J]. Cur Drug Saf, 2009,4(1):55-61.
[3] Unwin RJ, Luft FC, Shirley DG. Pathophysiology and management of hypokalemia: a clinical perspective[J]. Nat Rev Nephrol,2011,7(2): 75-84.
[4] Paltiel O, Salakhov E, Ronen I, et al. Management of severe hypokalemia in hospitalized patients: a study of quality of care based on computerized databases[J]. Arch Intern Med, 2001,161(8):1089-1095.
[5] Paice BJ, Paterson KR, Onyanga-Omara F, et al. Record linkage study of hypokalaemia in hospitalized patients[J]. Postgrad Med J, 1986,62(725):187-191.
[6] Burghen GA, Etteldorf JN, Fisher JN, et al. Comparison of high-dose and low-dose insulin by continuous intravenous infusion in the treatment of diabetic ketoacidosis in children[J]. Diabetes Care, 1980,3(1):15-20.
[7] Mimran A, Ribstein J, Sissmann J. Effects of calcium antagonists on adrenaline-induced hypokalaemia[J]. Drugs, 1993,46(Suppl 2):103-107.
[8] Kelley DE, Gharib H, Kennedy FP, et al. Thyrotoxic periodic paralysis. Report of 10 cases and review of electromyographic findings[J]. Arch Int Med, 1989,149(11):2597-2600.
[9] 叶任高,陆再英.内科学[M].5版.北京:人民卫生出版社,2001:765.
[10] Sukor N.Endocrine hypertension--current understanding and comprehensive management review[J]. Eur J Intern Med, 2011,22(5):433-440.
[11] Abbas H, Kothari N, Bogra J.Hypokalemic periodic paralysis[J]. Natl J Maxillofac Surg, 2012,3(2):220-221.
[12] Venance SL, Cannon SC, Fialho D, et al. The primary periodic paralyses: diagnosis, pathogenesis and treatment[J]. Brain, 2006,129(1):8-17.
[13] Gennari FJ .Hypokalemia[J]. N Engl J Med,1998,339(7):451-458.
姜兆顺
10.3969/j.issn.1002-266X.2015.06.028
R442.9
B
1002-266X(2015)06-0071-03
2014-11-15)

