聚合物稀溶液环流同轴电纺制备药物零级控释纳米纤维
徐方亮, 徐 影, 余灯广
(1.天津渤海化工有限责任公司,天津 300452;2.上海理工大学环境与建筑工程学院,上海 200093;3.上海理工大学材料科学与工程学院,上海 200093)
聚合物稀溶液环流同轴电纺制备药物零级控释纳米纤维
徐方亮1, 徐 影2, 余灯广3
(1.天津渤海化工有限责任公司,天津 300452;2.上海理工大学环境与建筑工程学院,上海 200093;3.上海理工大学材料科学与工程学院,上海 200093)
研究了应用聚合物稀溶液环流同轴电纺制备药物零级控释纳米纤维.以聚丙烯腈(PAN)为成纤聚合物,以阿昔洛韦为药物模型,并以2%(质量/体积)的PAN稀溶液为鞘液实施同轴电纺工艺,制备芯鞘结构载药纳米纤维.通过电镜观察,纳米纤维具有线性形貌和芯鞘结构特征;X-射线晶体衍射结果证明,阿昔洛韦以无定形态存在于PAN基材中;体外溶出实验结果表明,芯鞘纳米纤维能够消除药物初期爆释效应,调控近80%的药物零级方式释放.
同轴电纺;芯鞘纳米纤维;零级控释;聚丙烯腈;鞘液
近年来电流体动力学技术(包括高压静电纺丝(简称电纺)、高压静电喷雾和喷射打印)研究迅速发展,尤其是电纺纳米纤维的应用,研究文献急剧增加[1].电纺通过高压静电场与所处理聚合物流体之间的相互作用,在几十微秒内将流体干燥并拉伸成丝,收集成无纺纳米纤维膜[2].所制备的纳米纤维具有一系列的独特性能,如直径小、表面积大、孔隙率高等,这些性能引起了它们在众多领域的尝试性应用研究.在生物医药领域,通过将药物和聚合物基材一起共溶纺丝,能够制备出新型载药纳米纤维,开发出新型纳米给药系统[3].
作为电纺的一个分支,同轴电纺采用一种具有套筒结构特征的纺丝头实施电纺工艺,制备具有芯鞘结构特征的纳米纤维[4].一般认为,在同轴电纺过程中,外鞘流体必须具有良好的成丝性能,才能获得芯鞘结构[5].文献[6]认为Yu等打破了这一传统认识,报道一系列新型同轴电纺技术,实现了一些新可能,如从不可纺高浓度聚合物溶液中制备纤维,调控纳米纤维直径并进而控制自组装纳米颗粒粒径,系统地提高纳米纤维的质量等[7].
普通电纺载药纳米纤维由于表面积巨大和药物的均匀分布,药物容易产生初期爆释效应,不利于获得药物缓控释效果[8].本研究应用低浓度空白聚丙烯腈溶液为鞘液,应用载有抗病毒药物阿昔洛韦的聚丙烯腈溶液为芯液,实施同轴电纺工艺,制备具有薄层包裹特征的芯鞘纳米纤维,以消除初期爆释效应,获得更好的药物缓控释效果.
1 实 验
1.1 材料与设备
阿昔洛韦(acyclovir,ACY)从大连美伦生物技术公司购买,聚丙烯腈(polyacrylonitrile,PAN)来自浙江上虞百胜化工公司,N,N-二甲基乙酰胺(DMAc)与亚甲基蓝由上海联试化工试剂公司提供,其余化学试剂均为分析纯.
所使用的设备包括:ZGF2000/2μA直流高压发生器(上海苏特电器有限公司),KDS100微量注射泵(美国,Cole-Parmer公司),Quanta FEG450扫描电镜(SEM,荷兰FEI公司),Tecnai G2 F30透射电镜(TEM,荷兰FEI公司),D/Max-BRX-射线晶体衍射仪(日本,RigaKu公司),RCZ-8G智能溶出仪(天津市天大天发科技有限公司),UV-2102 PC型分光光度计(上海优尼科有限公司),自制同轴纺丝头.
1.2 实验方法
1.2.1 纺丝液调配与电纺工艺实施
芯液配制:将15.0 g PAN,1.0 g ACY共溶于100 mL DMAc中,在80℃磁力搅拌24 h成淡黄色透明溶液,即为芯液.在预实验中,芯液中加入质量比为0.000 5%的亚甲基蓝作为显色剂.
鞘液配制:将2.0 g PAN溶解于100 m L DMAc中,在80℃磁力搅拌24 h成浅黄色透明溶液,即为鞘液.
经预实验,电压值固定为15 k V,纤维接受距离为20 cm,芯液流量固定为1.0 m L/h.当鞘液流量为0 mL/h时,即为单射流电纺,制备出没有结构特征的均一纳米纤维F1(monolithic nanofibers F1);当鞘液流量为0.2 mL/h时,为稀溶液环流同轴电纺,制备出芯鞘纳米纤维F2(core-sheath nanofibers F2).
1.2.2 纳米纤维的形态和结构
通过SEM观察纳米纤维,观察前在氮气保护下进行表面喷金处理,统计纳米纤维直径及其分布;通过TEM观察纳米纤维F2的结构特征.
1.2.3 纳米纤维中成分的状态
以CuKα射线为光源,在5~60°范围内对纳米纤维和原料进行广角X-射线衍射分析(XRD). 1.2.4 药物体外溶出特征
根据《中国药典》2010版附录XD释放度测定第二法浆法,测定纳米纤维中ACY的体外释放特征.体外溶出条件:溶出介质为900 m L双蒸水,转速为50 r/min,温度为37±0.1℃.按预定时间取样5 m L,经0.22μm微孔滤膜过滤,适当稀释后进行测定(每个样品重复次数n=6).
2 结果与讨论
2.1 同轴电纺工艺
图1为同轴电纺系统组成示意图,组件包括高压发生器、同轴纺丝头、2台泵和纤维收集装置.系统的实体组装实施如图2(a)所示.同轴电纺工艺能够以同轴纺丝头为模板,单步地将其结构特征“复制”到产品上,获得芯鞘结构纳米纤维[6].本研究中的自制同轴纺丝头如图2(a)所示,芯管内径为0.3 mm,外径为0.6 mm,鞘部的内径为1.2 mm.
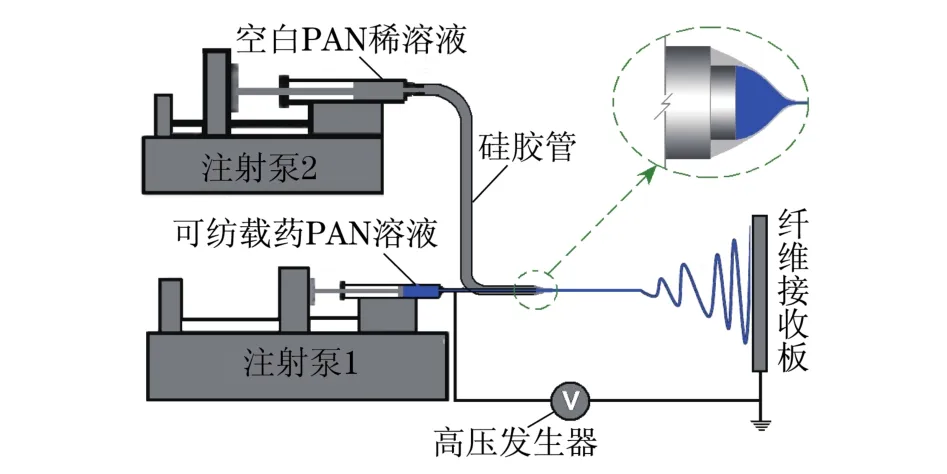
图1 同轴电纺示意图Fig.1 Diagram of the modified coaxial electrospinning
使用数码相机对电纺过程进行拍摄,一个典型的单射流过程如图2(b)所示,该过程包括3个步骤:泰勒锥形成(如图2(c)所示)、直线射流和不稳定区.图2(d)显示一个典型的同轴电纺过程,在亚甲基蓝的指示下,可以清晰地辨别出泰勒锥的芯鞘结构,如图2(e)所示.

图2 同轴电纺的实施Fig.2 Implementation of coaxial electrospinning
2.2 纳米纤维的形态和结构
如图3(a)和3(b)所示,SEM结果表明,纤维F1和F2具有良好的线性形态;纤维中没有因固相分离而形成的纳米颗粒.纤维直径分布如图3(c)所示,分别为420±120 nm和270±40 nm.由于外鞘稀溶液能使芯液在电纺过程中相对长时间处于流体状态,充分发挥静电场的拉伸作用,因此,纤维F2直径更小.TEM观察表明,外鞘液能在PAN载药芯部形成一个20 nm的包裹层,如图3(d)所示.
2.3 纳米纤维中成分的状态
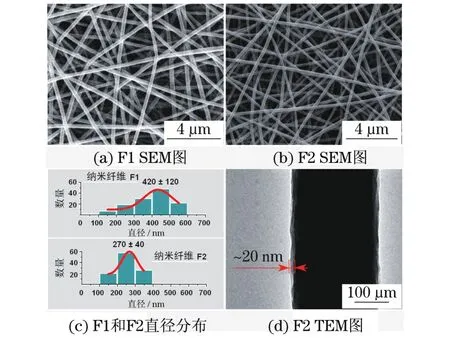
图3 纳米纤维的场发射扫描电子显微镜图Fig.3 FESEM and TEM images of the nanofibers
如图4(a)所示(见下页),ACY在衍射角2θ为 23.2°,26.0°,29.3°时出现特征峰,说明ACY原料药为晶体.PAN在2θ为16.7°处有尖锐峰,说明其存在一定的结晶结构.在纤维F1和F2的衍射图样中,ACY特征峰完全消失,说明ACY在PAN纤维内部以无定型态存在.ACY分子中有羟基基团,因此,能够提供质子与PAN中的-C≡N基团形成氢键,如图4(b)所示(见下页),使得ACY与PAN之间具有良好的相容性,能有效阻止ACY分子之间通过氢键重新形成晶体,如图4(c)所示(见下页).
2.4 药物体外溶出特征
药物的最大吸收峰λmax为252 nm,配制系列标准溶液,以最大峰位置的紫外吸光度A对质量浓度C(μg/mL)作图,得标准曲线方程为A=0.059 08C+ 0.005 15(相关系数R=0.999 9),线性范围为2~20μg/m L.通过测定样品的吸光度,应用标准曲线方程,计算ACY的溶出量和累积溶出百分率,以药物的累积释放百分率对时间作图,如图5所示(见下页).溶出1 h后,F1和F2分别释放的ACY为35.7%和6.8%,说明通过普通单射流电纺制备的均一纳米纤维具有明显的药物初期爆释效应,而在外面包裹了薄层空白PAN的芯鞘纳米纤维F2则能有效地消除药物的初期爆释效应.以纳米纤维在12 h内药物累积释放百分率Q(%)对时间t(h)进行线性拟合,Q=2.14+6.42t,R=0.993 5,说明在此期间内,芯鞘纳米纤维能够控制约80%(质量比)的ACY以零级方式控释(12 h时累积释放量为78.1%).
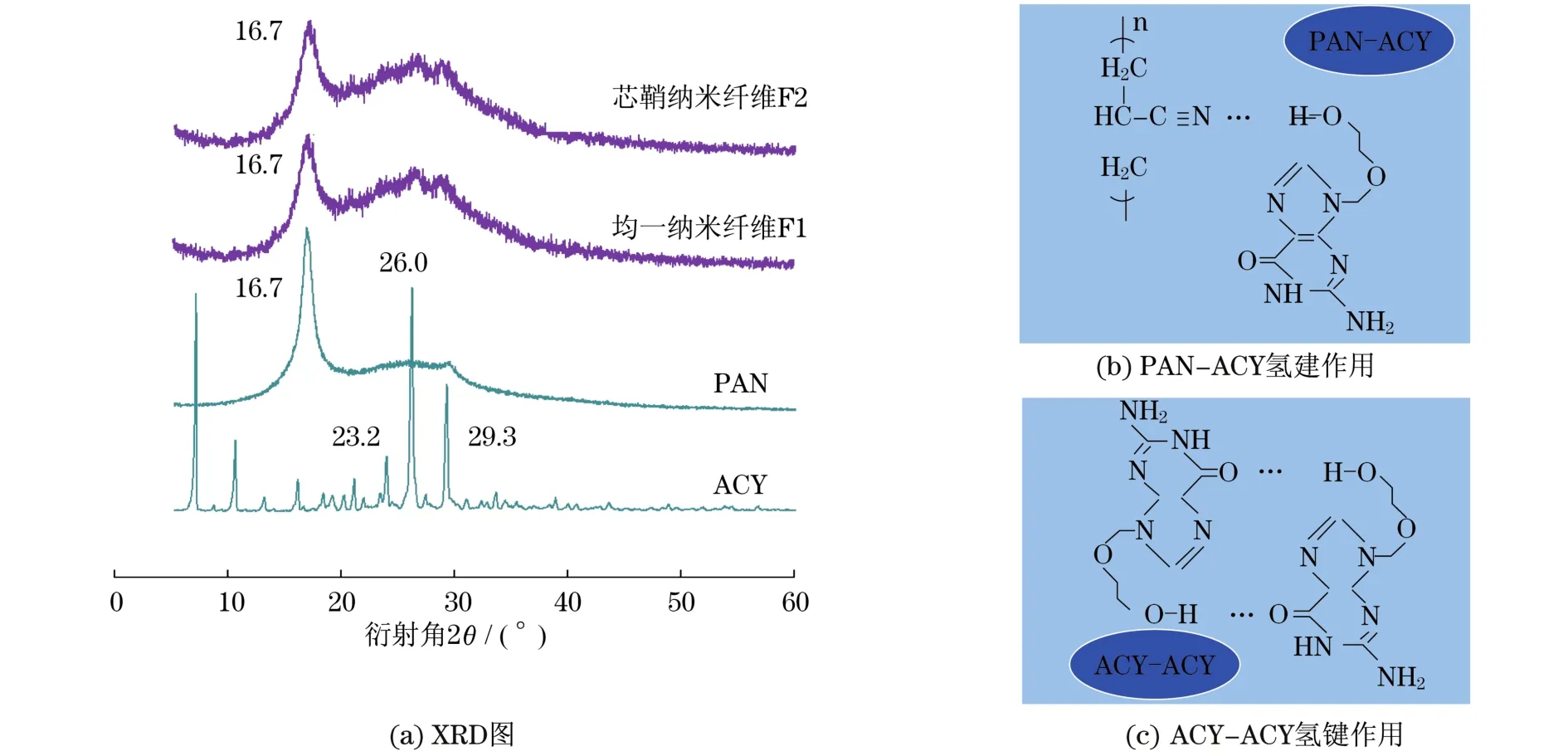
图4 纳米纤维和原料的XRD图Fig.4 XRD patterns of the nanofibers and the components
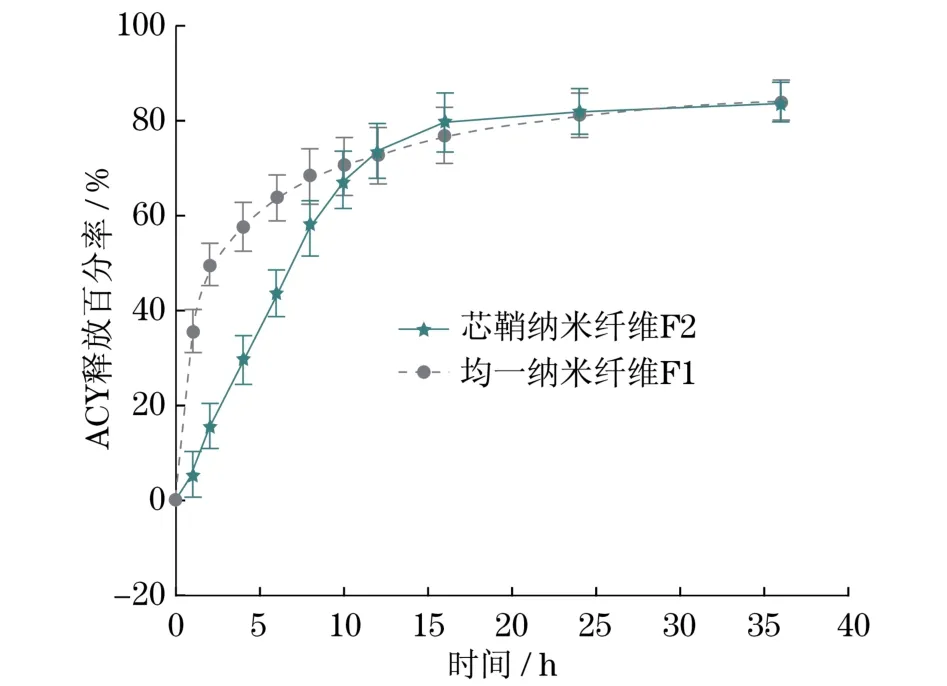
图5 纤维F1和F2的体外药物缓释特征(n=6)Fig.5 In vitro drug sustained release profiles of nanofibers F1 and F2(n=6)
3 结 论
与单射流电纺相比,PAN稀溶液环流同轴电纺能够制备出具有芯鞘结构特征的纳米纤维,并通过对载药芯部进行空白包裹,能有效地消除药物ACY的初期爆释效应,获得了良好的药物零级控释效果.由于“不可纺”的流体有很多种(如小分子溶液、聚合物稀溶液、悬浮液及乳液等),因此,基于不可纺鞘液的改进型同轴电纺能够极大地提高电纺工艺的纳米结构制备能力,为开发更多的功能纳米材料提供可能.
[1] 李保国,华泽钊,刘占杰.高压静电场制备微胶囊研究[J].上海理工大学学报,2000,22(3):189-193.
[2] Chen G,Xu Y,Yu D,et al.Structure-tunable Janus fibers fabricated using spinnerets with varying port angles[J].Chemical Communications,2015,51(22): 4623-3626.
[3] 余灯广,张晓飞,申夏夏,等.电纺载药纳米纤维改善难溶药物溶解性能研究[J].药学学报,2009,44(10): 1179-1182.
[4] Wu Y H,Yu D G,Li X Y,et al.Fast-dissolving sweet sedative nanofiber membranes[J].Journal Materials Sciencs,2015,50(10):3604-3613.
[5] Yu D G,Liu F,Cui L,et al.Coaxial electrospinning using a concentric Teflon spinneret to prepare biphasicrelease nanofibers of helicid[J].RSC Advance,2013,3 (39):17775-17783.
[6] Agarwal S,Greiner A,Wendorff J H.Functional materials by electrospinning of polymers[J].Progress in Polymer Science,2013,38(6):963-991.
[7] Yu D G,Williams G R,X Wang,et al.Dual drug release nanocomposites prepared using a combination of electrospraying and electrospinning[J].RSC Advance,2013,3(14):4652-4658.
[8] Liu W Y,Thomopoulos S,Xia Y N.Electrospun nanofibers for regenerative medicine[J].Advanced Healthcare Materials,2012,1(1):10-25.
(编辑:石 瑛)
Zero-Order Controlled Release Nanofibers Fabricated Using Coaxial Electrospinning with Polymer Dilute Solution as a Sheath Fluid
XUFangliang1, XU Ying2, YU Dengguang3
(1.Tianjin Bohai Chemical Industry Co.Ltd.,Tianjin 300452,China;2.School of Environment and Architecture,University of Shanghai for Science and Technology,Shanghai 200093,China;3.School of Materials Science and Engineering,University of Shanghai for Science and Technology,Shanghai 200093,China)
The present study reports zero-order controlled release drug-loaded nanofibers fabricated using a modified coaxial electrospinning,in which a 2%(weight/volume)dilute solution of polyacrylonitrile(PAN)was exploited as a sheath fluid.With PAN and acyclovir(ACY)as the filament-forming matrix and active pharmaceutical ingredient,respectively,the prepared nanofibers are of linear morphologies and clear core-sheath structures,which were verified by electron microscopic observations.X-ray diffraction tests demonstrate that ACY presents in the PAN matrix in an amorphous status.In vitro dissolution tests show that near 80%of the contained ACY in the nanofibers is freed in a zero-order manner without initial burst effect.
coaxial electrospinning;core-sheath nanofibers;zero-order controlled release;polyacrylonitrile;sheath fluid
R 944;TQ 340.1
A
2014-01-15
国家自然科学基金资助项目(51373101);上海市自然科学基金资助项目(13ZR1428900);上海市教委科研创新重点资助项目(13ZZ113)
徐方亮(1966-),男,工程师.研究方向:痕量分析.E-mail:xfl20030707@sina.com
余灯广(1969-),男,副研究员.研究方向:电流体动力学.E-mail:ydg017@usst.edu.cn
1007-6735(2015)02-0165-04
10.13255/j.cnki.ju sst.2015.02.013

