SnO2负载硅钨杂多酸盐的制备及催化性能研究
白丽梅,刘思晗,乌英嘎,谢立娟,王 斌,刘宗瑞
(内蒙古民族大学化学化工学院,内蒙 古通辽 028043)
SnO2负载硅钨杂多酸盐的制备及催化性能研究
白丽梅,刘思晗,乌英嘎,谢立娟,王 斌,刘宗瑞∗
(内蒙古民族大学化学化工学院,内蒙 古通辽 028043)
制备固载型αK5H[SiW11Zn(H2O)O39]·15H2O/SnO2催化剂,并用IR、XRD对其结构进行了表征.探讨了醇酸摩尔比、催化剂用量、反应时间、带水剂用量等因素对乳酸丁酯酯化率的影响.实验结果表明:在醇酸摩尔比为1.5、50%α-SiW11Zn/SnO2用量为0.4g、反应时间4h、带水剂用量为13mL时,酯化率可以达到90.0%,且催化剂重复使用性能良好.
硅钨酸盐;二氧化锡;乳酸丁酯
乳酸丁酯[1-3]是一种良好的溶剂,可用作硝酸纤维素漆、印刷油墨、天然树脂及合成树脂等的溶剂,并且也是一种重要的合成食用香料.传统工业合成中以硫酸为催化剂,通过乳酸和正丁醇酯化合成.但硫酸腐蚀设备,且转化率低并产生大量酸性废液.随着环境保护法规的不断完善,开发能取代硫酸的新型催化剂已成了化工生产中普遍关注的问题.其中杂多酸催化剂与硫酸相比,具有催化活性好、高选择性、不腐蚀设备等优点[4-5].但多酸也存在比表面积小、易溶于极性溶剂且不易回收等缺陷[6-7],在实际的应用中受到一定限制.本文采用纳米级的SnO2固载硅钨杂多酸盐作为催化剂,进行酯化反应.制得的SnO2粉末细小,比表面积大[8].针对以上问题将硅钨杂多酸盐固载在二氧化锡上,既可以增加比表面积又可以实现重复利用.
1 实验部分
1.1 主要仪器与试剂
仪器:Nicolet 5700型傅里叶红外光谱仪(美国尼高力);XRD-6000型X射线衍射仪(日本岛津).
试剂:硅酸钠、钨酸钠、氯化钾、硫酸锌、结晶四氯化锡、无水乙醇、盐酸、氢氧化钠、乳酸、正丁醇、环己烷等试剂均为分析纯,α-SiW11Zn[9](自制).
1.2 催化剂的制备
1.2.1 纳米二氧化锡的制备[10]将0.264g NaOH和0.7012g SnCl4·H2O先后溶解于由13mL无水乙醇和27mL去离子水组成的混合溶液中,搅拌10min,然后转移到容积为50mL的高压釜中,密封后放入电热恒温干燥箱,在150℃下保持18h;反应完成后,自然冷却至室温;反复用去离子水和乙醇洗涤后,在80℃的烘干箱中烘干,得到纳米SnO2样品.
1.2.2 α-SiW11Zn/SnO2的制备 将一定量的硅钨杂多酸盐分散在一定量的无水乙醇中,再把SnO2粉末缓慢加入α-SiW11Zn乙醇溶液中,在磁力搅拌器上搅拌至乙醇挥发完全,在300℃下焙烧4h,即可制得SnO2固载α-SiW11Zn催化剂,表示为α-SiW11Zn/SnO2.
1.3 乳酸丁酯的合成
在配有冷凝管、温度计、分水器的三颈烧瓶中按一定化学计量比加入乳酸、丁醇、带水剂环己烷及催化剂α-SiW11Zn/SnO2,磁力搅拌并加热回流3h,冷却,经离心收集催化剂,将混合液移至分液漏斗中经蒸馏水萃取,将水层分离,取样测试其酸值.收集酯层,用无水硫酸镁干燥酯层后,将未反应的正丁醇先常压蒸馏出来,再将温度升至180~185℃,收集该馏分得到无色液体即为产品.
1.4 分析测试
用GB/T 1668-2008方法测定反应前后酸值.按下列公式计算酯化率.

其中:V0、V1为反应前、后滴定所需NaOH水溶液的体积.
2 结果与讨论
2.1 催化剂表征
2.1.1 XRD分析 图1为SnO2、α-SiW11Zn及其固载型杂多酸盐的XRD谱图.由图1(c)中可以看出α-SiW11Zn固载量≤50%时,无明显的归属于α-SiW11Zn的衍射峰,表明α-SiW11Zn均匀分散于载体表面.图1(b)当α-SiW11Zn负载量为70%时,在XRD谱图的6°-10°出现了微弱的α-SiW11Zn的特征峰.在其他范围内衍射峰的位置出现了宽化现象,与纯SnO2的吸收峰相似,说明在α-SiW11Zn/SnO2中α-SiW11Zn处于无定形态,而α-SiW11Zn/SnO2是一种非晶态复合物.
2.1.2 FT-IR分析 图2为样品的红外光谱图.由图2(a)可见,在700~1100cm-1范围内出现了杂多阴离子的4种特征吸收峰1002.82cm-1(Si-Oa)、956.53cm-1(W-Od)、898.68cm-1(W-Ob-W)、784.90 cm-1(W-Oc-W),证明合成的配合物具有keggin型结构.在图中可以清晰的看到随着α-SiW11Zn负载量的增加归属于α-SiW11Zn的特征吸收峰相对强度增强.

图1 样品的XRD谱图Fig.1 XRD pattern of the samples

图2 样品的FT-IR谱图Fig.2 FTIR spectrum of the samples
2.2 不同因素对酯化率的影响
2.2.1 不同负载量催化剂对酯化率的影响 在催化剂用量为0.3g,反应时间3h,环己烷用量10 mL,乳酸用量0.05mol,醇酸摩尔比为1.5的条件下,研究杂多酸盐负载量对酯化率的影响.结果如表1所示,酯化率随着α-SiW11Zn负载量的增加而升高.但负载量70%的催化剂与50%的催化剂相比酯化率没有大幅提高,故从节约成本的角度选用50%α-SiW11Zn/SnO2作酯化反应催化剂.
2.2.2 醇酸摩尔比对反应的影响 在催化剂用量为0.3 g,反应时间3h,环己烷用量10mL,乳酸用量0.05mol,通过改变正丁醇的加入量来研究醇酸摩尔比对酯化率的影响.由图3可以看出,固定酸的用量,而增加醇的用量,有利于酯化率的提高.当醇酸摩尔比为1.5时酯化率最高.但当醇的用量过高时反而在一定程度上使酸和催化剂的相对浓度降低,不利于反应的正向进行,导致酯化率降低.因此适宜的醇酸摩尔比为1.5.
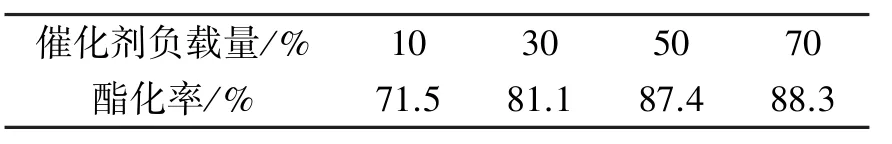
表1 催化剂负载量对酯化率的影响Tab.1 Influence of catalyst loading on esterification rate
2.2.3 带水剂用量对酯化率的影响 在催化剂用量为0.3g,反应时间3h,乳酸用量0.05 mol,醇酸摩尔比为1.5的条件下,研究带水剂环己烷用量对反应酯化率的影响.由图4可以看出,带水剂用量的不同对酯化反应有一定影响,酯化反应产生的水与带水剂形成低共沸物被带出反应体系,有利于反应的正向进行,但当带水剂过多,反而使反应物及催化剂浓度降低,不利于反应,所以选择的最佳带水剂用量为13mL.

图3 醇酸摩尔比对酯化率的影响 Fig.3 Effect of different ratio of lactate acid and butyl alcohol on esterification rate
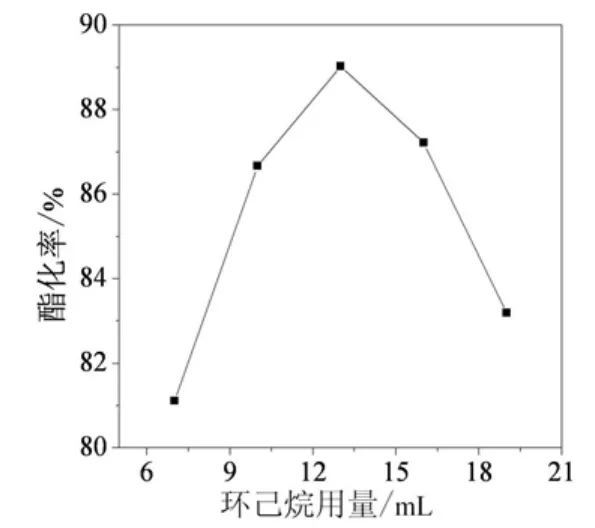
图4 环己烷用量对酯化率的影响Fig.4 Effect of different volume of cyclohexane on esterification rate
2.2.4 催化剂用量对酯化率的影响 乳酸用量为0.05mol,醇酸摩尔比为1.5,反应时间3h,带水剂环己烷用量10mL的条件下,研究催化剂用量对酯化率的影响.由图5可知,催化率用量过少,反应速率慢,酯化率较低.催化剂用量增多,酯化率也随之升高,当催化剂用量为0.4g时,酯化率最高.催化剂再增加时,酯化率基本保持不变.因此适宜的催化剂用量为0.4g.
2.2.5 反应时间对酯化率的影响 在催化剂用量为0.3g,带水剂环己烷用量10mL,乳酸物质的量0.05mol,醇酸摩尔比为1.5,研究反应时间对反应酯化率的影响.由图5可以看出随着时间的延长酯化率也随之升高,但反应时间过长副反应增多反而会使酯化率降低.故适宜的反应时间为4h.

图5 催化剂用量对酯化率的影响Fig.5 Effect of the amount of catalyst on esterification rate

图6 反应时间对酯化率的影响Fig.6 Effect of different reaction time on esterification rate
2.3 反应稳定性考察
由单因素实验中得到α-SiW11Zn/SnO2催化乳酸丁酯最佳实验条件,即乳酸用量为0.05mol,醇酸摩尔比为1.5,α-SiW11Zn负载量为50%,催化剂用量为0.4g,环己烷用量为13 mL,反应时间4h.在此条件下进行4次反应稳定性考察,实验结果如表2所示,在最佳条件下能够稳定催化合成乳酸丁酯,酯化率平均可达90.0%.
2.4 催化剂重复使用对酯化率的影响
在适宜实验条件下,酯化反应结束后,静置,将上层反应液离心倾出,催化剂留在瓶中进行重复试验.由表3可见催化剂重复使用4次酯化率仍可达70%以上,说明催化剂具有可重复使用及活性高的特点.

表2 平行试验Tab.2 Parallel experiment

表3 负载型催化剂重复使用次数对酯化率的影响Tab.3 Influence of the reused times of the supported catalyst on esterification rate
2.5 产品检测与表征
图7为乳酸正丁酯的IR图,其中3 465 cm-1为-OH振动峰,1 741 cm-1为 酯基伸缩振动峰,在2 875、2939、2962cm-1处为烷烃伸缩振动峰,在1 242、1 209、1 130、1 045 cm-1出现了C=O伸缩振动峰,与文献值[11]基本相符,证明为乳酸丁酯.
3 结论
1)α-SiW11Zn/SnO2催化合成乳酸丁酯的适宜条件为乳酸用量为0.05mol,醇酸摩尔比为1.5,α-SiW11Zn负载量为50%,催化剂用量为0.4g,环己烷用量为13 mL,反应时间4 h,乳酸丁酯的酯化率可达90.0 %.
2)α-SiW11Zn/SnO2催化剂制备方法相对简单,无污染,可重复利用,是一种环保型催化剂,拥有良好的应有前景.

图7 乳酸丁酯FT-IR谱图Fig.7 FTIR spectrum of butyl lactate
[1]张应军,程海军.固体超强酸SO42-/TiO2-MoO3催化合成乳酸丁酯[J].中国钼业,2009,33(1):27-29.
[2]刘美艳,俞善信.乳酸正丁酯合成中催化剂的研究进展[J].化工文摘,2007(6):51-56.
[3]俞善信,文瑞明,龙立平.固体酸催化合成乳酸正丁酯[J].常德师范学院学报,2003,15(1):29-32.
[4]于海云,王虎,刘宗瑞.磷钨钼杂多酸催化合成乳酸正丁酯[J].内蒙古民族大学学报:自然科学版,2012,27(1):15-17.
[5]邓庆瑞,庞清宇,段莉梅.CdS-TiO2纳米复合材料在太阳光照射下的光催化性能[J].内蒙古民族大学学报:自然科学版,2014,29(3):267-269.
[6]刘梅,施翔宇,赵景联.二氧化钛固载杂多酸光催化耦合降解酸性品红染料的研究[J].水工业市场,2011(9):68-71.
[7]王恩波,胡长文,许林.多酸化学导论[M].北京:化学工业出版社,1998.
[8]何则强,熊利芝,梁凯.PW12/SnO2催化合成α-亚麻酸植物甾醇酯[J].中国油脂,2010,35(2):33-36.
[9]马荣华,刘春涛,瞿伦玉.十一钨锌杂多配合物的合成、表征及催化性能[J].无机化学学报,2000,16(5):815-819.
[10]陈国帅.二氧化锡纳米结构的制备及其光学性质研究[D].扬州:扬州大学,2013.
[11]化工部科技情报所.化工产品手册(有机化工原料上册)[M].北京:化学工业出版社,1985:333.
责任编辑:高 山
Study on Preparation and Catalytic Performance of SnO2Loaded Silicotungstic Acid Complex
BAI Limei,LIU Sihan,WU Yingga,XIE Lijuan,WANG Bin,LIU Zongrui
(College of Chemistry and Chemical Engineering,Inner Mongolia University for the Nationalities,Tongliao 028043,China)
The supported catalysts αK5H[SiW11Zn(H2O)O39]·15H2O/SnO2were prepared by dipping method and characterized by IR and XRD spectrum.The effect of mole ratio of butanol and lactic acid,a⁃mount of catalyst,reaction time and volume of cyclohexane on esterification rate of butyl lactate was stud⁃ied.The esterification rate can be more than 90.0%when mole ratio of butanol and lactic acid was 1.5,amount of 50% α-SiW11Zn/SnO2was 0.4 g,reaction time was 4 h,volume of cyclohexane was 13 mL. More importantly,the catalyst displayed fine recyclable property.
silicotungstic acid salt;SnO2;butyl lactate
0643.3
A
1008-8423(2015)03-0326-04
10.13501/j.cnki.42-1569/n.2015.09.025
2015-08-01.
国家自然科学基金项目(21261014);内蒙古自然科学基金项目(2012MS0207);内蒙古民族大学硕士研究生科研创新基金项目(NMDSS1422).
白丽梅(1989-),女(蒙古族),硕士生,主要从事多酸功能材料化学的研究;∗
刘宗瑞(1954-),男,教授,主要从事多酸功能材料化学的研究.

