解读反应式“A+B→C+D”
李红晶
物质间的很多反应可以用“A+B→C+D”来表示,该反应式所表示的反应内涵丰富、综合性强,同时具有灵活性、迷惑性等特点。它不仅考查学生对基础知识掌握的程度,而且还能考查他们的观察、分析、判断、推理和运用能力。本文就如何全面的理解该反应式浅谈以下几点,仅供参考,望读者能从中得到启迪。
一、反应式与反应类型的关系
1.与基本反应类型的关系
在化合反应、分解反应、置换反应和复分解反应四种基本反应类型中,置换反应和复分解反应可用“A+BC+D”反应式表示,如Fe+H2SO4=FeSO4+H2↑、NaOH+HCl=NaCl+H2O等;而化合反应和分解反应则不可以,因为它们所进行的反应是“多变一”和“一变多”的反应,不存在物质间相互反应生成另外两种物质的情况。
2.与不属于基本反应类型的关系
在不属于基本反应类型的一些反应中,也有不少反应可以用该式表示,如一些氧化—还原反应,CO+CuO△Cu+CO2;有机物的燃烧,CH4+2O2点燃CO2+2H2O;减少酸性氧化物的反应,2NaOH+CO2=Na2CO3+H2O等。
二、反应式表示的基本反应类型及其之间的异同
1.置换反应
(1)金属单质置换非金属单质。常见的是较活泼金属(金属活动性顺序中排在H前面,K、Ca、Na除外)与酸的反应(酸为稀盐酸和稀硫酸),如Zn+H2SO4=ZnSO4+H2↑。
(2)金属单质置换金属单质。常见的是较活泼金属从盐溶液中置换出金属活动性顺序中位于其后的金属,如Fe+CuSO4=FeSO4+Cu。常温下能与水反应的金属,如K、Ca、Na等,不能与盐溶液发生置换反应。
(3)非金属单质置换金属单质。常见的是一些具有还原性的非金属单质(如H2、C等)与金属氧化物的反应,如H2+CuO△Cu+H2O。
2.复分解反应
(1)酸与碱反应生成盐和水,又称中和反应,如2NaOH+H2SO4=Na2SO4+2H2O。
(2)酸与盐反应生成新酸和新盐,如HCl+AgNO3=AgCl↓+HNO3。
(3)碱与盐反应生成新碱和新盐,如2NaOH+CuSO4=Cu(OH)2↓+Na2SO4。
(4)盐与盐反应生成两种新盐,如BaCl2+Na2SO4=BaSO4↓+2NaCl。
(5)酸与碱性氧化物反应生成盐和水,如H2SO4+MgO=MgSO4+H2O。
3.置换反应和复分解反应的相同点和不同点
(1)相同点:①都是在反应中进行物质组成成分的交换。②反应物A和B所含原子个数之和与生成物C和D所含原子个数之和相等。
(2)不同点:①置换反应是单质和化合物交换成分,而复分解反应是两种化合物间进行互换成分,即置换反应是“一换一”,复分解反应是“二换二”。②置换反应中一定有元素化合价的改变,而复分解反应中没有元素化合价的改变。③复分解反应一般在溶液中进行,而置换反应不一定。④复分解反应中的反应物和生成物均无单质出现,在生成物中必有一种属于盐类。
三、反应式的应用
1.判断有关论述的正误
【例1】对于化学反应“A+B→C+D”,下列说法错误的是()
A.若A和B为化合物,则该反应一定为复分解反应
B.若A、C为单质,B、D为化合物,则该反应一定是置换反应
C.若A为可溶性碱,B为可溶性盐,则C和D可能是两种沉淀物
D.若C和D为盐和水,则该反应一定是中和反应
【解析】分析各选项:A项,当A和B为化合物时,该反应不一定是复分解反应,如CO2+2NaOH=Na2CO3+H2O、CO+CuO△Cu+CO2,复分解反应不但要求反应物是两种化合物,还要求生成物是两种化合物,同时,两种反应物还要互相交换成分,错误;B项,符合置换反应的特征要求,即一种单质和一种化合物反应,生成另外一种单质和一种化合物,正确;C项,表述正确,如Ba(OH)2+CuSO4=BaSO4↓+Cu(OH)2↓;D项,中和反应不仅要求生成物为盐和水,更要求反应物必须是酸和碱,如NaOH+HCl=NaCl+H2O,而酸与碱性氧化物的反应,如2HCl+CuO=CuCl2+H2O,碱与酸性氧化物的反应,如2NaOH+CO2=Na2CO3+H2O,两种反应的生成物虽然都是盐和水,但都不是中和反应,错误。
2.判断反应物或生成物
【例2】有些化学反应可用“A+B→C+D”表示。
(1)常温下发生反应:A+酸→C+盐,则其中A、C的类别可能是:A,C。
(2)若该反应为置换反应,D为Cu,则化合物B可能是(填化学式)。
(3)若该反应为置换反应,D为H2、B为稀H2SO4,则A的选择应满足的条件是。
【解析】(1)从基本反应类型看,有以下三种情况:①若为置换反应,A为金属单质,C为非金属单质,如Zn+2HCl=H2↑+ZnCl2。②若为复分解反应,又可分为三种情况:(a)A为盐,C为酸,如AgNO3+HCl=HNO3+AgCl↓;(b)A为碱性氧化物,C为氧化物,如CuO+H2SO4=H2O+CuSO4;(c)A为碱,C为氧化物,如NaOH+HCl=H2O+NaCl,即中和反应等。
(2)因为是置换反应,D为Cu,则B有两种可能:一是可溶性铜盐溶液,如CuSO4、CuCl2、Cu(NO3)2等,其中一个反应方程式为Fe+CuSO4=FeSO4+Cu;二是CuO,它与非金属单质H2或C反应,如H2+CuO△H2O+Cu。
(3)由已知条件可知A应是金属,该金属须是排在金属活动性顺序中H前面的金属(K、Ca、Na除外),如Zn、Mg、Fe等。
3.书写化学方程式
【例3】写出符合反应式“A+B→C+D”的化学方程式。
(1)A、B均为氧化物:。
(2)C、D均为氧化物:。
(3)A、B、C、D为不同类别的物质:。
(4)D为水的置换反应、复分解反应和不属于基本反应类型的反应各一个:,,。
【解析】解答此题的关键是对反应式“A+B→C+D”的理解和熟悉,以及对反应式内涵的掌握和运用。此题答案多样,例如,(1)CO+CuO△Cu+CO2;(2)CH4+2O2点燃CO2+2H2O;(3)NaOH+HCl=NaCl+H2O;(4)H2+CuO△Cu+H2O,MgO+2HCl=MgCl2+H2O,CO2+2NaOH=Na2CO3+H2O。
4.综合运用
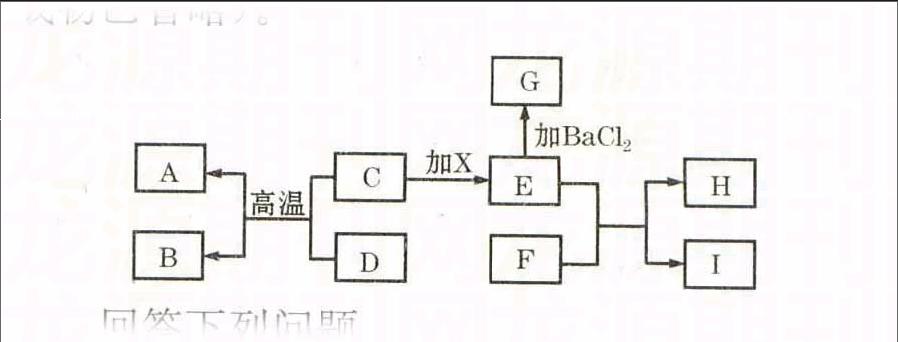
【例4】在下图有关物质转化关系中,各物质均是初中化学常见的物质。其中A为红色金属单质,B能参与植物的光合作用,C、D为黑色粉末,F为可用于改良酸性土壤的碱,G为难溶性物质,H为难溶性蓝色物质(图中部分生成物已省略)。
回答下列问题。
(1)用化学式表示:D,G。
(2)写出E与F反应的化学方程式:。
(3)光合作用生成的淀粉在人体内变成葡萄糖(C6H12O6),葡萄糖在酶的催化作用下发生缓慢氧化,同时放出能量,写出葡萄糖发生缓慢氧化反应的化学方程式:。
【解析】从图示可看出,其中“C+D高温A+B”和“E+F→H+I”与反应式“A+B→C+D”相吻合,为我们的理解打下基础。由题中A为红色金属单质,可知A为Cu;B能参与植物的光合作用,可知B为CO2;由C、D为黑色粉末且反应可以得到A、B,可知C、D应为C和CuO,结合C和X可得到E,E又能与BaCl2反应生成难溶性物质G,可知C为CuO,X为H2SO4,G为BaSO4;又由于F为可改良酸性土壤的碱,可知F为Ca(OH)2;由H为难溶性蓝色物质,可知H为Cu(OH)2;由E和F相互反应可生成H和I,可知E为CuSO4,I为CaSO4,即E和F的反应为CuSO4+Ca(OH)2=Cu(OH)2↓+CaSO4。关于葡萄糖缓慢氧化的反应方程式为C6H12O6+6O2酶6H2O+6CO2。
四、应用时需注意的几个问题
1.注意反应式表述的多向性
反应式“A+B→C+D”可表述的反应具有多向性,不只是表述一类反应,所以运用时要依据具体情况,以实际条件为准,进行分析和判断。
2.注意有关概念的全面性和严谨性
运用该反应式时要涉及不少概念,如置换反应、复分解反应、中和反应等,要注意不能以偏概全,不要断章取义,要严格按照要求去判断。如“某反应中的生成物为盐和水,则该反应一定是中和反应”,此表述不对,它忽视了反应物必须是酸和碱这一前提条件。
3.注意反应发生的条件和要求
反应式“A+B→C+D”表述的任何一个反应都有一定的条件要求,不可忽视,否则就易出错。如复分解反应一般应在溶液中进行;反应物若为碱与盐或盐与盐,则反应物都必须是可溶的,生成物一定要有沉淀、气体或水。
4.注意答案的不唯一性
根据题设要求,不少此类题目的答案具有开放性,即答案不唯一性,要注意全面考虑和分析。